Trandate 50mg, 100mg, 200mg Labetalol Gebruik, bijwerkingen en dosering. Prijs in online apotheek. Generieke medicijnen zonder recept.
Wat is Tradate en hoe wordt het gebruikt?
Trandate 50 mg is een receptgeneesmiddel dat wordt gebruikt om de symptomen van hoge bloeddruk (hypertensie) te behandelen. Tradate 50 mg kan alleen of in combinatie met andere medicijnen worden gebruikt.
Trandate behoort tot een klasse geneesmiddelen die bètablokkers, alfa-activiteit, wordt genoemd.
Wat zijn de mogelijke bijwerkingen van Trandate?
Tradate kan ernstige bijwerkingen veroorzaken, waaronder:
- duizeligheid,
- trage hartslag,
- zwakke pols,
- flauwvallen,
- langzame ademhaling,
- kortademigheid,
- zwelling,
- snelle gewichtstoename,
- ernstige hoofdpijn,
- wazig zien,
- bonzen in je nek of oren,
- verlies van eetlust,
- maagpijn (rechtsboven),
- griepachtige symptomen,
- jeuk,
- donkere urine, en
- geel worden van de huid of ogen (geelzucht)
Roep meteen medische hulp in als u een van de bovenstaande symptomen heeft.
De meest voorkomende bijwerkingen van Tradate 200 mg zijn:
- duizeligheid,
- slaperigheid,
- vermoeidheid,
- misselijkheid,
- braken,
- plotselinge warmte,
- roodheid van de huid,
- zweten,
- gevoelloosheid, en
- tintelend gevoel in je hoofdhuid
Vertel het uw arts als u een bijwerking heeft die u hindert of die niet weggaat.
Dit zijn niet alle mogelijke bijwerkingen van Tradate. Vraag uw arts of apotheker om meer informatie.
OMSCHRIJVING
Trandate (labetalol) Tabletten zijn adrenerge receptorblokkers die zowel selectieve alfa1-adrenerge als niet-selectieve bèta-adrenerge receptorblokkerende werkingen hebben in een enkele stof.
Labetalolhydrochloride (HCl) is een racemaat dat chemisch wordt aangeduid als 2-hydroxy-5-[1-hydroxy-2-[(1methyl-3-fenylpropyl)amino]ethyl]benzamide-monohydrochloride en heeft de volgende structuur:
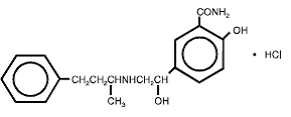
Labetalol HCl heeft de empirische formule C19H24N2O3•HCl en een molecuulgewicht van 364,9. Het heeft twee asymmetrische centra en bestaat daarom als een moleculair complex van twee diastereoisomere paren. Dilevalol, de R,R' stereo-isomeer, maakt 25% uit van racemisch labetalol.
Labetalol HCl is een wit of gebroken wit kristallijn poeder, oplosbaar in water.
Trandate 50 mg tabletten bevatten 100, 200 of 300 mg labetalol HCl en worden oraal ingenomen. De tabletten bevatten ook de inactieve ingrediënten maïszetmeel, FD&C Yellow No. 6 (alleen 100- en 300 mg-tabletten), hydroxypropylmethylcellulose, lactose, magnesiumstearaat, gepregelatineerd maïszetmeel, natriumbenzoaat (alleen 200 mg-tabletten), talk ( alleen tabletten van 100 mg) en titaandioxide.
INDICATIES
Trandate (labetalol) Tabletten zijn geïndiceerd voor de behandeling van hypertensie. Trandate (labetalol) Tabletten kunnen alleen of in combinatie met andere antihypertensiva worden gebruikt, met name thiazide en lisdiuretica.
DOSERING EN ADMINISTRATIE
DOSERING MOET GENDIVIDUALISEERD ZIJN. De aanbevolen aanvangsdosering is tweemaal daags 100 mg, ongeacht of het alleen wordt gebruikt of wordt toegevoegd aan een diuretisch regime. Na 2 of 3 dagen, waarbij de bloeddruk in staande positie als indicator wordt gebruikt, kan de dosering om de 2 of 3 dagen worden getitreerd in stappen van 100 mg bid. De gebruikelijke onderhoudsdosering van labetalol HCl ligt tussen 200 en 400 mg tweemaal daags.
Aangezien het volledige antihypertensieve effect van labetalol HCl gewoonlijk wordt waargenomen binnen de eerste 1 tot 3 uur na de initiële dosis of dosisverhoging, kan klinisch worden vastgesteld dat er geen overdreven hypotensieve respons is in de kantooromgeving. De antihypertensieve effecten van voortgezette dosering kunnen worden gemeten bij volgende bezoeken, ongeveer 12 uur na een dosis, om te bepalen of verdere titratie noodzakelijk is.
Patiënten met ernstige hypertensie kunnen 1200 tot 2400 mg per dag nodig hebben, met of zonder thiazidediuretica. Indien bijwerkingen (voornamelijk misselijkheid of duizeligheid) optreden bij tweemaal daags toegediende doses, kan dezelfde totale dagelijkse dosis, driemaal daags toegediend, de verdraagbaarheid verbeteren en verdere titratie vergemakkelijken. Titratiestappen mogen niet hoger zijn dan 200 mg tweemaal daags.
Wanneer een diureticum wordt toegevoegd, kan een additief antihypertensief effect worden verwacht. In sommige gevallen kan dit een aanpassing van de dosering van labetalol HCl noodzakelijk maken. Zoals met de meeste antihypertensiva, zijn de optimale doseringen van Trandate (labetalol) tabletten meestal lager bij patiënten die ook een diureticum krijgen.
Bij het overzetten van patiënten van andere antihypertensiva, moeten Trandate (labetalol) tabletten worden geïntroduceerd zoals aanbevolen en moet de dosering van de bestaande therapie geleidelijk worden verlaagd.
Oudere patiënten
Net als bij de algemene patiëntenpopulatie kan de behandeling met labetalol worden gestart met tweemaal daags 100 mg en naar boven worden getitreerd in stappen van 100 mg tweemaal daags, zoals vereist voor het onder controle houden van de bloeddruk. Aangezien sommige oudere patiënten labetalol echter langzamer afbreken, kan een adequate bloeddrukcontrole worden bereikt bij een lagere onderhoudsdosering in vergelijking met de algemene populatie. De meerderheid van de oudere patiënten zal tussen 100 en 200 mg tweemaal daags nodig hebben
HOE GELEVERD
Trandate (labetalol) tabletten, 100 mg lichtoranje, ronde, filmomhulde tabletten met breukgleuf aan één kant gegraveerd met "TRANDATE (labetalol) 100", flessen van 100 ( NDC 65483-391-10) en 500 ( NDC 65483-391-50) en eenheidsdosisverpakkingen van 100 tabletten ( NDC 65483-391-11).
Trandate (labetalol) tabletten, 200 mg , witte, ronde, filmomhulde tabletten met breukgleuf aan één kant gegraveerd met "TRANDATE (labetalol) 200", flessen van 100 ( NDC 65483-392-10) en 500 ( NDC 65483-392-50) en eenheidsdosisverpakkingen van 100 tabletten ( NDC 65483-392-22).
Trandate (labetalol) tabletten, 300 mg , middenoranje, ronde, filmomhulde tabletten met breukgleuf aan één kant gegraveerd met "TRANDATE (labetalol) 300", flessen van 100 ( NDC 65483-393-10) en 500 ( NDC 65483-393-50) en eenheidsdosisverpakkingen van 100 tabletten ( NDC 65483-393-33).
Trandate (labetalol) Tabletten moeten worden bewaard tussen 2 ° en 30 ° C (36 ° en 86 ° F). Trandate (labetalol) Tabletten in de eenheidsdosisdozen moeten worden beschermd tegen overmatig vocht.
Prometheus Laboratories Inc. Gefabriceerd in Canada door WellSpring Pharmaceutical Canada Corp. Oakville, ON L6H 1M5 voor Prometheus Laboratories Inc. San Diego, CA 92121. Herzien: november 2010
BIJWERKINGEN
De meeste bijwerkingen zijn mild en van voorbijgaande aard en treden vroeg in de loop van de behandeling op. In gecontroleerde klinische onderzoeken met een duur van 3 tot 4 maanden was stopzetting van Trandate (labetalol) tabletten vanwege een of meer bijwerkingen vereist bij 7% van alle patiënten. In dezelfde onderzoeken leidden andere middelen met uitsluitend bètablokkerende activiteit die in de controlegroepen werden gebruikt tot stopzetting bij 8% tot 10% van de patiënten, en een centraal werkende alfa-agonist leidde tot stopzetting bij 30% van de patiënten.
De incidentiepercentages van bijwerkingen die in de volgende tabel worden vermeld, zijn afgeleid van multicenter, gecontroleerde klinische onderzoeken waarin labetalol HCl, placebo, metoprolol en propranolol werden vergeleken over behandelingsperioden van 3 en 4 maanden. Waar de frequentie van bijwerkingen voor labetalol HCl en placebo vergelijkbaar is, is het oorzakelijk verband onzeker. De percentages zijn gebaseerd op bijwerkingen die door de onderzoeker als waarschijnlijk geneesmiddelgerelateerd worden beschouwd. Als alle meldingen worden bekeken, zijn de percentages iets hoger (bijvoorbeeld duizeligheid 20%; misselijkheid 14%; vermoeidheid 11%), maar de algemene conclusies zijn ongewijzigd.
De bijwerkingen werden spontaan gemeld en zijn representatief voor de incidentie van bijwerkingen die kunnen worden waargenomen bij een correct geselecteerde hypertensieve patiëntenpopulatie, dwz een groep die patiënten met bronchospastische ziekte, duidelijk congestief hartfalen of andere contra-indicaties voor behandeling met bètablokkers uitsluit .
Klinische onderzoeken omvatten ook onderzoeken met dagelijkse doses tot 2.400 mg bij patiënten met ernstiger hypertensie. Sommige bijwerkingen namen toe met toenemende dosis, zoals weergegeven in de volgende tabel die de volledige Amerikaanse database met therapeutische onderzoeken weergeeft voor bijwerkingen die duidelijk of mogelijk dosisgerelateerd zijn.
Daarnaast zijn een aantal andere, minder vaak voorkomende bijwerkingen gemeld:
Lichaam als geheel: Koorts.
Cardiovasculair: Hypotensie, en zelden, syncope, bradycardie, hartblok.
Centrale en perifere zenuwstelsel: Paresthesie, meestal beschreven als tinteling van de hoofdhuid. In de meeste gevallen was het licht en van voorbijgaande aard en trad het gewoonlijk op aan het begin van de behandeling.
Collageen aandoeningen: Systemische lupus erythematosus, positieve antinucleaire factor.
Ogen: Droge ogen.
Immunologisch systeem: Antimitochondriale antilichamen.
Lever en galwegen: Levernecrose, hepatitis, cholestatische geelzucht, verhoogde leverfunctietesten.
Musculoskeletaal systeem: Spierkrampen, toxische myopathie.
Ademhalingssysteem: Bronchospasme.
Huid en aanhangsels: Huiduitslag van verschillende typen, zoals gegeneraliseerde maculopapulaire, lichenoïde, urticariële, bulleuze lichen planus, psoriaform en erytheem in het gezicht; Ziekte van Peyronie; omkeerbare alopecia.
Urinewegen: Moeite met mictie, inclusief acute urineblaasretentie.
Overgevoeligheid: Zeldzame meldingen van overgevoeligheid (bijv. uitslag, urticaria, pruritus, angio-oedeem, dyspneu) en anafylactoïde reacties.
Na goedkeuring voor het op de markt brengen in het Verenigd Koninkrijk, werd een onderzoek met gecontroleerde vrijgave uitgevoerd onder ongeveer 6.800 patiënten voor verdere evaluatie van de veiligheid en werkzaamheid van dit product. De resultaten van dit onderzoek geven aan dat het type, de ernst en de incidentie van bijwerkingen vergelijkbaar waren met de bovengenoemde.
Mogelijke bijwerkingen
Daarnaast zijn andere bijwerkingen die hierboven niet zijn vermeld, gemeld met andere bèta-adrenerge blokkers.
Centraal zenuwstelsel
Omkeerbare mentale depressie die vordert tot catatonie, een acuut reversibel syndroom dat wordt gekenmerkt door desoriëntatie voor tijd en plaats, geheugenverlies op korte termijn, emotionele labiliteit, enigszins vertroebeld sensorium en verminderde prestaties op psychometrie.
Cardiovasculair
Intensivering van AV-blok (zie CONTRA-INDICATIES ).
Allergisch
Koorts gecombineerd met pijn en keelpijn, laryngospasme, ademnood.
hematologisch
Agranulocytose, trombocytopenische of niet-trombocytopenische purpura.
gastro-intestinaal
Mesenteriale trombose, ischemische colitis.
Het oculomucocutane syndroom geassocieerd met de bètablokker practolol is niet gemeld met labetalol HCl.
Klinische laboratoriumtests
Er zijn reversibele verhogingen van serumtransaminasen bij 4% van de patiënten die met labetalol HCl werden behandeld en getest, en, zeldzamer, reversibele verhogingen van bloedureum.
DRUG-INTERACTIES
In één onderzoek ondervond 2,3% van de patiënten die labetalol HCl in combinatie met tricyclische antidepressiva gebruikten tremor, in vergelijking met 0,7% dat werd gemeld bij alleen labetalol HCl. De bijdrage van elk van de behandelingen aan deze bijwerking is onbekend, maar de mogelijkheid van een geneesmiddelinteractie kan niet worden uitgesloten.
Geneesmiddelen met bètablokkerende eigenschappen kunnen het bronchusverwijdende effect van bèta-receptoragonisten bij patiënten met bronchospasmen afzwakken; daarom kunnen doses hoger dan de normale anti-astmatische dosis van bèta-agonistische bronchusverwijders nodig zijn.
Van cimetidine is aangetoond dat het de biologische beschikbaarheid van labetalol HCl verhoogt. Aangezien dit zou kunnen worden verklaard door een verhoogde absorptie of door een verandering in het levermetabolisme van labetalol HCl, moet speciale aandacht worden besteed aan het bepalen van de dosis die nodig is voor bloeddrukcontrole bij dergelijke patiënten.
Er is synergisme aangetoond tussen halothaananesthesie en intraveneus toegediende labetalol HCl. Tijdens gecontroleerde hypotensieve anesthesie met gebruik van labetalol HCl in combinatie met halothaan, mogen geen hoge concentraties (3% of meer) halothaan worden gebruikt omdat de mate van hypotensie zal toenemen en vanwege de mogelijkheid van een grote vermindering van het hartminuutvolume en een toename van centrale veneuze druk. De anesthesist moet worden geïnformeerd wanneer een patiënt labetalol HCl krijgt.
Labetalol HCl verzacht de reflextachycardie die wordt geproduceerd door nitroglycerine zonder het hypotensieve effect ervan te voorkomen. Als labetalol HCl wordt gebruikt met nitroglycerine bij patiënten met angina pectoris, kunnen aanvullende antihypertensieve effecten optreden.

Voorzichtigheid is geboden als labetalol gelijktijdig wordt gebruikt met calciumantagonisten van het verapamil-type.
Zowel digitalisglycosiden als bètablokkers vertragen de atrioventriculaire geleiding en verlagen de hartslag. Gelijktijdig gebruik kan het risico op bradycardie verhogen.
Risico op anafylactische reactie
Tijdens het gebruik van bètablokkers kunnen patiënten met een voorgeschiedenis van ernstige anafylactische reactie op een verscheidenheid aan allergenen reactiever zijn op herhaalde blootstelling, hetzij per ongeluk, diagnostisch of therapeutisch. Dergelijke patiënten reageren mogelijk niet op de gebruikelijke doses epinefrine die worden gebruikt om allergische reacties te behandelen.
Geneesmiddel-/laboratoriumtestinteracties
De aanwezigheid van labetalolmetabolieten in de urine kan leiden tot vals verhoogde niveaus van urinaire catecholamines, metanefrine, normetanefrine en vanillylamandelzuur, gemeten met fluorimetrische of fotometrische methoden. Bij het screenen van patiënten waarvan wordt vermoed dat ze een feochromocytoom hebben en die worden behandeld met labetalol HCl, moet een specifieke methode, zoals een hoogwaardige vloeistofchromatografische test met vaste-fase-extractie (bijv. J Chromatogr 385:241,1987), worden gebruikt om de catecholaminespiegels te bepalen. .
Van Labetalol HCl is ook gemeld dat het een vals-positieve test voor amfetamine produceert bij het screenen van urine op de aanwezigheid van medicijnen met behulp van de in de handel verkrijgbare testmethoden TOXI-LAB® A (dunnelaagchromatografische test) en EMIT-dau® (radio-enzymatische test). Wanneer patiënten die worden behandeld met labetalol een positieve urinetest op amfetamine hebben met behulp van deze technieken, moet dit worden bevestigd met behulp van meer specifieke methoden, zoals een gaschromatografische massaspectrometertechniek.
WAARSCHUWINGEN
Leverletsel
Ernstige hepatocellulaire schade, in ten minste één geval bevestigd door hernieuwde behandeling, komt zelden voor bij behandeling met labetalol. De leverbeschadiging is meestal reversibel, maar levernecrose en overlijden zijn gemeld. Verwonding is opgetreden na zowel kortdurende als langdurige behandeling en kan langzaam progressief zijn ondanks minimale symptomen. Soortgelijke leveraandoeningen zijn gemeld met een verwante onderzoeksverbinding, dilevalol HCl, waaronder twee sterfgevallen. Dilevalol HCl is een van de vier isomeren van labetalol HCl. Voor patiënten die labetalol gebruiken, zou periodieke bepaling van geschikte leverlaboratoriumtests dus geschikt zijn. Bij het eerste symptoom/teken van leverdisfunctie (bijv. pruritus, donkere urine, aanhoudende anorexia, geelzucht, gevoeligheid van het rechter bovenste kwadrant of onverklaarbare "griepachtige" symptomen) moeten geschikte laboratoriumtests worden uitgevoerd. Als de patiënt laboratoriumgegevens heeft van leverbeschadiging of geelzucht, moet de behandeling met labetalol worden stopgezet en niet opnieuw worden gestart.
Hartfalen
Sympathische stimulatie is een essentieel onderdeel dat de bloedsomloop ondersteunt bij congestief hartfalen. Bètablokkade brengt een potentieel risico met zich mee dat de myocardiale contractiliteit verder wordt verlaagd en ernstiger falen wordt veroorzaakt. Hoewel bètablokkers moeten worden vermeden bij duidelijk congestief hartfalen, kan labetalol HCl indien nodig met voorzichtigheid worden gebruikt bij patiënten met een voorgeschiedenis van hartfalen die goed worden gecompenseerd. Congestief hartfalen is waargenomen bij patiënten die labetalol HCl kregen. Labetalol HCl heft de inotrope werking van digitalis op de hartspier niet op.
Bij patiënten zonder een voorgeschiedenis van hartfalen
Bij patiënten met latente hartinsufficiëntie kan aanhoudende depressie van het myocardium met bètablokkers gedurende een bepaalde periode in sommige gevallen leiden tot hartfalen. Bij het eerste teken of symptoom van dreigend hartfalen moeten patiënten volledig worden gedigitaliseerd en/of een diureticum krijgen en moet de respons nauwkeurig worden geobserveerd. Als hartfalen aanhoudt ondanks adequate digitalisering en diuretica, moet de behandeling met Trandate (labetalol) tabletten worden stopgezet (geleidelijk, indien mogelijk).
Exacerbatie van ischemische hartziekte na abrupte ontwenning
Angina pectoris is niet gemeld na stopzetting van labetalol HCl. Er is echter overgevoeligheid voor catecholamines waargenomen bij patiënten die zijn gestopt met de behandeling met bètablokkers; verergering van angina en, in sommige gevallen, myocardinfarct zijn opgetreden na abrupte stopzetting van een dergelijke therapie. Bij stopzetting van chronisch toegediende Trandate (labetalol)-tabletten, vooral bij patiënten met ischemische hartziekte, moet de dosering geleidelijk worden verlaagd over een periode van 1 tot 2 weken en moet de patiënt zorgvuldig worden gecontroleerd. Als angina aanzienlijk verslechtert of als acute coronaire insufficiëntie optreedt, moet de behandeling met Trandate (labetalol) tabletten onmiddellijk worden hervat, in ieder geval tijdelijk, en moeten andere maatregelen worden genomen die geschikt zijn voor de behandeling van onstabiele angina. Patiënten dienen gewaarschuwd te worden tegen onderbreking of stopzetting van de behandeling zonder advies van de arts. Omdat coronaire hartziekte vaak voorkomt en mogelijk niet wordt herkend, kan het verstandig zijn om de behandeling met Trandate (labetalol) tabletten niet abrupt te staken bij patiënten die worden behandeld voor hypertensie.
Niet-allergische bronchospasme (bijv. chronische bronchitis en emfyseem): Patiënten met bronchospastische aandoeningen mogen in het algemeen geen bètablokkers krijgen. Trandate (labetalol) Tabletten kunnen echter met voorzichtigheid worden gebruikt bij patiënten die niet reageren op andere antihypertensiva of deze niet kunnen verdragen. Het is verstandig om bij gebruik van Trandate (labetalol)-tabletten de kleinste effectieve dosis te gebruiken, zodat remming van endogene of exogene bèta-agonisten tot een minimum wordt beperkt.
feochromocytoom
Van Labetalol HCl is aangetoond dat het effectief is bij het verlagen van de bloeddruk en het verlichten van symptomen bij patiënten met feochromocytoom. Bij enkele patiënten met deze tumor zijn echter paradoxale hypertensieve reacties gemeld; wees daarom voorzichtig bij het toedienen van labetalol HCl aan patiënten met feochromocytoom.
Diabetes mellitus en hypoglykemie
Bèta-adrenerge blokkade kan het optreden van tekenen en symptomen (bijv. tachycardie) van acute hypoglykemie voorkomen. Dit is vooral belangrijk bij labiele diabetici. Bètablokkade vermindert ook de afgifte van insuline als reactie op hyperglykemie; het kan daarom nodig zijn om de dosis van antidiabetica aan te passen.
Zware operatie
Stop de behandeling met chronische bètablokkers niet routinematig vóór de operatie. Het effect van de alfa-adrenerge activiteit van labetalol is in deze setting niet geëvalueerd.
Er is een synergie aangetoond tussen labetalol HCl en halothaananesthesie (zie: PREVENTIEVE MAATREGELEN : DRUG-INTERACTIES ).
PREVENTIEVE MAATREGELEN
Algemeen
Verminderde leverfunctie
Trandate (labetalol) Tabletten moeten met voorzichtigheid worden gebruikt bij patiënten met een verminderde leverfunctie, aangezien het metabolisme van het geneesmiddel kan worden verminderd.
Intraoperatief Floppy Iris Syndroom (IFIS) is waargenomen tijdens cataractchirurgie bij sommige patiënten die werden behandeld met alfa-1-blokkers (labetalol is een alfa/bètablokker). Deze variant van het kleine-pupilsyndroom wordt gekenmerkt door de combinatie van een slappe iris die opzwelt als reactie op intraoperatieve irrigatiestromen, progressieve intraoperatieve miosis ondanks preoperatieve dilatatie met standaard mydriatica, en mogelijke verzakking van de iris naar de phaco-emulsificatie-incisies. De oogarts van de patiënt moet voorbereid zijn op mogelijke aanpassingen aan de chirurgische techniek, zoals het gebruik van irishaken, irisdilatatieringen of visco-elastische stoffen. Het lijkt geen voordeel te hebben om te stoppen met de behandeling met alfa-1-blokkers voorafgaand aan een cataractoperatie.
Geelzucht of leverfunctiestoornis
(zien WAARSCHUWINGEN ).
Laboratorium testen
Zoals bij elk nieuw geneesmiddel dat gedurende langere perioden wordt toegediend, moeten laboratoriumparameters met regelmatige tussenpozen worden gecontroleerd. Bij patiënten met bijkomende ziekten, zoals een verminderde nierfunctie, moeten geschikte tests worden uitgevoerd om deze aandoeningen te controleren.
Carcinogenese, mutagenese, verminderde vruchtbaarheid
Langdurige orale doseringsstudies met labetalol HCl gedurende 18 maanden bij muizen en gedurende 2 jaar bij ratten toonden geen bewijs van carcinogenese. Studies met labetalol HCl met behulp van dominante letale testen bij ratten en muizen en het blootstellen van micro-organismen volgens gemodificeerde Ames-tests toonden geen bewijs van mutagenese.
Zwangerschap
Teratogene effecten
Zwangerschap Categorie C: Er zijn teratogene onderzoeken uitgevoerd met labetalol bij ratten en konijnen bij orale doses tot respectievelijk ongeveer zes en vier keer de maximaal aanbevolen dosis voor de mens (MRHD). Er werd geen reproduceerbaar bewijs van foetale misvormingen waargenomen. Verhoogde foetale resorpties werden waargenomen bij beide soorten bij doses die de MRHD benaderden. Een teratologisch onderzoek uitgevoerd met labetalol bij konijnen bij IV-doses tot 1,7 maal de MRHD bracht geen bewijs van geneesmiddelgerelateerde schade aan de foetus aan het licht. Er zijn geen adequate en goed gecontroleerde onderzoeken bij zwangere vrouwen. Labetalol mag alleen tijdens de zwangerschap worden gebruikt als het mogelijke voordeel opweegt tegen het mogelijke risico voor de foetus.
Nietteratogene effecten
Hypotensie, bradycardie, hypoglykemie en ademhalingsdepressie zijn gemeld bij zuigelingen van moeders die tijdens de zwangerschap werden behandeld met labetalol HCl voor hypertensie. Orale toediening van labetalol aan ratten tijdens de late dracht door spenen in doses van twee tot vier keer de MRHD veroorzaakte een afname van de neonatale overleving.
Bevalling
Labetalol HCl dat aan zwangere vrouwen met hypertensie werd gegeven, leek het gebruikelijke verloop van de bevalling en de bevalling niet te beïnvloeden.
Moeders die borstvoeding geven
Kleine hoeveelheden labetalol (ongeveer 0,004% van de maternale dosis) worden uitgescheiden in de moedermelk. Voorzichtigheid is geboden wanneer Trandate (labetalol) tabletten worden toegediend aan een zogende vrouw.
Pediatrisch gebruik
De veiligheid en werkzaamheid bij pediatrische patiënten zijn niet vastgesteld.
Oudere patiënten
Net als bij de algemene populatie hebben sommige oudere patiënten (60 jaar en ouder) tijdens de behandeling met labetalol orthostatische hypotensie, duizeligheid of een licht gevoel in het hoofd gehad. Omdat oudere patiënten over het algemeen meer kans hebben dan jongere patiënten om orthostatische symptomen te ervaren, moeten ze worden gewaarschuwd voor de mogelijkheid van dergelijke bijwerkingen tijdens de behandeling met labetalol.
OVERDOSERING
Overdosering met labetalol HCl veroorzaakt overmatige hypotensie die houdingsgevoelig is en soms overmatige bradycardie. Patiënten moeten in rugligging worden geplaatst en hun benen moeten indien nodig worden geheven om de bloedtoevoer naar de hersenen te verbeteren. Als overdosering met labetalol HCl volgt op orale inname, kan maagspoeling of farmacologisch geïnduceerd braken (met siroop van ipecac) nuttig zijn om het geneesmiddel kort na inname te verwijderen. Indien nodig dienen de volgende aanvullende maatregelen te worden genomen:
Overmatige bradycardie- atropine of epinefrine toedienen.
Hartfalen- een digitalisglycoside en een diureticum toedienen. Dopamine of dobutamine kunnen ook nuttig zijn.
Hypotensie- vasopressoren toedienen, bijv. noradrenaline. Er is farmacologisch bewijs dat noradrenaline mogelijk het favoriete medicijn is.
bronchospasme - epinefrine en/of een vernevelde bèta-2-agonist toedienen.
epileptische aanvallen - diazepam toedienen.
Bij ernstige overdosering van bètablokkers die leidt tot hypotensie en/of bradycardie, is aangetoond dat glucagon effectief is bij toediening in grote doses (5 tot 10 mg snel gedurende 30 seconden, gevolgd door een continue infusie van 5 mg per uur die kan worden verminderd als de patiënt verbetert).
Noch hemodialyse noch peritoneale dialyse verwijdert een significante hoeveelheid labetalol HCl uit de algemene bloedsomloop (
De orale LD50-waarde van labetalol HCl bij de muis is ongeveer 600 mg/kg en bij de rat > 2 g/kg. De IV LD50 bij deze soorten is 50 tot 60 mg/kg.
CONTRA-INDICATIES
Trandate (labetalol) Tabletten zijn gecontra-indiceerd bij bronchiale astma, openlijk hartfalen, meer dan eerstegraads hartblok, cardiogene shock, ernstige bradycardie, andere aandoeningen die gepaard gaan met ernstige en langdurige hypotensie en bij patiënten met een voorgeschiedenis van overgevoeligheid voor onderdeel van het product (zie WAARSCHUWINGEN ).
Bètablokkers, zelfs die met schijnbare cardioselectiviteit, mogen niet worden gebruikt bij patiënten met een voorgeschiedenis van obstructieve luchtwegaandoeningen, waaronder astma.
KLINISCHE FARMACOLOGIE
Labetalol HCl combineert zowel selectieve, competitieve, alfa1-adrenerge blokkerende als niet-selectieve, competitieve, bèta-adrenerge blokkerende activiteit in één enkele stof. Bij de mens zijn de verhoudingen van alfa- tot bètablokkade geschat op ongeveer 1:3 en 1:7 na respectievelijk orale en intraveneuze (IV) toediening. Bèta2-agonistactiviteit is aangetoond bij dieren waarbij minimale bèta1-agonistactiviteit (ISA) is gedetecteerd. Bij dieren is bij doses hoger dan die vereist voor alfa- of bèta-adrenerge blokkade een membraanstabiliserend effect aangetoond.
farmacodynamiek
Het vermogen van labetalol HCl om alfa-receptoren bij de mens te blokkeren, is aangetoond door verzwakking van het pressoreffect van fenylefrine en door een significante vermindering van de pressorrespons veroorzaakt door onderdompeling van de hand in ijskoud water ("koude-pressortest"). De bèta1-receptorblokkade van Labetalol HCl bij de mens werd aangetoond door een kleine afname van de hartslag in rust, verzwakking van tachycardie geproduceerd door isoproterenol of inspanning, en door verzwakking van de reflextachycardie tot de hypotensie veroorzaakt door amylnitriet. Bèta2-receptorblokkade werd aangetoond door remming van de door isoproterenol geïnduceerde daling van de diastolische bloeddruk. Zowel de alfa- als de bètablokkerende werking van oraal toegediende labetalol HCl dragen bij aan een verlaging van de bloeddruk bij hypertensieve patiënten. Labetalol HCl zorgde consequent, op dosisgerelateerde wijze, voor een afgezwakte verhoging van de door inspanning geïnduceerde bloeddruk en hartslag, en in hun dubbele product. De longcirculatie tijdens inspanning werd niet beïnvloed door de dosering van labetalol HCl.
Eenmalige orale doses labetalol HCl toegediend aan patiënten met coronaire hartziekte hadden geen significant effect op de sinusfrequentie, intraventriculaire geleiding of QRS-duur. De atrioventriculaire (AV) geleidingstijd was licht verlengd bij twee van de zeven patiënten. In een ander onderzoek verlengde IV-labetalol HCl de AV-knoopgeleidingstijd en de atriale effectieve refractaire periode enigszins met slechts kleine veranderingen in de hartslag. De effecten op AV-nodale refractairiteit waren inconsistent.
Labetalol HCl veroorzaakt dosisafhankelijke bloeddrukdalingen zonder reflextachycardie en zonder significante verlaging van de hartslag, vermoedelijk door een mengsel van alfa- en bètablokkerende effecten. Hemodynamische effecten zijn variabel, met kleine, niet-significante veranderingen in het hartminuutvolume die in sommige onderzoeken worden gezien, maar niet in andere, en kleine afnames van de totale perifere weerstand. Verhoogde plasmarenines zijn verlaagd.
Doses van labetalol HCl die hypertensie onder controle hielden, hadden geen invloed op de nierfunctie bij patiënten met lichte tot ernstige hypertensie met een normale nierfunctie.
Vanwege de alfa1-receptorblokkerende activiteit van labetalol HCl wordt de bloeddruk meer verlaagd in staande dan in rugligging, en kunnen symptomen van orthostatische hypotensie (2%), waaronder zeldzame gevallen van syncope, optreden. Na orale toediening, wanneer orthostatische hypotensie is opgetreden, is deze van voorbijgaande aard en komt deze soms voor wanneer de aanbevolen startdosering en titratiestappen nauwkeurig worden gevolgd (zie DOSERING EN ADMINISTRATIE ). Symptomatische orthostatische hypotensie treedt het meest waarschijnlijk op 2 tot 4 uur na een dosis, vooral na het gebruik van hoge aanvangsdoses of bij grote dosisveranderingen.
De piekeffecten van enkelvoudige orale doses labetalol HCl treden binnen 2 tot 4 uur op. De duur van het effect hangt af van de dosis en duurt ten minste 8 uur na een enkelvoudige orale dosis van 100 mg en meer dan 12 uur na een enkelvoudige orale dosis van 300 mg. De maximale, steady-state bloeddrukrespons bij orale, tweemaal daagse dosering treedt binnen 24 tot 72 uur op.
Het antihypertensieve effect van labetalol heeft een lineaire correlatie met de logaritme van de labetalol-plasmaconcentratie, en er is ook een lineaire correlatie tussen de afname van door inspanning geïnduceerde tachycardie die optreedt 2 uur na orale toediening van labetalol HCl en de logaritme van de plasmaconcentratie.
Ongeveer 70% van het maximale bètablokkerende effect is aanwezig gedurende 5 uur na toediening van een enkele orale dosis van 400 mg, met de suggestie dat ongeveer 40% na 8 uur blijft.
De anti-angineuze werkzaamheid van labetalol HCl is niet onderzocht. Bij 37 patiënten met hypertensie en coronaire hartziekte verhoogde labetalol HCl de incidentie of ernst van angina-aanvallen niet.
Verergering van angina en, in sommige gevallen, myocardinfarct en ventriculaire ritmestoornissen zijn gemeld na abrupte stopzetting van de behandeling met bèta-adrenerge blokkers bij patiënten met coronaire hartziekte. Abrupt staken van deze middelen bij patiënten zonder coronaire hartziekte heeft geleid tot voorbijgaande symptomen, waaronder trillen, zweten, hartkloppingen, hoofdpijn en malaise. Er zijn verschillende mechanismen voorgesteld om deze verschijnselen te verklaren, waaronder een verhoogde gevoeligheid voor catecholamines vanwege een groter aantal bètareceptoren.
Hoewel bèta-adrenerge receptorblokkade nuttig is bij de behandeling van angina en hypertensie, zijn er ook situaties waarin sympathische stimulatie van vitaal belang is. Bij patiënten met een ernstig beschadigd hart kan een adequate ventriculaire functie bijvoorbeeld afhangen van sympathische aandrijving. Bèta-adrenerge blokkade kan AV-blok verergeren door de noodzakelijke faciliterende effecten van sympathische activiteit op geleiding te voorkomen. Bèta2-adrenerge blokkade resulteert in passieve bronchiale vernauwing door interferentie met endogene adrenerge bronchusverwijdende activiteit bij patiënten die onderhevig zijn aan bronchospasme, en het kan ook interfereren met exogene bronchusverwijders bij dergelijke patiënten.
Farmacokinetiek en metabolisme
Labetalol HCl wordt volledig geabsorbeerd uit het maagdarmkanaal met piekplasmaspiegels die 1 tot 2 uur na orale toediening optreden. De relatieve biologische beschikbaarheid van labetalol HCl-tabletten in vergelijking met een drank is 100%. De absolute biologische beschikbaarheid (fractie van het geneesmiddel dat de systemische circulatie bereikt) van labetalol in vergelijking met een IV-infusie is 25%; dit komt door een uitgebreid "first-pass" metabolisme. Ondanks het 'first-pass'-metabolisme is er een lineair verband tussen orale doses van 100 tot 3.000 mg en piekplasmaspiegels. De absolute biologische beschikbaarheid van labetalol is verhoogd bij toediening met voedsel.
De plasmahalfwaardetijd van labetalol na orale toediening is ongeveer 6 tot 8 uur. Steady-state plasmaspiegels van labetalol tijdens herhaalde dosering worden bereikt op ongeveer de derde dag van dosering. Bij patiënten met een verminderde lever- of nierfunctie verandert de eliminatiehalfwaardetijd van labetalol niet; de relatieve biologische beschikbaarheid bij patiënten met een leverfunctiestoornis is echter verhoogd als gevolg van een verminderd "first-pass"-metabolisme.
Het metabolisme van labetalol vindt voornamelijk plaats via conjugatie met glucuronidemetabolieten. Deze metabolieten zijn aanwezig in plasma en worden uitgescheiden in de urine en via de gal in de feces. Ongeveer 55% tot 60% van een dosis verschijnt binnen de eerste 24 uur na toediening in de urine als conjugaten of onveranderd labetalol.
Van labetalol is aangetoond dat het de placentabarrière passeert bij mensen. In dierstudies passeerden slechts verwaarloosbare hoeveelheden van het geneesmiddel de bloed-hersenbarrière. Labetalol is voor ongeveer 50% aan eiwit gebonden. Noch hemodialyse noch peritoneale dialyse verwijdert een significante hoeveelheid labetalol HCl uit de algemene bloedsomloop (
Oudere patiënten
Sommige farmacokinetische onderzoeken geven aan dat de eliminatie van labetalol bij oudere patiënten verminderd is. Daarom, hoewel oudere patiënten de behandeling kunnen starten met de momenteel aanbevolen dosering van 100 mg tweemaal daags, zullen oudere patiënten over het algemeen lagere onderhoudsdoseringen nodig hebben dan niet-oudere patiënten.
PATIËNT INFORMATIE
Zoals bij alle geneesmiddelen met bètablokkerende activiteit, is bepaald advies aan patiënten die worden behandeld met labetalol HCl gerechtvaardigd. Deze informatie is bedoeld om te helpen bij een veilig en effectief gebruik van dit medicijn. Het is geen onthulling van alle mogelijke nadelige of beoogde effecten. Hoewel er geen incident van het abrupte ontwenningsverschijnsel (exacerbatie van angina pectoris) is gemeld met labetalol HCl, mag de toediening van Trandate (labetalol) tabletten niet worden onderbroken of stopgezet zonder advies van een arts. Patiënten die worden behandeld met Trandate (labetalol) tabletten dienen een arts te raadplegen bij tekenen of symptomen van dreigend hartfalen of leverdisfunctie (zie WAARSCHUWINGEN ). Ook kan een voorbijgaande tinteling van de hoofdhuid optreden, meestal wanneer de behandeling met Trandate 200 mg tabletten wordt gestart (zie: ONGEWENSTE REACTIES ).
