Amoxil 250mg, 500mg, 625mg, 1000mg Amoxicillin Gebruik, bijwerkingen en dosering. Prijs in online apotheek. Generieke medicijnen zonder recept.
Wat is Amoxicilline en hoe wordt het gebruikt?
Wat is Amoxil 1000 mg?
Amoxil is een receptgeneesmiddel dat wordt gebruikt voor de behandeling van de symptomen van veel verschillende soorten bacteriële infecties zoals tonsillitis, bronchitis, longontsteking en infecties van het oor, de neus, de keel, de huid of de urinewegen. Amoxil 1000 mg kan alleen of in combinatie met andere medicijnen worden gebruikt.
Amoxil behoort tot een klasse geneesmiddelen die Penicillines, Amino, wordt genoemd.
Wat zijn de mogelijke bijwerkingen van Amoxil?
Amoxil kan ernstige bijwerkingen veroorzaken, waaronder:
- netelroos,
- moeite met ademhalen,
- zwelling van uw gezicht, lippen, tong of keel,
- koorts,
- keelpijn,
- brandende ogen,
- huid pijn,
- rode of paarse huiduitslag met blaarvorming en vervelling,
- ernstige maagpijn, en
- diarree die waterig of bloederig is (zelfs als het maanden na uw laatste dosis optreedt)
Roep meteen medische hulp in als u een van de bovenstaande symptomen heeft.
De meest voorkomende bijwerkingen van Amoxil zijn:
- misselijkheid,
- braken,
- diarree, en
- uitslag
Vertel het uw arts als u een bijwerking heeft die u hindert of die niet weggaat.
Dit zijn niet alle mogelijke bijwerkingen van Amoxil. Vraag uw arts of apotheker om meer informatie.
Bel uw arts voor medisch advies over bijwerkingen. U kunt bijwerkingen melden aan de FDA op 1-800-FDA-1088.
OMSCHRIJVING
Formuleringen van AMOXIL bevatten amoxicilline, een semisynthetisch antibioticum, een analoog van ampicilline, met een breed spectrum van bactericide activiteit tegen veel Gram-positieve en Gram-negatieve micro-organismen. Chemisch gezien is het (2S,5,R,6,R)-6-[(,R)-(-)-2-amino-2-(p-hydroxyfenyl)acetamido]-3,3-dimethyl-7- oxo-4-thia-1-azabicyclo[3.2.0]heptaan-2-carbonzuurtrihydraat. Het kan structureel worden weergegeven als:
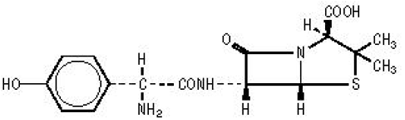
De molecuulformule van amoxicilline is C16H19N3O5S•3H2O en het molecuulgewicht is 419,45.
Capsules : Elke capsule AMOXIL, met koningsblauwe ondoorzichtige dop en roze ondoorzichtige romp, bevat 250 mg of 500 mg amoxicilline als trihydraat. De dop en het lichaam van de capsule van 250 mg zijn bedrukt met de productnaam AMOXIL 1000 mg en 250; de dop en het lichaam van de 500 mg capsule zijn bedrukt met AMOXIL 1000 mg en 500. Inactieve ingrediënten: D&C Red No. 28, FD&C Blue No. 1, FD&C Red No. 40, gelatine, magnesiumstearaat en titaniumdioxide.
Elke tablet bevat 500 mg of 875 mg amoxicilline als trihydraat. Elke filmomhulde, capsulevormige, roze tablet heeft de inscriptie AMOXIL 500 mg, gecentreerd op respectievelijk 500 of 875. De tablet van 875 mg heeft een breukstreep op de achterkant. Inactieve ingrediënten: Colloïdaal siliciumdioxide, crospovidon, FD & C Red No. 30 aluminiumlak, hypromellose, magnesiumstearaat, microkristallijne cellulose, polyethyleenglycol, natriumzetmeelglycolaat en titaniumdioxide.
Poeder voor orale suspensie Elke 5 ml gereconstitueerde suspensie bevat 125 mg, 200 mg, 250 mg of 400 mg amoxicilline als trihydraat. Elke 5 ml van de 125 mg gereconstitueerde suspensie bevat 0,11 mEq (2,51 mg) natrium. Elke 5 ml van de gereconstitueerde suspensie van 200 mg bevat 0,15 mEq (3,39 mg) natrium. Elke 5 ml van de gereconstitueerde suspensie van 250 mg bevat 0,15 mEq (3,36 mg) natrium; elke 5 ml van de gereconstitueerde suspensie van 400 mg bevat 0,19 mEq (4,33 mg) natrium. Inactieve ingrediënten: FD & C Red No. 3, smaakstoffen, silicagel, natriumbenzoaat, natriumcitraat, sucrose en xanthaangom.
INDICATIES
Infecties van oor, neus en keel
AMOXIL® is geïndiceerd voor de behandeling van infecties veroorzaakt door gevoelige (ALLEEN -lactamase-negatieve) isolaten van Streptococcus-soorten. (alleen α- en β-hemolytische isolaten), Streptococcus pneumoniae, Staphylococcus spp. of Haemophilus influenzae.
Infecties van het urogenitale kanaal
AMOXIL® is geïndiceerd voor de behandeling van infecties veroorzaakt door gevoelige (ALLEEN -lactamase-negatieve) isolaten van Escherichia coli, Proteus mirabilis of Enterococcus faecalis.
Infecties van de huid en huidstructuur
AMOXIL® is geïndiceerd voor de behandeling van infecties veroorzaakt door gevoelige (ALLEEN -lactamase-negatieve) isolaten van Streptococcus spp. (alleen α- en β-hemolytische isolaten), Staphylococcus spp. of E. coli.
Infecties van de onderste luchtwegen
AMOXIL® is geïndiceerd voor de behandeling van infecties veroorzaakt door gevoelige (ALLEEN -lactamase-negatieve) isolaten van Streptococcus spp. (alleen α- en β-hemolytische isolaten), S. pneumoniae, Staphylococcus spp. of H. influenzae.
Helicobacter Pylori-infectie
Drievoudige therapie voor Helicobacter Pylori met claritromycine en lansoprazol
AMOXIL, in combinatie met claritromycine plus lansoprazol als drievoudige therapie, is geïndiceerd voor de behandeling van patiënten met H. pylori-infectie en ulcus duodeni (een actieve of 1 jaar durende voorgeschiedenis van een zweer in de twaalfvingerige darm) om H. pylori uit te roeien. Het is aangetoond dat de uitroeiing van H. pylori het risico op herhaling van een ulcus duodeni vermindert.
Duale therapie voor H. Pylori met Lansoprazol
AMOXIL, in combinatie met lansoprazol capsules met vertraagde afgifte als tweevoudige therapie, is geïndiceerd voor de behandeling van patiënten met H. pylori-infectie en ulcus duodeni (actieve of 1 jaar geschiedenis van een ulcus duodeni) die allergisch of intolerant zijn voor claritromycine of bij wie resistentie tegen claritromycine bekend is of wordt vermoed. (Zien de bijsluiter van claritromycine , Microbiologie .) Uitroeiing van H. pylori is aangetoond dat het risico op herhaling van zweren in de twaalfvingerige darm vermindert.
Gebruik
Om de ontwikkeling van resistente bacteriën te verminderen en de effectiviteit van AMOXIL (amoxicilline) en andere antibacteriële geneesmiddelen te behouden, mag AMOXIL 250 mg alleen worden gebruikt voor de behandeling van infecties waarvan is aangetoond of waarvan wordt vermoed dat ze door bacteriën worden veroorzaakt. Wanneer informatie over cultuur en gevoeligheid beschikbaar is, moet hiermee rekening worden gehouden bij het selecteren of wijzigen van antibacteriële therapie. Bij gebrek aan dergelijke gegevens kunnen lokale epidemiologie en gevoeligheidspatronen bijdragen aan de empirische selectie van therapie.
DOSERING EN ADMINISTRATIE
Dosering voor volwassen en pediatrische patiënten > 3 maanden oud
De behandeling moet worden voortgezet gedurende minimaal 48 tot 72 uur nadat de patiënt asymptomatisch is geworden of bewijs van bacteriële uitroeiing is verkregen. Het wordt aanbevolen om elke infectie veroorzaakt door Streptococcus pyogenes ten minste 10 dagen te behandelen om het optreden van acute reumatische koorts te voorkomen. Bij sommige infecties kan therapie gedurende enkele weken nodig zijn. Het kan nodig zijn om de klinische en/of bacteriologische follow-up gedurende enkele maanden na het staken van de therapie voort te zetten.
Dosering bij pasgeborenen en zuigelingen van ≤ 12 weken (≤ 3 maanden)
De behandeling moet worden voortgezet gedurende minimaal 48 tot 72 uur nadat de patiënt asymptomatisch is geworden of bewijs van bacteriële uitroeiing is verkregen. Het wordt aanbevolen om elke infectie veroorzaakt door Streptococcus pyogenes ten minste 10 dagen te behandelen om het optreden van acute reumatische koorts te voorkomen. Vanwege een onvolledig ontwikkelde nierfunctie die de eliminatie van amoxicilline in deze leeftijdsgroep beïnvloedt, is de aanbevolen maximale dosis AMOXIL 30 mg/kg/dag verdeeld over de 12 uur. Er zijn momenteel geen doseringsaanbevelingen voor pediatrische patiënten met een verminderde nierfunctie.
Dosering voor H. Pylori-infectie
Drievoudige therapie
De aanbevolen orale dosis voor volwassenen is 1 gram AMOXIL 1000 mg, 500 mg claritromycine en 30 mg lansoprazol, alle tweemaal daags (elke 12 uur) gedurende 14 dagen.
Dubbele therapie
De aanbevolen orale dosis voor volwassenen is 1 gram AMOXIL 625 mg en 30 mg lansoprazol, elk driemaal daags (elke 8 uur) gedurende 14 dagen. Raadpleeg de volledige voorschrijfinformatie voor claritromycine en lansoprazol.
Dosering bij nierinsufficiëntie
- Bij patiënten met een verminderde nierfunctie is in het algemeen geen dosisverlaging nodig, tenzij de nierfunctiestoornis ernstig is.
- Ernstig gestoorde patiënten met een glomerulaire filtratiesnelheid van
- Patiënten met een glomerulaire filtratiesnelheid van 10 tot 30 ml/min dienen om de 12 uur 500 mg of 250 mg te krijgen, afhankelijk van de ernst van de infectie.
- Patiënten met een glomerulaire filtratiesnelheid van minder dan 10 ml/min dienen elke 24 uur 500 mg of 250 mg te krijgen, afhankelijk van de ernst van de infectie.
- Hemodialysepatiënten moeten elke 24 uur 500 mg of 250 mg krijgen, afhankelijk van de ernst van de infectie. Ze moeten zowel tijdens als aan het einde van de dialyse een extra dosis krijgen.
Aanwijzingen voor het mengen van orale suspensie
Tik op de fles totdat alle poeder vrij kan stromen. Voeg ongeveer 1/3 van de totale hoeveelheid water toe voor reconstitutie (zie tabel 2) en schud krachtig tot het natte poeder. Voeg de rest van het water toe en schud opnieuw krachtig.
Na reconstitutie moet de benodigde hoeveelheid suspensie direct op de tong van het kind worden geplaatst om te worden ingeslikt. Alternatieve toedieningswijzen zijn om de vereiste hoeveelheid suspensie toe te voegen aan flesvoeding, melk, vruchtensap, water, ginger ale of koude dranken. Deze voorbereidingen moeten dan onmiddellijk worden genomen.
OPMERKING: SCHUD DE MONDELINGE SUSPENSIE GOED VOOR GEBRUIK. Houd de fles goed gesloten. Elk ongebruikt deel van de gereconstitueerde suspensie moet na 14 dagen worden weggegooid. Koeling heeft de voorkeur, maar is niet vereist.
HOE GELEVERD
Doseringsvormen en sterke punten
Capsules
250mg, 500mg. Elke capsule AMOXIL 625 mg, met koningsblauwe ondoorzichtige dop en roze ondoorzichtige romp, bevat 250 mg of 500 mg amoxicilline als trihydraat. De dop en het lichaam van de capsule van 250 mg zijn bedrukt met de productnaam AMOXIL en 250; de dop en het lichaam van de 500 mg capsule zijn bedrukt met AMOXIL en 500.
Tabletten
500mg, 875mg. Elke tablet bevat 500 mg of 875 mg amoxicilline als trihydraat. Elke filmomhulde, capsulevormige, roze tablet heeft de inscriptie AMOXIL gecentreerd op respectievelijk 500 of 875. De tablet van 875 mg heeft een breukstreep op de achterkant.
Poeder voor orale suspensie
125 mg/5 ml, 200 mg/5 ml, 250 mg/5 ml, 400 mg/5 ml. Elke 5 ml gereconstitueerde suspensie met aardbeiensmaak bevat 125 mg amoxicilline als trihydraat. Elke 5 ml gereconstitueerde suspensie met kauwgomsmaak bevat 200 mg, 250 mg of 400 mg amoxicilline als trihydraat.
Opslag en behandeling
Capsules: Elke capsule AMOXIL, met koningsblauwe ondoorzichtige dop en roze ondoorzichtige romp, bevat 250 mg of 500 mg amoxicilline als trihydraat. De dop en het lichaam van de capsule van 250 mg zijn bedrukt met de productnaam AMOXIL en 250; de dop en het lichaam van de 500 mg capsule zijn bedrukt met AMOXIL en 500.
250 mg-capsule
NDC 43598-025-01 Flessen van 100 NDC 43598-025-05 Flessen van 500
500 mg-capsule
NDC 43598-005-01 Flessen van 100 NDC 43598-005-05 Flessen van 500
Elke tablet bevat 500 mg of 875 mg amoxicilline als trihydraat. Elke filmomhulde, capsulevormige, roze tablet heeft de inscriptie AMOXIL gecentreerd op respectievelijk 500 of 875. De tablet van 875 mg heeft een breukstreep op de achterkant.
500 mg-tablet
NDC 43598-024-01 Flessen van 100 NDC 43598-024-05 Flessen van 500
875 mg-tablet
NDC 43598-019-01 Flessen van 100 NDC 43598-019-14 Flessen van 20
Poeder voor orale suspensie: Elke 5 ml gereconstitueerde suspensie met aardbeiensmaak bevat 125 mg amoxicilline als trihydraat. Elke 5 ml gereconstitueerde suspensie met kauwgomsmaak bevat 200 mg, 250 mg of 400 mg amoxicilline als trihydraat.
125 mg/5 ml
NDC 43598-022-80 80 ml fles NDC 43598-022-52 Fles van 100 ml NDC 43598-022-53 Fles van 150 ml
200 mg/5 ml
NDC 43598-023-50 Fles van 50 ml NDC 43598-023-51 Fles van 75 ml NDC 43598-023-52 Fles van 100 ml
250 mg/5 ml
NDC 43598-009-80 80 ml fles NDC 43598-009-52 Fles van 100 ml NDC 43598-009-53 Fles van 150 ml
400 mg/5 ml
NDC 43598-007-50 Fles van 50 ml NDC 43598-007-51 Fles van 75 ml NDC 43598-007-52 Fles van 100 ml
Bewaren bij of beneden 20°C (68°F) -250 mg en 500 mg capsules en 125 mg en 250 mg ongereconstitueerd poeder.
Bewaren bij of beneden 25°C (77°F) -500 mg en 875 mg tabletten en 200 mg en 400 mg ongereconstitueerd poeder.
Doseer in een strakke container.
Vervaardigd. Door: Dr. Reddy's Laboratories Tennessee, LLC. Bristol, TN 37620. Herzien: september 2015
BIJWERKINGEN
Het volgende wordt in meer detail besproken in andere secties van de etikettering:
- Anafylactische reacties [zie WAARSCHUWINGEN EN VOORZORGSMAATREGELEN ]
- CDAD [zie WAARSCHUWINGEN EN VOORZORGSMAATREGELEN ]
Ervaring met klinische proeven
Omdat klinische onderzoeken onder sterk uiteenlopende omstandigheden worden uitgevoerd, kunnen de bijwerkingen die in de klinische onderzoeken van een geneesmiddel zijn waargenomen niet direct worden vergeleken met de percentages in de klinische onderzoeken van een ander geneesmiddel en komen mogelijk niet overeen met de percentages die in de praktijk worden waargenomen.
De meest voorkomende bijwerkingen (> 1%) die werden waargenomen in klinische onderzoeken met AMOXIL-capsules, -tabletten of orale suspensie, waren diarree, huiduitslag, braken en misselijkheid.
Drievoudige therapie : De meest gemelde bijwerkingen bij patiënten die drievoudige therapie kregen (amoxicilline/claritromycine/lansoprazol) waren diarree (7%), hoofdpijn (6%) en smaakverstoring (5%).
Dubbele therapie : De meest gemelde bijwerkingen bij patiënten die amoxicilline/lansoprazol dubbel kregen, waren diarree (8%) en hoofdpijn (7%). Raadpleeg voor meer informatie over bijwerkingen van claritromycine of lansoprazol de rubriek Bijwerkingen van hun bijsluiters.
Postmarketing of andere ervaring
Naast bijwerkingen die in klinische onderzoeken zijn gemeld, zijn de volgende bijwerkingen vastgesteld tijdens postmarketinggebruik van penicillines. Omdat ze vrijwillig worden gerapporteerd vanuit een populatie van onbekende omvang, kunnen schattingen van de frequentie niet worden gemaakt. Deze voorvallen zijn gekozen voor opname vanwege een combinatie van hun ernst, frequentie van rapportage of mogelijk causaal verband met AMOXIL.
- Infecties en parasitaire aandoeningen : Mucocutane candidiasis.
- gastro-intestinaal : Zwarte harige tong en hemorragische/pseudomembraneuze colitis. Symptomen van pseudomembraneuze colitis kunnen optreden tijdens of na antibacteriële behandeling [zie: WAARSCHUWINGEN EN VOORZORGSMAATREGELEN ].
- Overgevoeligheidsreacties : Anafylaxie [zie WAARSCHUWINGEN EN VOORZORGSMAATREGELEN ]. Serumziekte-achtige reacties, erythemateuze maculopapulaire huiduitslag, erythema multiforme, Stevens-Johnson-syndroom, exfoliatieve dermatitis, toxische epidermale necrolyse, acute gegeneraliseerde exanthemateuze pustulosis, overgevoeligheidsvasculitis en urticaria zijn gemeld.
- Lever Er is een matige stijging van AST en/of ALT waargenomen, maar de betekenis van deze bevinding is onbekend. Leverfunctiestoornissen waaronder cholestatische geelzucht, levercholestase en acute cytolytische hepatitis zijn gemeld.
- nier : Kristalurie is gemeld [zie OVERDOSERING ].
- Hemische en lymfatische systemen : Anemie, waaronder hemolytische anemie, trombocytopenie, trombocytopenische purpura, eosinofilie, leukopenie en agranulocytose zijn gemeld. Deze reacties zijn gewoonlijk reversibel na stopzetting van de behandeling en er wordt aangenomen dat ze overgevoeligheidsverschijnselen zijn.
- Centraal zenuwstelsel : Reversibele hyperactiviteit, agitatie, angst, slapeloosheid, verwardheid, convulsies, gedragsveranderingen en/of duizeligheid zijn gemeld
- Diversen : Er is melding gemaakt van tandverkleuring (bruine, gele of grijze verkleuring). De meeste meldingen deden zich voor bij pediatrische patiënten. Verkleuring werd in de meeste gevallen verminderd of geëlimineerd door poetsen of gebitsreiniging.
DRUG-INTERACTIES
probenecide
Probenecide vermindert de renale tubulaire secretie van amoxicilline. Gelijktijdig gebruik van amoxicilline en probenecide kan leiden tot verhoogde en verlengde bloedspiegels van amoxicilline.
Orale anticoagulantia
Abnormale verlenging van de protrombinetijd (increased international normalized ratio [INR]) is gemeld bij patiënten die amoxicilline en orale anticoagulantia kregen. Wanneer gelijktijdig anticoagulantia worden voorgeschreven, dient passende controle te worden uitgevoerd. Aanpassingen in de dosis van orale anticoagulantia kunnen nodig zijn om het gewenste niveau van anticoagulatie te handhaven.
Allopurinol
De gelijktijdige toediening van allopurinol en amoxicilline verhoogt de incidentie van huiduitslag bij patiënten die beide geneesmiddelen krijgen in vergelijking met patiënten die alleen amoxicilline krijgen. Het is niet bekend of deze versterking van amoxicilline-uitslag te wijten is aan allopurinol of de hyperurikemie die bij deze patiënten aanwezig is.
Orale anticonceptiva
AMOXIL kan de darmflora beïnvloeden, wat leidt tot een lagere oestrogeenreabsorptie en verminderde werkzaamheid van gecombineerde orale oestrogeen/progesteron-anticonceptiva.

Andere antibacteriële middelen
Chlooramfenicol, macroliden, sulfonamiden en tetracyclines kunnen de bacteriedodende effecten van penicilline verstoren. Dit is in vitro aangetoond; de klinische betekenis van deze interactie is echter niet goed gedocumenteerd.
Effecten op laboratoriumtests
Hoge urineconcentraties van ampicilline kunnen leiden tot vals-positieve reacties bij het testen op de aanwezigheid van glucose in urine met behulp van CLINITEST®, Benedict's Solution of Fehling's Solution. Aangezien dit effect ook kan optreden bij amoxicilline, wordt aanbevolen glucosetests te gebruiken op basis van enzymatische glucose-oxidasereacties (zoals CLINISTIX®).
Na toediening van ampicilline of amoxicilline aan zwangere vrouwen is een voorbijgaande afname van de plasmaconcentratie van totaal geconjugeerd oestriol, oestriolglucuronide, geconjugeerd oestron en estradiol waargenomen.
WAARSCHUWINGEN
Inbegrepen als onderdeel van de PREVENTIEVE MAATREGELEN sectie.
PREVENTIEVE MAATREGELEN
Anafylactische reacties
Ernstige en soms fatale overgevoeligheidsreacties (anafylactische reacties) zijn gemeld bij patiënten die penicillinetherapie kregen, waaronder amoxicilline. Hoewel anafylaxie vaker voorkomt na parenterale therapie, is het voorgekomen bij patiënten die orale penicillines kregen. Deze reacties komen vaker voor bij personen met een voorgeschiedenis van overgevoeligheid voor penicilline en/of een voorgeschiedenis van gevoeligheid voor meerdere allergenen. Er zijn meldingen geweest van personen met een voorgeschiedenis van overgevoeligheid voor penicilline die ernstige reacties hebben gehad bij behandeling met cefalosporines. Alvorens de behandeling met AMOXIL te starten, moet zorgvuldig worden nagegaan of er eerder overgevoeligheidsreacties op penicillines, cefalosporines of andere allergenen zijn opgetreden.
Clostridium Difficile Geassocieerde Diarree
Clostridium difficile-geassocieerde diarree (CDAD) is gemeld bij gebruik van bijna alle antibacteriële middelen, waaronder AMOXIL, en kan in ernst variëren van lichte diarree tot fatale colitis. Behandeling met antibacteriële middelen verandert de normale flora van de dikke darm, wat leidt tot overgroei van C. difficile.
C. difficile produceert de toxinen A en B die bijdragen aan de ontwikkeling van CDAD. Hypertoxine-producerende stammen van C. difficile veroorzaken verhoogde morbiditeit en mortaliteit, aangezien deze infecties ongevoelig kunnen zijn voor antimicrobiële therapie en mogelijk colectomie vereisen. CDAD moet worden overwogen bij alle patiënten die diarree krijgen na antibacterieel gebruik. Een zorgvuldige medische voorgeschiedenis is noodzakelijk, aangezien is gemeld dat CDAD meer dan 2 maanden na toediening van antibacteriële middelen optreedt.
Als CDAD wordt vermoed of bevestigd, moet mogelijk worden gestopt met het gebruik van antibiotica dat niet is gericht tegen C. difficile. Gepast vocht- en elektrolytenbeheer, eiwitsuppletie, antibioticabehandeling van C. difficile en chirurgische evaluatie moeten worden ingesteld zoals klinisch geïndiceerd.
Ontwikkeling van geneesmiddelresistente bacteriën
Het is onwaarschijnlijk dat het voorschrijven van AMOXIL bij afwezigheid van een bewezen of sterk vermoede bacteriële infectie voordelen biedt voor de patiënt en verhoogt het risico op de ontwikkeling van geneesmiddelresistente bacteriën
Gebruik bij patiënten met mononucleosis
Een hoog percentage patiënten met mononucleosis die amoxicilline krijgen, ontwikkelt een erythemateuze huiduitslag. Daarom mag amoxicilline niet worden toegediend aan patiënten met mononucleosis.
Fenylketonurie
Amoxil 250 mg kauwtabletten bevatten aspartaam dat fenylalanine bevat. Elke kauwtablet van 200 mg bevat 1,82 mg fenylalanine; elke kauwtablet van 400 mg bevat 3,64 mg fenylalanine. De orale suspensies van Amoxil bevatten geen fenylalanine en kunnen worden gebruikt door fenylketonurie.
Niet-klinische toxicologie
Carcinogenese, mutagenese, verminderde vruchtbaarheid
Er zijn geen langetermijnstudies bij dieren uitgevoerd om het carcinogene potentieel te evalueren. Er zijn geen onderzoeken uitgevoerd om het mutageen potentieel van alleen amoxicilline te detecteren; de volgende informatie is echter beschikbaar uit tests met een 4:1-mengsel van amoxicilline en kaliumclavulanaat (AUGMENTIN). AUGMENTIN was niet-mutageen in de bacteriële mutatietest van Ames en de gistgenconversietest. AUGMENTIN was zwak positief in de muislymfoomtest, maar de trend naar verhoogde mutatiefrequenties in deze test trad op bij doses die ook geassocieerd waren met verminderde celoverleving. AUGMENTIN was negatief in de micronucleustest bij muizen en in de dominante letale test bij muizen. Kaliumclavulanaat alleen werd getest in de Ames-bacteriële mutatietest en in de micronucleustest bij muizen, en was negatief in elk van deze testen. In een reproductieonderzoek van meerdere generaties bij ratten werden geen verslechtering van de vruchtbaarheid of andere nadelige effecten op de voortplanting waargenomen bij doses tot 500 mg/kg (ongeveer 2 maal de dosis van 3 g voor de mens op basis van het lichaamsoppervlak).
Gebruik bij specifieke populaties
Zwangerschap
Teratogene effecten
Zwangerschap Categorie B. Er zijn reproductieonderzoeken uitgevoerd bij muizen en ratten met doses tot 2000 mg/kg (3 en 6 maal de dosis van 3 g voor de mens, gebaseerd op het lichaamsoppervlak). Er waren geen aanwijzingen voor schade aan de foetus als gevolg van amoxicilline. Er zijn echter geen adequate en goed gecontroleerde onderzoeken bij zwangere vrouwen. Omdat reproductiestudies bij dieren niet altijd voorspellend zijn voor de respons bij de mens, mag amoxicilline alleen tijdens de zwangerschap worden gebruikt als dit duidelijk nodig is.
Bevalling
Orale ampicilline wordt slecht geabsorbeerd tijdens de bevalling. Het is niet bekend of het gebruik van amoxicilline bij de mens tijdens de bevalling of de bevalling onmiddellijke of uitgestelde nadelige effecten heeft op de foetus, de duur van de bevalling verlengt of de kans op de noodzaak van een verloskundige ingreep vergroot.
Moeders die borstvoeding geven
Van penicillines is aangetoond dat ze worden uitgescheiden in de moedermelk. Het gebruik van amoxicilline door moeders die borstvoeding geven, kan leiden tot sensibilisatie bij zuigelingen. Voorzichtigheid is geboden wanneer amoxicilline wordt toegediend aan een zogende vrouw.
Pediatrisch gebruik
Vanwege een onvolledig ontwikkelde nierfunctie bij pasgeborenen en jonge zuigelingen kan de eliminatie van amoxicilline vertraagd zijn. De dosering van AMOXIL 625 mg moet worden aangepast bij pediatrische patiënten van 12 weken of jonger (≤ 3 maanden). [Zien DOSERING EN ADMINISTRATIE ]
Geriatrisch gebruik
Er is een analyse van klinische onderzoeken met AMOXIL 250 mg uitgevoerd om te bepalen of proefpersonen van 65 jaar en ouder anders reageren dan jongere proefpersonen. Deze analyses hebben geen verschillen in respons tussen ouderen en jongere patiënten geïdentificeerd, maar een grotere gevoeligheid van sommige oudere personen kan niet worden uitgesloten.
Van dit geneesmiddel is bekend dat het grotendeels door de nieren wordt uitgescheiden en het risico op toxische reacties op dit geneesmiddel kan groter zijn bij patiënten met een verminderde nierfunctie. Omdat oudere patiënten een grotere kans hebben op een verminderde nierfunctie, moet voorzichtigheid worden betracht bij het kiezen van de dosering en kan het nuttig zijn om de nierfunctie te controleren.
Dosering bij nierinsufficiëntie
Amoxicilline wordt voornamelijk uitgescheiden door de nieren en aanpassing van de dosering is gewoonlijk vereist bij patiënten met een ernstige nierfunctiestoornis (GFR Dosering bij nierinsufficiëntie voor specifieke aanbevelingen bij patiënten met nierinsufficiëntie.
OVERDOSERING
In geval van overdosering, stop met medicatie, behandel symptomatisch en stel zo nodig ondersteunende maatregelen in. Een prospectieve studie bij 51 pediatrische patiënten in een antigifcentrum suggereerde dat overdoseringen van minder dan 250 mg/kg amoxicilline niet gepaard gaan met significante klinische symptomen.
Interstitiële nefritis resulterend in oligurisch nierfalen is gemeld bij een klein aantal patiënten na overdosering met amoxicilline1.
Kristalurie, in sommige gevallen leidend tot nierfalen, is ook gemeld na overdosering met amoxicilline bij volwassen en pediatrische patiënten. In geval van overdosering moeten voldoende vochtinname en diurese worden gehandhaafd om het risico op amoxicillinekristallurie te verminderen.
Nierinsufficiëntie lijkt reversibel te zijn bij stopzetting van de toediening van het geneesmiddel. Hoge bloedspiegels kunnen gemakkelijker optreden bij patiënten met een verminderde nierfunctie vanwege een verminderde renale klaring van amoxicilline. Amoxicilline kan door hemodialyse uit de bloedsomloop worden verwijderd.
CONTRA-INDICATIES
AMOXIL 625 mg is gecontra-indiceerd bij patiënten die een ernstige overgevoeligheidsreactie hebben gehad (bijv. anafylaxie of Stevens-Johnson-syndroom) op AMOXIL of op andere β-lactam-antibiotica (bijv. penicillines en cefalosporines).
KLINISCHE FARMACOLOGIE
Werkingsmechanisme
Amoxicilline is een antibacterieel medicijn. [zien Microbiologie ].
Farmacokinetiek
Absorptie
Amoxicilline is stabiel in aanwezigheid van maagzuur en wordt snel geabsorbeerd na orale toediening. Het effect van voedsel op de absorptie van amoxicilline uit de tabletten en suspensie van AMOXIL is gedeeltelijk onderzocht; De formuleringen van 400 mg en 875 mg zijn alleen onderzocht bij toediening aan het begin van een lichte maaltijd.
Oraal toegediende doses van 250 mg en 500 mg amoxicillinecapsules resulteren in gemiddelde piekbloedspiegels 1 tot 2 uur na toediening in het bereik van respectievelijk 3,5 mcg/ml tot 5,0 mcg/ml en 5,5 mcg/ml tot 7,5 mcg/ml .
De gemiddelde farmacokinetische parameters van amoxicilline uit een open, tweedelige, cross-over bio-equivalentiestudie met een enkelvoudige dosis bij 27 volwassenen, waarbij 875 mg AMOXIL werd vergeleken met 875 mg AUGMENTIN® (kalium amoxicilline/clavulanaat), toonden aan dat de tablet van 875 mg AMOXIL 500 mg een AUC0-∞ van 35,4 ± 8,1 mcg•uur/ml en een Cmax van 13,8 ± 4,1 mcg/ml. De dosering was aan het begin van een lichte maaltijd na een nacht vasten.
Oraal toegediende doses amoxicillinesuspensie, 125 mg/5 ml en 250 mg/5 ml, resulteren in gemiddelde piekbloedspiegels 1 tot 2 uur na toediening in het bereik van 1,5 mcg/ml tot 3,0 mcg/ml en 3,5 mcg/ml tot 5,0 mcg/ml, respectievelijk.
Orale toediening van enkelvoudige doses van 400 mg kauwtabletten en 400 mg/5 ml suspensie van AMOXIL 625 mg aan 24 volwassen vrijwilligers leverde vergelijkbare farmacokinetische gegevens op:
Verdeling
Amoxicilline diffundeert gemakkelijk in de meeste lichaamsweefsels en vloeistoffen, met uitzondering van hersen- en ruggenmergvocht, behalve wanneer de hersenvliezen ontstoken zijn. In bloedserum is amoxicilline voor ongeveer 20% eiwitgebonden. Na een dosis van 1 gram en met behulp van een speciale skin window-techniek om de niveaus van het antibioticum te bepalen, werd opgemerkt dat therapeutische niveaus werden gevonden in de interstitiële vloeistof.
Metabolisme en uitscheiding
De halfwaardetijd van amoxicilline is 61,3 minuten. Ongeveer 60% van een oraal toegediende dosis amoxicilline wordt binnen 6 tot 8 uur in de urine uitgescheiden. Detecteerbare serumspiegels worden waargenomen tot 8 uur na een oraal toegediende dosis amoxicilline. Aangezien het grootste deel van amoxicilline onveranderd in de urine wordt uitgescheiden, kan de uitscheiding worden vertraagd door gelijktijdige toediening van probenecide (zie DRUG-INTERACTIES ].
Microbiologie
Werkingsmechanisme
Amoxicilline is vergelijkbaar met penicilline in zijn bacteriedodende werking tegen gevoelige bacteriën tijdens het stadium van actieve vermenigvuldiging. Het werkt door de remming van de biosynthese van de celwand die leidt tot de dood van de bacteriën.
Mechanisme van weerstand
Resistentie tegen amoxicilline wordt voornamelijk gemedieerd door enzymen, bètalactamasen genaamd, die de bètalactamring van amoxicilline splitsen, waardoor deze inactief wordt.
Van amoxicilline is aangetoond dat het werkzaam is tegen de meeste isolaten van de onderstaande bacteriën, zowel in vitro als bij klinische infecties zoals beschreven in de AANWIJZINGEN EN GEBRUIK sectie.
Gram-positieve bacteriën
Enterococcus faecalis Staphylococcus spp. Streptococcus pneumoniae Streptococcus spp. (alfa- en bèta-hemolytisch)
Gram-negatieve bacteriën
Escherichia coli Haemophilus influenzae Helicobacter pylori Proteus mirabilis
Gevoeligheidstestmethoden
Indien beschikbaar, moet het laboratorium voor klinische microbiologie cumulatieve in vitro gevoeligheidstestresultaten voor antimicrobiële geneesmiddelen die in lokale ziekenhuizen en praktijkgebieden worden gebruikt, aan de arts verstrekken als periodieke rapporten die het gevoeligheidsprofiel van nosocomiale en door de gemeenschap verworven pathogenen beschrijven. Deze rapporten moeten de arts helpen bij het selecteren van de meest effectieve antimicrobiële stof.
Verdunningstechnieken: Kwantitatieve methoden worden gebruikt om antimicrobiële minimale remmende concentraties (MIC's) te bepalen. Deze MIC's geven schattingen van de gevoeligheid van bacteriën voor antimicrobiële verbindingen. De MIC's moeten worden bepaald met behulp van een gestandaardiseerde testmethode -(bouillon of agar)2,4. De MIC-waarden moeten worden geïnterpreteerd volgens de criteria in tabel 4.
Verspreidingstechnieken: Kwantitatieve methoden die het meten van zonediameters vereisen, kunnen ook reproduceerbare schattingen opleveren van de gevoeligheid van bacteriën voor antimicrobiële verbindingen3,4. De zonegrootte moet worden bepaald met behulp van een gestandaardiseerde testmethode3.
Gevoeligheid voor amoxicilline van Enterococcus spp., Enterobacteriaceae en H. influenzae kan worden afgeleid door ampicilline te testen4. Gevoeligheid voor amoxicilline van Staphylococcus spp. en bèta-hemolytische Streptococcus spp. kan worden afgeleid door penicilline te testen4. De meeste isolaten van Enterococcus spp. die resistent zijn tegen ampicilline of amoxicilline, produceren een bètalactamase van het TEM-type. Een bètalactamasetest kan een snelle manier zijn om resistentie tegen ampicilline en amoxicilline vast te stellen4.
Gevoeligheid voor amoxicilline van Streptococcus pneumoniae (niet-meningitis isolaten) kan worden afgeleid door het testen van penicilline of oxacilline4. De interpretatieve criteria voor S. pneumoniae voor amoxicilline worden gegeven in Tabel 44.
Een rapport met de melding "vatbaar" geeft aan dat het antimicrobiële middel de groei van het pathogeen waarschijnlijk zal remmen als de antimicrobiële verbinding een concentratie bereikt op de infectieplaats die nodig is om de groei van het pathogeen te remmen. Een rapport van "Intermediair" geeft aan dat het resultaat als dubbelzinnig moet worden beschouwd en dat, als het micro-organisme niet volledig vatbaar is voor alternatieve, klinisch haalbare geneesmiddelen, de test moet worden herhaald. Deze categorie impliceert mogelijke klinische toepasbaarheid op lichaamsplaatsen waar het medicijn fysiologisch geconcentreerd is. Deze categorie biedt ook een bufferzone die voorkomt dat kleine ongecontroleerde technische factoren grote interpretatieverschillen veroorzaken. Een rapport van "Resistent" geeft aan dat het antimicrobiële middel de groei van de ziekteverwekker waarschijnlijk niet remt als de antimicrobiële verbinding de concentratie bereikt die gewoonlijk op de infectieplaats kan worden bereikt; andere therapie moet worden gekozen.
Gevoeligheidstesten voor Helicobacter Pylori
In-vitro-gevoeligheidstestmethoden voor amoxicilline voor het bepalen van minimale remmende concentraties (MIC's) en zonegroottes zijn niet gestandaardiseerd, gevalideerd of goedgekeurd voor het testen van H. pylori. Monsters voor H. pylori- en claritromycinegevoeligheidstestresultaten moeten worden verkregen op isolaten van patiënten bij wie drievoudige therapie faalt. Als claritromycine-resistentie wordt gevonden, moet een niet-claritromycine-bevattend regime worden gebruikt.
Kwaliteitscontrole
Gestandaardiseerde procedures voor gevoeligheidstests2,3,4 vereisen het gebruik van laboratoriumcontroles om de nauwkeurigheid en precisie van de voorraden en reagentia die in de test worden gebruikt, en de technieken van de personen die de testcontrole uitvoeren, te controleren en te verzekeren. Standaard amoxicillinepoeder moet het volgende bereik van MIC-waarden bieden zoals vermeld in tabel 54. Voor de diffusietechniek moeten de criteria in tabel 5 worden bereikt.
Klinische studies
H. pylori-uitroeiing om het risico op herhaling van duodenumzweren te verminderen
Gerandomiseerde, dubbelblinde klinische onderzoeken uitgevoerd in de Verenigde Staten bij patiënten met H. pylori en ulcus duodeni (gedefinieerd als een actieve zweer of een voorgeschiedenis van een zweer binnen 1 jaar) evalueerden de werkzaamheid van lansoprazol in combinatie met amoxicillinecapsules en claritromycinetabletten als drievoudige 14-daagse therapie, of in combinatie met amoxicilline capsules als tweevoudige 14-daagse therapie, voor de uitroeiing van H. pylori. Op basis van de resultaten van deze onderzoeken werden de veiligheid en werkzaamheid van 2 verschillende eradicatieregimes vastgesteld: Drievoudige therapie: Amoxicilline 1 gram tweemaal daags/claritromycine 500 mg tweemaal daags/lansoprazol 30 mg tweemaal daags (zie Tabel 6). Duale therapie: Amoxicilline 1 gram driemaal daags/lansoprazol 30 mg driemaal daags (zie tabel 7. Alle behandelingen duurden 14 dagen. Uitroeiing van H. pylori werd gedefinieerd als 2 negatieve testen (kweek en histologie) 4 tot 6 weken na de einde van de behandeling Tripletherapie bleek effectiever te zijn dan alle mogelijke duale therapiecombinaties Duale therapie bleek effectiever dan beide monotherapieën Uitroeiing van H. pylori bleek het risico op herhaling van ulcus duodeni te verminderen.
REFERENTIES
1. Swanson-Biearman B, Dean BS, Lopez G, Krenzelok EP. De effecten van inname van penicilline en cefalosporine bij kinderen jonger dan zes jaar. Dierenarts Hum Toxicol. 1988; 30: 66-67.
2. Instituut voor klinische en laboratoriumnormen (CLSI). Methoden voor verdunning Antimicrobiële gevoeligheidstests voor bacteriën die aeroob groeien; Goedgekeurde standaard – tiende editie. CLSI-document M07-A10, Clinical and Laboratory Standards Institute, 950 West Valley Road, Suite 2500, Wayne, Pennsylvania 19087, VS, 2015.
3. Instituut voor klinische en laboratoriumnormen (CLSI). Prestatienormen voor gevoeligheidstests voor antimicrobiële schijfdiffusie; Goedgekeurde standaard - Twaalfde editie. CLSI-document M02-A12, Clinical and Laboratory Standards Institute, 950 West Valley Road, Suite 2500, Wayne, Pennsylvania 19087, VS, 2015.
4. Instituut voor klinische en laboratoriumnormen (CLSI). Prestatienormen voor antimicrobiële gevoeligheidstesten; Vijfentwintigste informatief supplement, CLSI-document M100-S25. CLSI-document M100-S25, Clinical and Laboratory Standards Institute, 950 West Valley Road, Suite 2500, Wayne, Pennsylvania 19087, VS, 2015.
PATIËNT INFORMATIE
- Patiënten moeten erop worden gewezen dat AMOXIL elke 8 uur of elke 12 uur kan worden ingenomen, afhankelijk van de voorgeschreven dosis.
- Patiënten moeten erop worden gewezen dat antibacteriële geneesmiddelen, waaronder AMOXIL, alleen mogen worden gebruikt om bacteriële infecties te behandelen. Ze behandelen geen virale infecties (bijv. verkoudheid). Wanneer AMOXIL 250 mg wordt voorgeschreven om een bacteriële infectie te behandelen, moet de patiënt worden verteld dat hoewel het gebruikelijk is om zich vroeg in de loop van de therapie beter te voelen, de medicatie precies zoals voorgeschreven moet worden ingenomen. Het overslaan van doses of het niet voltooien van de volledige behandelingskuur kan: (1) de effectiviteit van de onmiddellijke behandeling verminderen, en (2) de kans vergroten dat bacteriën resistentie ontwikkelen en in de toekomst niet meer kunnen worden behandeld met AMOXIL 625 mg of andere antibacteriële geneesmiddelen .
- Patiënten moeten erop worden gewezen dat diarree een veelvoorkomend probleem is dat wordt veroorzaakt door antibiotica en dat het meestal stopt wanneer het antibioticum wordt stopgezet. Soms kunnen patiënten na het starten van de behandeling met antibiotica waterige en bloederige ontlasting ontwikkelen (met of zonder maagkrampen en koorts), zelfs pas 2 maanden of langer nadat ze hun laatste dosis van het antibioticum hebben ingenomen. Als dit gebeurt, moeten patiënten zo snel mogelijk contact opnemen met hun arts.
- Patiënten moeten zich ervan bewust zijn dat AMOXIL een geneesmiddel uit de penicillineklasse bevat dat bij sommige personen allergische reacties kan veroorzaken.
