Luvox 100mg, 50mg Fluvoxamine Gebruik, bijwerkingen en dosering. Prijs in online apotheek. Generieke medicijnen zonder recept.
Wat is Luvox (fluvoxaminemaleaat) en hoe wordt het gebruikt?
Luvox 100 mg is een receptgeneesmiddel dat wordt gebruikt om de symptomen van een obsessief-compulsieve stoornis te behandelen. Luvox kan alleen of in combinatie met andere medicijnen worden gebruikt.
Luvox 100 mg behoort tot een klasse geneesmiddelen die antidepressiva, SSRI's, worden genoemd.
Het is niet bekend of Luvox 100 mg veilig en effectief is bij kinderen jonger dan 8 jaar.
Wat zijn de mogelijke bijwerkingen van Luvox?
Luvox kan ernstige bijwerkingen veroorzaken, waaronder:
- ongerustheid,
- race gedachten,
- risicovol gedrag,
- slaapproblemen (slapeloosheid),
- gevoelens van extreem geluk of prikkelbaarheid,
- wazig zien,
- tunnelvisie,
- oogpijn of zwelling,
- halo ronde lichten zien,
- convulsies (toevallen),
- veranderingen in gewicht of eetlust,
- gemakkelijk blauwe plekken of ongewone bloedingen,
- hoofdpijn,
- verwardheid,
- geheugen problemen,
- ernstige zwakte,
- verlies van coördinatie,
- onvast voelen,
- zeer stijve (starre) spieren,
- hoge koorts,
- zweten,
- verwardheid,
- snelle of onregelmatige hartslagen,
- trillingen,
- duizeligheid,
- agitatie,
- hallucinaties,
- zweten,
- rillen
- snelle hartslag,
- spierstijfheid,
- spiertrekkingen,
- misselijkheid,
- braken, en
- diarree
Roep meteen medische hulp in als u een van de bovenstaande symptomen heeft.
De meest voorkomende bijwerkingen van Luvox 50 mg zijn:
- slaperigheid,
- duizeligheid,
- schudden,
- angstig voelen,
- depressieve bui,
- slaapproblemen (slapeloosheid),
- maagklachten,
- gas,
- verlies van eetlust,
- misselijkheid,
- braken,
- diarree,
- droge mond,
- geeuwen,
- keelpijn,
- spierpijn,
- zweten,
- uitslag,
- zware menstruatie,
- verminderde zin in seks,
- abnormale ejaculatie, en
- moeite met een orgasme
Vertel het uw arts als u een bijwerking heeft die u hindert of die niet weggaat.
Dit zijn niet alle mogelijke bijwerkingen van Luvox. Vraag uw arts of apotheker om meer informatie.
Bel uw arts voor medisch advies over bijwerkingen. U kunt bijwerkingen melden aan de FDA op 1-800-FDA-1088.
SUICIDALITEIT EN ANTIDEPRESSANTE DRUGS
Antidepressiva verhoogden het risico op suïcidaal denken en gedrag (suïcidaliteit) bij kinderen, adolescenten en jonge volwassenen in kortdurende onderzoeken naar depressieve stoornis (MDD) en andere psychiatrische stoornissen, vergeleken met placebo. Iedereen die het gebruik van Fluvox 50 mgaminemaleaattabletten of een ander antidepressivum bij een kind, adolescent of jongvolwassene overweegt, moet dit risico afwegen tegen de klinische noodzaak. Kortdurende onderzoeken lieten geen toename zien van het risico op suïcidaliteit bij gebruik van antidepressiva in vergelijking met placebo bij volwassenen ouder dan 24 jaar; er was een vermindering van het risico met antidepressiva vergeleken met placebo bij volwassenen van 65 jaar en ouder. Depressie en bepaalde andere psychiatrische stoornissen zijn zelf geassocieerd met een verhoogd risico op zelfmoord. Patiënten van alle leeftijden die beginnen met een behandeling met antidepressiva, moeten op de juiste manier worden gecontroleerd en nauwlettend worden geobserveerd op klinische verergering, suïcidaliteit of ongewone gedragsveranderingen. Families en zorgverleners moeten worden geïnformeerd over de noodzaak van nauwgezette observatie en communicatie met de voorschrijver. Fluvox 50 mgaminemaleaattabletten zijn niet goedgekeurd voor gebruik bij pediatrische patiënten, behalve voor patiënten met een obsessieve-compulsieve stoornis (OCS). [Zien WAARSCHUWINGEN EN VOORZORGSMAATREGELEN - Klinische verslechtering en zelfmoordrisico ].
OMSCHRIJVING
Fluvoxaminemaleaat is een selectieve serotonine (5-HT) heropnameremmer (SSRI) die behoort tot de chemische reeks, de 2-aminoethyloxime-ethers van aralkylketonen.
Het wordt chemisch aangeduid als 5-methoxy-4'-(trifluormethyl)valerofenon-(E)-O-(2-aminoethyl)oximemaleaat (1:1) en heeft de empirische formule C15H21O2N2F3•C4H4O4. Het molecuulgewicht is 434,41. De structuurformule is:
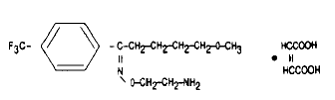
Fluvox 100 mgaminemaleaat is een wit tot gebroken wit, geurloos, kristallijn poeder dat slecht oplosbaar is in water, vrij oplosbaar in ethanol en chloroform en praktisch onoplosbaar in diethylether.
Fluvoxaminemaleaattabletten zijn verkrijgbaar in sterkten van 25 mg, 50 mg en 100 mg voor orale toediening. Naast het werkzame bestanddeel, fluvox 100 mgaminemaleaat, bevat elke tablet de volgende inactieve ingrediënten: carnaubawas, hypromellose, mannitol, polyethyleenglycol, polysorbaat 80, gepregelatineerd zetmeel (aardappel), siliciumdioxide, natriumstearylfumaraat, zetmeel (maïs), en titaandioxide. De tabletten van 50 mg en 100 mg bevatten ook synthetische ijzeroxiden.
INDICATIES
Obsessief-compulsieve stoornis
Fluvoxaminemaleaattabletten zijn geïndiceerd voor de behandeling van obsessies en dwanghandelingen bij patiënten met een obsessieve compulsieve stoornis (OCS), zoals gedefinieerd in DSM-III-R of DSM-IV. De obsessies of dwanghandelingen veroorzaken duidelijk leed, zijn tijdrovend of belemmeren het sociaal of beroepsmatig functioneren aanzienlijk.
Obsessieve-compulsieve stoornis wordt gekenmerkt door terugkerende en aanhoudende ideeën, gedachten, impulsen of beelden (obsessies) die egodystonisch en/of repetitief, doelgericht en opzettelijk gedrag (compulsies) zijn die door de persoon als buitensporig of onredelijk worden herkend.
De werkzaamheid van Fluvox 100 mgaminemaleaattabletten werd vastgesteld in vier onderzoeken bij poliklinische patiënten met OCS: twee onderzoeken van 10 weken bij volwassenen, een onderzoek van 10 weken bij pediatrische patiënten (8-17 jaar) en een onderhoudsonderzoek bij volwassenen [zie Klinische studies ].
DOSERING EN ADMINISTRATIE
volwassenen
De aanbevolen startdosering voor Fluvox 50 mgaminemaleaattabletten bij volwassen patiënten is 50 mg, toegediend als een enkele dagelijkse dosis voor het slapengaan. In de gecontroleerde klinische onderzoeken naar de werkzaamheid van Fluvoxaminemaleaat-tabletten bij OCS, werden patiënten getitreerd binnen een dosisbereik van 100 tot 300 mg/dag. Dientengevolge moet de dosis elke 4 tot 7 dagen worden verhoogd in stappen van 50 mg, voor zover getolereerd, totdat het maximale therapeutische voordeel is bereikt, en mag niet hoger zijn dan 300 mg per dag. Het is raadzaam om een totale dagelijkse dosis van meer dan 100 mg in twee verdeelde doses te geven. Als de doses niet gelijk zijn, moet de grotere dosis voor het slapengaan worden gegeven.
Pediatrische populatie (kinderen en adolescenten)
De aanbevolen startdosering voor Fluvoxaminemaleaat tabletten bij pediatrische populaties (leeftijd 8-17 jaar) is 25 mg, toegediend als een enkele dagelijkse dosis voor het slapengaan. In een gecontroleerd klinisch onderzoek dat de werkzaamheid van Fluvoxaminemaleaat-tabletten bij OCS vaststelde, werden pediatrische patiënten (8-17 jaar) getitreerd binnen een dosisbereik van 50 tot 200 mg/dag. Artsen dienen bij het doseren van pediatrische patiënten rekening te houden met leeftijds- en geslachtsverschillen. De maximale dosis bij kinderen tot 11 jaar mag niet hoger zijn dan 200 mg/dag. Therapeutisch effect bij vrouwelijke kinderen kan worden bereikt met lagere doses. Dosisaanpassing bij adolescenten (tot de maximale dosis voor volwassenen van 300 mg) kan geïndiceerd zijn om therapeutisch voordeel te bereiken. De dosis moet elke 4 tot 7 dagen worden verhoogd in stappen van 25 mg, voor zover getolereerd, totdat het maximale therapeutische voordeel is bereikt. Het is raadzaam om een totale dagelijkse dosis van meer dan 50 mg in twee verdeelde doses te geven. Als de twee verdeelde doses niet gelijk zijn, moet de grotere dosis voor het slapengaan worden gegeven.
Oudere of leverfunctiestoornissen
Bij oudere patiënten en patiënten met een leverfunctiestoornis is een verminderde klaring van fluvoxaminemaleaat waargenomen. Daarom kan het passend zijn om de aanvangsdosis en de daaropvolgende dosistitratie voor deze patiëntengroepen aan te passen.
Overschakelen van een patiënt naar of van een monoamineoxidaseremmer (MAOI) bedoeld voor de behandeling van psychiatrische stoornissen
Er moeten ten minste 14 dagen verstrijken tussen het stopzetten van een MAO-remmer bedoeld voor de behandeling van psychiatrische stoornissen en het starten van de behandeling met Fluvox 50 mgaminemaleaattabletten. Omgekeerd moet er ten minste 14 dagen worden gewacht na het stoppen met Fluvox 100 mgaminemaleaattabletten voordat wordt gestart met een MAO-remmer die bedoeld is voor de behandeling van psychiatrische stoornissen [zie CONTRA-INDICATIES ].
Gebruik van fluvoxaminemaleaattabletten met andere MAO-remmers zoals linezolid of methyleenblauw
Start Fluvoxaminemaleaat Mylan niet bij een patiënt die wordt behandeld met linezolid of intraveneus methyleenblauw, omdat er een verhoogd risico is op het serotoninesyndroom. Bij een patiënt die een meer dringende behandeling van een psychiatrische aandoening nodig heeft, moeten andere interventies, waaronder ziekenhuisopname, worden overwogen [zie CONTRA-INDICATIES ].
In sommige gevallen kan een patiënt die al wordt behandeld met Fluvox 50 mgaminemaleaattabletten dringend worden behandeld met linezolid of intraveneus methyleenblauw. Als er geen aanvaardbare alternatieven voor linezolid of intraveneuze behandeling met methyleenblauw beschikbaar zijn en de mogelijke voordelen van linezolid of intraveneuze behandeling met methyleenblauw opwegen tegen de risico's van het serotoninesyndroom bij een bepaalde patiënt, moet Fluvoxaminemaleaat Mylan onmiddellijk worden stopgezet en linezolid of intraveneuze methyleenblauw kan worden toegediend. De patiënt moet gedurende twee weken of tot 24 uur na de laatste dosis linezolid of intraveneus methyleenblauw, afhankelijk van wat zich het eerst voordoet, worden gecontroleerd op symptomen van het serotoninesyndroom. Therapie met Fluvox 100 mgaminemaleaattabletten kan 24 uur na de laatste dosis linezolid of intraveneus methyleenblauw worden hervat [zie WAARSCHUWINGEN EN VOORZORGSMAATREGELEN ].
Het risico van toediening van methyleenblauw via niet-intraveneuze routes (zoals orale tabletten of door lokale injectie) of in intraveneuze doses die veel lager zijn dan 1 mg/kg met Fluvox 100 mgaminemaleaattabletten is onduidelijk. De arts moet zich niettemin bewust zijn van de mogelijkheid van optredende symptomen van het serotoninesyndroom bij dergelijk gebruik [zie: WAARSCHUWINGEN EN VOORZORGSMAATREGELEN ].
Onderhoud/voortzetting Verlengde behandeling
Men is het er algemeen over eens dat een obsessieve-compulsieve stoornis enkele maanden of langer aanhoudende farmacologische therapie vereist. Het voordeel van het handhaven van patiënten met OCS op Fluvoxaminemaleaat-tabletten na het bereiken van een respons gedurende een gemiddelde duur van ongeveer 4 weken in een enkelblinde fase van 10 weken waarin patiënten werden getitreerd om effect te sorteren, werd aangetoond in een gecontroleerd onderzoek [zie Klinische proeven ].
De arts die ervoor kiest om Fluvoxaminemaleaat-tabletten gedurende langere perioden te gebruiken, moet periodiek de bruikbaarheid van het geneesmiddel op de lange termijn voor de individuele patiënt opnieuw evalueren.
Stopzetting van de behandeling met fluvoxaminemaleaattabletten
Symptomen geassocieerd met stopzetting van andere SSRI's of SNRI's zijn gemeld [zie: WAARSCHUWINGEN EN VOORZORGSMAATREGELEN ]. Patiënten moeten op deze symptomen worden gecontroleerd wanneer de behandeling wordt stopgezet. Waar mogelijk wordt een geleidelijke verlaging van de dosis aanbevolen in plaats van abrupt stoppen. Als ondraaglijke symptomen optreden na een verlaging van de dosis of na stopzetting van de behandeling, kan worden overwogen om de eerder voorgeschreven dosis te hervatten. Vervolgens kan de arts doorgaan met het verlagen van de dosis, maar in een meer geleidelijk tempo.
HOE GELEVERD
Doseringsvormen en sterke punten
Fluvoxamine Maleate Tabletten USP zijn verkrijgbaar als:
Tabletten 25 mg: niet-gescoord, wit, elliptisch, filmomhuld (met aan één kant de inscriptie "1222")
Tabletten 50 mg: geel, elliptisch, filmomhuld met breukgleuf (met de inscriptie "1225" aan de ene kant en met breukstreep aan de andere kant)
Tabletten 100 mg: breukstreep, beige, elliptisch, filmomhuld (met de inscriptie “1221” aan de ene kant en breukstreep aan de andere kant)
Opslag en behandeling
Fluvox 50 mgamine Maleaat-tabletten USP zijn verkrijgbaar in de volgende sterktes, kleuren, opdrukken en presentaties:
niet gescoord, wit, elliptisch, filmomhuld (ingeslagen "1222" aan één kant)
Flessen van 100 ............. NDC 62559-158-01
breukstreep, geel, elliptisch, filmomhuld (ingeslagen "1225" aan de ene kant en breuklijn aan de andere)
Flessen van 100 ............. NDC 62559-159-01
gekerfd, beige, elliptisch, filmomhuld (ingeslagen "1221" aan de ene kant en gekerfd aan de andere kant)
Flessen van 100 ............. NDC 62559-160-01
Buiten bereik van kinderen houden.
Fluvoxaminemaleaattabletten moeten worden beschermd tegen hoge vochtigheid en bewaard bij 20° tot 25°C (68° tot 77°F); excursies toegestaan tot 15° tot 30°C (59° tot 86°F) [zie USP-gecontroleerde kamertemperatuur ].
Doseer in strakke containers.
Gefabriceerd door: ANI Pharmaceuticals, Inc., Baudette, MN 56623. Herzien: juli 2021
BIJWERKINGEN
Omdat klinische onderzoeken onder sterk uiteenlopende omstandigheden worden uitgevoerd, kunnen de bijwerkingen die in de klinische onderzoeken van een geneesmiddel zijn waargenomen niet direct worden vergeleken met de percentages in de klinische onderzoeken van een ander geneesmiddel en komen mogelijk niet overeen met de percentages die in de praktijk worden waargenomen.
Bijwerkingen die leiden tot stopzetting van de behandeling
Van de 1087 patiënten met ocs en depressieve patiënten die werden behandeld met fluvoxaminemaleaat in gecontroleerde klinische onderzoeken in Noord-Amerika, stopte 22% vanwege een bijwerking. Bijwerkingen die leidden tot stopzetting bij ten minste 2% van de met fluvoxaminemaleaat behandelde patiënten in deze onderzoeken waren: misselijkheid (9%), slapeloosheid (4%), slaperigheid (4%), hoofdpijn (3%) en asthenie, braken nervositeit, opwinding en duizeligheid (elk 2%).
Incidentie in gecontroleerde onderzoeken
Vaak waargenomen bijwerkingen in gecontroleerde klinische onderzoeken
Fluvox 100 mgaminemaleaattabletten zijn onderzocht in 10 weken durende gecontroleerde kortetermijnonderzoeken naar OCS (N=320) en depressie (N=1350). Over het algemeen waren de bijwerkingenpercentages vergelijkbaar in de twee datasets en in het pediatrische OCS-onderzoek. De vaakst waargenomen bijwerkingen die verband houden met het gebruik van Fluvoxaminemaleaat-tabletten en die waarschijnlijk verband houden met het geneesmiddel (incidentie van 5% of meer en ten minste tweemaal die voor placebo), afgeleid van tabel 2 waren: misselijkheid, slaperigheid, slapeloosheid, asthenie, nervositeit, dyspepsie, abnormale ejaculatie, zweten, anorexia, tremor en braken. In een pool van twee onderzoeken waarbij alleen patiënten met OCS betrokken waren, werden de volgende aanvullende reacties geïdentificeerd met behulp van de bovenstaande regel: anorgasmie, verminderd libido, droge mond, rhinitis, smaakverstoring en urinaire frequentie. In een onderzoek bij pediatrische patiënten met OCS werden de volgende aanvullende reacties geïdentificeerd met behulp van de bovenstaande regel: agitatie, depressie, dysmenorroe, winderigheid, hyperkinesie en huiduitslag.
Bijwerkingen die optreden bij een incidentie van 1%
Tabel 2 geeft een overzicht van de bijwerkingen die bij volwassenen voorkwamen met een frequentie van 1% of meer, en die vaker voorkwamen dan in de placebogroep, bij patiënten die werden behandeld met Fluvoxaminemaleaattabletten in twee kortdurende placebogecontroleerde OCS-onderzoeken (10 weken) en depressie onderzoeken (6 weken) waarin patiënten werden gedoseerd in een spreiding van in het algemeen 100 tot 300 mg/dag. Deze tabel toont het percentage patiënten in elke groep dat op enig moment tijdens hun behandeling minstens één keer een reactie had. Gemelde bijwerkingen werden geclassificeerd met behulp van een standaard op COSTART gebaseerde Dictionary-terminologie.
De voorschrijver dient zich ervan bewust te zijn dat deze cijfers niet kunnen worden gebruikt om de incidentie van bijwerkingen in de loop van de normale medische praktijk te voorspellen, waarbij de kenmerken van de patiënt en andere factoren kunnen verschillen van die in de klinische onderzoeken. Evenzo kunnen de genoemde frequenties niet worden vergeleken met cijfers die zijn verkregen uit andere klinische onderzoeken met verschillende behandelingen, toepassingen en onderzoekers. De aangehaalde cijfers bieden de voorschrijvende arts echter enige basis voor het schatten van de relatieve bijdrage van medicamenteuze en niet-medicamenteuze factoren aan de incidentie van bijwerkingen in de bestudeerde populatie.
TABEL 2: BIJ BEHANDELING OPKOMENDE ONGEWENSTE REACTIE-INCIDENTIEPERCENTEN PER LICHAAMSSYSTEEM BIJ VOLWASSEN OCS- EN DEPRESSIEPOPULATIES GECOMBINEERD1
Bijwerkingen in OCS Placebo-gecontroleerde onderzoeken die duidelijk verschillen (gedefinieerd als ten minste een tweevoudig verschil) in frequentie van de gepoolde reactiepercentages bij OCS en depressie Placebo-gecontroleerde onderzoeken
De reacties in OCS-onderzoeken met een tweevoudige afname in snelheid vergeleken met reactiesnelheden in OCS- en depressieonderzoeken waren dysfagie en amblyopie (meestal wazig zien). Bovendien was er een afname van ongeveer 25% in misselijkheid.
De reacties in OCS-onderzoeken met een tweevoudige toename in snelheid vergeleken met reactiepercentages in OCS- en depressieonderzoeken waren: asthenie, abnormale ejaculatie (meestal vertraagde ejaculatie), angst, rhinitis, anorgasmie (bij mannen), depressie, verminderd libido, faryngitis agitatie, impotentie, myoclonus/twitch, dorst, gewichtsverlies, krampen in de benen, spierpijn en urineretentie. Deze reacties worden vermeld in volgorde van afnemende snelheid in de OCS-onderzoeken.
Andere bijwerkingen bij pediatrische OCS-populaties
Bij pediatrische patiënten (N=57) die werden behandeld met Fluvox 100 mgaminemaleaattabletten, was het algemene profiel van bijwerkingen over het algemeen vergelijkbaar met dat waargenomen in onderzoeken bij volwassenen, zoals weergegeven in tabel 2. De volgende bijwerkingen, die echter niet in tabel 2 voorkomen, werden gemeld bij twee of meer van de pediatrische patiënten en kwamen vaker voor met Fluvoxaminemaleaat-tabletten dan met placebo: toename van hoest, dysmenorroe, ecchymose, emotionele labiliteit, epistaxis, hyperkinesie, manische reactie, huiduitslag, sinusitis en gewichtsafname.
Mannelijke en vrouwelijke seksuele disfunctie met SSRI's
Hoewel veranderingen in seksueel verlangen, seksuele prestaties en seksuele bevrediging vaak optreden als manifestaties van een psychiatrische stoornis en met het ouder worden, kunnen ze ook een gevolg zijn van farmacologische behandeling. Er zijn met name aanwijzingen dat selectieve serotonineheropnameremmers (SSRI's) dergelijke ongewenste seksuele ervaringen kunnen veroorzaken.
Betrouwbare schattingen van de incidentie en ernst van ongewenste ervaringen met seksuele begeerte, prestatie en bevrediging zijn echter moeilijk te verkrijgen, deels omdat patiënten en artsen misschien terughoudend zijn om ze te bespreken. Dienovereenkomstig onderschatten schattingen van de incidentie van ongewenste seksuele ervaringen en prestaties die in de productetikettering worden vermeld, hun werkelijke incidentie.
Tabel 3 geeft de incidentie weer van seksuele bijwerkingen die zijn gemeld door ten minste 2% van de patiënten die Fluvox 100 mgaminemaleaattabletten gebruikten in placebogecontroleerde onderzoeken bij depressie en OCS.
TABEL 3: PERCENTAGE PATINTEN MELDING VAN SEKSUELE BIJWERKINGEN IN PLACEBO-GECONTROLEERDE PROEVEN VOOR VOLWASSENEN BIJ OCS EN DEPRESSIE
Er zijn geen adequate en goed gecontroleerde onderzoeken naar seksuele disfunctie bij behandeling met fluvoxamine.
Behandeling met Fluvox 50 mgamine is in verband gebracht met verschillende gevallen van priapisme. In die gevallen met een bekend resultaat herstelden de patiënten zonder gevolgen en na stopzetting van fluvox 50 mgamine.
Hoewel het moeilijk is om het precieze risico van seksuele disfunctie in verband met het gebruik van SSRI's te kennen, moeten artsen routinematig informeren naar dergelijke mogelijke bijwerkingen.
Veranderingen in vitale functies
Vergelijkingen van fluvoxaminemaleaat- en placebogroepen in afzonderlijke pools van kortdurende OCS- en depressieonderzoeken op (1) mediane verandering vanaf baseline op verschillende variabelen van vitale functies en op (2) incidentie van patiënten die voldoen aan criteria voor mogelijk belangrijke veranderingen ten opzichte van baseline op verschillende vitale tekenvariabelen lieten geen belangrijke verschillen zien tussen fluvoxaminemaleaat en placebo.
Laboratoriumveranderingen
Vergelijkingen van fluvoxaminemaleaat- en placebogroepen in afzonderlijke pools van kortdurende OCS- en depressieonderzoeken op (1) mediane verandering ten opzichte van baseline op verschillende serumchemie-, hematologie- en urineanalysevariabelen en op (2) incidentie van patiënten die voldoen aan criteria voor mogelijk belangrijke veranderingen vanaf baseline op verschillende serumchemie-, hematologie- en urineanalysevariabelen lieten geen belangrijke verschillen zien tussen fluvox 100 mgaminemaleaat en placebo.
ECG-wijzigingen
Vergelijkingen van fluvox 50 mgaminemaleaat- en placebogroepen in afzonderlijke pools van kortdurende OCS- en depressieonderzoeken op (1) gemiddelde verandering ten opzichte van baseline op verschillende ECG-variabelen en op (2) incidentie van patiënten die voldoen aan criteria voor mogelijk belangrijke veranderingen ten opzichte van baseline op verschillende ECG's variabelen lieten geen belangrijke verschillen zien tussen fluvoxaminemaleaat en placebo.
Andere reacties waargenomen tijdens de premarketingbeoordeling van Fluvox 100 mgaminemaleaattabletten
Tijdens klinische premarketingonderzoeken uitgevoerd in Noord-Amerika en Europa, werden meerdere doses fluvoxaminemaleaat toegediend voor een gecombineerd totaal van 2737 patiëntenblootstellingen bij patiënten met OCS of depressieve stoornis. Ongewenste reacties in verband met deze blootstelling werden geregistreerd door klinische onderzoekers met behulp van beschrijvende terminologie naar eigen keuze. Bijgevolg is het niet mogelijk om een zinvolle schatting te geven van het aantal personen dat bijwerkingen ervaart zonder eerst gelijkaardige soorten ongewenste reacties te groeperen in een beperkt (dwz verminderd) aantal standaardreactiecategorieën.
In de volgende tabellen is een standaard op COSTART gebaseerde Dictionary-terminologie gebruikt om gerapporteerde bijwerkingen te classificeren. Als de COSTART-term voor een reactie zo algemeen was dat deze niet informatief was, werd deze vervangen door een meer informatieve term. De gepresenteerde frequenties vertegenwoordigen daarom het aandeel van de 2737 patiënten die zijn blootgesteld aan meerdere doses fluvox 100 mgaminemaleaat die ten minste één keer een reactie van het genoemde type hebben ervaren terwijl ze fluvoxaminemaleaat kregen. Alle gemelde reacties zijn opgenomen in de onderstaande lijst, met de volgende uitzonderingen: 1) de reacties die al zijn vermeld in tabel 2, waarin de incidentiepercentages van veelvoorkomende bijwerkingen in placebogecontroleerde klinische onderzoeken naar OCS en depressie worden weergegeven, zijn uitgesloten; 2) die reacties waarvoor een geneesmiddeloorzaak niet waarschijnlijk werd geacht, worden weggelaten; 3) reacties waarvoor de COSTART-term te vaag was om klinisch zinvol te zijn en niet kon worden vervangen door een meer informatieve term; en 4) reacties die bij slechts één patiënt werden gemeld en als niet potentieel ernstig werden beschouwd, zijn niet opgenomen. Het is belangrijk te benadrukken dat, hoewel de gemelde reacties tijdens de behandeling met fluvoxaminemaleaat optraden, er geen causaal verband met fluvoxaminemaleaat is vastgesteld.
Reacties worden verder ingedeeld in lichaamssysteemcategorieën en opgesomd in volgorde van afnemende frequentie met behulp van de volgende definities: frequente bijwerkingen worden gedefinieerd als bijwerkingen die bij een of meer gevallen optreden bij ten minste 1/100 patiënten; zeldzame bijwerkingen zijn bijwerkingen die optreden bij 1/100 en 1/1000 patiënten; en zeldzame bijwerkingen komen voor bij minder dan 1/1000 patiënten.
Lichaam als geheel - Frequent: malaise; Onregelmatig: fotosensitiviteitsreactie en zelfmoordpoging.
Cardiovasculair systeem - Vaak: syncope.
Spijsverteringsstelsel - Onregelmatig: gastro-intestinale bloeding en melena; Zelden: hematemesis.
Hemische en lymfatische systemen - Onregelmatig: bloedarmoede en ecchymose; Zelden: purpura.
Metabole en voedingssystemen - Frequent: gewichtstoename en gewichtsverlies.
Zenuwstelsel - Frequent: hyperkinesie, manische reactie en myoclonus; Onregelmatig: abnormale dromen, acathisie, convulsie, dyskinesie, dystonie, euforie, extrapiramidaal syndroom en spiertrekkingen; Zelden: ontwenningssyndroom.
Ademhalingssysteem - Onregelmatig: epistaxis. Zelden: bloedspuwing en laryngisme.
Huid - Zelden: urticaria.
Urogenitaal systeem* - Onregelmatig: hematurie, menorragie en vaginale bloeding; Zelden: hematospermie.
* Op basis van het aantal mannen of vrouwen, naargelang het geval.
Postmarketingrapporten
De volgende bijwerkingen zijn vastgesteld tijdens het gebruik van Fluvox 100 mgaminemaleaattabletten na goedkeuring. Omdat deze reacties vrijwillig worden gemeld door een populatie van onbekende grootte, is het niet altijd mogelijk om op betrouwbare wijze hun frequentie te schatten of een oorzakelijk verband met blootstelling aan geneesmiddelen vast te stellen.
Vrijwillige meldingen van bijwerkingen bij patiënten die Fluvox 50 mgaminemaleaattabletten gebruiken en die sinds de introductie op de markt zijn ontvangen en waarvan het oorzakelijk verband met het gebruik van Fluvoxaminemaleaattabletten onbekend is, zijn onder meer: acuut nierfalen, agranulocytose, amenorroe, anafylactische reactie, angio-oedeem, aplastische anemie, bulleuze eruptie , Henoch-Schoenlein purpura, hepatitis, ileus, pancreatitis, porfyrie, Stevens-Johnson-syndroom, toxische epidermale necrolyse, vasculitis en ventriculaire tachycardie (inclusief torsades de pointes).
DRUG-INTERACTIES
Mogelijke interacties met geneesmiddelen die remmen of worden gemetaboliseerd door cytochroom P450-iso-enzymen
Meerdere hepatische cytochroom P450-iso-enzymen zijn betrokken bij de oxidatieve biotransformatie van een groot aantal structureel verschillende geneesmiddelen en endogene verbindingen. De beschikbare kennis over de relatie tussen fluvoxamine en het cytochroom P450 iso-enzymsysteem is voornamelijk verkregen uit farmacokinetische interactiestudies die zijn uitgevoerd bij gezonde vrijwilligers, maar er zijn ook enkele voorlopige in vitro gegevens beschikbaar. Gebaseerd op een bevinding van substantiële interacties van fluvox 50 mgamine met bepaalde van deze geneesmiddelen [zie de latere delen van deze rubriek en ook WAARSCHUWINGEN EN VOORZORGSMAATREGELEN ] en beperkte in vitro gegevens voor CYP3A4, blijkt dat fluvox 100 mgamine verschillende cytochroom P450 iso-enzymen remt waarvan bekend is dat ze betrokken zijn bij het metabolisme van andere geneesmiddelen, zoals: CYP1A2 (bijv. warfarine, theofylline, propranolol, tizanidine), CYP2C9 (bijv. , warfarine), CYP3A4 (bijv. alprazolam) en CYP2C19 (bijv. omeprazol).
In vitro gegevens suggereren dat fluvoxamine een relatief zwakke remmer van CYP2D6 is.
Ongeveer 7% van de normale populatie heeft een genetische code die leidt tot verminderde activiteit van CYP2D6. Dergelijke personen zijn aangeduid als "slechte metaboliseerders" (PM) van geneesmiddelen zoals puinoquin, dextromethorfan en tricyclische antidepressiva. Hoewel geen van de geneesmiddelen die zijn onderzocht op geneesmiddelinteracties een significante invloed hadden op de farmacokinetiek van fluvox 50 mgamine, toonde een in vivo onderzoek naar de farmacokinetiek van een enkelvoudige dosis fluvoxamine bij 13 PM-patiënten veranderde farmacokinetische eigenschappen in vergelijking met 16 "extensieve metaboliseerders" (EM): gemiddelde Cmax, AUC , en de halfwaardetijd waren met respectievelijk 52%, 200% en 62% verhoogd in de PM in vergelijking met de EM-groep. Dit suggereert dat fluvox 100 mgamine, althans gedeeltelijk, wordt gemetaboliseerd door CYP2D6. Voorzichtigheid is geboden bij patiënten waarvan bekend is dat ze verminderde niveaus van CYP2D6-activiteit hebben en bij patiënten die gelijktijdig geneesmiddelen krijgen waarvan bekend is dat ze dit cytochroom P450-iso-enzym remmen (bijv. kinidine).
Het metabolisme van fluvoxamine is niet volledig gekarakteriseerd en de effecten van krachtige cytochroom P450 iso-enzymremming, zoals de ketoconazolremming van CYP3A4, op het metabolisme van fluvox 100 mgamine zijn niet onderzocht.
Een klinisch significante fluvoxamine-interactie is mogelijk met geneesmiddelen met een nauwe therapeutische verhouding zoals pimozide, warfarine, theofylline, bepaalde benzodiazepinen, omeprazol en fenytoïne. Als Fluvox 100 mgaminemaleaattabletten samen moeten worden toegediend met een geneesmiddel dat wordt geëlimineerd via oxidatief metabolisme en een smal therapeutisch venster heeft, moeten de plasmaspiegels en/of farmacodynamische effecten van het laatstgenoemde geneesmiddel nauwlettend worden gecontroleerd, ten minste totdat steady-state-omstandigheden zijn bereikt. bereikt [zie CONTRA-INDICATIES , WAARSCHUWINGEN EN VOORZORGSMAATREGELEN ].
CZS-actieve geneesmiddelen
Antipsychotica: Zien WAARSCHUWINGEN EN VOORZORGSMAATREGELEN .
Benzodiazepinen: Zien WAARSCHUWINGEN EN VOORZORGSMAATREGELEN .
Alprazolam: Zien WAARSCHUWINGEN EN VOORZORGSMAATREGELEN .
diazepam: Zien WAARSCHUWINGEN EN VOORZORGSMAATREGELEN .
Lorazepam: Een onderzoek met meerdere doses fluvoxaminemaleaat (50 mg tweemaal daags) bij gezonde mannelijke vrijwilligers (N=12) en een enkele dosis lorazepam (4 mg enkele dosis) gaf geen significante farmacokinetische interactie aan. Gemiddeld veroorzaakten zowel lorazepam alleen als lorazepam met fluvoxamine een aanzienlijke afname van het cognitief functioneren; de gelijktijdige toediening van fluvoxamine en lorazepam leidde echter niet tot grotere gemiddelde verlagingen in vergelijking met alleen lorazepam.
Alcohol: Studies met enkelvoudige doses van 40 g ethanol (orale toediening in de ene studie en intraveneuze toediening in de andere) en meervoudige doseringen met fluvox 100 mgaminemaleaat (50 mg tweemaal daags) lieten geen effect zien van een van beide geneesmiddelen op de farmacokinetiek of farmacodynamiek van de andere. Net als bij andere psychotrope geneesmiddelen, moeten patiënten worden geadviseerd geen alcohol te gebruiken tijdens het gebruik van Fluvoxaminemaleaat.
Carbamazepine: Verhoogde carbamazepinespiegels en symptomen van toxiciteit zijn gemeld bij gelijktijdige toediening van fluvox 100 mgaminemaleaat en carbamazepine.
Clozapine: Zien WAARSCHUWINGEN EN VOORZORGSMAATREGELEN .
Lithium: Net als bij andere serotonerge geneesmiddelen kan lithium de serotonerge effecten van fluvoxamine versterken en daarom moet de combinatie met voorzichtigheid worden gebruikt. Er zijn epileptische aanvallen gemeld bij gelijktijdige toediening van fluvox 50 mgaminemaleaat en lithium.
Methadon: Zien WAARSCHUWINGEN EN VOORZORGSMAATREGELEN .
Monoamineoxidaseremmers: Zien DOSERING EN ADMINISTRATIE , CONTRA-INDICATIES , WAARSCHUWINGEN EN VOORZORGSMAATREGELEN .
Pimozide: Zien CONTRA-INDICATIES , WAARSCHUWINGEN EN VOORZORGSMAATREGELEN .
Ramelteon: Zien WAARSCHUWINGEN EN VOORZORGSMAATREGELEN .
Serotonerge geneesmiddelen: Zien DOSERING EN ADMINISTRATIE , CONTRA-INDICATIES , WAARSCHUWINGEN EN VOORZORGSMAATREGELEN .
tacrine: In een onderzoek onder 13 gezonde, mannelijke vrijwilligers werd een enkele dosis van 40 mg tacrine toegevoegd aan fluvox 50 mgamine 100 mg/dag toegediend in steady-state geassocieerd met vijf- en achtvoudige verhogingen van respectievelijk de Cmax en AUC van tacrine, vergeleken met de toediening van alleen tacrine. Vijf proefpersonen ondervonden misselijkheid, braken, zweten en diarree na gelijktijdige toediening, consistent met de cholinerge effecten van tacrine.
Thioridazine: Zien CONTRA-INDICATIES , WAARSCHUWINGEN EN VOORZORGSMAATREGELEN .
Tizanidine: Zien CONTRA-INDICATIES , WAARSCHUWINGEN EN VOORZORGSMAATREGELEN .
Tricyclische antidepressiva (TCA's): Aanzienlijk verhoogde plasma-TCA-spiegels zijn gemeld bij gelijktijdige toediening van fluvoxaminemaleaat en amitriptyline, clomipramine of imipramine. Voorzichtigheid is geboden bij gelijktijdige toediening van Fluvoxaminemaleaattabletten en TCA's; plasma TCA-concentraties moeten mogelijk worden gecontroleerd en de dosis TCA moet mogelijk worden verlaagd.
Triptanen: Er zijn zeldzame postmarketingmeldingen geweest van het serotoninesyndroom bij gebruik van een SSRI en een triptan. Als gelijktijdige behandeling van fluvox 50 mgamine met een triptan klinisch gerechtvaardigd is, wordt zorgvuldige observatie van de patiënt geadviseerd, vooral tijdens de start van de behandeling en bij dosisverhogingen [zie WAARSCHUWINGEN EN VOORZORGSMAATREGELEN ].
Sumatriptan: Er zijn zeldzame postmarketingmeldingen geweest waarin patiënten werden beschreven met zwakte, hyperreflexie en coördinatiestoornissen na het gebruik van een selectieve serotonineheropnameremmer (SSRI) en sumatriptan. Als gelijktijdige behandeling met sumatriptan en een SSRI (bijv. fluoxetine, fluvoxamine, paroxetine, sertraline) klinisch gerechtvaardigd is, wordt passende observatie van de patiënt geadviseerd.
Tryptofaan: Tryptofaan kan de serotonerge effecten van fluvoxamine versterken en daarom moet de combinatie met voorzichtigheid worden gebruikt. Ernstig braken is gemeld bij gelijktijdige toediening van fluvoxaminemaleaat en tryptofaan [zie: WAARSCHUWINGEN EN VOORZORGSMAATREGELEN ].
Andere medicijnen
Alosetron: Zien CONTRA-IDICATIES , WAARSCHUWINGEN EN VOORZORGSMAATREGELEN , en Lotronex™(alosetron) bijsluiter.
Digoxine: Toediening van 100 mg fluvox 100 mg amine per dag gedurende 18 dagen (N=8) had geen significante invloed op de farmacokinetiek van een enkelvoudige intraveneuze dosis digoxine van 1,25 mg.
Diltiazem: Bradycardie is gemeld bij gelijktijdige toediening van fluvoxaminemaleaat en diltiazem.
Mexiletine: Zien WAARSCHUWINGEN EN VOORZORGSMAATREGELEN .
Propranolol en andere bètablokkers: Gelijktijdige toediening van fluvoxaminemaleaat 100 mg per dag en propranolol 160 mg per dag bij normale vrijwilligers resulteerde in een gemiddelde vijfvoudige toename (bereik 2 tot 17) van de minimale propranololplasmaconcentraties. In deze studie was er een lichte versterking van de door propranolol geïnduceerde verlaging van de hartslag en verlaging van de diastolische inspanningsdruk.
Eén geval van bradycardie en hypotensie en een tweede geval van orthostatische hypotensie zijn gemeld bij gelijktijdige toediening van fluvoxaminemaleaat en metoprolol.
Als propranolol of metoprolol gelijktijdig wordt toegediend met Fluvox 50 mgaminemaleaattabletten, wordt een verlaging van de initiële bètablokkerdosis en een voorzichtigere dosistitratie aanbevolen. Er is geen dosisaanpassing nodig voor Fluvoxaminemaleaattabletten.
Gelijktijdige toediening van fluvoxaminemaleaat 100 mg per dag met atenolol 100 mg per dag (N=6) had geen invloed op de plasmaconcentraties van atenolol. In tegenstelling tot propranolol en metoprolol, die een levermetabolisme ondergaan, wordt atenolol voornamelijk via de nieren uitgescheiden.
Theofylline: Zien WAARSCHUWINGEN EN VOORZORGSMAATREGELEN .
Warfarine en andere geneesmiddelen die de hemostase verstoren (NSAID's, aspirine, enz.): Zien WAARSCHUWINGEN EN VOORZORGSMAATREGELEN .
Effecten van roken op het metabolisme van fluvoxamine
Bij rokers was het metabolisme van fluvox 100 mgamine 25% hoger dan bij niet-rokers.
Elektroconvulsietherapie (ECT)
Er zijn geen klinische onderzoeken die de voordelen of risico's van gecombineerd gebruik van ECT en fluvox 100 mgaminemaleaat aantonen.
Drugsmisbruik en afhankelijkheid
Gecontroleerde stof
Fluvoxaminemaleaattabletten zijn geen gereguleerde stof.
Afhankelijkheid
De mogelijkheid van misbruik, tolerantie en lichamelijke afhankelijkheid met fluvox 100 mgaminemaleaat is onderzocht in een niet-menselijk primaatmodel. Er werden geen aanwijzingen gevonden voor afhankelijkheidsverschijnselen. De stopzettingseffecten van Fluvoxaminemaleaat-tabletten werden niet systematisch geëvalueerd in gecontroleerde klinische onderzoeken. Fluvoxaminemaleaattabletten zijn in klinische onderzoeken niet systematisch onderzocht op mogelijke misbruik, maar er waren geen aanwijzingen voor het zoeken naar geneesmiddelen in klinische onderzoeken. Er moet echter worden opgemerkt dat patiënten met een risico op afhankelijkheid van geneesmiddelen systematisch werden uitgesloten van onderzoeksstudies met fluvox 100 mgaminemaleaat. Over het algemeen is het niet mogelijk om op basis van preklinische of premarketing klinische ervaring te voorspellen in hoeverre een op het CZS actief geneesmiddel zal worden misbruikt, omgeleid en/of misbruikt zodra het op de markt is gebracht. Daarom dienen artsen patiënten zorgvuldig te evalueren op een voorgeschiedenis van drugsmisbruik en dergelijke patiënten nauwlettend te volgen, hen te observeren op tekenen van misbruik of misbruik van fluvoxaminemaleaat (dwz ontwikkeling van tolerantie, verhoging van de dosis, gedrag bij het zoeken naar geneesmiddelen).
WAARSCHUWINGEN
Inbegrepen als onderdeel van de PREVENTIEVE MAATREGELEN sectie.
PREVENTIEVE MAATREGELEN
Klinische verslechtering en zelfmoordrisico
Patiënten met een depressieve stoornis (MDD), zowel volwassenen als kinderen, kunnen een verergering van hun depressie ervaren en/of het optreden van zelfmoordgedachten en -gedrag (suïcidaliteit) of ongewone gedragsveranderingen, ongeacht of ze antidepressiva gebruiken of niet, en dit risico kan aanhouden totdat significante remissie optreedt. Zelfmoord is een bekend risico op depressie en bepaalde andere psychiatrische stoornissen, en deze stoornissen zelf zijn de sterkste voorspellers van zelfmoord. Er bestaat echter al lang de bezorgdheid dat antidepressiva een rol kunnen spelen bij het veroorzaken van verergering van depressie en het optreden van suïcidaliteit bij bepaalde patiënten tijdens de vroege fasen van de behandeling. Gepoolde analyses van kortdurende placebogecontroleerde onderzoeken met antidepressiva (SSRI's en andere) toonden aan dat deze geneesmiddelen het risico op zelfmoordgedachten en -gedrag (suïcidaliteit) verhogen bij kinderen, adolescenten en jonge volwassenen (18-24 jaar) met een depressieve stoornis ( MDD) en andere psychiatrische stoornissen. Kortdurende onderzoeken lieten geen toename zien van het risico op suïcidaliteit bij gebruik van antidepressiva in vergelijking met placebo bij volwassenen ouder dan 24 jaar; er was een afname met antidepressiva vergeleken met placebo bij volwassenen van 65 jaar en ouder.
De gepoolde analyses van placebogecontroleerde onderzoeken bij kinderen en adolescenten met MDD, obsessieve compulsieve stoornis (OCS) of andere psychiatrische stoornissen omvatten in totaal 24 kortetermijnonderzoeken met 9 antidepressiva bij meer dan 4400 patiënten. De gepoolde analyses van placebogecontroleerde onderzoeken bij volwassenen met MDD of andere psychiatrische stoornissen omvatten in totaal 295 kortetermijnonderzoeken (mediane duur van 2 maanden) van 11 antidepressiva bij meer dan 77.000 patiënten. Er was een aanzienlijke variatie in het risico op suïcidaliteit tussen geneesmiddelen, maar een tendens naar een toename bij de jongere patiënten voor bijna alle onderzochte geneesmiddelen. Er waren verschillen in absoluut risico op suïcidaliteit tussen de verschillende indicaties, met de hoogste incidentie bij MDD. De risicoverschillen (geneesmiddel versus placebo) waren echter relatief stabiel binnen leeftijdscategorieën en tussen indicaties. Deze risicoverschillen (drug-placebo verschil in het aantal gevallen van suïcidaliteit per 1000 behandelde patiënten) worden gegeven in Tabel 1.
TABEL 1: VERSCHILLEN DRUG-PLACEBO IN AANTAL GEVALLEN VAN SUICIDALITEIT PER 1000 BEHANDELDE PATINTEN
In geen van de pediatrische onderzoeken kwamen zelfmoorden voor. Er waren zelfmoorden in de onderzoeken bij volwassenen, maar het aantal was niet voldoende om een conclusie te trekken over het effect van het geneesmiddel op zelfmoord.
Het is niet bekend of het suïcidaliteitsrisico zich uitstrekt tot langdurig gebruik, dat wil zeggen langer dan enkele maanden. Er is echter substantieel bewijs uit placebogecontroleerde onderhoudsonderzoeken bij volwassenen met depressie dat het gebruik van antidepressiva het opnieuw optreden van depressie kan vertragen.
Alle patiënten die voor welke indicatie dan ook met antidepressiva worden behandeld, moeten op de juiste manier worden gecontroleerd en nauwlettend worden geobserveerd op klinische verergering, suïcidaliteit en ongewone gedragsveranderingen, vooral tijdens de eerste paar maanden van een medicamenteuze behandeling, of op tijdstippen van dosisveranderingen, ofwel verhogingen of afneemt.
De volgende symptomen, angst, agitatie, paniekaanvallen, slapeloosheid, prikkelbaarheid, vijandigheid, agressiviteit, impulsiviteit, acathisie (psychomotorische rusteloosheid), hypomanie en manie, zijn gemeld bij volwassen en pediatrische patiënten die ook werden behandeld met antidepressiva voor depressieve stoornis evenals voor andere indicaties, zowel psychiatrisch als niet-psychiatrisch. Hoewel er geen oorzakelijk verband is tussen het ontstaan van dergelijke symptomen en ofwel de verergering van depressie en/of het ontstaan van suïcidale impulsen, bestaat er bezorgdheid dat dergelijke symptomen een voorbode kunnen zijn van opkomende suïcidaliteit.
Bij patiënten bij wie de depressie aanhoudend erger is, of die opkomende suïcidaliteit ervaren of symptomen die een voorbode kunnen zijn van een verergering van depressie of suïcidaliteit, moet worden overwogen om het therapeutische regime te veranderen, met inbegrip van het mogelijk stopzetten van de medicatie, vooral als deze symptomen ernstig en abrupt zijn. bij aanvang, of maakten geen deel uit van de symptomen die de patiënt vertoonde.
Als de beslissing is genomen om de behandeling te staken, moet de medicatie zo snel mogelijk worden afgebouwd, maar met de erkenning dat abrupte stopzetting gepaard kan gaan met bepaalde symptomen en risico's [zie DOSERING EN ADMINISTRATIE ].
Families en verzorgers van patiënten die worden behandeld met antidepressiva voor depressieve stoornis of andere indicaties, zowel psychiatrische als niet-psychiatrische, moeten worden gewaarschuwd voor de noodzaak om patiënten te controleren op het optreden van agitatie, prikkelbaarheid, ongebruikelijke gedragsveranderingen en de andere hierboven beschreven symptomen , evenals de opkomst van suïcidaliteit, en om dergelijke symptomen onmiddellijk aan zorgverleners te melden. Dergelijke monitoring moet dagelijkse observatie door families en zorgverleners omvatten. Voorschriften voor Fluvoxaminemaleaat-tabletten moeten worden geschreven voor de kleinste hoeveelheid tabletten in overeenstemming met goed patiëntenbeheer, om het risico op overdosering te verminderen.
Patiënten screenen op bipolaire stoornis
Een depressieve episode kan de eerste presentatie van een bipolaire stoornis zijn. Over het algemeen wordt aangenomen (hoewel niet vastgesteld in gecontroleerde onderzoeken) dat de behandeling van een dergelijke episode met alleen een antidepressivum de kans op neerslag van een gemengde/manische episode kan vergroten bij patiënten met een risico op een bipolaire stoornis. Of een van de hierboven beschreven symptomen een dergelijke conversie vertegenwoordigen, is niet bekend. Echter, voordat de behandeling met een antidepressivum wordt gestart, moeten patiënten met depressieve symptomen adequaat worden gescreend om te bepalen of ze een risico lopen op een bipolaire stoornis; een dergelijke screening moet een gedetailleerde psychiatrische geschiedenis omvatten, inclusief een familiegeschiedenis van zelfmoord, bipolaire stoornis en depressie. Opgemerkt moet worden dat Fluvox 50 mgaminemaleaattabletten niet zijn goedgekeurd voor gebruik bij de behandeling van bipolaire depressie.
serotonine syndroom
De ontwikkeling van een mogelijk levensbedreigend serotoninesyndroom is gemeld met alleen SNRI's en SSRI's, waaronder Fluvoxaminemaleaattabletten, maar vooral bij gelijktijdig gebruik van serotonerge geneesmiddelen (waaronder triptanen, tricyclische antidepressiva, fentanyl, lithium, tramadol, tryptofaan, busipiron, amfetaminen). , en sint-janskruid) en met geneesmiddelen die het metabolisme van serotonine aantasten (met name MAO-remmers, zowel die bedoeld voor de behandeling van psychiatrische stoornissen als andere, zoals linezolid en intraveneus methyleenblauw).
Symptomen van het serotoninesyndroom kunnen zijn: veranderingen in de mentale toestand (bijv. agitatie, hallucinaties, delirium en coma), autonome instabiliteit (bijv. tachycardie, labiele bloeddruk, duizeligheid, diaforese, blozen, hyperthermie), neuromusculaire aberraties (bijv. tremor, stijfheid, myoclonus, hyperreflexie, coördinatiestoornissen), toevallen en/of gastro-intestinale symptomen (bijv. misselijkheid, braken, diarree). Patiënten moeten worden gecontroleerd op het optreden van het serotoninesyndroom.
Gelijktijdig gebruik van Fluvoxaminemaleaat-tabletten met MAO-remmers bedoeld voor de behandeling van psychiatrische stoornissen is gecontra-indiceerd. Fluvoxaminemaleaattabletten mogen ook niet worden gestart bij een patiënt die wordt behandeld met MAO-remmers zoals linezolid of intraveneus methyleenblauw. Alle rapporten met methyleenblauw die informatie verschaften over de toedieningsweg, hadden betrekking op intraveneuze toediening in het dosisbereik van 1 mg/kg tot 8 mg/kg. Er zijn geen meldingen geweest van toediening van methyleenblauw via andere routes (zoals orale tabletten of lokale weefselinjectie) of in lagere doses. Er kunnen omstandigheden zijn waarin het nodig is om een behandeling met een MAO-remmer zoals linezolid of intraveneus methyleenblauw te starten bij een patiënt die Fluvox 50 mgaminemaleaattabletten gebruikt. Fluvox 50 mgaminemaleaattabletten moeten worden stopgezet voordat de behandeling met de MAO-remmer wordt gestart [zie CONTRA-INDICATIES , DOSERING EN ADMINISTRATIE ].
Als gelijktijdig gebruik van Fluvoxaminemaleaat-tabletten met andere serotonerge geneesmiddelen, waaronder triptanen, tricyclische antidepressiva, fentanyl, lithium, tramadol, buspiron, tryptofaan, amfetaminen en sint-janskruid klinisch gerechtvaardigd is, moeten patiënten op de hoogte worden gebracht van een mogelijk verhoogd risico op het serotoninesyndroom, vooral tijdens de start van de behandeling en dosisverhogingen.
De behandeling met Fluvoxaminemaleaat-tabletten en alle gelijktijdig gebruikte serotonerge middelen moet onmiddellijk worden stopgezet als de bovenstaande gebeurtenissen optreden en er moet een ondersteunende symptomatische behandeling worden gestart.
Hoeksluiting glaucoom
De pupilverwijding die optreedt na gebruik van veel antidepressiva, waaronder Fluvoxaminemaleaat-tabletten, kan een aanval van hoeksluiting veroorzaken bij een patiënt met anatomisch nauwe hoeken die geen patente iridectomie hebben ondergaan.
Potentiële thioridazine-interactie
Het effect van fluvoxamine (25 mg tweemaal daags gedurende één week) op de steady-state-concentraties van thioridazine werd geëvalueerd bij 10 mannelijke opgenomen patiënten met schizofrenie. De concentraties van thioridazine en zijn twee actieve metabolieten, mesoridazine en sulforidazine, namen drievoudig toe na gelijktijdige toediening van fluvox 100 mgamine.
Toediening van thioridazine veroorzaakt een dosisafhankelijke verlenging van het QTc-interval, wat gepaard gaat met ernstige ventriculaire aritmieën, zoals torsades de pointes-type aritmieën, en plotselinge dood. Het is waarschijnlijk dat deze ervaring de mate van risico onderschat die kan optreden bij hogere doses thioridazine. Bovendien kan het effect van fluvox 100 mgamine nog meer uitgesproken zijn wanneer het in hogere doses wordt toegediend. Daarom mogen fluvoxamine en thioridazine niet gelijktijdig worden toegediend [zie: CONTRA-INDICATIES ].
Potentiële Tizanidine-interactie
Fluvoxamine is een krachtige remmer van CYP1A2 en tizanidine is een CYP1A2-substraat. Het effect van fluvox 50 mgamine (100 mg per dag gedurende 4 dagen) op de farmacokinetiek en farmacodynamiek van een enkele dosis van 4 mg tizanidine is onderzocht bij 10 gezonde mannelijke proefpersonen. De Cmax van tizanidine was ongeveer 12-voudig verhoogd (bereik 5-voudig tot 32-voudig), de eliminatiehalfwaardetijd was bijna 3-voudig verhoogd en de AUC nam 33-voudig toe (bereik 14-voudig tot 103-voudig). Het gemiddelde maximale effect op de bloeddruk was een verlaging van de systolische bloeddruk met 35 mm Hg, een verlaging van de diastolische bloeddruk met 20 mm Hg en een verlaging van de hartslag met 4 slagen/min. De slaperigheid was significant toegenomen en de prestaties op de psychomotorische taak waren significant verminderd. Fluvoxamine en tizanidine mogen niet samen worden gebruikt [zie: CONTRA-INDICATIES ].
Potentiële Pimozide-interactie
Pimozide wordt gemetaboliseerd door het cytochroom P4503A4-iso-enzym en er is aangetoond dat ketoconazol, een krachtige remmer van CYP3A4, het metabolisme van dit geneesmiddel blokkeert, wat resulteert in verhoogde plasmaconcentraties van het oorspronkelijke geneesmiddel. Een verhoogde plasmaconcentratie van pimozide veroorzaakt QT-verlenging en is in verband gebracht met torsades de pointes-type ventriculaire tachycardie, soms fataal. Zoals hieronder vermeld, is een aanzienlijke farmacokinetische interactie waargenomen voor fluvox 100 mgamine in combinatie met alprazolam, een geneesmiddel waarvan bekend is dat het wordt gemetaboliseerd door CYP3A4. Hoewel niet definitief is aangetoond dat fluvox 100 mgamine een krachtige CYP3A4-remmer is, is dit waarschijnlijk wel het geval, gezien de aanzienlijke interactie van fluvox 50 mgamine met alprazolam. Daarom wordt aanbevolen fluvoxamine niet te gebruiken in combinatie met pimozide [zie: CONTRA-INDICATIES ].
Potentiële Alosetron-interactie
Omdat alosetron wordt gemetaboliseerd door een verscheidenheid aan leverenzymen die CYP-geneesmiddelen metaboliseren, kunnen inductoren of remmers van deze enzymen de klaring van alosetron veranderen. Fluvox 50 mgamine is een bekende krachtige remmer van CYP1A2 en remt ook CYP3A4, CYP2C9 en CYP2C19. In een farmacokinetisch onderzoek kregen 40 gezonde vrouwelijke proefpersonen fluvox 100 mgamine in oplopende doses van 50 mg tot 200 mg per dag gedurende 16 dagen, met gelijktijdige toediening van 1 mg alosetron op de laatste dag. Fluvox 50 mgamine verhoogde de gemiddelde plasmaconcentratie van alosetron (AUC) ongeveer 6 keer en verlengde de halfwaardetijd met ongeveer 3 keer. [Zien CONTRA-INDICATIES en Lotronex™ (alosetron) bijsluiter].
Andere potentieel belangrijke geneesmiddelinteracties
Benzodiazepinen
Benzodiazepinen die worden gemetaboliseerd door hepatische oxidatie (bijv. alprazolam, midazolam, triazolam, enz.) moeten met voorzichtigheid worden gebruikt omdat de klaring van deze geneesmiddelen waarschijnlijk wordt verminderd door fluvoxamine. De klaring van benzodiazepinen die worden gemetaboliseerd door glucuronidering (bijv. lorazepam, oxazepam, temazepam) wordt waarschijnlijk niet beïnvloed door fluvox 100 mgamine.
Alprazolam
Wanneer fluvoxaminemaleaat (100 mg eenmaal daags) en alprazolam (1 mg eenmaal daags) gelijktijdig werden toegediend tot steady-state, waren de plasmaconcentraties en andere farmacokinetische parameters (AUC, Cmax, T½) van alprazolam ongeveer tweemaal de waargenomen wanneer alprazolam alleen werd toegediend; orale klaring was met ongeveer 50% verminderd. De verhoogde plasma-alprazolamconcentraties resulteerden in verminderde psychomotorische prestaties en geheugen. Deze interactie, die niet is onderzocht met hogere doses fluvoxamine, kan meer uitgesproken zijn als een dagelijkse dosis van 300 mg gelijktijdig wordt toegediend, vooral omdat fluvox 50 mgamine een niet-lineaire farmacokinetiek vertoont over het doseringsbereik van 100-300 mg. Als alprazolam gelijktijdig wordt toegediend met Fluvox 50 mgaminemaleaattabletten, moet de initiële dosis alprazolam ten minste worden gehalveerd en wordt titratie naar de laagste effectieve dosis aanbevolen. Er is geen dosisaanpassing nodig voor Fluvox 100 mgaminemaleaattabletten.
diazepam
Gelijktijdige toediening van Fluvoxaminemaleaat en diazepam wordt over het algemeen niet aanbevolen. Omdat fluvoxamine de klaring van zowel diazepam als zijn actieve metaboliet, Ndesmethyldiazepam, vermindert, is er een grote kans op substantiële accumulatie van beide soorten tijdens chronische gelijktijdige toediening.
Bewijs dat de conclusie ondersteunt dat het niet raadzaam is om fluvoxamine en diazepam gelijktijdig toe te dienen, is afgeleid van een onderzoek waarin gezonde vrijwilligers die 150 mg/dag fluvox 50 mgamine gebruikten, een enkelvoudige orale dosis van 10 mg diazepam kregen toegediend. Bij deze proefpersonen (N=8) was de klaring van diazepam met 65% verminderd en die van N-desmethyldiazepam tot een niveau dat te laag was om te meten in de loop van de 2 weken durende studie.
Het is waarschijnlijk dat deze ervaring de mate van accumulatie die kan optreden bij herhaalde toediening van diazepam aanzienlijk onderschat. Bovendien, zoals opgemerkt met alprazolam, kan het effect van fluvox 50 mgamine zelfs meer uitgesproken zijn wanneer het in hogere doses wordt toegediend.
Dienovereenkomstig dienen diazepam en fluvoxamine gewoonlijk niet gelijktijdig te worden toegediend.
Clozapine
Verhoogde serumspiegels van clozapine zijn gemeld bij patiënten die fluvox 100 mgaminemaleaat en clozapine gebruikten. Aangezien clozapine-gerelateerde aanvallen en orthostatische hypotensie dosisgerelateerd lijken te zijn, kan het risico op deze bijwerkingen groter zijn bij gelijktijdige toediening van fluvoxamine en clozapine. Patiënten moeten nauwlettend worden gecontroleerd wanneer fluvoxaminemaleaat en clozapine gelijktijdig worden gebruikt.

methadon
Aanzienlijk verhoogde methadonverhoudingen (plasmaniveau:dosis) zijn gemeld wanneer fluvox 50 mgaminemaleaat werd toegediend aan patiënten die een onderhoudsbehandeling met methadon kregen, met symptomen van opioïde-intoxicatie bij één patiënt. Ontwenningsverschijnselen van opioïden werden gemeld na stopzetting van fluvoxaminemaleaat bij een andere patiënt.
Mexiletine
Het effect van steady-state fluvoxamine (50 mg tweemaal daags gedurende 7 dagen) op de farmacokinetiek van een enkelvoudige dosis mexiletine (200 mg) werd geëvalueerd bij 6 gezonde Japanse mannen. De klaring van mexiletine was met 38% verminderd na gelijktijdige toediening met fluvox 100 mgamine in vergelijking met alleen mexiletine. Als fluvoxamine en mexiletine gelijktijdig worden toegediend, moeten de serummexiletinespiegels worden gecontroleerd.
Ramelteon
Wanneer fluvox 50 mgamine 100 mg tweemaal daags werd toegediend gedurende 3 dagen voorafgaand aan gelijktijdige toediening van een enkelvoudige dosis van ramelteon 16 mg en fluvoxamine, nam de AUC voor ramelteon ongeveer 190-voudig toe en de Cmax nam ongeveer 70-voudig toe in vergelijking met alleen toegediende ramelteon. Ramelteon mag niet worden gebruikt in combinatie met fluvoxamine.
theofylline
Het effect van steady-state fluvox 50 mgamine (50 mg tweemaal daags) op de farmacokinetiek van een enkele dosis theofylline (375 mg als 442 mg aminofylline) werd geëvalueerd bij 12 gezonde, niet-rokende, mannelijke vrijwilligers. De klaring van theofylline was ongeveer 3-voudig verminderd. Daarom, als theofylline gelijktijdig wordt toegediend met fluvoxaminemaleaat, moet de dosis worden verlaagd tot een derde van de gebruikelijke dagelijkse onderhoudsdosis en moeten de plasmaconcentraties van theofylline worden gecontroleerd. Er is geen dosisaanpassing nodig voor Fluvox 100 mgaminemaleaattabletten.
Warfarine en andere geneesmiddelen die de hemostase verstoren (NSAID's, aspirine, enz.)
De afgifte van serotonine door bloedplaatjes speelt een belangrijke rol bij hemostase. Epidemiologische studies van de case-control en cohort-opzet hebben een verband aangetoond tussen het gebruik van psychotrope geneesmiddelen die de heropname van serotonine verstoren en het optreden van bloedingen in het bovenste deel van het maagdarmkanaal. Deze onderzoeken hebben ook aangetoond dat gelijktijdig gebruik van een NSAID of aspirine dit risico op bloedingen kan vergroten. Daarom moeten patiënten worden gewaarschuwd voor het gelijktijdig gebruik van dergelijke geneesmiddelen met fluvoxamine [zie: WAARSCHUWINGEN EN VOORZORGSMAATREGELEN ].
Warfarine
Wanneer fluvox 50 mgaminemaleaat (50 mg driemaal daags) gedurende twee weken gelijktijdig met warfarine werd toegediend, namen de plasmaconcentraties van warfarine toe met 98% en werden de protrombinetijden verlengd. Daarom moet de protrombinetijd van patiënten die orale anticoagulantia en fluvoxaminemaleaat krijgen, gecontroleerd worden en hun dosis anticoagulantia dienovereenkomstig worden aangepast. Er is geen dosisaanpassing nodig voor Fluvoxaminemaleaattabletten.
Stopzetting van de behandeling met Fluvox 100 mgaminemaleaattabletten
Tijdens het op de markt brengen van Fluvoxaminemaleaattabletten en andere SSRI's en SNRI's (serotonine- en noradrenalineheropnameremmers), zijn er spontane meldingen geweest van bijwerkingen die optraden na stopzetting van deze geneesmiddelen, met name bij abrupte, waaronder de volgende: dysfore stemming, prikkelbaarheid, opwinding, duizeligheid , sensorische stoornissen (bijv. paresthesieën, zoals elektrische schokken), angst, verwardheid, hoofdpijn, lethargie, emotionele labiliteit, slapeloosheid en hypomanie. Hoewel deze voorvallen over het algemeen zelfbeperkend zijn, zijn er meldingen geweest van ernstige ontwenningsverschijnselen.
Patiënten moeten op deze symptomen worden gecontroleerd wanneer de behandeling met Fluvox 50 mgaminemaleaattabletten wordt stopgezet. Waar mogelijk wordt een geleidelijke verlaging van de dosis aanbevolen in plaats van abrupt stoppen. Als ondraaglijke symptomen optreden na een verlaging van de dosis of na stopzetting van de behandeling, kan worden overwogen om de eerder voorgeschreven dosis te hervatten. Vervolgens kan de arts doorgaan met het verlagen van de dosis, maar in een meer geleidelijk tempo [zie DOSERING EN ADMINISTRATIE ].
Abnormale bloeding
SSRI's en SNRI's, waaronder fluvoxaminemaleaattabletten, kunnen het risico op bloedingen verhogen. Gelijktijdig gebruik van aspirine, niet-steroïde anti-inflammatoire geneesmiddelen, warfarine en andere anticoagulantia kan dit risico vergroten. Case-reports en epidemiologische studies (case-control en cohort-design) hebben een verband aangetoond tussen het gebruik van geneesmiddelen die de heropname van serotonine verstoren en het optreden van gastro-intestinale bloedingen. Bloedingen gerelateerd aan SSRI's en SNRI's varieerden van ecchymosen, hematomen, epistaxis en petechiën tot levensbedreigende bloedingen.
Patiënten moeten worden gewaarschuwd voor het risico op bloedingen bij gelijktijdig gebruik van Fluvox 100 mgaminemaleaattabletten en NSAID's, aspirine of andere geneesmiddelen die de stolling beïnvloeden (zie WAARSCHUWINGEN EN VOORZORGSMAATREGELEN ].
Activering van manie/hypomanie
Tijdens premarketingonderzoeken waarbij voornamelijk depressieve patiënten betrokken waren, trad hypomanie of manie op bij ongeveer 1% van de met fluvoxamine behandelde patiënten. In een tien weken durende pediatrische OCS-studie kregen 2 van de 57 patiënten (4%) die werden behandeld met fluvoxamine manische reacties, vergeleken met geen van de 63 placebopatiënten. Activering van manie/hypomanie is ook gemeld bij een klein deel van de patiënten met een ernstige affectieve stoornis die werden behandeld met andere in de handel verkrijgbare antidepressiva. Zoals met alle antidepressiva moet Fluvoxaminemaleaat met voorzichtigheid worden gebruikt bij patiënten met een voorgeschiedenis van manie.
epileptische aanvallen
Tijdens premarketingonderzoeken werden epileptische aanvallen gemeld bij 0,2% van de met fluvoxamine behandelde patiënten. Voorzichtigheid is geboden wanneer het geneesmiddel wordt toegediend aan patiënten met een voorgeschiedenis van convulsieve aandoeningen. Fluvox 100 mgamine moet worden vermeden bij patiënten met onstabiele epilepsie en patiënten met gecontroleerde epilepsie moeten zorgvuldig worden gecontroleerd. De behandeling met fluvoxamine moet worden gestaakt als er epileptische aanvallen optreden of als de frequentie van aanvallen toeneemt.
Hyponatriëmie
Hyponatriëmie kan optreden als gevolg van behandeling met SSRI's en SNRI's, waaronder fluvoxaminemaleaattabletten. In veel gevallen lijkt deze hyponatriëmie het gevolg te zijn van het syndroom van ongepast antidiuretisch hormoon (SIADH). Gevallen met serumnatrium lager dan 110 mmol/L zijn gemeld. Oudere patiënten lopen mogelijk een groter risico op het ontwikkelen van hyponatriëmie met SSRI's en SNRI's [zie: Gebruik bij specifieke populaties ]. Ook kunnen patiënten die diuretica gebruiken of die anderszins een volumedepletie hebben, een groter risico lopen. Stopzetting van Fluvox 100 mgaminemaleaattabletten moet worden overwogen bij patiënten met symptomatische hyponatriëmie en er moet passende medische interventie worden ingesteld.
Tekenen en symptomen van hyponatriëmie zijn onder meer hoofdpijn, concentratieproblemen, geheugenstoornissen, verwardheid, zwakte en onvastheid, wat kan leiden tot vallen. Tekenen en symptomen die gepaard gaan met ernstigere en/of acute gevallen omvatten hallucinaties, syncope, toevallen, coma, ademstilstand en overlijden.
Gebruik bij patiënten met gelijktijdige ziekte
Nauwkeurig gecontroleerde klinische ervaring met Fluvox 50 mgaminemaleaattabletten bij patiënten met gelijktijdige systemische ziekte is beperkt. Voorzichtigheid is geboden bij het toedienen van Fluvoxaminemaleaat tabletten aan patiënten met ziekten of aandoeningen die de hemodynamische reacties of het metabolisme kunnen beïnvloeden.
Fluvoxaminemaleaattabletten zijn niet geëvalueerd of in noemenswaardige mate gebruikt bij patiënten met een recente voorgeschiedenis van een myocardinfarct of instabiele hartziekte. Patiënten met deze diagnoses werden systematisch uitgesloten van veel klinische onderzoeken tijdens de premarketingtests van het product. Evaluatie van de elektrocardiogrammen voor patiënten met depressie of OCS die deelnamen aan premarketingonderzoeken toonden geen verschillen aan tussen fluvox 100 mgamine en placebo bij het optreden van klinisch belangrijke ECG-veranderingen.
Patiënten met leverinsufficiëntie
Bij patiënten met leverdisfunctie was de klaring van fluvox 50 mgamine met ongeveer 30% verminderd. Patiënten met een leverfunctiestoornis moeten beginnen met een lage dosis Fluvoxaminemaleaat Mylan en deze langzaam verhogen onder zorgvuldige controle.
Laboratorium testen
Er worden geen specifieke laboratoriumtests aanbevolen.
Seksuele disfunctie
Het gebruik van SSRI's, inclusief Fluvoxaminemaleaat-tabletten, kan symptomen van seksuele disfunctie veroorzaken [zie: ONGEWENSTE REACTIES 4)]. Bij mannelijke patiënten kan het gebruik van SSRI's leiden tot vertraging of falen van de ejaculatie, verminderd libido en erectiestoornissen. Bij vrouwelijke patiënten kan het gebruik van SSRI's leiden tot een verminderd libido en een vertraagd of afwezig orgasme.
Het is belangrijk voor voorschrijvers om te informeren naar de seksuele functie voordat met Fluvoxaminemaleaat wordt gestart en om specifiek te informeren naar veranderingen in de seksuele functie tijdens de behandeling, omdat seksuele functie mogelijk niet spontaan wordt gemeld. Bij het evalueren van veranderingen in seksuele functie is het verkrijgen van een gedetailleerde geschiedenis (inclusief timing van het begin van de symptomen) belangrijk omdat seksuele symptomen andere oorzaken kunnen hebben, waaronder de onderliggende psychiatrische stoornis. Bespreek mogelijke managementstrategieën om patiënten te ondersteunen bij het nemen van weloverwogen beslissingen over de behandeling.
Informatie over patiëntbegeleiding
Adviseer de patiënt om de door de FDA goedgekeurde patiëntetikettering te lezen ( Medicatiegids ).
Voorschrijvers of andere gezondheidswerkers moeten patiënten, hun families en hun verzorgers informeren over de voordelen en risico's van de behandeling met Fluvoxaminemaleaat Mylan en hen adviseren bij het juiste gebruik. Er is een medicatiehandleiding voor patiënten over "Antidepressiva, depressie en andere ernstige psychische aandoeningen en zelfmoordgedachten of -handelingen" beschikbaar voor Fluvox 100 mgaminemaleaattabletten. De voorschrijver of gezondheidswerker moet patiënten, hun families en hun zorgverleners instrueren om de medicatiehandleiding te lezen en moet hen helpen de inhoud ervan te begrijpen. Patiënten moeten de kans krijgen om de inhoud van de medicatiehandleiding te bespreken en om antwoord te krijgen op eventuele vragen. De volledige tekst van de medicatiehandleiding is herdrukt aan het einde van dit document.
Patiënten moeten op de hoogte worden gebracht van de volgende problemen en moeten worden gevraagd hun voorschrijver te waarschuwen als deze optreden tijdens het gebruik van Fluvox 100 mgaminemaleaattabletten.
Klinische verslechtering en zelfmoordrisico
Patiënten, hun families en hun verzorgers moeten worden aangemoedigd alert te zijn op het optreden van angst, agitatie, paniekaanvallen, slapeloosheid, prikkelbaarheid, vijandigheid, agressiviteit, impulsiviteit, acathisie (psychomotorische rusteloosheid), hypomanie, manie, andere ongewone gedragsveranderingen verergering van depressie en zelfmoordgedachten, vooral in het begin van de behandeling met antidepressiva en wanneer de dosis omhoog of omlaag wordt aangepast. Families en verzorgers van patiënten moeten worden geadviseerd om dagelijks te kijken naar het optreden van dergelijke symptomen, aangezien veranderingen abrupt kunnen zijn. Dergelijke symptomen moeten worden gemeld aan de voorschrijver van de patiënt of zorgverlener, vooral als ze ernstig zijn, abrupt beginnen of geen deel uitmaken van de symptomen van de patiënt. Symptomen zoals deze kunnen in verband worden gebracht met een verhoogd risico op zelfmoordgedachten en -gedrag en duiden op de noodzaak van zeer nauwgezette monitoring en mogelijk veranderingen in de medicatie [zie GEVAARLIJKE WAARSCHUWING: , WAARSCHUWINGEN EN VOORZORGSMAATREGELEN ]
serotonine syndroom
Patiënten moeten worden gewaarschuwd voor het risico op het serotoninesyndroom, met name bij gelijktijdig gebruik van fluvoxamine met andere serotonerge middelen (waaronder triptanen, tricyclische antidepressiva, fentanyl, lithium, tramadol, tryptofaan, buspiron, amfetaminen en sint-janskruid) [zien WAARSCHUWINGEN EN VOORZORGSMAATREGELEN ].
Hoeksluiting glaucoom
Patiënten moeten erop worden gewezen dat het gebruik van Fluvoxaminemaleaat Mylan lichte pupilverwijding kan veroorzaken, wat bij daarvoor gevoelige personen kan leiden tot een episode van geslotenhoekglaucoom. Reeds bestaand glaucoom is bijna altijd openhoekglaucoom omdat geslotenhoekglaucoom, indien gediagnosticeerd, definitief kan worden behandeld met iridectomie. Openhoekglaucoom is geen risicofactor voor geslotenhoekglaucoom. Patiënten willen misschien worden onderzocht om te bepalen of ze vatbaar zijn voor hoeksluiting en een profylactische procedure ondergaan (bijv. iridectomie), als ze vatbaar zijn [zie WAARSCHUWINGEN EN VOORZORGSMAATREGELEN ].
Interferentie met cognitieve of motorische prestaties
Aangezien elk psychoactief medicijn het beoordelingsvermogen, het denken of de motoriek kan aantasten, moeten patiënten worden gewaarschuwd voor het bedienen van gevaarlijke machines, waaronder auto's, totdat ze er zeker van zijn dat de behandeling met Fluvox 100 mgaminemaleaattabletten hun vermogen om dergelijke activiteiten uit te voeren niet nadelig beïnvloedt.
Zwangerschap
- Adviseer zwangere vrouwen om hun zorgverlener op de hoogte te stellen als ze zwanger worden of van plan zijn zwanger te worden tijdens de behandeling met Fluvoxaminemaleaat.
- Adviseer patiënten dat Fluvoxaminemaleaat-tabletten laat in de zwangerschap gebruiken, kan leiden tot een verhoogd risico op neonatale complicaties die langdurige ziekenhuisopname, ademhalingsondersteuning, sondevoeding en/of aanhoudende pulmonale hypertensie van de pasgeborene (PPHN) vereisen.
- Adviseer vrouwen dat er een risico op terugval bestaat bij het staken van antidepressiva.
- Adviseer vrouwen dat er een zwangerschapsblootstellingsregister is dat de zwangerschapsuitkomsten controleert bij vrouwen die tijdens de zwangerschap aan Fluvoxaminemaleaat-tabletten zijn blootgesteld [zie Gebruik bij specifieke populaties ].
Borstvoeding
Adviseer vrouwen die borstvoeding geven en die Fluvox 100 mgaminemaleaattabletten gebruiken om baby's te controleren op diarree, braken, verminderde slaap en opwinding en om medische hulp in te roepen als ze deze symptomen opmerken [zie Gebruik bij specifieke populaties ].
Gelijktijdige medicatie
Patiënten dienen te worden geadviseerd hun arts op de hoogte te stellen als zij geneesmiddelen op recept of vrij verkrijgbare medicijnen gebruiken of van plan zijn te gebruiken, aangezien er een kans bestaat op klinisch belangrijke interacties met Fluvox 50 mgaminemaleaattabletten.
Patiënten moeten worden gewaarschuwd voor het gelijktijdig gebruik van fluvoxamine en NSAID's, aspirine of andere geneesmiddelen die de stolling beïnvloeden, aangezien het gecombineerde gebruik van psychotrope geneesmiddelen die de heropname van serotonine verstoren en deze middelen in verband zijn gebracht met een verhoogd risico op bloedingen [zie WAARSCHUWINGEN EN VOORZORGSMAATREGELEN ].
Vanwege de mogelijkheid van een verhoogd risico op ernstige bijwerkingen, waaronder ernstige verlaging van de bloeddruk en sedatie wanneer fluvoxamine en tizanidine samen worden gebruikt, mag fluvox 50 mgamine niet worden gebruikt met tizanidine (zie WAARSCHUWINGEN EN VOORZORGSMAATREGELEN ].
Vanwege de mogelijkheid van een verhoogd risico op ernstige bijwerkingen wanneer fluvoxamine en alosetron samen worden gebruikt, mag fluvox 50 mgamine niet worden gebruikt met LotronexTM (alosetron) [zie WAARSCHUWINGEN EN VOORZORGSMAATREGELEN ].
Seksuele disfunctie
Adviseer patiënten dat het gebruik van Fluvox 50 mgaminemaleaat tabletten symptomen van seksuele disfunctie kan veroorzaken bij zowel mannelijke als vrouwelijke patiënten. Informeer patiënten dat ze eventuele veranderingen in de seksuele functie en mogelijke managementstrategieën met hun zorgverlener moeten bespreken [zie WAARSCHUWINGEN EN VOORZORGSMAATREGELEN ].
Alcohol
Net als bij andere psychotrope geneesmiddelen, moeten patiënten worden geadviseerd geen alcohol te gebruiken tijdens het gebruik van Fluvox 50 mgaminemaleaattabletten.
Allergische reacties
Patiënten moeten worden geadviseerd om hun arts te informeren als ze huiduitslag, netelroos of een gerelateerd allergisch fenomeen krijgen tijdens de behandeling met Fluvoxaminemaleaat-tabletten.
Alle vermelde merknamen zijn de geregistreerde handelsmerken van hun respectievelijke eigenaren en zijn geen handelsmerken van ANI Pharmaceuticals, Inc.
Niet-klinische toxicologie
Carcinogenese, mutagenese, verminderde vruchtbaarheid
Carcinogenese
Er was geen bewijs van carcinogeniteit bij ratten die oraal werden behandeld met fluvoxaminemaleaat gedurende 30 maanden of hamsters die oraal werden behandeld met fluvox 50 mgaminemaleaat gedurende 20 (vrouwtjes) of 26 (mannetjes) maanden. De dagelijkse doses in de groepen met hoge doses in deze onderzoeken werden in de loop van het onderzoek verhoogd van minimaal 160 mg/kg tot maximaal 240 mg/kg bij ratten en van minimaal 135 mg/kg tot maximaal van 240 mg/kg bij hamsters. De maximale dosis van 240 mg/kg is respectievelijk ongeveer 5 en 6 keer (bij hamsters en ratten), de MRHD die aan kinderen wordt gegeven op basis van mg/m².
Mutagenese
Er werd geen bewijs van genotoxisch potentieel waargenomen in een micronucleustest bij muizen, een in vitro chromosoomafwijkingstest of de Ames-microbiële mutageentest met of zonder metabolische activering.
Aantasting van de vruchtbaarheid
In een onderzoek waarin mannelijke en vrouwelijke ratten fluvox 100 mgamine (60, 120 of 240 mg/kg) kregen toegediend voor en tijdens de paring en dracht, was de vruchtbaarheid verminderd bij orale doses van 120 mg/kg (3 maal de MRHD gegeven aan adolescenten op een mg/m²-basis) of hoger, zoals blijkt uit een verhoogde latentie tot paring, verminderd aantal zaadcellen, verminderd epididymaal gewicht en verminderd zwangerschapspercentage. Bovendien was het aantal implantaties en embryo's afgenomen bij de hoogste dosis (6 keer de MRHD bij adolescenten op basis van mg/m²). De dosis zonder effect voor verminderde vruchtbaarheid was 60 mg/kg (1,6 maal de MRHD gegeven aan adolescenten op basis van mg/m²).
Gebruik bij specifieke populaties
Zwangerschap
Zwangerschapsblootstellingsregister
Er is een register voor blootstelling aan zwangerschap dat de zwangerschapsuitkomsten controleert bij vrouwen die tijdens de zwangerschap aan antidepressiva zijn blootgesteld. Zorgaanbieders worden aangemoedigd om patiënten te registreren door de National Pregnancy Registry for Antidepressants te bellen op 1-844-405-6185 of online te bezoeken op https://womensmentalhealth.org/clinical-and-research-programs/pregnancyregistry/antidepressants/.
Risico Samenvatting
Langdurige ervaring met fluvox 100 mgamine bij zwangere vrouwen gedurende tientallen jaren, op basis van gepubliceerde observationele onderzoeken, heeft geen duidelijk met het geneesmiddel geassocieerd risico op ernstige geboorteafwijkingen of miskraam aangetoond (zie Gegevens ). Er zijn risico's verbonden aan onbehandelde depressie tijdens de zwangerschap en risico's van aanhoudende pulmonale hypertensie van de pasgeborene (PPHN) en slechte neonatale aanpassing met blootstelling aan selectieve serotonineheropnameremmers (SSRI's), waaronder fluvoxamine, tijdens de zwangerschap (zie Klinische overwegingen ).
Wanneer drachtige ratten oraal werden behandeld met fluvoxamine gedurende de gehele periode van organogenese, werd een verhoogde embryofoetale sterfte en verhoogde incidentie van foetale oogafwijkingen (gevouwen netvlies) waargenomen bij doses ≥ 3 maal de maximaal aanbevolen dosis voor de mens (MRHD) van 300 mg/dag gegeven aan adolescenten op basis van mg/m². Bovendien werd een verminderd foetaal lichaamsgewicht waargenomen bij een dosis die 6 keer hoger was dan de MRHD die aan adolescenten werd gegeven op basis van mg/m². Er waren geen nadelige ontwikkelingseffecten bij konijnen die werden behandeld met fluvoxamine tijdens de periode van organogenese tot een dosis die 2 maal de MRHD was die aan adolescenten werd gegeven op basis van mg/m². Wanneer fluvox 50 mgamine oraal werd toegediend aan ratten tijdens dracht en lactatie, werd een verhoogde mortaliteit van de jongen bij de geboorte waargenomen bij een dosis die tweemaal zo hoog was als de MRHD die aan adolescenten werd gegeven op basis van mg/m². Daarnaast werden afnames in het lichaamsgewicht en de overleving van de jongen waargenomen bij doses die ≥ 0,13 keer de MRHD zijn die aan adolescenten wordt gegeven (zie Gegevens ).
Het geschatte achtergrondrisico van ernstige geboorteafwijkingen en miskraam voor de aangegeven populatie is niet bekend. Alle zwangerschappen hebben een achtergrondrisico op geboorteafwijking, verlies of andere nadelige gevolgen. In de algemene bevolking van de VS zijn de geschatte achtergrondrisico's van ernstige geboorteafwijkingen en miskramen bij klinisch erkende zwangerschappen respectievelijk 2 tot 4% en 15 tot 20%.
Klinische overwegingen
Ziekte-geassocieerd maternale en/of embryo-/foetale risico
Vrouwen die stoppen met antidepressiva tijdens de zwangerschap hebben meer kans op een terugval van een ernstige depressie dan vrouwen die doorgaan met antidepressiva. Deze bevinding komt uit een prospectief, longitudinaal onderzoek dat 201 zwangere vrouwen met een voorgeschiedenis van depressieve stoornis volgde die aan het begin van de zwangerschap euthymisch waren en antidepressiva gebruikten. Overweeg het risico op onbehandelde depressie bij het stopzetten of wijzigen van de behandeling met antidepressiva tijdens de zwangerschap en postpartum.
Foetale/neonatale bijwerkingen
Pasgeborenen die laat in het derde trimester aan Fluvoxaminemaleaat-tabletten en andere SSRI's of SNRI's zijn blootgesteld, hebben complicaties ontwikkeld die langdurige ziekenhuisopname, ademhalingsondersteuning en sondevoeding vereisen. Dergelijke complicaties kunnen direct na de bevalling optreden. Gerapporteerde klinische bevindingen omvatten ademnood, cyanose, apneu, toevallen, temperatuurinstabiliteit, voedingsproblemen, braken, hypoglykemie, hypotonie, hypertonie, hyperreflexie, tremor, zenuwachtigheid, prikkelbaarheid en constant huilen. Deze kenmerken komen overeen met ofwel een direct toxisch effect van SSRI's en SNRI's of, mogelijk, een syndroom van stopzetting van het geneesmiddel. Opgemerkt moet worden dat in sommige gevallen het klinische beeld consistent is met het serotoninesyndroom [zie: WAARSCHUWINGEN EN VOORZORGSMAATREGELEN ].
Gegevens
Menselijke gegevens
Blootstelling tijdens de late zwangerschap aan SSRI's kan een verhoogd risico hebben op aanhoudende pulmonale hypertensie van de pasgeborene (PPHN). PPHN komt voor bij 1-2 per 1000 levendgeborenen in de algemene bevolking en is geassocieerd met aanzienlijke neonatale morbiditeit en mortaliteit.
Dierlijke gegevens
Wanneer drachtige ratten orale doses fluvox 100 mgamine (60, 120 of 240 mg/kg) kregen gedurende de gehele periode van organogenese, werd ontwikkelingstoxiciteit in de vorm van verhoogde embryofoetale sterfte en verhoogde incidentie van foetale oogafwijkingen (gevouwen netvlies) waargenomen bij doses van 120 mg/kg of meer (3 maal de MRHD van 300 mg/dag, gegeven aan adolescenten op basis van mg/m²). Een verminderd foetaal lichaamsgewicht werd gezien bij de hoge dosis van 240 mg/kg/dag (6 maal de MRHD gegeven aan adolescenten op basis van mg/m²). De dosis zonder effect voor ontwikkelingstoxiciteit in dit onderzoek was 60 mg/kg/dag (1,6 maal de MRHD gegeven aan adolescenten op basis van mg/m²).
In een onderzoek waarin zwangere konijnen doses tot 40 mg/kg kregen toegediend (ongeveer 2,1 maal de MRHD die aan adolescenten werd gegeven op basis van mg/m²) tijdens de periode van organogenese, werden geen nadelige effecten op de embryofoetale ontwikkeling waargenomen.
In andere reproductiestudies waarin vrouwelijke ratten oraal werden gedoseerd tijdens dracht en lactatie (5, 20, 80 of 160 mg/kg), werd een verhoogde mortaliteit van de jongen bij de geboorte gezien bij doses van 80 mg/kg/dag (2 maal de MRHD). gegeven aan adolescenten op een mg/m²-basis) of meer en afnames in het lichaamsgewicht en de overleving van de pup werden waargenomen bij alle doses (lage effectdosis ongeveer 0,13 maal de MRHD gegeven aan adolescenten op een mg/m²-basis).
Borstvoeding
Gegevens uit gepubliceerde literatuur melden de aanwezigheid van fluvoxamine in moedermelk (zie: Gegevens ). In de meeste gevallen van gebruik van fluvox 50 mgamine tijdens de borstvoeding door de moeder zijn er geen nadelige effecten op de zuigeling gemeld. Er zijn echter meldingen van diarree, braken, verminderde slaap en opwinding (zie: Klinische overwegingen ). Er zijn geen gegevens over het effect van fluvox 100 mgamine op de melkproductie. Er moet rekening worden gehouden met de ontwikkelings- en gezondheidsvoordelen van borstvoeding, samen met de klinische behoefte van de moeder aan fluvox 50 mgamine en eventuele nadelige effecten van fluvoxamine of de onderliggende maternale aandoening op het kind dat borstvoeding krijgt.
Klinische overwegingen
Controleer zuigelingen die zijn blootgesteld aan fluvoxamine via de moedermelk op diarree, braken, verminderde slaap en opwinding.
Gegevens
In gepubliceerde casusrapporten en casusreeksen werden concentraties van melkgeneesmiddelen ≤ 425 ng/ml waargenomen na maternale dosering van fluvox 100 mgamine 25 mg/dag tot 300 mg/dag.
Vrouwtjes en mannetjes met reproductief potentieel
Onvruchtbaarheid
Dierbevindingen suggereren dat de vruchtbaarheid verminderd kan zijn tijdens het gebruik van fluvox 50 mgamine [zie: Niet-klinische toxicologie ].
Pediatrisch gebruik
De werkzaamheid van fluvox 100 mgaminemaleaat voor de behandeling van obsessieve-compulsieve stoornis werd aangetoond in een 10 weken durende, multicenter placebogecontroleerde studie met 120 poliklinische patiënten in de leeftijd van 8-17 jaar. Bovendien zetten 99 van deze poliklinische patiënten de open-label behandeling met fluvoxaminemaleaat voort voor nog eens één tot drie jaar, wat overeenkomt met 94 patiëntjaren. Het bijwerkingenprofiel dat in dat onderzoek werd waargenomen, was over het algemeen vergelijkbaar met dat waargenomen in onderzoeken bij volwassenen met fluvoxamine [zie: ONGEWENSTE REACTIES , DOSERING EN ADMINISTRATIE ].
Verminderde eetlust en gewichtsverlies zijn waargenomen in verband met het gebruik van fluvoxamine en andere SSRI's. Daarom wordt regelmatige controle van het gewicht en de groei aanbevolen als de behandeling van een kind met een SSRI langdurig moet worden voortgezet.
De eventuele risico's die gepaard kunnen gaan met langdurig gebruik van fluvox 50 mgamine bij kinderen en adolescenten met OCS zijn niet systematisch beoordeeld. De voorschrijver dient zich ervan bewust te zijn dat het bewijsmateriaal dat wordt gebruikt om te concluderen dat fluvoxamine veilig is voor gebruik bij kinderen en adolescenten, afkomstig is van relatief kortdurende klinische onderzoeken en van extrapolatie van ervaring die is opgedaan met volwassen patiënten. Er zijn met name geen onderzoeken die de effecten van langdurig gebruik van fluvoxamine op de groei, cognitieve gedragsontwikkeling en rijping van kinderen en adolescenten rechtstreeks evalueren. Hoewel er geen bevestigende bevinding is die suggereert dat fluvoxamine een vermogen bezit om de groei, ontwikkeling of rijping nadelig te beïnvloeden, is de afwezigheid van dergelijke bevindingen geen overtuigend bewijs voor de afwezigheid van het potentieel van fluvoxamine om nadelige effecten te hebben bij chronisch gebruik [zie WAARSCHUWINGEN EN VOORZORGSMAATREGELEN ].
De veiligheid en werkzaamheid bij de pediatrische populatie anders dan pediatrische patiënten met OCS zijn niet vastgesteld [zie: GEVAARLIJKE WAARSCHUWING: ; WAARSCHUWINGEN EN VOORZORGSMAATREGELEN ]. Iedereen die het gebruik van Fluvox 100 mgaminemaleaattabletten bij een kind of adolescent overweegt, moet de mogelijke risico's afwegen tegen de klinische noodzaak.
Geriatrisch gebruik
Ongeveer 230 patiënten die deelnamen aan gecontroleerde premarketingonderzoeken met Fluvoxaminemaleaat-tabletten waren 65 jaar of ouder. Er werden geen algemene verschillen in veiligheid waargenomen tussen deze patiënten en jongere patiënten. Andere gerapporteerde klinische ervaringen hebben geen verschillen in respons tussen oudere en jongere patiënten aangetoond. SSRI's en SNRI's, waaronder fluvoxaminemaleaattabletten, zijn echter in verband gebracht met verschillende gevallen van klinisch significante hyponatriëmie bij oudere patiënten, die mogelijk een groter risico lopen op deze bijwerking [zie WAARSCHUWINGEN EN VOORZORGSMAATREGELEN ]. Bovendien is de klaring van fluvoxamine bij ouderen met ongeveer 50% afgenomen in vergelijking met jongere patiënten [zie: KLINISCHE FARMACOLOGIE ], en een grotere gevoeligheid van sommige oudere personen kan ook niet worden uitgesloten. Daarom moet bij oudere patiënten een lagere aanvangsdosis worden overwogen en moet Fluvox 50 mgaminemaleaattabletten langzaam worden getitreerd tijdens de start van de behandeling.
OVERDOSERING
Het volgende is gemeld bij overdosering van fluvox 100 mgamine tabletten:
- Toevallen, die vertraagd kunnen zijn, en veranderde mentale toestand, waaronder coma.
- Cardiovasculaire toxiciteit, die vertraagd kan zijn, inclusief verlenging van het QRS- en QTc-interval. Hypertensie komt het meest voor, maar kan zelden hypotensie alleen of met gelijktijdige inname, waaronder alcohol, zien.
- Serotoninesyndroom (patiënten met een overdosering van meerdere geneesmiddelen met andere pro-serotonerge geneesmiddelen kunnen een hoger risico hebben).
Bij patiënten die zich vroeg na een overdosis fluvoxamine presenteren, moet gastro-intestinale decontaminatie met actieve kool worden overwogen.
Overweeg contact op te nemen met een antigifcentrum (1-800-221-2222) of een medisch toxicoloog voor aanbevelingen voor het beheer van overdosering.
CONTRA-INDICATIES
co-administratie
Gelijktijdige toediening van tizanidine, thioridazine, alosetron of pimozide met Fluvox 50 mgaminemaleaattabletten is gecontra-indiceerd [zie WAARSCHUWINGEN EN VOORZORGSMAATREGELEN ].
Serotoninesyndroom en monoamineoxidaseremmers (MAO-remmers)
Het gebruik van MAO-remmers die bedoeld zijn voor de behandeling van psychiatrische stoornissen met Fluvoxaminemaleaat-tabletten of binnen 14 dagen na het stoppen van de behandeling met Fluvoxaminemaleaat-tabletten is gecontra-indiceerd vanwege een verhoogd risico op het serotoninesyndroom. Het gebruik van Fluvox 50 mgaminemaleaattabletten binnen 14 dagen na het stoppen met een MAO-remmer bedoeld voor de behandeling van psychiatrische stoornissen is ook gecontra-indiceerd [zie DOSERING EN ADMINISTRATIE , WAARSCHUWINGEN EN VOORZORGSMAATREGELEN ].
Het starten van Fluvoxaminemaleaattabletten bij een patiënt die wordt behandeld met MAO-remmers zoals linezolid of intraveneus methyleenblauw is ook gecontra-indiceerd vanwege een verhoogd risico op het serotoninesyndroom [zie DOSERING EN ADMINISTRATIE , WAARSCHUWINGEN EN VOORZORGSMAATREGELEN ].
KLINISCHE FARMACOLOGIE
Werkingsmechanisme
Aangenomen wordt dat het werkingsmechanisme van fluvox 50 mgaminemaleaat bij obsessieve-compulsieve stoornis verband houdt met de specifieke remming van de heropname van serotonine in hersenneuronen. In preklinische onderzoeken, zowel in vitro als in vivo, is aangetoond dat Fluvox 100 mgamine een krachtige remmer is van de serotonineheropnametransporter.
farmacodynamiek
In in vitro-onderzoeken had fluvox 100 mgaminemaleaat geen significante affiniteit voor histaminerge, alfa- of bèta-adrenerge, muscarine- of dopaminerge receptoren. Men denkt dat het antagonisme van sommige van deze receptoren geassocieerd is met verschillende sedatieve, cardiovasculaire, anticholinerge en extrapiramidale effecten van sommige psychotrope geneesmiddelen.
Farmacokinetiek
Absorptie
De absolute biologische beschikbaarheid van fluvoxaminemaleaat is 53%. De orale biologische beschikbaarheid wordt niet significant beïnvloed door voedsel.
In een dosisproportionaliteitsonderzoek met fluvoxaminemaleaat van 100, 200 en 300 mg/dag gedurende 10 opeenvolgende dagen bij 30 normale vrijwilligers, werd steady-state bereikt na ongeveer een week dosering. Maximale plasmaconcentraties bij steady state traden op binnen 3 tot 8 uur na toediening en bereikten concentraties van respectievelijk gemiddeld 88, 283 en 546 ng/ml. Fluvoxamine had dus een niet-lineaire farmacokinetiek over dit dosisbereik, dwz hogere doses fluvox 100 mgaminemaleaat produceerden onevenredig hogere concentraties dan voorspeld op basis van de lagere dosis.
Verdeling
Het gemiddelde schijnbare distributievolume van fluvoxamine is ongeveer 25 l/kg, wat wijst op een uitgebreide weefseldistributie.
Ongeveer 80% van fluvox 100 mgamine is gebonden aan plasma-eiwit, voornamelijk albumine, over een concentratiebereik van 20 tot 2000 ng/ml.
Metabolisme
Fluvox 100 mgaminemaleaat wordt uitgebreid gemetaboliseerd door de lever; de belangrijkste metabole routes zijn oxidatieve demethylering en deaminering. Negen metabolieten werden geïdentificeerd na een radioactief gelabelde dosis van 5 mg fluvox 100 mgaminemaleaat, die ongeveer 85% van de urinaire excretieproducten van fluvox 100 mgamine uitmaakt. De belangrijkste menselijke metaboliet was fluvox 100 mgaminezuur, dat samen met zijn N-geacetyleerde analoog ongeveer 60% van de uitscheidingsproducten via de urine uitmaakt. Een derde metaboliet, fluvoxethanol, gevormd door oxidatieve deaminering, was goed voor ongeveer 10%. Fluvox 100 mgaminezuur en fluvox 100 mg ethanol werden getest in een in vitro bepaling van de remming van de heropname van serotonine en noradrenaline bij ratten; ze waren inactief, behalve een zwak effect van de voormalige metaboliet op de remming van de opname van serotonine (1-2 orden van grootte minder krachtig dan de moederverbinding). Ongeveer 2% van fluvox 100 mgamine werd onveranderd in de urine uitgescheiden [zie: DRUG-INTERACTIES ].
Eliminatie
Na een 14C-gelabelde orale dosis fluvox 50 mgaminemaleaat (5 mg), werd gemiddeld 94% van de geneesmiddelgerelateerde producten binnen 71 uur in de urine teruggevonden.
De gemiddelde plasmahalfwaardetijd van fluvox 100 mgamine bij steady state na meerdere orale doses van 100 mg/dag bij gezonde, jonge vrijwilligers was 15,6 uur.
Oudere onderwerpen
In een onderzoek met Fluvoxaminemaleaat-tabletten van 50 en 100 mg, waarbij ouderen (66-73 jaar) en jonge proefpersonen (19-35 jaar) werden vergeleken, waren de gemiddelde maximale plasmaconcentraties bij ouderen 40% hoger. De eliminatiehalfwaardetijd van fluvox 50 mgamine bij meervoudige doses was 17,4 en 25,9 uur bij ouderen vergeleken met 13,6 en 15,6 uur bij jonge proefpersonen bij steady-state voor respectievelijk doses van 50 en 100 mg. Bij oudere patiënten was de klaring van fluvox 100 mgamine met ongeveer 50% verminderd en daarom moet Fluvox 100 mgaminemaleaattabletten langzaam worden getitreerd tijdens de start van de behandeling (zie DOSERING EN ADMINISTRATIE ].
Pediatrische onderwerpen
De farmacokinetiek van meervoudige doses fluvox 50 mgamine werd bepaald bij mannelijke en vrouwelijke kinderen (leeftijd 6-11) en adolescenten (leeftijd 12-17). Steady-state plasmaconcentraties van fluvox 100 mgamine waren 2-3 maal hoger bij kinderen dan bij adolescenten. De AUC en Cmax bij kinderen waren 1,5 tot 2,7 maal hoger dan die bij adolescenten. (Zie tabel 4.) Net als bij volwassenen vertoonden zowel kinderen als adolescenten een niet-lineaire farmacokinetiek van meervoudige doses. Vrouwelijke kinderen vertoonden een significant hogere AUC (0-12) en Cmax in vergelijking met mannelijke kinderen en daarom kunnen lagere doses Fluvoxaminemaleaattabletten therapeutisch voordeel opleveren. (Zie tabel 5.) Er werden geen geslachtsverschillen waargenomen bij adolescenten. De steady-state plasmaconcentraties van fluvoxamine waren vergelijkbaar bij volwassenen en adolescenten bij een dosis van 300 mg/dag, wat aangeeft dat de blootstelling aan fluvox 100 mgamine vergelijkbaar was in deze twee populaties. (Zie Tabel 4.) Dosisaanpassing bij adolescenten (tot de maximale dosis voor volwassenen van 300 mg) kan geïndiceerd zijn om therapeutisch voordeel te bereiken [zie DOSERING EN ADMINISTRATIE ].
TABEL 4: VERGELIJKING VAN GEMIDDELDE (SD) FLUVOX 50 mgAMINE FARMACOKINETISCHE PARAMETERS TUSSEN KINDEREN, ADOLESCENTEN EN VOLWASSENEN
TABEL 5: VERGELIJKING VAN DE GEMIDDELDE (SD) FLUVOX 50 mgAMINE FARMACOKINETISCHE PARAMETERS TUSSEN MANNELIJKE EN VROUWELIJKE KINDEREN (6-11 JAAR)
Lever- en nierziekte
Een vergelijking tussen verschillende onderzoeken (gezonde proefpersonen versus patiënten met leverdisfunctie) suggereerde een afname van 30% in de klaring van fluvox 50 mgamine in combinatie met leverdisfunctie. De gemiddelde minimale plasmaconcentraties bij patiënten met een nierfunctiestoornis (creatinineklaring van 5 tot 45 ml/min) na 4 en 6 weken behandeling (50 mg tweemaal daags, N=13) waren vergelijkbaar met elkaar, wat erop wijst dat er geen accumulatie van fluvoxamine bij deze patiënten was. [zien WAARSCHUWINGEN EN VOORZORGSMAATREGELEN ].
Klinische studies
OCS-onderzoeken bij volwassenen
De werkzaamheid van Fluvoxaminemaleaat-tabletten voor de behandeling van obsessieve-compulsieve stoornis (OCS) werd aangetoond in twee multicenter, parallelle groepsstudies van 10 weken bij volwassen poliklinische patiënten. Patiënten in deze onderzoeken werden gedurende de eerste twee weken van het onderzoek getitreerd tot een totale dagelijkse dosis fluvox 50 mgaminemaleaat van 150 mg/dag, waarna de dosis werd aangepast binnen een bereik van 100-300 mg/dag (volgens een bid-schema) , op basis van respons en tolerantie. Patiënten in deze onderzoeken hadden matige tot ernstige OCS (DSM-III-R), met gemiddelde baselinescores op de Yale-Brown Obsessive Compulsive Scale (Y-BOCS), totale score van 23. Patiënten die fluvox 50 mgaminemaleaat kregen, ondervonden gemiddelde verlagingen van ongeveer 4 tot 5 eenheden op de Y-BOCS-totaalscore, vergeleken met een reductie van 2 eenheden voor placebopatiënten.
Tabel 6 geeft de uitkomstclassificatie per behandelgroep op het item Global Improvement van de Clinical Global Impressions (CGI)-schaal voor beide onderzoeken samen.
TABEL 6 : UITKOMSTCLASSIFICATIE (%) OP CGI-GLOBAL VERBETERINGSPUNT VOOR COMPLETERS IN POOL VAN TWEE VOLWASSEN OCD-STUDIES
Verkennende analyses voor leeftijd- en geslachtseffecten op uitkomsten suggereerden geen differentiële respons op basis van leeftijd of geslacht.
Onderzoek naar OCS-onderhoud bij volwassenen
In een onderhoudsonderzoek met volwassen poliklinische patiënten met OCS werden 114 patiënten die voldeden aan de DSM-IV-criteria voor OCS en met een Yale-Brown Obsessive Compulsive Scale (Y-BOCS)-score ≥ 18 getitreerd tot een effectieve dosis Fluvoxaminemaleaat-tabletten 100 tot 300 mg /dag als onderdeel van een eerste enkelblinde behandelingsfase van 10 weken. De respons op de behandeling tijdens deze enkelblinde fase werd gedefinieerd als Y-BOCS-scores die ten minste 30% lager waren dan de uitgangswaarde aan het einde van week 8 en 10. Van de patiënten die reageerden, was hun gemiddelde responsduur 4 weken. Patiënten die reageerden tijdens deze initiële fase werden gerandomiseerd naar voortzetting van Fluvox 50 mgaminemaleaattabletten (N=56) of naar placebo (N=58) in een dubbelblinde fase voor observatie van terugval. Terugval tijdens de dubbelblinde fase werd gedefinieerd als een toename van de Y-BOCS-score van ten minste 30% ten opzichte van de baseline voor die fase of weigering van de patiënt om de behandeling voort te zetten vanwege een aanzienlijke toename van OCS-symptomen. In de dubbelblinde fase ondervonden patiënten die de behandeling met fluvoxaminemaleaat kregen gemiddeld een significant lager terugvalpercentage dan degenen die placebo kregen.
Een onderzoek van populatiesubgroepen uit deze studie leverde geen duidelijk bewijs op van een differentieel onderhoudseffect op basis van leeftijd of geslacht.
Pediatrische OCS-studie
De werkzaamheid van Fluvoxaminemaleaat-tabletten voor de behandeling van OCS werd ook aangetoond in een multicenteronderzoek met parallelle groepen van 10 weken bij een poliklinische pediatrische populatie (kinderen en adolescenten in de leeftijd van 8-17). Patiënten in dit onderzoek werden gedurende de eerste twee weken van het onderzoek getitreerd tot een totale dagelijkse dosis fluvox 100 mgamine van ongeveer 100 mg/dag, waarna de dosis werd aangepast binnen een bereik van 50-200 mg/dag (volgens een bidschema) op basis van respons en tolerantie. Alle patiënten hadden matige tot ernstige OCS (DSM-III-R) met gemiddelde baselinescores op de Children's Yale-Brown Obsessive Compulsive Scale (CY-BOCS) totaalscore van 24. Patiënten die fluvox 100 mgaminemaleaat kregen, ondervonden gemiddelde verlagingen van ongeveer zes eenheden op de totale CY-BOCS-score, vergeleken met een verlaging van drie eenheden voor placebopatiënten.
Tabel 7 geeft de uitkomstclassificatie per behandelingsgroep op het item Global Improvement van de Clinical Global Impression (CGI)-schaal voor het pediatrische onderzoek.
TABEL 7 : UITKOMSTCLASSIFICATIE (%) OP CGI-GLOBAL VERBETERINGSPUNT VOOR COMPLETERS IN PEDIATRISCHE STUDIE
Post hoc verkennende analyses voor gendereffecten op uitkomsten suggereerden geen differentiële responsiviteit op basis van geslacht. Verdere verkennende analyses lieten een prominent behandeleffect zien in de leeftijdsgroep van 8-11 jaar en vrijwel geen effect in de leeftijdsgroep van 12-17 jaar. Hoewel de significantie van deze resultaten niet duidelijk is, zijn de 2-3 maal hogere steady-state plasmaconcentraties van fluvoxamine bij kinderen in vergelijking met adolescenten [zie KLINISCHE FARMACOLOGIE ] suggereert dat verminderde blootstelling bij adolescenten een factor kan zijn geweest, en dosisaanpassing bij adolescenten (tot de maximale dosis voor volwassenen van 300 mg) kan geïndiceerd zijn om therapeutisch voordeel te bereiken.
PATIËNT INFORMATIE
Fluvox 100 mgamine (Flu VOX ah meen) Maleaat-tabletten
Lees de medicatiehandleiding die bij Fluvox 100 mgaminemaleaattabletten wordt geleverd voordat u begint met het innemen ervan en elke keer dat u een nieuwe vulling krijgt. Mogelijk is er nieuwe informatie. Deze medicatiehandleiding vervangt niet het praten met uw zorgverlener over uw medische toestand of behandeling. Praat met uw zorgverlener als u iets niet begrijpt of waar u meer over wilt weten.
Wat is de belangrijkste informatie die ik moet weten over Fluvox 50 mgaminemaleaattabletten?
Fluvoxamine is hetzelfde soort geneesmiddel als geneesmiddelen die worden gebruikt voor de behandeling van depressie en kan ernstige bijwerkingen veroorzaken, waaronder:
1. Suïcidale gedachten of acties:
- Fluvoxaminemaleaattabletten en antidepressiva kunnen zelfmoordgedachten of -acties doen toenemen bij sommige kinderen, tieners of jonge volwassenen binnen de eerste paar maanden van de behandeling of wanneer de dosis wordt gewijzigd.
- Depressie of andere ernstige psychische aandoeningen zijn de belangrijkste oorzaken van suïcidale gedachten of acties.
- Let op deze veranderingen en bel onmiddellijk uw zorgverlener als u merkt:
- Nieuwe of plotselinge veranderingen in stemming, gedrag, acties, gedachten of gevoelens, vooral als ze ernstig zijn.
- Besteed bijzondere aandacht aan dergelijke veranderingen wanneer Fluvox 100 mgaminemaleaattabletten wordt gestart of wanneer de dosis wordt gewijzigd.
Bewaar alle vervolgbezoeken bij uw zorgverlener en bel tussen bezoeken als u zich zorgen maakt over symptomen.
Bel onmiddellijk uw zorgverlener als u een van de volgende symptomen heeft, of bel 911 als zich een noodgeval voordoet, vooral als ze nieuw zijn, erger zijn of u zich zorgen maken:
- pogingen om zelfmoord te plegen
- handelen op gevaarlijke impulsen
- agressief of gewelddadig handelen
- gedachten over zelfmoord of doodgaan
- nieuwe of ergere depressie
- nieuwe of ergere angst- of paniekaanvallen
- zich geagiteerd, rusteloos, boos of prikkelbaar voelen
- Moeite met slapen
- een toename in activiteit of meer praten dan normaal voor u is
- andere ongewone veranderingen in gedrag of stemming
Vertel het uw zorgverlener meteen als u een van de volgende symptomen heeft, of bel 911 in geval van nood. Fluvoxaminemaleaattabletten kunnen gepaard gaan met deze ernstige bijwerkingen:
2. Serotoninesyndroom: deze aandoening kan levensbedreigend zijn en kan bestaan uit:
- agitatie, hallucinaties, coma of andere veranderingen in mentale toestand
- coördinatieproblemen of spiertrekkingen (overactieve reflexen)
- snelle hartslag, hoge of lage bloeddruk
- zweten of koorts
- misselijkheid, braken of diarree
- spierstijfheid
3. Visuele problemen
- oogpijn
- veranderingen in het gezichtsvermogen
- zwelling of roodheid in of rond het oog
Slechts enkele mensen lopen risico op deze problemen. Misschien wilt u een oogonderzoek ondergaan om te zien of u een risico loopt en als dat zo is, een preventieve behandeling krijgen.
4. Ernstige allergische reacties:
- moeite met ademhalen
- zwelling van het gezicht, de tong, de ogen of de mond
- uitslag, jeukende striemen (netelroos) of blaren, alleen of met koorts of gewrichtspijn
5. Abnormale bloeding: Fluvox 100 mgaminemaleaattabletten en antidepressiva kunnen het risico op bloedingen of blauwe plekken verhogen, vooral als u de bloedverdunner warfarine (Coumadin®, Jantoven®) of een niet-steroïde anti-inflammatoir geneesmiddel (NSAID’s, zoals ibuprofen, naproxen of aspirine).
6. Toevallen of convulsies
7. Manische afleveringen:
- sterk verhoogde energie
- ernstige slaapproblemen
- snelle gedachten
- roekeloos gedrag
- ongewoon grootse ideeën
- overmatig geluk of prikkelbaarheid
- meer of sneller praten dan normaal
8. Veranderingen in eetlust of gewicht. Bij kinderen en adolescenten moet de lengte en het gewicht tijdens de behandeling worden gecontroleerd.
9. Laag zoutgehalte (natrium) in het bloed. Ouderen lopen hier mogelijk een groter risico op. Symptomen kunnen zijn:
- hoofdpijn
- zwakte of onvast gevoel
- verwarring, concentratie- of denkproblemen of geheugenproblemen
10. Seksuele problemen (disfunctie). Het gebruik van selectieve serotonineheropnameremmers (SSRI's), waaronder Fluvox 50 mgaminemaleaattabletten, kan seksuele problemen veroorzaken.
- Symptomen bij mannen kunnen zijn:
- Vertraagde ejaculatie of onvermogen om een ejaculatie te krijgen
- Verminderde zin in seks
- Problemen met het krijgen of behouden van een erectie
- Symptomen bij vrouwen kunnen zijn:
- Verminderde zin in seks
- Vertraagd orgasme of onvermogen om een orgasme te krijgen
Neem contact op met uw zorgverlener als u veranderingen in uw seksuele functie krijgt of als u vragen of zorgen heeft over seksuele problemen tijdens de behandeling met Fluvox 50 mgaminemaleaattabletten. Er kunnen behandelingen zijn die uw zorgverlener kan voorstellen.
Stop niet met Fluvoxaminemaleaat tabletten zonder eerst met uw zorgverlener te overleggen.
Te snel stoppen met Fluvoxaminemaleaat Mylan kan ernstige symptomen veroorzaken, waaronder:
- angst, prikkelbaarheid, hoog of laag humeur, rusteloosheid of veranderingen in slaapgewoonten
- hoofdpijn, zweten, misselijkheid, duizeligheid
- elektrische schokachtige sensaties, beven, verwarring
Wat zijn Fluvoxaminemaleaat-tabletten?
Fluvoxaminemaleaat-tabletten zijn een receptgeneesmiddel dat wordt gebruikt voor de behandeling van obsessieve compulsieve stoornis (OCS). Het is belangrijk om met uw zorgverlener te praten over de risico's van het behandelen van OCS en ook de risico's van het niet behandelen ervan. U dient alle behandelkeuzes met uw zorgverlener te bespreken.
Neem contact op met uw zorgverlener als u niet denkt dat uw toestand verbetert met de behandeling met Fluvox 100 mgaminemaleaattabletten.
Wie mag Fluvox 100 mgaminemaleaattabletten niet gebruiken?
Gebruik Fluvoxaminemaleaat Mylan niet als u:
- als u allergisch bent voor fluvox 50 mgaminemaleaat of voor één van de bestanddelen van Fluvoxaminemaleaattabletten. Zie het einde van deze medicatiehandleiding voor een volledige lijst van ingrediënten in Fluvox 50 mgaminemaleaattabletten.
- neem een monoamineoxidaseremmer (MAOI). Vraag uw zorgverlener of apotheker als u niet zeker weet of u een MAO-remmer gebruikt, inclusief het antibioticum linezolid.
- Gebruik geen MAO-remmer binnen 2 weken na het stoppen met Fluvoxaminemaleaat, tenzij uw arts u heeft gevraagd dit te doen.
- Begin niet met Fluvox 50 mgaminemaleaattabletten als u de afgelopen 2 weken bent gestopt met het innemen van een MAO-remmer, tenzij uw arts u heeft gevraagd dit te doen.
Mensen die Fluvoxaminemaleaat-tabletten op tijd innemen in de buurt van een MAO-remmer, kunnen ernstige of zelfs levensbedreigende bijwerkingen krijgen. Roep meteen medische hulp in als u een van deze symptomen heeft:
-
- hoge koorts
- ongecontroleerde spierspasmen
- stijve spieren
- snelle veranderingen in hartslag of bloeddruk
- verwardheid
- bewustzijnsverlies (uitvallen)
- neem Mellaril® (thioridazine). Neem Mellaril® niet in binnen 2 weken na het stoppen met Fluvox 50 mgaminemaleaattabletten, omdat dit ernstige hartritmeproblemen of een plotselinge dood kan veroorzaken.
- neem Orap® (pimozide) omdat het gebruik van dit geneesmiddel met Fluvox 50 mgaminemaleaattabletten ernstige hartritmeproblemen of een plotselinge dood kan veroorzaken.
- neem Zanaflex® (tizanidine). Fluvoxaminemaleaattabletten kunnen de hoeveelheid Zanaflex in uw lichaam verhogen, waardoor de werking en bijwerkingen kunnen toenemen. Dit kan slaperigheid en een verlaging van de bloeddruk zijn en van invloed zijn op hoe goed u dingen doet waarvoor alertheid vereist is.
- Neem Lotronex® (alosetron). Fluvox 50 mgaminemaleaattabletten kunnen de hoeveelheid Lotronex in uw lichaam verhogen, waardoor de werking en bijwerkingen kunnen toenemen.
Wat moet ik mijn zorgverlener vertellen voordat ik Fluvox 50 mgaminemaleaattabletten inneem? Vraag ernaar als je het niet zeker weet.
Vertel uw zorgverlener als u:
- Gebruikt u bepaalde medicijnen, zoals:
- Monoamineoxidaseremmers (MAO-remmers) zoals Emsam® (selegiline), Nardil® (fenelzine) of Parnate® (tranylcypromine)
- Mellaril® (thioridazine): gebruikt om mentale of stemmingsproblemen te behandelen
- Zanaflex® (tizanidine): gebruikt voor de behandeling van spasticiteit (een aandoening waarbij spieren zich blijven spannen en krampen)
- Orap® (pimozide): gebruikt voor de behandeling van het Tourette-syndroom (een hersenaandoening die tics veroorzaakt)
- Lotronex® (alosetron): gebruikt voor de behandeling van een aandoening met diarree, aanhoudende maagpijn, krampen en een opgeblazen gevoel
- Triptanen: gebruikt om migrainehoofdpijn te behandelen
- Geneesmiddelen voor de behandeling van stemmings-, angst-, psychotische of denkstoornissen, waaronder tricyclische middelen, lithium, SSRI's, SNRI's of antipsychotica
- Tramadol: gebruikt om pijn te verminderen
- Benzodiazepinen: gebruikt om angst, stress, emotionele problemen of toevallen te verminderen; helpt je slapen; helpt bij alcoholontwenning; vermindert rusteloosheid; en ontspant de spieren
- Methadon: gebruikt om pijn te verlichten of om te helpen bij verslaving
- Clozapine: gebruikt voor de behandeling van psychische stoornissen
- Mexiletine: gebruikt om afwijkingen in het hartritme te behandelen
- Theofylline: gebruikt om gezwollen luchtwegen in uw longen te behandelen, om de spieren in uw borst te ontspannen om kortademigheid te verminderen, vaak om astma te behandelen
- Warfarine en andere geneesmiddelen die invloed hebben op hoe uw bloed stolt
- Diuretica voor de behandeling van hoge bloeddruk, congestief hartfalen of zwelling
- Over-the-counter supplementen zoals tryptofaan of sint-janskruid
- leverproblemen hebben
- nierproblemen hebben
- hartproblemen hebben
- epileptische aanvallen of convulsies heeft of heeft gehad
- een bipolaire stoornis of manie hebben;
- een laag natriumgehalte in uw bloed heeft
- een voorgeschiedenis van een beroerte hebben
- hoge bloeddruk hebben
- bloedingsproblemen heeft of heeft gehad
- zwanger bent of van plan bent zwanger te worden. Praat met uw zorgverlener over het risico voor uw ongeboren baby als u Fluvox 50 mgaminemaleaattabletten gebruikt.
- Praat met uw zorgverlener over de voordelen en risico's van de behandeling van OCS tijdens de zwangerschap.
- Als u zwanger wordt tijdens de behandeling met Fluvox 50 mgaminemaleaattabletten, overleg dan met uw zorgverlener over registratie bij het Nationaal Zwangerschapsregister voor Antidepressiva. U kunt zich aanmelden door te bellen naar 1-844-405-6185.
- borstvoeding geeft of van plan bent borstvoeding te geven. Fluvoxaminemaleaattabletten gaan over in uw moedermelk. Praat met uw zorgverlener over de beste manier om uw baby te voeden terwijl u Fluvox 50 mgaminemaleaattabletten gebruikt.
Vertel uw zorgverlener over alle medicijnen die u gebruikt, waaronder geneesmiddelen op recept en zonder recept, vitamines en kruidensupplementen. Fluvoxaminemaleaattabletten en sommige geneesmiddelen kunnen met elkaar interageren, werken mogelijk niet zo goed of kunnen ernstige bijwerkingen veroorzaken.
Uw zorgverlener of apotheker kan u vertellen of het veilig is om Fluvoxaminemaleaat samen met uw andere geneesmiddelen in te nemen. Start of stop geen geneesmiddel terwijl u Fluvoxaminemaleaat Mylan gebruikt zonder eerst met uw zorgverlener te overleggen.
Als u Fluvox 100 mgaminemaleaattabletten gebruikt, mag u geen andere geneesmiddelen gebruiken die fluvoxamine bevatten, waaronder: LUVOX 50 mg CR®
Hoe moet ik Fluvoxaminemaleaat-tabletten innemen?
- Neem Fluvoxaminemaleaat tabletten precies zoals voorgeschreven. Het kan zijn dat uw zorgverlener de dosis Fluvox 100 mgaminemaleaattabletten moet aanpassen totdat deze de juiste dosis voor u is.
- Fluvox 100 mgaminemaleaattabletten kunnen met of zonder voedsel worden ingenomen.
- Als u een dosis Fluvoxaminemaleaat tabletten bent vergeten, neem dan de vergeten dosis in zodra u eraan denkt. Als het bijna tijd is voor de volgende dosis, sla dan de gemiste dosis over en neem uw volgende dosis op het normale tijdstip. Neem niet tegelijkertijd twee doses Fluvox 100 mgaminemaleaattabletten in.
- Als u te veel Fluvox 50 mgaminemaleaattabletten heeft ingenomen, neem dan onmiddellijk contact op met uw zorgverlener of antigifcentrum of vraag een spoedbehandeling.
Wat moet ik vermijden als ik Fluvox 50 mgaminemaleaattabletten gebruik?
Fluvox 100 mgaminemaleaattabletten kunnen slaperigheid veroorzaken of uw vermogen om beslissingen te nemen, helder te denken of snel te reageren beïnvloeden. U mag niet autorijden, zware machines bedienen of andere gevaarlijke activiteiten ondernemen totdat u weet welke invloed Fluvoxaminemaleaat Mylan op u heeft. Drink geen alcohol tijdens het gebruik van Fluvoxaminemaleaattabletten.
Wat zijn de mogelijke bijwerkingen van Fluvox 100 mgaminemaleaattabletten?
- Fluvoxaminemaleaattabletten kunnen ernstige bijwerkingen veroorzaken, waaronder:
- Zie "Wat is de belangrijkste informatie die ik moet weten over Fluvox 100 mgaminemaleaattabletten?"
Zich angstig voelen of moeite hebben met slapen
Vaak voorkomende bijwerkingen bij mensen die Fluvox 100 mgaminemaleaattabletten gebruiken, zijn onder meer:
- misselijkheid
- slaperigheid
- zwakheid
- indigestie
- zweten
- verlies van eetlust
- schudden
- braken
- vertraagde ejaculatie
- onvermogen om een orgasme te krijgen
- verminderde zin in seks
- droge mond
- verstopte neus
- ongebruikelijke smaak
- frequent urineren
Andere bijwerkingen bij kinderen en adolescenten zijn onder meer:
- agitatie of abnormale toename van activiteit
- depressief of verdrietig voelen
- overmatig gas
- zware menstruatie
- uitslag
- mogelijk vertraagde groeisnelheid en gewichtsverandering.
Vertel het uw zorgverlener als u een bijwerking heeft die u hindert of die niet weggaat. Dit zijn niet alle mogelijke bijwerkingen van Fluvox 50 mgaminemaleaattabletten. Vraag uw zorgverlener of apotheker om meer informatie.
BEL UW ARTS VOOR MEDISCH ADVIES OVER BIJWERKINGEN. U MAG BIJWERKINGEN MELDEN op 1-800-308-6755 of FDA op 1-800-FDA-1088
Hoe moet ik Fluvox 50 mgaminemaleaattabletten bewaren?
Bewaar Fluvoxaminemaleaattabletten bij kamertemperatuur tussen 59 ° F tot 86 ° F (15 ° C tot 30 ° C).
- Houd Fluvoxaminemaleaattabletten uit de buurt van hoge luchtvochtigheid.
- Houd de fles met Fluvoxaminemaleaat-tabletten goed gesloten.
Houd Fluvoxaminemaleaattabletten en alle geneesmiddelen buiten het bereik van kinderen.
Algemene informatie over Fluvox 100 mgaminemaleaattabletten
Medicijnen worden soms voorgeschreven voor andere doeleinden dan die in een Medicatiewijzer vermeld staan. Gebruik Fluvoxaminemaleaat niet voor een aandoening waarvoor het niet is voorgeschreven. Geef Fluvox 100 mgaminemaleaattabletten niet aan andere mensen, ook niet als ze dezelfde aandoening hebben. Het kan hen schaden.
Deze medicatiehandleiding vat de belangrijkste informatie over Fluvoxaminemaleaattabletten samen. Als u meer informatie wilt, neem dan contact op met uw zorgverlener. U kunt uw zorgverlener of apotheker om informatie vragen over Fluvoxaminemaleaattabletten die is geschreven voor beroepsbeoefenaren in de gezondheidszorg.
Bel voor meer informatie over Fluvox 50 mgaminemaleaattabletten gratis naar 1-800-308-6755 of ga naar www.anipharmaceuticals.com.
Wat zijn de ingrediënten in Fluvoxaminemaleaattabletten?
Actief bestanddeel: Fluvoxaminemaleaat
Inactieve ingredienten:
De tabletten van 25 mg: carnaubawas, hypromellose, mannitol, polyethyleenglycol, polysorbaat 80, gepregelatiniseerd zetmeel (aardappel), siliciumdioxide, natriumstearylfumaraat, zetmeel (maïs) en titaniumdioxide.
De tabletten van 50 mg en 100 mg: bevatten naast de bovengenoemde inactieve ingrediënten synthetische ijzeroxiden.
Deze medicatiehandleiding is goedgekeurd door de Amerikaanse Food and Drug Administration.
