Elavil 10mg, 25mg, 50mg Amitriptyline Gebruik, bijwerkingen en dosering. Prijs in online apotheek. Generieke medicijnen zonder recept.
Wat is Elavil en hoe wordt het gebruikt?
Elavil 10 mg is een receptgeneesmiddel dat wordt gebruikt om de symptomen van angst of agitatie met depressie en schizofrenie met depressie te behandelen. Elavil kan alleen of in combinatie met andere medicijnen worden gebruikt.
Elavil behoort tot een klasse geneesmiddelen die psychotherapeutische combo's worden genoemd.
Het is niet bekend of Elavil veilig en effectief is bij kinderen.
Wat zijn de mogelijke bijwerkingen van Elavil 25 mg?
Elavil kan ernstige bijwerkingen veroorzaken, waaronder:
- gemakkelijk blauwe plekken of bloedingen,
- aanhoudend brandend maagzuur,
- schudden,
- maskerachtige gezichtsuitdrukkingen,
- spiertrekkingen,
- ernstige maagpijn,
- verminderd seksueel verlangen,
- vergrote of pijnlijke borsten,
- zwarte ontlasting,
- braaksel dat op koffiedik lijkt,
- ernstige duizeligheid,
- flauwvallen,
- toevallen,
- oogpijn, roodheid of zwelling,
- visie verandert,
- koorts,
- Spierstijfheid,
- ernstige verwarring,
- zweten, en
- snelle of onregelmatige hartslag
Roep meteen medische hulp in als u een van de bovenstaande symptomen heeft.
De meest voorkomende bijwerkingen van Elavil zijn:
- slaperigheid,
- duizeligheid,
- droge mond,
- wazig zien,
- constipatie,
- gewichtstoename, en
- moeite met urineren
Vertel het uw arts als u een bijwerking heeft die u hindert of die niet weggaat.
Dit zijn niet alle mogelijke bijwerkingen van Elavil. Vraag uw arts of apotheker om meer informatie.
Bel uw arts voor medisch advies over bijwerkingen. U kunt bijwerkingen melden aan de FDA op 1-800-FDA-1088.
Suïcidaliteit en antidepressiva
Antidepressiva verhoogden het risico op suïcidaal denken en gedrag (suïcidaliteit) bij kinderen, adolescenten en jonge volwassenen in kortdurende onderzoeken naar depressieve stoornis (MDD) en andere psychiatrische stoornissen, vergeleken met placebo. Iedereen die het gebruik van amitriptylinehydrochloride-tabletten of een ander antidepressivum bij een kind, adolescent of jongvolwassene overweegt, moet dit risico afwegen tegen de klinische noodzaak. Kortdurende onderzoeken lieten geen toename zien van het risico op suïcidaliteit bij gebruik van antidepressiva in vergelijking met placebo bij volwassenen ouder dan 24 jaar; er was een vermindering van het risico met antidepressiva vergeleken met placebo bij volwassenen van 65 jaar en ouder. Depressie en bepaalde andere psychiatrische stoornissen zijn zelf geassocieerd met een verhoogd risico op zelfmoord. Patiënten van alle leeftijden die beginnen met een behandeling met antidepressiva, moeten op de juiste manier worden gecontroleerd en nauwlettend worden geobserveerd op klinische verergering, suïcidaliteit of ongewone gedragsveranderingen. Families en zorgverleners moeten worden geïnformeerd over de noodzaak van nauwgezette observatie en communicatie met de voorschrijver. Amitriptylinehydrochloride-tabletten zijn niet goedgekeurd voor gebruik bij pediatrische patiënten (zie WAARSCHUWINGEN: Klinische verslechtering en zelfmoordrisico, PATINTINFORMATIE en VOORZORGSMAATREGELEN: Gebruik bij kinderen .)
OMSCHRIJVING
Amitriptyline HCl is 3-(10,11-dihydro-5H-dibenzo[a,d]cyclohepteen-5-ylideen)-N,N-dimethyl-1-propaanaminehydrochloride. De empirische formule is C20H23N•HCl en de structuurformule is:
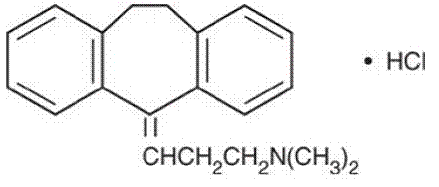
Amitriptyline HCl, een dibenzocycloheptadieenderivaat, heeft een molecuulgewicht van 313,87. Het is een witte, geurloze, kristallijne verbinding die goed oplosbaar is in water.
Amitriptyline HCl wordt geleverd als tabletten van 10 mg, 25 mg, 50 mg, 75 mg, 100 mg of 150 mg. Elke tablet bevat de volgende inactieve ingrediënten: colloïdaal siliciumdioxide, hypromellose, lactosemonohydraat, magnesiumstearaat, microkristallijne cellulose, polyethyleenglycol, polysorbaat, natriumzetmeelglycolaat en titaniumdioxide. De tabletten van 10 mg bevatten ook FD&C blue #1 lake. De tabletten van 25 mg bevatten ook D&C yellow #10 lake en FD&C blue #2 lake. De tabletten van 50 mg bevatten ook synthetisch zwart ijzeroxide, synthetisch rood ijzeroxide en synthetisch geel ijzeroxide. De 75 mg tabletten bevatten ook FD&C geel #6 lak. De tabletten van 100 mg bevatten ook D&C rood #33 meer en FD&C rood #40 meer. De tabletten van 150 mg bevatten ook FD&C blue #2 lake en FD&C yellow #6 lake.
INDICATIES
Voor de verlichting van symptomen van depressie. Endogene depressie zal eerder worden verlicht dan andere depressieve toestanden.
DOSERING EN ADMINISTRATIE
De dosering moet op een laag niveau worden gestart en geleidelijk worden verhoogd, waarbij zorgvuldig moet worden gelet op de klinische respons en eventuele aanwijzingen voor intolerantie.
Initiële dosering voor volwassenen
Voor poliklinische patiënten is 75 mg amitriptyline HCl per dag in verdeelde doses gewoonlijk voldoende. Indien nodig kan dit worden verhoogd tot in totaal 150 mg per dag. Verhogingen worden bij voorkeur in de late namiddag en/of het slapengaan aangebracht. Een sedatief effect kan duidelijk zijn voordat het antidepressieve effect wordt opgemerkt, maar een adequaat therapeutisch effect kan tot 30 dagen duren voordat het zich ontwikkelt.
Een alternatieve methode om de therapie bij poliklinische patiënten te starten, is om te beginnen met 50 tot 100 mg amitriptyline HCl voor het slapengaan. Dit kan zo nodig worden verhoogd met 25 of 50 mg in de dosis voor het slapengaan tot een totaal van 150 mg per dag.
In het ziekenhuis opgenomen patiënten kunnen aanvankelijk 100 mg per dag nodig hebben. Indien nodig kan dit geleidelijk worden verhoogd tot 200 mg per dag. Een klein aantal gehospitaliseerde patiënten kan wel 300 mg per dag nodig hebben.
Adolescente en oudere patiënten
Over het algemeen worden voor deze patiënten lagere doseringen aanbevolen. Driemaal daags tien mg met 20 mg voor het slapengaan kan voldoende zijn bij adolescente en oudere patiënten die geen hogere doseringen verdragen.
Onderhoud
De gebruikelijke onderhoudsdosering van amitriptyline HCl is 50 tot 100 mg per dag. Bij sommige patiënten is 40 mg per dag voldoende. Voor onderhoudstherapie kan de totale dagelijkse dosering in een enkele dosis worden gegeven, bij voorkeur voor het slapengaan. Wanneer een bevredigende verbetering is bereikt, moet de dosering worden verlaagd tot de laagste hoeveelheid die verlichting van de symptomen handhaaft. Het is aangewezen om de onderhoudstherapie 3 maanden of langer voort te zetten om de kans op terugval te verkleinen.
Gebruik bij pediatrische patiënten
Gezien het gebrek aan ervaring met het gebruik van dit geneesmiddel bij pediatrische patiënten, wordt het momenteel niet aanbevolen voor patiënten jonger dan 12 jaar.
Plasmaniveaus
Vanwege de grote variatie in de absorptie en distributie van tricyclische antidepressiva in lichaamsvloeistoffen, is het moeilijk om plasmaspiegels en therapeutisch effect direct te correleren. Het bepalen van plasmaspiegels kan echter nuttig zijn bij het identificeren van patiënten die toxische effecten lijken te hebben en mogelijk te hoge spiegels hebben, of patiënten bij wie een gebrek aan absorptie of niet-naleving wordt vermoed. Vanwege de langere darmpassagetijd en het verminderde levermetabolisme bij oudere patiënten, zijn de plasmaspiegels over het algemeen hoger voor een gegeven orale dosis amitriptylinehydrochloride dan bij jongere patiënten.
Oudere patiënten moeten zorgvuldig worden gecontroleerd en kwantitatieve serumspiegels moeten worden verkregen zoals klinisch aangewezen. Dosering dient te worden aangepast op basis van de klinische respons van de patiënt en niet op basis van plasmaspiegels.**
HOE GELEVERD
10 mg tabletten zijn blauwe, ronde, filmomhulde tabletten zonder breuklijn, met de inscriptie "2101" aan de ene kant en de inscriptie "V" aan de andere kant. Ze worden als volgt geleverd:
Flessen van 30: NDC 0603-2212-16 Flessen van 90: NDC 0603-2212-02 Flessen van 100: NDC 0603-2212-21 Flessen van 1000: NDC 0603-2212-32
25 mg tabletten zijn gele, ronde, filmomhulde tabletten zonder breuklijn, met de inscriptie "2102" aan de ene kant en de inscriptie "V" aan de andere kant. Ze worden als volgt geleverd:
Flessen van 90: NDC 0603-2213-02 Flessen van 100: NDC 0603-2213-21 Flessen van 1000: NDC 0603-2213-32 Flessen van 2500: NDC 0603-2213-30
50 mg tabletten zijn beige, ronde, filmomhulde tabletten zonder breuklijn, met de inscriptie "2103" aan de ene kant en de inscriptie "V" aan de andere kant. Ze worden als volgt geleverd:
Flessen van 100: NDC 0603-2214-21 Flessen van 1000: NDC 0603-2214-32
75 mg tabletten zijn oranje, ronde, niet-gescoorde, filmomhulde tabletten, met de inscriptie "2104" en "V". Ze worden als volgt geleverd:
Flessen van 100: NDC 0603-2215-21 Flessen van 300: NDC 0603-2215-25
100 mg tabletten zijn mauve, ronde, niet-gescoorde, filmomhulde tabletten, met de inscriptie "2105" en "V". Ze worden als volgt geleverd:
Flessen van 100: NDC 0603-2216-21 Flessen van 300: NDC 0603-2216-25
150 mg tabletten zijn blauwe, capsulevormige, filmomhulde tabletten zonder breuklijn, met de inscriptie "2106" aan de ene kant en de inscriptie "V" aan de andere kant. Ze worden als volgt geleverd:
Flessen van 100: NDC 0603-2217-21 Flessen van 300: NDC 0603-2217-25
Opslag en behandeling
Opslag
Bewaren in een goed gesloten container. Bewaren bij 20°-25°C (68°-77°F) [zie USP-gecontroleerde kamertemperatuur ]. Bovendien moeten amitriptyline-tabletten worden beschermd tegen licht en worden bewaard in een goed gesloten, lichtbestendige container
REFERENTIES
Ayd FJ Jr: Amitriptyline-therapie voor depressieve reacties. Psychosomatiek 1960; 1:320-325.
Diamond S: Menselijke metaboliseerder van amitriptyline gelabeld met koolstof 14. Curr Ther Res, maart 1965, pp 170-175.
Dorfman W: Klinische ervaringen met amitriptyline: een voorlopig rapport. Psychosomatiek 1960; 1: 153– 155.
Fallette JM, Stasney CR, Mintz AA: Amitriptyline-vergiftiging behandeld met fysostigmine. Zuid-Med J 1970; 63: 1492-1493.
Hollister LE, Overall JE, Johnson M, et al: gecontroleerde vergelijking van amitriptyline, imipramine en placebo bij gehospitaliseerde depressieve patiënten. J Nerv Ment Dis 1964; 139: 370-375.
Hordern A, Burt CG, Holt NF: Depressieve toestanden: een farmacotherapeutisch onderzoek, Springfield-onderzoek. Springfield, Ill, Charles C. Thomas, 1965. Jenike MA: behandeling van affectieve ziekte bij ouderen met medicijnen en elektroconvulsietherapie. J Geriatr Psychiatrie 1989; 22(1):77-112.
Klerman GL, Cole JO: Klinische farmacologie van imipramine en verwante antidepressiva. Int J Psychiatrie 1976; 3: 267-304.
Liu B, Anderson G, Mittman N, et al: Gebruik van selectieve serotonineheropnameremmers of tricyclische antidepressiva en risico op heupfracturen bij ouderen. Lancet 1998; 351(9112):1303-1307.
McConaghy N, Joffe AD, Kingston WA, et al: Correlatie van klinische kenmerken van depressieve poliklinische patiënten met respons op amitriptyline en protriptyline. Br J Psychiatrie 1968; 114: 103-106.
McDonald IM, Perkins M, Marjerrison G, et al: een gecontroleerde vergelijking van amitriptyline en elektroconvulsietherapie bij de behandeling van depressie. Am J Psychiatry 1966;122:1427-1431.
Slovis T, Ott J, Teitelbaum D, et al: Physostigmine-therapie bij acute tricyclische antidepressiva-vergiftiging. Clin Toxicol 1971; 4:451–459.
Symposium over depressie met speciale onderzoeken naar een nieuw antidepressivum, amitriptyline. Dis Nerv Syst, (Sect 2) mei 1961, pp 5-56.
*Gebaseerd op een maximaal aanbevolen dosis amitriptyline van 150 mg/dag of 3 mg/kg/dag voor een patiënt van 50 kg.
**Hollister LE: Monitoring van tricyclische antidepressiva plasmaconcentraties. JAMA 1979; 241(23):2530-2533.
Elavil 25 mg tabletten zijn gele, ronde, filmomhulde tabletten zonder breuklijn, met de inscriptie “2102” aan de ene kant en de inscriptie “V” aan de andere kant. Ze worden als volgt geleverd: Flessen van 100: NDC 69874-422-10
Gefabriceerd door: Qualitest Pharmaceuticals/Vintage Pharmaceuticals, Huntsville, AL 35811. Gefabriceerd voor: Thompson Medical Solutions, Birmingham, AL 35242. Herzien: april 2016
BIJWERKINGEN
Geen informatie verstrektDRUG-INTERACTIES
Geneesmiddelen gemetaboliseerd door P450 2D6
De biochemische activiteit van het geneesmiddel metaboliserende isozym cytochroom P450 2D6 (debrisoquin hydroxylase) is verminderd in een subgroep van de blanke populatie (ongeveer 7 tot 10% van de blanken zijn zogenaamde "slechte metaboliseerders"); betrouwbare schattingen van de prevalentie van verminderde P450 2D6-isozymactiviteit onder Aziatische, Afrikaanse en andere populaties zijn nog niet beschikbaar. Slechte metaboliseerders hebben hoger dan verwachte plasmaconcentraties van tricyclische antidepressiva (TCA's) wanneer ze de gebruikelijke doses krijgen. Afhankelijk van de fractie van het geneesmiddel die door P450 2D6 wordt gemetaboliseerd, kan de toename van de plasmaconcentratie klein of vrij groot zijn (8-voudige toename van de plasma-AUC van de TCA).
Bovendien remmen bepaalde geneesmiddelen de activiteit van dit isozym en zorgen ervoor dat normale metaboliseerders lijken op slechte metaboliseerders. Een persoon die stabiel is op een bepaalde dosis TCA kan abrupt toxisch worden wanneer een van deze remmende geneesmiddelen als gelijktijdige therapie wordt gegeven. De geneesmiddelen die cytochroom P450 2D6 remmen, omvatten enkele die niet door het enzym worden gemetaboliseerd (kinidine; cimetidine) en vele die substraten zijn voor P450 2D6 (veel andere antidepressiva, fenothiazinen en de type 1C-antiaritmica propafenon en flecaïnide). Hoewel alle selectieve serotonineheropnameremmers (SSRI's), bijv. fluoxetine, sertraline en paroxetine, P450 2D6 remmen, kunnen ze variëren in de mate van remming. De mate waarin SSRI-TCA-interacties klinische problemen kunnen opleveren, hangt af van de mate van remming en de farmacokinetiek van de betrokken SSRI. Niettemin is voorzichtigheid geboden bij gelijktijdige toediening van TCA's met een van de SSRI's en ook bij het overschakelen van de ene klasse naar de andere. Van bijzonder belang is dat er voldoende tijd moet verstrijken voordat de TCA-behandeling wordt gestart bij een patiënt die wordt gestopt met fluoxetine, gezien de lange halfwaardetijd van de ouder en de actieve metaboliet (minimaal 5 weken kan nodig zijn).
Gelijktijdig gebruik van tricyclische antidepressiva met geneesmiddelen die cytochroom P450 2D6 kunnen remmen, kan lagere doses vereisen dan gewoonlijk wordt voorgeschreven voor het tricyclische antidepressivum of het andere geneesmiddel. Bovendien kan, wanneer een van deze andere geneesmiddelen uit de gelijktijdige therapie wordt gestaakt, een verhoogde dosis tricyclische antidepressiva nodig zijn. Het is wenselijk om de TCA-plasmaspiegels te controleren wanneer een TCA gelijktijdig wordt toegediend met een ander geneesmiddel waarvan bekend is dat het een remmer van P450 2D6 is.
Monoamineoxidaseremmers
Zien CONTRA-INDICATIES sectie. Guanethidine of soortgelijk werkende verbindingen; schildklier medicatie; alcohol, barbituraten en andere CZS-depressiva; en disulfiram – zie WAARSCHUWINGEN sectie. Wanneer amitriptylinehydrochloride wordt gegeven met anticholinergica of sympathicomimetica, waaronder epinefrine in combinatie met lokale anesthetica, is nauwlettend toezicht en zorgvuldige aanpassing van de dosering vereist.
Hyperpyrexie is gemeld wanneer amitriptylinehydrochloride wordt toegediend met anticholinergica of met neuroleptica, vooral bij warm weer.
Paralytische ileus kan optreden bij patiënten die tricyclische antidepressiva gebruiken in combinatie met anticholinergica.
Van cimetidine is gemeld dat het het levermetabolisme van bepaalde tricyclische antidepressiva vermindert, waardoor de eliminatie wordt vertraagd en de steady-state-concentraties van deze geneesmiddelen toenemen. Klinisch significante effecten zijn gemeld met de tricyclische antidepressiva bij gelijktijdig gebruik met cimetidine. Verhogingen van de plasmaspiegels van tricyclische antidepressiva en van de frequentie en ernst van bijwerkingen, met name anticholinergica, zijn gemeld wanneer cimetidine aan het geneesmiddelregime werd toegevoegd. Stopzetting van cimetidine bij goed gecontroleerde patiënten die tricyclische antidepressiva en cimetidine krijgen, kan de plasmaspiegels en werkzaamheid van de antidepressiva verlagen.
Voorzichtigheid is geboden als patiënten gelijktijdig grote doses ethchlorvynol krijgen. Voorbijgaand delier is gemeld bij patiënten die werden behandeld met één gram ethchlorvynol en 75 tot 150 mg amitriptylinehydrochloride.
BIJWERKINGEN
Binnen elke categorie zijn de volgende bijwerkingen gerangschikt naar afnemende ernst. In de lijst zijn enkele bijwerkingen opgenomen die niet zijn gemeld met dit specifieke medicijn. Farmacologische overeenkomsten tussen de tricyclische antidepressiva vereisen echter dat elk van de reacties in overweging wordt genomen wanneer amitriptyline wordt toegediend.
Cardiovasculair: Myocardinfarct; hartinfarct; niet-specifieke ECG-veranderingen en veranderingen in AV-geleiding; hartblok; aritmieën; hypotensie, in het bijzonder orthostatische hypotensie; syncope; hypertensie; tachycardie; hartkloppingen.
CNS en neuromusculair: coma; toevallen; hallucinaties; waanidee; verwarde toestanden; desoriëntatie; incoördinatie; ataxie; trillingen; perifere neuropathie; gevoelloosheid, tintelingen en paresthesieën van de ledematen; extrapiramidale symptomen waaronder abnormale onwillekeurige bewegingen en tardieve dyskinesie; dysartrie; verstoorde concentratie; spanning; ongerustheid; slapeloosheid; rusteloosheid; nachtmerries; slaperigheid; duizeligheid; zwakheid; vermoeidheid; hoofdpijn; syndroom van ongepaste secretie van ADH (antidiuretisch hormoon); oorsuizen; verandering in EEG-patronen.
Anticholinergisch: Paralytische ileus; hyperpyrexie; urineretentie; verwijding van de urinewegen; constipatie; wazig zien, accommodatiestoornis, verhoogde oogdruk, mydriasis; droge mond.
Allergisch: Huiduitslag; netelroos; fotosensibilisatie; oedeem van gezicht en tong.
Hematologische: Beenmergdepressie waaronder agranulocytose, leukopenie, trombocytopenie; purpura; eosinofilie.
Gastro-intestinaal: Zelden hepatitis (inclusief veranderde leverfunctie en geelzucht); misselijkheid; epigastrische nood; braken; anorexia; stomatitis; eigenaardige smaak; diarree; parotis zwelling; zwarte tong.
Endocrien: Testiculaire zwelling en gynaecomastie bij de man; borstvergroting en galactorroe bij de vrouw; verhoogd of verlaagd libido; impotentie; verhoging en verlaging van de bloedsuikerspiegel.
Ander: alopecia; oedeem; gewichtstoename of -verlies; urinaire frequentie; verhoogde transpiratie.
Ontwenningsverschijnselen: Na langdurige toediening kan abrupte stopzetting van de behandeling misselijkheid, hoofdpijn en malaise veroorzaken. Van geleidelijke dosisverlagingen is gemeld dat ze binnen twee weken voorbijgaande symptomen veroorzaken, waaronder prikkelbaarheid, rusteloosheid en droom- en slaapstoornissen.
Deze symptomen wijzen niet op een verslaving. Er zijn zeldzame gevallen gemeld van manie of hypomanie die optrad binnen 2 tot 7 dagen na stopzetting van chronische therapie met tricyclische antidepressiva.
Causaal verband onbekend: Andere reacties, gemeld onder omstandigheden waarin geen oorzakelijk verband kon worden vastgesteld, worden vermeld als waarschuwingsinformatie voor artsen.
Lichaam als geheel: Lupusachtig syndroom (migrerende artritis, positieve ANA en reumafactor).
spijsvertering: Leverfalen, ageusie.
Postmarketing bijwerkingen
Een syndroom dat lijkt op het maligne neurolepticasyndroom (MNS) is zeer zelden gemeld na het starten of verhogen van de dosis amitriptylinehydrochloride, met en zonder gelijktijdige medicatie waarvan bekend is dat ze NMS veroorzaken. Symptomen zijn onder meer spierstijfheid, koorts, veranderingen in de mentale toestand, diaforese, tachycardie en tremor.
Zeer zeldzame gevallen van serotoninesyndroom (SS) zijn gemeld met amitriptylinehydrochloride in combinatie met andere geneesmiddelen die een erkende associatie hebben met SS.
Zeer zeldzame gevallen van cardiomyopathie zijn gemeld met amitriptyline.
WAARSCHUWINGEN
Klinische verslechtering en zelfmoordrisico
Patiënten met een depressieve stoornis (MDD), zowel volwassenen als kinderen, kunnen een verergering van hun depressie ervaren en/of het optreden van zelfmoordgedachten en -gedrag (suïcidaliteit) of ongewone gedragsveranderingen, ongeacht of ze antidepressiva gebruiken of niet, en dit risico kan aanhouden totdat significante remissie optreedt. Zelfmoord is een bekend risico op depressie en bepaalde andere psychiatrische stoornissen, en deze stoornissen zelf zijn de sterkste voorspellers van zelfmoord. Er bestaat echter al lang de bezorgdheid dat antidepressiva een rol kunnen spelen bij het veroorzaken van verergering van depressie en het optreden van suïcidaliteit bij bepaalde patiënten tijdens de vroege fasen van de behandeling. Gepoolde analyses van kortdurende placebogecontroleerde onderzoeken met antidepressiva (SSRI's en andere) toonden aan dat deze geneesmiddelen het risico op zelfmoordgedachten en -gedrag (suïcidaliteit) verhogen bij kinderen, adolescenten en jonge volwassenen (1824 jaar) met een depressieve stoornis ( MDD) en andere psychiatrische stoornissen. Kortdurende onderzoeken lieten geen toename zien van het risico op suïcidaliteit bij gebruik van antidepressiva in vergelijking met placebo bij volwassenen ouder dan 24 jaar; er was een afname met antidepressiva vergeleken met placebo bij volwassenen van 65 jaar en ouder.
De gepoolde analyses van placebogecontroleerde onderzoeken bij kinderen en adolescenten met MDD, obsessieve compulsieve stoornis (OCS) of andere psychiatrische stoornissen omvatten in totaal 24 kortetermijnonderzoeken met 9 antidepressiva bij meer dan 4400 patiënten. De gepoolde analyses van placebogecontroleerde onderzoeken bij volwassenen met MDD of andere psychiatrische stoornissen omvatten in totaal 295 kortetermijnonderzoeken (mediane duur van 2 maanden) van 11 antidepressiva bij meer dan 77.000 patiënten. Er was een aanzienlijke variatie in het risico op suïcidaliteit tussen geneesmiddelen, maar een tendens naar een toename bij de jongere patiënten voor bijna alle onderzochte geneesmiddelen. Er waren verschillen in absoluut risico op suïcidaliteit tussen de verschillende indicaties, met de hoogste incidentie bij MDD. De risicoverschillen (geneesmiddel versus placebo) waren echter relatief stabiel binnen leeftijdscategorieën en tussen indicaties. Deze risicoverschillen (drug-placebo verschil in het aantal gevallen van suïcidaliteit per 1000 behandelde patiënten) worden gegeven in Tabel 1.
In geen van de pediatrische onderzoeken kwamen zelfmoorden voor. Er waren zelfmoorden in de onderzoeken bij volwassenen, maar het aantal was niet voldoende om enige conclusie te trekken over het effect van het medicijn op zelfmoord.
Het is niet bekend of het suïcidaliteitsrisico zich uitstrekt tot langdurig gebruik, dat wil zeggen langer dan enkele maanden. Er is echter substantieel bewijs uit placebogecontroleerde onderhoudsonderzoeken bij volwassenen met depressie dat het gebruik van antidepressiva het opnieuw optreden van depressie kan vertragen.
Alle patiënten die voor welke indicatie dan ook met antidepressiva worden behandeld, moeten op de juiste manier worden gecontroleerd en nauwlettend worden geobserveerd op klinische verergering, suïcidaliteit en ongewone gedragsveranderingen, vooral tijdens de eerste paar maanden van een medicamenteuze behandeling, of op tijdstippen van dosisveranderingen, ofwel verhogingen of afneemt.
De volgende symptomen, angst, agitatie, paniekaanvallen, slapeloosheid, prikkelbaarheid, vijandigheid, agressiviteit, impulsiviteit, acathisie (psychomotorische rusteloosheid), hypomanie en manie, zijn gemeld bij volwassen en pediatrische patiënten die ook werden behandeld met antidepressiva voor depressieve stoornis evenals voor andere indicaties, zowel psychiatrisch als niet-psychiatrisch. Hoewel er geen oorzakelijk verband is tussen het ontstaan van dergelijke symptomen en ofwel de verergering van depressie en/of het ontstaan van suïcidale impulsen, bestaat er bezorgdheid dat dergelijke symptomen een voorbode kunnen zijn van opkomende suïcidaliteit.
Bij patiënten bij wie de depressie aanhoudend erger is, of die opkomende suïcidaliteit ervaren of symptomen die een voorbode kunnen zijn van een verergering van depressie of suïcidaliteit, moet worden overwogen om het therapeutische regime te veranderen, met inbegrip van het mogelijk stopzetten van de medicatie, vooral als deze symptomen ernstig en abrupt zijn. bij aanvang, of maakten geen deel uit van de symptomen van de patiënt.
Families en verzorgers van patiënten die worden behandeld met antidepressiva voor depressieve stoornis of andere indicaties, zowel psychiatrische als niet-psychiatrische, moeten worden gewaarschuwd voor de noodzaak om patiënten te controleren op het optreden van agitatie, prikkelbaarheid, ongewone gedragsveranderingen en de andere symptomen hierboven beschreven, evenals de opkomst van suïcidaliteit, en om dergelijke symptomen onmiddellijk aan zorgverleners te melden. Dergelijke monitoring moet dagelijkse observatie door families en zorgverleners omvatten. Voorschriften voor amitriptylinehydrochloride-tabletten moeten worden geschreven voor de kleinste hoeveelheid tabletten in overeenstemming met goed patiëntenbeheer, om het risico op overdosering te verminderen.
Patiënten screenen op bipolaire stoornis
Een depressieve episode kan de eerste presentatie van een bipolaire stoornis zijn. Over het algemeen wordt aangenomen (hoewel niet vastgesteld in gecontroleerde onderzoeken) dat de behandeling van een dergelijke episode met alleen een antidepressivum de kans op neerslag van een gemengde/manische episode kan vergroten bij patiënten met een risico op een bipolaire stoornis. Of een van de hierboven beschreven symptomen een dergelijke conversie vertegenwoordigen, is niet bekend. Echter, voordat de behandeling met een antidepressivum wordt gestart, moeten patiënten met depressieve symptomen adequaat worden gescreend om te bepalen of ze een risico lopen op een bipolaire stoornis; een dergelijke screening moet een gedetailleerde psychiatrische geschiedenis omvatten, inclusief een familiegeschiedenis van zelfmoord, bipolaire stoornis en depressie. Opgemerkt moet worden dat amitriptylinehydrochloride-tabletten niet zijn goedgekeurd voor gebruik bij de behandeling van bipolaire depressie.
Amitriptylinehydrochloride kan de antihypertensieve werking van guanethidine of vergelijkbare stoffen blokkeren.
Het moet met voorzichtigheid worden gebruikt bij patiënten met een voorgeschiedenis van convulsies en, vanwege de atropine-achtige werking, bij patiënten met een voorgeschiedenis van urineretentie of gesloten kamerhoekglaucoom. Bij patiënten met kamerhoekglaucoom kunnen zelfs gemiddelde doses een aanval uitlokken.
Patiënten met cardiovasculaire aandoeningen moeten nauwlettend in de gaten worden gehouden. Van tricyclische antidepressiva, waaronder amitriptylinehydrochloride, is gemeld dat ze, vooral wanneer ze in hoge doses worden gegeven, aritmieën, sinustachycardie en verlenging van de geleidingstijd veroorzaken. Myocardinfarct en beroerte zijn gemeld bij geneesmiddelen van deze klasse.
Nauwlettend toezicht is vereist wanneer amitriptylinehydrochloride wordt toegediend aan patiënten met hyperthyreoïdie of aan patiënten die schildkliermedicatie krijgen.
Amitriptylinehydrochloride kan de respons op alcohol en de effecten van barbituraten en andere CZS-depressiva versterken. Bij patiënten die mogelijk overmatig alcohol gebruiken, moet er rekening mee worden gehouden dat de potentiëring het gevaar kan vergroten dat inherent is aan elke zelfmoordpoging of overdosering. Delirium is gemeld bij gelijktijdige toediening van amitriptyline en disulfiram.
Hoeksluiting glaucoom
De pupilverwijding die optreedt na het gebruik van veel antidepressiva, waaronder amitriptylinehydrochloride-tabletten, kan een aanval van hoeksluiting veroorzaken bij een patiënt met anatomisch nauwe hoeken die geen patente iridectomie heeft.
Gebruik tijdens de zwangerschap
Zwangerschap Categorie C
Teratogene effecten werden niet waargenomen bij muizen, ratten of konijnen wanneer amitriptyline oraal werd toegediend in doses van 2 tot 40 mg/kg/dag (tot 13 maal de maximaal aanbevolen dosis voor de mens*). Studies in de literatuur hebben aangetoond dat amitriptyline teratogeen is bij muizen en hamsters wanneer het via verschillende toedieningswegen wordt toegediend in doses van 28 tot 100 mg/kg/dag (9 tot 33 maal de maximaal aanbevolen dosis voor de mens), waardoor meerdere misvormingen ontstaan. Een andere studie bij ratten meldde dat een orale dosis van 25 mg/kg/dag (8 maal de maximaal aanbevolen dosis voor de mens) vertragingen veroorzaakte in de ossificatie van de wervellichamen van de foetus zonder andere tekenen van embryotoxiciteit. Bij konijnen werd gemeld dat een orale dosis van 60 mg/kg/dag (20 maal de maximaal aanbevolen dosis voor de mens) onvolledige osificatie van de schedelbeenderen veroorzaakte.
Van amitriptyline is aangetoond dat het de placenta passeert. Hoewel er geen oorzakelijk verband is vastgesteld, zijn er enkele meldingen geweest van bijwerkingen, waaronder effecten op het centrale zenuwstelsel, misvormingen van ledematen of ontwikkelingsachterstand, bij zuigelingen van wie de moeder amitriptyline had gebruikt tijdens de zwangerschap. Er zijn geen adequate en goed gecontroleerde onderzoeken bij zwangere vrouwen. Amitriptylinehydrochloride mag alleen tijdens de zwangerschap worden gebruikt als het mogelijke voordeel voor de moeder het mogelijke risico voor de foetus rechtvaardigt.
Moeders die borstvoeding geven
Amitriptyline wordt uitgescheiden in de moedermelk. In één rapport waarin een patiënte 100 mg/dag amitriptyline kreeg terwijl ze haar baby borstvoeding gaf, werden niveaus van 83 tot 141 ng/ml gedetecteerd in het serum van de moeder. In de moedermelk werden gehaltes van 135 tot 151 ng/ml gevonden, maar in het serum van de zuigeling kon geen spoor van het geneesmiddel worden gevonden.
Vanwege het potentieel voor ernstige bijwerkingen van amitriptyline bij zuigelingen die borstvoeding geven, moet worden besloten of de borstvoeding moet worden gestaakt of dat het geneesmiddel moet worden gestaakt, rekening houdend met het belang van het geneesmiddel voor de moeder.
Gebruik bij pediatrische patiënten
Gezien het gebrek aan ervaring met het gebruik van dit geneesmiddel bij pediatrische patiënten, wordt het momenteel niet aanbevolen voor patiënten jonger dan 12 jaar.
PREVENTIEVE MAATREGELEN
Schizofrene patiënten kunnen verhoogde symptomen van psychose ontwikkelen; patiënten met paranoïde symptomatologie kunnen dergelijke symptomen overdrijven. Depressieve patiënten, vooral degenen met een bekende manisch-depressieve aandoening, kunnen een verschuiving naar manie of hypomanie ervaren. In deze omstandigheden kan de dosis amitriptyline worden verlaagd of kan gelijktijdig een belangrijk kalmeringsmiddel zoals perfenazine worden toegediend.
De mogelijkheid van zelfmoord bij depressieve patiënten blijft bestaan totdat significante remissie optreedt. Potentieel suïcidale patiënten mogen geen toegang hebben tot grote hoeveelheden van dit medicijn. Voorschriften moeten worden geschreven voor de kleinst mogelijke hoeveelheid.
Gelijktijdige toediening van amitriptylinehydrochloride en elektroshocktherapie kan de risico's van een dergelijke therapie vergroten. Een dergelijke behandeling moet worden beperkt tot patiënten voor wie ze essentieel is.
Indien mogelijk moet het medicijn enkele dagen vóór een electieve operatie worden stopgezet.
Zowel verhoging als verlaging van de bloedsuikerspiegel zijn gemeld.
Amitriptylinehydrochloride moet met voorzichtigheid worden gebruikt bij patiënten met een verminderde leverfunctie.
Informatie voor patiënten
Voorschrijvers of andere gezondheidswerkers moeten patiënten, hun families en hun verzorgers informeren over de voordelen en risico's van de behandeling met amitriptylinehydrochloridetabletten en moeten hen adviseren bij het juiste gebruik ervan. Een patiënt Medicatiegids over "Antidepressiva, depressie en andere ernstige psychische aandoeningen en zelfmoordgedachten of -acties" is beschikbaar voor amitriptylinehydrochloride-tabletten. De voorschrijver of zorgverlener moet patiënten, hun families en hun zorgverleners instrueren om de Medicatiegids en zou hen moeten helpen de inhoud ervan te begrijpen. Patiënten moeten de kans krijgen om de inhoud van de Medicatiegids en om antwoord te krijgen op al hun vragen. De volledige tekst van de Medicatiegids wordt herdrukt aan het einde van dit document.
Patiënten moeten op de hoogte worden gebracht van de volgende problemen en moeten worden gevraagd hun voorschrijver te waarschuwen als deze optreden tijdens het gebruik van amitriptylinehydrochloride-tabletten.
Tijdens de behandeling met amitriptylinehydrochloride moeten patiënten worden geïnformeerd over de mogelijke verslechtering van de mentale en/of fysieke vermogens die nodig zijn voor het uitvoeren van gevaarlijke taken, zoals het bedienen van machines of het besturen van een motorvoertuig.
Patiënten moeten erop worden gewezen dat het gebruik van amitriptylinehydrochloride-tabletten lichte papillaire verwijding kan veroorzaken, wat bij daarvoor gevoelige personen kan leiden tot een episode van geslotenhoekglaucoom. Reeds bestaand glaucoom is bijna altijd openhoekglaucoom, omdat geslotenhoekglaucoom, indien gediagnosticeerd, definitief kan worden behandeld met iridectomie. Openhoekglaucoom is geen risicofactor voor geslotenhoekglaucoom. Patiënten willen mogelijk worden onderzocht om te bepalen of ze vatbaar zijn voor hoeksluiting en een profylactische procedure ondergaan (bijv. iridectomie), als ze vatbaar zijn.
Klinische verslechtering en zelfmoordrisico
Patiënten, hun families en hun verzorgers moeten worden aangemoedigd alert te zijn op het optreden van angst, agitatie, paniekaanvallen, slapeloosheid, prikkelbaarheid, vijandigheid, agressiviteit, impulsiviteit, acathisie (psychomotorische rusteloosheid), hypomanie, manie, andere ongewone gedragsveranderingen verergering van depressie en zelfmoordgedachten, vooral in het begin van de behandeling met antidepressiva en wanneer de dosis omhoog of omlaag wordt aangepast. Families en verzorgers van patiënten moeten worden geadviseerd om dagelijks te kijken naar het optreden van dergelijke symptomen, aangezien veranderingen abrupt kunnen zijn. Dergelijke symptomen moeten aan de voorschrijver van de patiënt of gezondheidswerker worden gemeld, vooral als ze ernstig zijn, abrupt beginnen of geen deel uitmaken van de symptomen die de patiënt vertoont. Symptomen zoals deze kunnen in verband worden gebracht met een verhoogd risico op zelfmoordgedachten en -gedrag en duiden op een noodzaak tot zeer nauwgezette monitoring en mogelijk wijzigingen in de medicatie.
Pediatrisch gebruik
De veiligheid en werkzaamheid bij pediatrische patiënten zijn niet vastgesteld (zie: DOOS WAARSCHUWING: en WAARSCHUWINGEN - Klinische verslechtering en zelfmoordrisico ). Iedereen die het gebruik van amitriptylinehydrochloride-tabletten bij een kind of adolescent overweegt, moet de mogelijke risico's afwegen tegen de klinische noodzaak.
Geriatrisch gebruik
Klinische ervaring heeft geen verschillen in respons tussen oudere en jongere patiënten aangetoond. Over het algemeen moet de dosiskeuze voor een oudere patiënt voorzichtig zijn, meestal beginnend aan het lage uiteinde van het doseringsbereik, als gevolg van de grotere frequentie van verminderde leverfunctie, gelijktijdige ziekte en andere medicamenteuze behandeling bij oudere patiënten.
Geriatrische patiënten zijn bijzonder gevoelig voor de anticholinerge bijwerkingen van tricyclische antidepressiva, waaronder amitriptylinehydrochloride. Perifere anticholinerge effecten zijn onder meer tachycardie, urineretentie, constipatie, droge mond, wazig zien en verergering van nauwekamerhoekglaucoom. Anticholinerge effecten op het centrale zenuwstelsel omvatten cognitieve stoornissen, psychomotorische vertraging, verwardheid, sedatie en delirium. Oudere patiënten die amitriptylinehydrochloride gebruiken, lopen mogelijk een verhoogd risico op vallen. Oudere patiënten moeten worden gestart met lage doses amitriptylinehydrochloride en nauwlettend worden geobserveerd (zie: DOSERING EN ADMINISTRATIE ).
OVERDOSERING
Sterfgevallen kunnen optreden door overdosering met deze klasse geneesmiddelen. Inname van meerdere geneesmiddelen (inclusief alcohol) komt vaak voor bij een opzettelijke overdosis tricyclische antidepressiva. Aangezien de behandeling complex en veranderlijk is, wordt aanbevolen dat de arts contact opneemt met een antigifcentrum voor actuele informatie over de behandeling. Tekenen en symptomen van toxiciteit ontwikkelen zich snel na een overdosis tricyclische antidepressiva; daarom is ziekenhuisbewaking zo snel mogelijk vereist.
manifestaties
Kritische manifestaties van overdosering zijn onder meer: hartritmestoornissen, ernstige hypotensie, convulsies en depressie van het CZS, waaronder coma. Veranderingen in het elektrocardiogram, met name in de QRS-as of -breedte, zijn klinisch significante indicatoren van tricyclische antidepressiva-toxiciteit. Bovendien zijn een verschuiving van de as naar rechts in het terminale QRS-complex samen met een verlengd QT-interval en sinustachycardie specifieke en gevoelige indicatoren van een eerste generatie tricyclische overdosering. De afwezigheid van deze bevindingen is niet exclusief. Verlengd PR-interval, ST-T-golfveranderingen, ventriculaire tachycardie en fibrillatie kunnen ook voorkomen.
Andere tekenen van overdosering kunnen zijn: verminderde myocardiale contractiliteit, verwardheid, verstoorde concentratie, voorbijgaande visuele hallucinaties, verwijde pupillen, stoornissen van de oogmotiliteit, agitatie, hyperactieve reflexen, polyradiculoneuropathie, stupor, slaperigheid, spierstijfheid, braken, hypothermie, hyperpyrexie of enige andere van de symptomen vermeld onder ONGEWENSTE REACTIES.
Beheer
Algemeen
Maak een ECG en start onmiddellijk hartbewaking. Bescherm de luchtwegen van de patiënt, breng een intraveneuze lijn aan en start maagdecontaminatie. Een minimum van zes uur observatie met hartbewaking en observatie op tekenen van CZS of ademhalingsdepressie, hypotensie, hartritmestoornissen en/of geleidingsblokkades en toevallen is noodzakelijk. Als er op enig moment tijdens de periode tekenen van toxiciteit optreden, is uitgebreide monitoring vereist. Er zijn casusrapporten van patiënten die bezwijken aan fatale ritmestoornissen laat na een overdosis; deze patiënten hadden klinisch bewijs van significante vergiftiging voorafgaand aan de dood en de meeste kregen onvoldoende gastro-intestinale decontaminatie. Controle van de geneesmiddelspiegels in plasma mag geen leidraad zijn voor de behandeling van de patiënt.
Gastro-intestinale decontaminatie
Alle patiënten die verdacht worden van een overdosis tricyclische antidepressiva, dienen maag-darmontsmetting te ondergaan. Dit moet een maagspoeling met een groot volume omvatten, gevolgd door actieve kool. Als het bewustzijn verminderd is, moet de luchtweg worden afgesloten voordat er wordt gespoeld. EMESIS IS GECONTRA-INDICEERD.
Cardiovasculair
Een maximale ledemaat-lead QRS-duur van ≥ 0,10 seconden kan de beste indicatie zijn voor de ernst van de overdosis. Intraveneus natriumbicarbonaat moet worden gebruikt om de serum-pH tussen 7,45 en 7,55 te houden. Als de pH-respons onvoldoende is, kan ook hyperventilatie worden toegepast. Gelijktijdig gebruik van hyperventilatie en natriumbicarbonaat moet met uiterste voorzichtigheid gebeuren, met frequente Ph-controle. Een pH > 7,60 of een pCO2
In zeldzame gevallen kan hemoperfusie gunstig zijn bij acute refractaire cardiovasculaire instabiliteit bij patiënten met acute toxiciteit. Van hemodialyse, peritoneale dialyse, wisseltransfusies en geforceerde diurese is echter in het algemeen gemeld dat ze niet effectief zijn bij vergiftiging met tricyclische antidepressiva.
CNS
Bij patiënten met CZS-depressie wordt vroege intubatie geadviseerd vanwege het potentieel voor abrupte verslechtering. Epileptische aanvallen moeten onder controle worden gehouden met benzodiazepinen, of, als deze niet effectief zijn, andere anti-epileptica (bijv. fenobarbital, fenytoïne).
Fysostigmine wordt niet aanbevolen, behalve voor de behandeling van levensbedreigende symptomen die niet reageerden op andere therapieën, en dan alleen in overleg met een antigifcentrum.
Psychiatrische follow-up
Aangezien overdosering vaak opzettelijk is, kunnen patiënten tijdens de herstelfase op andere manieren zelfmoord proberen te plegen. Psychiatrische verwijzing kan passend zijn.
Pediatrisch management
De principes voor het beheer van overdoseringen bij kinderen en volwassenen zijn vergelijkbaar. Het wordt sterk aanbevolen dat de arts contact opneemt met het plaatselijke antigifcentrum voor specifieke pediatrische behandeling.
CONTRA-INDICATIES
Amitriptylinehydrochloride is gecontra-indiceerd bij patiënten die eerder overgevoelig hiervoor zijn geweest. Het mag niet gelijktijdig met monoamineoxidaseremmers worden gegeven. Hyperpyretische crises, ernstige convulsies en overlijden zijn opgetreden bij patiënten die gelijktijdig tricyclische antidepressiva en monoamineoxidaseremmende geneesmiddelen kregen. Als het gewenst is om een monoamineoxidaseremmer te vervangen door amitriptylinehydrochloride, moet er minimaal 14 dagen verstrijken nadat de eerste is gestopt. Amitriptylinehydrochloride moet dan voorzichtig worden gestart met een geleidelijke verhoging van de dosering totdat een optimale respons is bereikt.
Amitriptylinehydrochloride mag niet samen met Cisapride worden gegeven vanwege het potentieel voor een verlengd QT-interval en een verhoogd risico op aritmie.
Dit medicijn wordt niet aanbevolen voor gebruik tijdens de acute herstelfase na een hartinfarct.
KLINISCHE FARMACOLOGIE
Amitriptylinehydrochloride is een antidepressivum met kalmerende effecten. Het werkingsmechanisme bij de mens is niet bekend. Het is geen monoamineoxidaseremmer en het werkt niet primair door stimulatie van het centrale zenuwstelsel.
Amitriptyline remt het membraanpompmechanisme dat verantwoordelijk is voor de opname van noradrenaline en serotonine in adrenerge en serotonerge neuronen. Farmacologisch kan deze werking de neuronale activiteit versterken of verlengen, aangezien heropname van deze biogene aminen fysiologisch belangrijk is bij het beëindigen van de overdrachtsactiviteit. Sommigen geloven dat deze interferentie met de heropname van noradrenaline en/of serotonine ten grondslag ligt aan de antidepressieve activiteit van amitriptyline.
Metabolisme
Studies bij de mens na orale toediening van 14C-gelabeld geneesmiddel gaven aan dat amitriptyline snel wordt geabsorbeerd en gemetaboliseerd. De radioactiviteit van het plasma was praktisch verwaarloosbaar, hoewel er na 4 tot 6 uur significante hoeveelheden radioactiviteit in de urine verschenen en de helft tot een derde van het geneesmiddel binnen 24 uur werd uitgescheiden.
Amitriptyline wordt gemetaboliseerd door N-demethylering en brughydroxylering bij mensen, konijnen en ratten. Vrijwel de gehele dosis wordt uitgescheiden als glucuronide- of sulfaatconjugaat van metabolieten, waarbij weinig onveranderd geneesmiddel in de urine verschijnt. Er kunnen andere metabole routes bij betrokken zijn.
PATIËNT INFORMATIE
Antidepressiva, depressie en andere ernstige psychische aandoeningen en zelfmoordgedachten of -acties
Lees de medicatiehandleiding die bij u of het antidepressivum van uw familielid wordt geleverd. Deze medicatiehandleiding gaat alleen over het risico op zelfmoordgedachten en -acties met antidepressiva. Praat met uw zorgverlener of die van uw gezinslid over:
- alle risico's en voordelen van behandeling met antidepressiva
- alle behandelingskeuzes voor depressie of andere ernstige psychische aandoeningen
Wat is de belangrijkste informatie die ik moet weten over antidepressiva, depressie en andere ernstige psychische aandoeningen, en zelfmoordgedachten of -acties?
- Besteed veel aandacht aan eventuele veranderingen, vooral plotselinge veranderingen, in stemming, gedrag, gedachten of gevoelens. Dit is erg belangrijk wanneer een antidepressivum wordt gestart of wanneer de dosis wordt gewijzigd.
- Bel de zorgverlener meteen om nieuwe of plotselinge veranderingen in stemming, gedrag, gedachten of gevoelens te melden.
- Houd alle vervolgbezoeken aan de zorgverlener zoals gepland. Bel indien nodig de zorgverlener tussen bezoeken, vooral als u zich zorgen maakt over symptomen.
Bel onmiddellijk een zorgverlener als u of uw gezinslid een van de volgende symptomen heeft, vooral als ze nieuw zijn, erger zijn of u zorgen baren:
- gedachten over zelfmoord of doodgaan
- pogingen om zelfmoord te plegen
- nieuwe of ergere depressie
- nieuwe of ergere angst
- zich erg geagiteerd of rusteloos voelen
- paniekaanvallen
- moeite met slapen (slapeloosheid)
- nieuwe of ergere prikkelbaarheid
- agressief handelen, boos of gewelddadig zijn
- handelen op gevaarlijke impulsen
- een extreme toename van activiteit en praten (manie)
- andere ongewone veranderingen in gedrag of stemming
- Visuele problemen: oogpijn, veranderingen in het gezichtsvermogen, zwelling of roodheid in of rond het oog
Wat moet ik nog meer weten over antidepressiva?
- Stop nooit met een antidepressivum zonder eerst met een zorgverlener te overleggen. Plotseling stoppen met een antidepressivum kan andere symptomen veroorzaken.
- Visuele problemen. Slechts enkele mensen lopen risico op deze problemen. Misschien wilt u een oogonderzoek ondergaan om te zien of u een risico loopt en als dat zo is, een preventieve behandeling krijgen.
- Antidepressiva zijn geneesmiddelen die worden gebruikt om depressie en andere ziekten te behandelen. Het is belangrijk om alle risico's van het behandelen van depressie te bespreken en ook de risico's van het niet behandelen ervan. Patiënten en hun families of andere zorgverleners moeten alle behandelkeuzes met de zorgverlener bespreken, niet alleen het gebruik van antidepressiva.
- Antidepressiva hebben andere bijwerkingen. Praat met de zorgverlener over de bijwerkingen van het geneesmiddel dat aan u of uw gezinslid is voorgeschreven.
- Antidepressiva kunnen een wisselwerking hebben met andere geneesmiddelen . Ken alle medicijnen die u of uw familielid gebruikt. Houd een lijst bij van alle medicijnen die u aan de zorgverlener kunt laten zien. Begin niet met nieuwe medicijnen zonder eerst met uw zorgverlener te overleggen.
- Niet alle antidepressiva die voor kinderen worden voorgeschreven, zijn door de FDA goedgekeurd voor gebruik bij kinderen. Praat met de zorgverlener van uw kind voor meer informatie.
Bel uw arts voor medisch advies over bijwerkingen. U kunt bijwerkingen melden aan de FDA op 1-800-FDA-1088.
Deze medicatiehandleiding is goedgekeurd door de Amerikaanse Food and Drug Administration voor alle antidepressiva.
