Provera 5mg, 10mg Medroxyprogesterone Gebruik, bijwerkingen en dosering. Prijs in online apotheek. Generieke medicijnen zonder recept.
Wat is Provera en hoe wordt het gebruikt?
Provera 10 mg is een receptgeneesmiddel dat wordt gebruikt voor de behandeling van symptomen van hevige menstruatiebloedingen, afwezige of onregelmatige menstruatiebloedingen en als anticonceptie. Provera 10 mg kan alleen of in combinatie met andere medicijnen worden gebruikt.
Provera 5 mg behoort tot een klasse geneesmiddelen die antineoplastische stoffen, hormonen en progestagenen worden genoemd.
Het is niet bekend of Provera veilig en effectief is bij kinderen.
Wat zijn de mogelijke bijwerkingen van Provera 10 mg?
Provera 5 mg kan ernstige bijwerkingen veroorzaken, waaronder:
- vaginale bloeding (als u al door de menopauze bent gegaan),
- duizeligheid,
- knobbeltje in de borst,
- depressie,
- slaapproblemen (slapeloosheid),
- duizeligheid,
- stemmingswisselingen,
- hoofdpijn,
- koorts,
- geel worden van de huid of ogen (geelzucht),
- zwelling in uw handen, enkels of voeten,
- pijn op de borst of druk,
- pijn die zich uitbreidt naar uw kaak of schouder,
- misselijkheid,
- zweten,
- plotselinge gevoelloosheid of zwakte,
- plotselinge ernstige hoofdpijn,
- onduidelijke spraak,
- zichtproblemen,
- problemen met uw evenwicht,
- plotselinge hoest,
- piepende ademhaling,
- snel ademhalen,
- bloed ophoesten, en
- pijn in uw been (of beide) met zwelling, warmte en roodheid
Roep meteen medische hulp in als u een van de bovenstaande symptomen heeft.
De meest voorkomende bijwerkingen van Provera 10 mg zijn:
- spotting of doorbraakbloeding,
- veranderingen in uw menstruatie,
- vaginale jeuk of afscheiding,
- gevoelige borsten of afscheiding,
- hoofdpijn,
- duizeligheid,
- nerveus of depressief voelen,
- blauwe plekken of zwelling van uw aderen,
- opgeblazen gevoel,
- vocht vasthouden,
- stemmingswisselingen,
- slaapproblemen (slapeloosheid),
- jeuk,
- uitslag,
- acne,
- haargroei,
- verlies van hoofdhaar,
- maagklachten,
- opgeblazen gevoel,
- misselijkheid,
- gewichtstoename, en
- veranderingen in het gezichtsvermogen of moeite met het dragen van contactlenzen
WAARSCHUWING
CARDIOVASCULAIRE AANDOENINGEN, BORSTKANKER EN MOGELIJKE DEMENTIE VOOR OESTROGEEN PLUS PROGESTIN-THERAPIE
Cardiovasculaire aandoeningen en waarschijnlijke dementie
Behandeling met oestrogeen plus progestageen mag niet worden gebruikt voor de preventie van hart- en vaatziekten of dementie. (Zien Klinische studies en WAARSCHUWINGEN , Cardiovasculaire aandoeningen en waarschijnlijke dementie .)
Het Women's Health Initiative (WHI) oestrogeen plus progestageen subonderzoek rapporteerde een verhoogd risico op diepe veneuze trombose (DVT), longembolie (PE), beroerte en myocardinfarct (MI) bij postmenopauzale vrouwen (50 tot 79 jaar oud) ) gedurende 5,6 jaar behandeling met dagelijkse orale geconjugeerde oestrogenen (CE) [0,625 mg] gecombineerd met medroxyprogesteronacetaat (MPA) [2,5 mg], vergeleken met placebo. (Zien Klinische studies en WAARSCHUWINGEN , Cardiovasculaire aandoeningen .)
De WHI Memory Study (WHIMS) oestrogeen plus progestageen aanvullende studie rapporteerde een verhoogd risico op het ontwikkelen van waarschijnlijke dementie bij postmenopauzale vrouwen van 65 jaar of ouder gedurende 4 jaar behandeling met dagelijkse CE (0,625 mg) gecombineerd met MPA (2,5 mg), relatief naar placebo. Het is niet bekend of deze bevinding van toepassing is op jongere postmenopauzale vrouwen. (Zien Klinische studies en WAARSCHUWINGEN , Waarschijnlijke dementie en PREVENTIEVE MAATREGELEN , Geriatrisch gebruik .)
Borstkanker
De WHI oestrogeen plus progestageen substudie toonde een verhoogd risico op invasieve borstkanker aan. (Zien Klinische studies en WAARSCHUWINGEN , Maligne neoplasma , Borstkanker .)
Bij gebrek aan vergelijkbare gegevens moet worden aangenomen dat deze risico's vergelijkbaar zijn voor andere doses CE en MPA, en andere combinaties en doseringsvormen van oestrogenen en progestagenen.
Progestagenen met oestrogenen moeten worden voorgeschreven in de laagste effectieve doses en voor de kortste duur in overeenstemming met de behandeldoelen en risico's voor de individuele vrouw.
OMSCHRIJVING
PROVERA®-tabletten bevatten medroxyprogesteronacetaat, een derivaat van progesteron. Het is een wit tot gebroken wit, geurloos kristallijn poeder, stabiel in lucht, smeltend tussen 200 en 210°C. Het is vrij oplosbaar in chloroform, oplosbaar in aceton en in dioxaan, matig oplosbaar in alcohol en in methanol, slecht oplosbaar in ether en onoplosbaar in water.
De chemische naam voor medroxyprogesteronacetaat is pregn-4-een-3, 20-dion, 17-(acetyloxy)-6-methyl-, (6α)-. De structuurformule is:
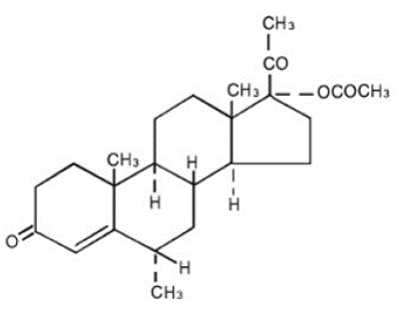
Elke PROVERA 5 mg tablet voor orale toediening bevat 2,5 mg, 5 mg of 10 mg medroxyprogesteronacetaat en de volgende inactieve ingrediënten: calciumstearaat, maïszetmeel, lactose, minerale olie, sorbinezuur, sucrose en talk. De tablet van 2,5 mg bevat FD&C Geel nr. 6.
INDICATIES
PROVERA 5 mg tabletten zijn geïndiceerd voor de behandeling van secundaire amenorroe en abnormale baarmoederbloedingen als gevolg van hormonale onbalans in afwezigheid van organische pathologie, zoals vleesbomen of baarmoederkanker. Ze zijn ook geïndiceerd voor gebruik bij de preventie van endometriumhyperplasie bij niet-gehysterectomiseerde postmenopauzale vrouwen die dagelijks oraal geconjugeerde oestrogenen 0,625 mg tabletten krijgen.
DOSERING EN ADMINISTRATIE
Secundaire amenorroe
PROVERA 10 mg tabletten kunnen worden gegeven in doseringen van 5 of 10 mg per dag gedurende 5 tot 10 dagen. Een dosis voor het induceren van een optimale secretoire transformatie van een endometrium dat adequaat is geprimed met endogeen of exogeen oestrogeen is 10 mg PROVERA 10 mg per dag gedurende 10 dagen. In gevallen van secundaire amenorroe kan de therapie op elk moment worden gestart. Progestageenonttrekkingsbloeding treedt meestal op binnen drie tot zeven dagen na het stoppen van de behandeling met PROVERA 10 mg.
Abnormale baarmoederbloeding als gevolg van hormonale onbalans bij afwezigheid van organische pathologie
Vanaf de berekende 16e of 21e dag van de menstruatiecyclus mag 5 of 10 mg PROVERA 10 mg dagelijks worden gegeven gedurende 5 tot 10 dagen. Om een optimale secretoire transformatie van een endometrium te produceren dat voldoende is geprimed met endogeen of exogeen oestrogeen, wordt aanbevolen 10 mg PROVERA 10 mg per dag gedurende 10 dagen vanaf de 16e dag van de cyclus. Progestageen-onttrekkingsbloeding treedt meestal op binnen drie tot zeven dagen na het stoppen van de behandeling met PROVERA. Patiënten met een voorgeschiedenis van terugkerende episodes van abnormale uteriene bloedingen kunnen baat hebben bij geplande menstruatiecycli met PROVERA.
Vermindering van endometriumhyperplasie bij postmenopauzale vrouwen die dagelijks 0,625 mg geconjugeerde oestrogenen krijgen
Wanneer oestrogeen wordt voorgeschreven aan een postmenopauzale vrouw met een baarmoeder, moet ook een progestageen worden gestart om het risico op endometriumkanker te verminderen. Een vrouw zonder baarmoeder heeft geen progestageen nodig. Het gebruik van oestrogeen, alleen of in combinatie met een progestageen, moet gebeuren met de laagste effectieve dosis en voor de kortste duur in overeenstemming met de behandeldoelen en risico's voor de individuele vrouw. Patiënten dienen periodiek opnieuw te worden geëvalueerd indien klinisch aangewezen (bijvoorbeeld met tussenpozen van 3 tot 6 maanden) om te bepalen of behandeling nog steeds noodzakelijk is (zie WAARSCHUWINGEN ). Voor vrouwen met een baarmoeder moeten adequate diagnostische maatregelen worden genomen, zoals endometriumafname, indien geïndiceerd, om maligniteit uit te sluiten in gevallen van niet-gediagnosticeerde aanhoudende of terugkerende abnormale vaginale bloedingen.
PROVERA-tabletten kunnen worden gegeven in doseringen van 5 of 10 mg per dag gedurende 12 tot 14 opeenvolgende dagen per maand, aan postmenopauzale vrouwen die dagelijks 0,625 mg geconjugeerde oestrogenen krijgen, beginnend op de 1e dag van de cyclus of de 16e dag van de cyclus.
Patiënten moeten worden gestart met de laagste dosis.
De laagste effectieve dosis PROVERA is niet vastgesteld.
HOE GELEVERD
PROVERA 10 mg tabletten zijn verkrijgbaar in de volgende sterktes en verpakkingsgrootten:
2,5 mg (gescoord, rond, oranje)
Flessen van 30 NDC 0009-0064-06 Flessen van 100 NDC 0009-0064-04
5 mg (gescoord, zeshoekig, wit)
Flessen van 100 NDC 0009-0286-03
10 mg (gescoord, rond, wit)
Flessen van 100 NDC 0009-0050-02 Flessen van 500 NDC 0009-0050-11
Bewaren bij een gecontroleerde kamertemperatuur van 20° tot 25°C (68° tot 77°F) [zie USP ].
“Buiten bereik van kinderen houden”
Gedistribueerd door: Pharmacia & Upjohn Company, Division of Pfizer Inc., NY, NY 10017. Herzien: aug. 2015
BIJWERKINGEN
Zien OMKADERDE WAARSCHUWINGEN , WAARSCHUWINGEN , en PREVENTIEVE MAATREGELEN .
Omdat klinische onderzoeken onder sterk uiteenlopende omstandigheden worden uitgevoerd, kunnen de bijwerkingen die in de klinische onderzoeken van een geneesmiddel zijn waargenomen niet direct worden vergeleken met de percentages in de klinische onderzoeken van een ander geneesmiddel en komen mogelijk niet overeen met de percentages die in de praktijk worden waargenomen.
De volgende bijwerkingen zijn gemeld bij vrouwen die PROVERA 10 mg tabletten gebruikten, zonder gelijktijdige behandeling met oestrogenen:
Urogenitaal systeem
Abnormale baarmoederbloeding (onregelmatig, toename, afname), verandering in menstruatie, doorbraakbloeding, spotting, amenorroe, veranderingen in cervicale erosie en cervicale secretie.
borsten
Gevoelige borsten, mastodynie of galactorroe zijn gemeld.
Cardiovasculair
Trombo-embolische aandoeningen waaronder tromboflebitis en longembolie zijn gemeld.
gastro-intestinaal
Misselijkheid, cholestatische geelzucht.
Huid
Gevoeligheidsreacties bestaande uit urticaria, pruritus, oedeem en gegeneraliseerde huiduitslag zijn opgetreden. Acne, Gevoeligheidsreacties bestaande uit urticaria, pruritus, oedeem en gegeneraliseerde huiduitslag zijn opgetreden. Acne, alopecia en hirsutisme zijn gemeld.
Ogen
Neuro-oculaire laesies, bijvoorbeeld retinale trombose en optische neuritis.
Centraal zenuwstelsel
Geestelijke depressie, slapeloosheid, slaperigheid, duizeligheid, hoofdpijn, nervositeit.
Diversen
Overgevoeligheidsreacties (bijvoorbeeld anafylaxie en anafylactoïde reacties, angio-oedeem), huiduitslag (allergisch) met en zonder pruritus, verandering in gewicht (toename of afname), pyrexie, oedeem/vochtretentie, vermoeidheid, verminderde glucosetolerantie.
De volgende bijwerkingen zijn gemeld bij behandeling met oestrogeen plus progestageen.
Urogenitaal systeem
Abnormale baarmoederbloeding / spotting of stroom; doorbraakbloeding; spotten; dysmenorroe/bekkenpijn; toename in omvang van baarmoederleiomyomata; vaginitis, waaronder vaginale candidiasis; verandering in hoeveelheid cervicale secretie; veranderingen in cervicale ectropion; eierstokkanker; endometriale hyperplasie; endometriumkanker.
borsten
Tederheid, vergroting, pijn, tepelafscheiding, galactorroe; fibrocystische borstveranderingen; borstkanker.
Cardiovasculair
Diepe en oppervlakkige veneuze trombose; longembolie; tromboflebitis; myocardinfarct; hartinfarct; verhoging van de bloeddruk.
gastro-intestinaal
Misselijkheid, braken; buikkrampen, opgeblazen gevoel; cholestatische geelzucht; verhoogde incidentie van galblaasaandoeningen; pancreatitis; vergroting van hepatische hemangiomen.
Huid
Chloasma of melasma dat kan aanhouden wanneer het medicijn wordt stopgezet; erythema multiforme; erythema nodosum; hemorragische uitbarsting; verlies van hoofdhaar; hirsutisme; jeuk, uitslag.
Ogen
Retinale vasculaire trombose, intolerantie voor contactlenzen.
Centraal zenuwstelsel
Hoofdpijn; migraine; duizeligheid; mentale depressie; chorea; nervositeit; stemmingsstoornissen; prikkelbaarheid; verergering van epilepsie, dementie.
Diversen
Toename of afname in gewicht; verminderde koolhydraattolerantie; verergering van porfyrie; oedeem; arthalgie; beenkrampen; veranderingen in libido; urticaria, angio-oedeem, anafylactoïde/anafylactische reacties; hypocalciëmie; verergering van astma; verhoogde triglyceriden.
DRUG-INTERACTIES
Geneesmiddel-laboratoriumtestinteracties
De volgende laboratoriumresultaten kunnen worden gewijzigd door het gebruik van oestrogeen plus progestageentherapie:
WAARSCHUWINGEN
Inbegrepen als onderdeel van de PREVENTIEVE MAATREGELEN sectie.
Zien OMKADERDE WAARSCHUWINGEN .
Cardiovasculaire aandoeningen
Een verhoogd risico op PE, DVT, beroerte en MI is gemeld bij behandeling met oestrogeen en progestageen. Als een van deze voorvallen optreedt of wordt vermoed, moet de behandeling met oestrogeen plus progestageen onmiddellijk worden stopgezet.
Risicofactoren voor arteriële vaatziekte (bijvoorbeeld hypertensie, diabetes mellitus, tabaksgebruik, hypercholesterolemie en obesitas) en/of veneuze trombo-embolie (VTE) (bijvoorbeeld persoonlijke voorgeschiedenis of familiegeschiedenis van VTE, obesitas en systemische lupus erythematosus) adequaat moet worden beheerd.
Hartinfarct
In het WHI-onderzoek naar oestrogeen plus progestageen werd een statistisch significant verhoogd risico op beroerte gemeld bij vrouwen van 50 tot 79 jaar die CE (0,625 mg) plus MPA (2,5 mg) kregen in vergelijking met vrouwen in dezelfde leeftijdsgroep die placebo kregen (33 versus 25 per 10.000 vrouwjaren). (Zien Klinische studies .) De toename van het risico werd aangetoond na het eerste jaar en hield aan. Als een beroerte optreedt of wordt vermoed, moet de behandeling met oestrogeen plus progestageen onmiddellijk worden stopgezet.
Coronaire hartziekte
In het WHI oestrogeen plus progestageen subonderzoek was er een statistisch niet-significant verhoogd risico op CHD voorvallen gemeld bij vrouwen die dagelijks CE (0,625 mg) plus MPA (2,5 mg) kregen in vergelijking met vrouwen die placebo kregen (41 versus 34 per 10.000 vrouwjaren). ). In jaar 1 werd een toename van het relatieve risico aangetoond en in de jaren 2 tot en met 5 werd een trend naar een afnemend relatief risico gemeld.
Bij postmenopauzale vrouwen met gedocumenteerde hartziekte (n = 2.763, gemiddelde 66,7 jaar oud), in een gecontroleerd klinisch onderzoek naar secundaire preventie van cardiovasculaire ziekte (Heart and Estrogen/Progestin Replacement Study [HERS]), behandeling met dagelijkse CE (0,625 mg ) plus MPA (2,5 mg) toonden geen cardiovasculair voordeel. Tijdens een gemiddelde follow-up van 4,1 jaar verminderde behandeling met CE plus MPA het totale aantal CHD-voorvallen bij postmenopauzale vrouwen met vastgestelde coronaire hartziekte niet. Er waren meer CHD-voorvallen in de met CE plus MPA behandelde groep dan in de placebogroep in jaar 1, maar niet in de daaropvolgende jaren. Tweeduizend driehonderdeenentwintig (2321) vrouwen uit de oorspronkelijke HERS-studie stemden ermee in om deel te nemen aan een open label-extensie van HERS, HERS II. De gemiddelde follow-up in HERS II was nog eens 2,7 jaar, voor een totaal van 6,8 jaar in totaal. De percentages van CHD-voorvallen waren vergelijkbaar bij vrouwen in de CE plus MPA-groep en de placebogroep in HERS, HERS II en in het algemeen.
Veneuze trombo-embolie
In het WHI oestrogeen plus progestageen subonderzoek werd een statistisch significant 2 maal hoger percentage VTE (DVT en PE) gerapporteerd bij vrouwen die dagelijks CE (0,625 mg) plus MPA (2,5 mg) kregen in vergelijking met vrouwen die placebo kregen (35 versus 17 per dag). 10.000 vrouwjaren). Statistisch significante risicoverhogingen voor zowel DVT (26 versus 13 per 10.000 vrouwjaren) als PE (18 versus 8 per 10.000 vrouwjaren) werden ook aangetoond. De toename van het VTE-risico werd gedurende het eerste jaar aangetoond en hield aan. (Zien Klinische studies .) Als een VTE optreedt of wordt vermoed, moet de behandeling met oestrogeen plus progestageen onmiddellijk worden stopgezet.
Indien mogelijk moeten oestrogenen plus progestagenen worden stopgezet ten minste 4 tot 6 weken vóór een operatie van het type dat gepaard gaat met een verhoogd risico op trombo-embolie, of tijdens perioden van langdurige immobilisatie.
Kwaadaardige neoplasma's
Borstkanker
De belangrijkste gerandomiseerde klinische studie die informatie geeft over borstkanker bij gebruikers van oestrogeen plus progestageen is de WHI-substudie van dagelijkse CE (0,625 mg) plus MPA (2,5 mg). Na een gemiddelde follow-up van 5,6 jaar rapporteerde de substudie oestrogeen plus progestageen een verhoogd risico op invasieve borstkanker bij vrouwen die dagelijks CE plus MPA gebruikten.
In dit deelonderzoek werd eerder gebruik van oestrogeen-alone of oestrogeen plus progestageentherapie gemeld door 26 procent van de vrouwen. Het relatieve risico op invasieve borstkanker was 1,24 en het absolute risico was 41 versus 33 gevallen per 10.000 vrouwjaren, voor CE plus MPA in vergelijking met placebo. Onder vrouwen die eerder hormoontherapie hadden gebruikt, was het relatieve risico op invasieve borstkanker 1,86, en het absolute risico was 46 versus 25 gevallen per 10.000 vrouwjaren, voor CE plus MPA in vergelijking met placebo. Onder vrouwen die geen eerdere hormoontherapie hadden gebruikt, was het relatieve risico op invasieve borstkanker 1,09, en het absolute risico was 40 versus 36 gevallen per 10.000 vrouwjaren, voor CE plus MPA in vergelijking met placebo. In dezelfde substudie waren invasieve borstkankers groter, hadden ze meer kans op klierpositief en werden ze in een verder gevorderd stadium gediagnosticeerd in de CE (0,625 mg) plus MPA (2,5 mg) groep in vergelijking met de placebogroep. Gemetastaseerde ziekte was zeldzaam zonder duidelijk verschil tussen de twee groepen. Andere prognostische factoren zoals histologisch subtype, graad en hormoonreceptorstatus verschilden niet tussen de groepen. (Zien Klinische studies .)
In overeenstemming met de klinische WHI-studie, hebben observationele studies ook een verhoogd risico op borstkanker gemeld bij behandeling met oestrogeen plus progestageen, en een kleiner risico op behandeling met alleen oestrogeen, na meerdere jaren van gebruik. Het risico nam toe met de duur van het gebruik en leek ongeveer 5 jaar na het stoppen van de behandeling terug te keren naar de uitgangswaarde (alleen de observationele onderzoeken hebben substantiële gegevens over het risico na het stoppen). Observationele studies suggereren ook dat het risico op borstkanker groter was en eerder duidelijk werd bij behandeling met oestrogeen plus progestageen dan bij behandeling met alleen oestrogeen. Deze onderzoeken hebben echter geen significante variatie gevonden in het risico op borstkanker tussen verschillende combinaties van oestrogeen en progestageen of toedieningswegen.
Van het gebruik van oestrogeen plus progestageen is gemeld dat het resulteert in een toename van abnormale mammogrammen die verdere evaluatie vereisen. Alle vrouwen dienen jaarlijks borstonderzoek te ondergaan door een zorgverlener en maandelijks zelfonderzoek van de borsten uit te voeren. Bovendien moeten mammografische onderzoeken worden gepland op basis van de leeftijd van de patiënt, risicofactoren en eerdere mammogramresultaten.
Endometriumkanker
Een verhoogd risico op endometriumkanker is gemeld bij het gebruik van ongehinderde oestrogeentherapie bij vrouwen met een baarmoeder. Het gerapporteerde risico op endometriumkanker bij oestrogeengebruikers zonder tegenstand is ongeveer 2 tot 12 keer groter dan bij niet-gebruikers en lijkt afhankelijk van de duur van de behandeling en van de oestrogeendosis. De meeste onderzoeken laten geen significant verhoogd risico zien in verband met het gebruik van oestrogenen gedurende minder dan 1 jaar. Het grootste risico lijkt geassocieerd te zijn met langdurig gebruik, met verhoogde risico's van 15 tot 24 keer gedurende 5 tot 10 jaar of langer. Het is aangetoond dat dit risico aanhoudt gedurende ten minste 8 tot 15 jaar nadat de oestrogeentherapie is stopgezet.
Klinische bewaking van alle vrouwen die oestrogeen- en progestageentherapie gebruiken, is belangrijk. In alle gevallen van niet-gediagnosticeerde aanhoudende of terugkerende abnormale genitale bloedingen moeten adequate diagnostische maatregelen worden genomen, inclusief endometriumafname indien geïndiceerd, om maligniteit uit te sluiten. Er is geen bewijs dat het gebruik van natuurlijke oestrogenen resulteert in een ander endometriumrisicoprofiel dan synthetische oestrogenen met een equivalente oestrogeendosis. Het is aangetoond dat het toevoegen van een progestageen aan oestrogeentherapie het risico op endometriumhyperplasie vermindert, wat een voorloper kan zijn van endometriumkanker.
Eierstokkanker
De WHI oestrogeen plus progestageen substudie rapporteerde een statistisch niet significant verhoogd risico op eierstokkanker. Na een gemiddelde follow-up van 5,6 jaar was het relatieve risico op eierstokkanker voor CE plus MPA versus placebo 1,58 (95 procent BI 0,77-3,24). Het absolute risico voor CE plus MPA was 4 versus 3 gevallen per 10.000 vrouwjaren. In sommige epidemiologische onderzoeken is het gebruik van oestrogeen plus progestageen en producten met alleen oestrogeen, in het bijzonder gedurende 5 jaar of langer, in verband gebracht met een verhoogd risico op eierstokkanker. De duur van de blootstelling die gepaard gaat met een verhoogd risico is echter niet consistent in alle epidemiologische onderzoeken en sommige rapporteren geen verband.
Waarschijnlijke dementie
In de WHIMS oestrogeen plus progestageen aanvullende studie van WHI werd een populatie van 4.532 postmenopauzale vrouwen in de leeftijd van 65 tot 79 jaar gerandomiseerd naar dagelijkse CE (0,625 mg) plus MPA (2,5 mg) of placebo. Na een gemiddelde follow-up van 4 jaar werd bij 40 vrouwen in de CE plus MPA-groep en 21 vrouwen in de placebogroep waarschijnlijke dementie vastgesteld. Het relatieve risico op waarschijnlijke dementie voor CE plus MPA versus placebo was 2,05 (95 procent BI, 1,21-3,48). Het absolute risico op waarschijnlijke dementie voor CE plus MPA versus placebo was 45 versus 22 gevallen per 10.000 vrouwjaren. Het is niet bekend of deze bevindingen van toepassing zijn op jongere postmenopauzale vrouwen. (Zien Klinische studies en PREVENTIEVE MAATREGELEN , Geriatrisch gebruik .)
Visuele afwijkingen
Beëindig de behandeling met oestrogeen plus progestageen in afwachting van onderzoek als er plotseling gedeeltelijk of volledig verlies van het gezichtsvermogen is, of een plotseling begin van proptosis, diplopie of migraine. Als onderzoek papiloedeem of retinale vasculaire laesies aan het licht brengt, moet de behandeling met oestrogeen plus progestageen permanent worden stopgezet.
PREVENTIEVE MAATREGELEN
Algemeen
Toevoeging van een progestageen wanneer een vrouw geen hysterectomie heeft gehad
Studies naar de toevoeging van een progestageen gedurende 10 of meer dagen van een cyclus van oestrogeentoediening, of dagelijks met oestrogeen in een continu regime, hebben een lagere incidentie van endometriumhyperplasie gerapporteerd dan zou worden veroorzaakt door oestrogeenbehandeling alleen. Endometriumhyperplasie kan een voorloper zijn van endometriumkanker.
Er zijn echter mogelijke risico's die kunnen worden geassocieerd met het gebruik van progestagenen met oestrogenen in vergelijking met regimes met alleen oestrogeen. Deze omvatten een verhoogd risico op borstkanker.
Onverwachte abnormale vaginale bloedingen
In geval van onverwachte abnormale vaginale bloedingen zijn adequate diagnostische maatregelen aangewezen.
Verhoogde bloeddruk
De bloeddruk moet met regelmatige tussenpozen worden gecontroleerd bij behandeling met oestrogeen en progestageen.
Hypertriglyceridemie
Bij vrouwen met reeds bestaande hypertriglyceridemie kan behandeling met oestrogeen plus progestageen gepaard gaan met verhogingen van plasmatriglyceriden die leiden tot pancreatitis. Overweeg stopzetting van de behandeling als pancreatitis optreedt.
Leverfunctiestoornis en/of verleden van cholestatische geelzucht
Oestrogenen plus progestagenen kunnen slecht worden gemetaboliseerd bij vrouwen met een verminderde leverfunctie. Voor vrouwen met een voorgeschiedenis van cholestatische geelzucht geassocieerd met oestrogeengebruik in het verleden of met zwangerschap, moet voorzichtigheid worden betracht en in geval van herhaling moet de medicatie worden stopgezet.
Vloeistofretentie
Progestagenen kunnen enige mate van vochtretentie veroorzaken. Vrouwen met aandoeningen die door deze factor kunnen worden beïnvloed, zoals hart- of nierinsufficiëntie, verdienen zorgvuldige observatie wanneer oestrogeen plus progestageen worden voorgeschreven.
Hypocalciëmie
Behandeling met oestrogeen plus progestageen moet met voorzichtigheid worden gebruikt bij vrouwen met hypoparathyreoïdie, aangezien door oestrogeen geïnduceerde hypocalciëmie kan optreden.
Verergering van andere aandoeningen
Behandeling met oestrogeen plus progestageen kan een verergering van astma, diabetes mellitus, epilepsie, migraine, porfyrie, systemische lupus erythematodes en hepatische hemangiomen veroorzaken en moet met voorzichtigheid worden gebruikt bij vrouwen met deze aandoeningen.
Patiënt informatie
Artsen wordt geadviseerd om de PATIËNT INFORMATIE bijsluiter met vrouwen voor wie zij PROVERA voorschrijven.
Er kan een verhoogd risico zijn op lichte geboorteafwijkingen bij kinderen van wie de moeder tijdens het eerste trimester van de zwangerschap wordt blootgesteld aan progestagenen. Het mogelijke risico voor de mannelijke baby is hypospadie, een aandoening waarbij de opening van de penis zich aan de onderkant bevindt in plaats van aan de punt van de penis. Deze aandoening komt van nature voor bij ongeveer 5 tot 8 per 1000 mannelijke geboorten. Het risico kan toenemen bij blootstelling aan PROVERA. Bij vrouwelijke baby's kunnen vergroting van de clitoris en fusie van de schaamlippen voorkomen. Er is echter geen duidelijk verband vastgesteld tussen hypospadie, vergroting van de clitoris en labiale fusie bij gebruik van PROVERA.
Informeer de patiënt over het belang van het melden van blootstelling aan PROVERA 5 mg tijdens de vroege zwangerschap.
Carcinogenese, mutagenese, verminderde vruchtbaarheid
kankerverwekkendheid
Het is aangetoond dat langdurige intramusculaire toediening van medroxyprogesteronacetaat borsttumoren veroorzaakt bij beagle-honden. Er was geen bewijs van een carcinogeen effect geassocieerd met de orale toediening van medroxyprogesteronacetaat aan ratten en muizen.
Langdurige continue toediening van oestrogeen plus progestageentherapie heeft een verhoogd risico op borstkanker en eierstokkanker aangetoond. (Zien WAARSCHUWINGEN en PREVENTIEVE MAATREGELEN .)
Genotoxiciteit
Medroxyprogesteronacetaat was niet mutageen in een reeks in vitro of in vivo genetische toxiciteitstests.
Vruchtbaarheid
Medroxyprogesteronacetaat in hoge doses is een antifertiliteitsgeneesmiddel en hoge doses zullen naar verwachting de vruchtbaarheid verminderen tot de stopzetting van de behandeling.
Zwangerschap
Zwangerschap Categorie X
PROVERA mag niet worden gebruikt tijdens de zwangerschap. (Zien CONTRA-INDICATIES .)
Er kunnen verhoogde risico's zijn op hypospadie, vergroting van de clitoris en labiale fusie bij kinderen van wie de moeder tijdens het eerste trimester van de zwangerschap wordt blootgesteld aan PROVERA 10 mg. Een duidelijk verband tussen deze aandoeningen bij het gebruik van PROVERA is echter niet vastgesteld.
Moeders die borstvoeding geven
PROVERA mag niet worden gebruikt tijdens het geven van borstvoeding. Detecteerbare hoeveelheden progestageen zijn geïdentificeerd in de moedermelk van moeders die borstvoeding geven en die progestagenen krijgen.
Pediatrisch gebruik
PROVERA 10 mg tabletten zijn niet geïndiceerd bij kinderen. Er zijn geen klinische onderzoeken uitgevoerd bij pediatrische patiënten.
Geriatrisch gebruik
Er zijn onvoldoende geriatrische vrouwen betrokken geweest bij klinische onderzoeken waarbij alleen PROVERA werd gebruikt om te bepalen of personen ouder dan 65 jaar verschillen van jongere proefpersonen in hun reactie op alleen PROVERA.
De onderzoeken naar het gezondheidsinitiatief voor vrouwen
In de WHI oestrogeen plus progestageen substudie (dagelijkse CE [0,625 mg] plus MPA [2,5 mg] versus placebo), was er een hoger relatief risico op niet-fatale beroerte en invasieve borstkanker bij vrouwen ouder dan 65 jaar. (Zien Klinische studies .)
Het geheugenonderzoek van het Women's Health Initiative
In de aanvullende WHIMS-onderzoeken bij postmenopauzale vrouwen van 65 tot 79 jaar oud was er een verhoogd risico op het ontwikkelen van waarschijnlijke dementie bij vrouwen die alleen oestrogeen of oestrogeen plus progestageen kregen in vergelijking met placebo. (Zien WAARSCHUWINGEN , Waarschijnlijke dementie .)
Aangezien beide aanvullende onderzoeken werden uitgevoerd bij vrouwen in de leeftijd van 65 tot 79 jaar, is het niet bekend of deze bevindingen van toepassing zijn op jongere postmenopauzale vrouwen. (Zien WAARSCHUWINGEN , Waarschijnlijke dementie .)
OVERDOSERING
Overdosering van behandeling met oestrogeen plus progestageen kan misselijkheid en braken, gevoelige borsten, duizeligheid, buikpijn, slaperigheid/vermoeidheid en onttrekkingsbloeding veroorzaken bij vrouwen. Behandeling van overdosering bestaat uit het staken van CE plus MPA samen met het instellen van passende symptomatische zorg.
CONTRA-INDICATIES
PROVERA 10 mg is gecontra-indiceerd bij vrouwen met een van de volgende aandoeningen:
KLINISCHE FARMACOLOGIE
Medroxyprogesteronacetaat (MPA), oraal of parenteraal toegediend in de aanbevolen doses aan vrouwen met voldoende endogeen oestrogeen, transformeert proliferatief in secretoir endometrium. Androgene en anabole effecten zijn opgemerkt, maar het medicijn is blijkbaar verstoken van significante oestrogene activiteit. Hoewel parenteraal toegediend MPA de productie van gonadotropine remt, wat op zijn beurt de folliculaire rijping en ovulatie voorkomt, wijzen de beschikbare gegevens erop dat dit niet gebeurt wanneer de gewoonlijk aanbevolen orale dosering wordt gegeven als een enkele dagelijkse dosis.
Farmacokinetiek
De farmacokinetiek van MPA werd bepaald bij 20 postmenopauzale vrouwen na toediening van een enkelvoudige dosis van acht PROVERA 2,5 mg tabletten of een enkelvoudige toediening van twee PROVERA 10 mg tabletten in nuchtere toestand. In een ander onderzoek werd de steady-state farmacokinetiek van MPA bepaald onder nuchtere omstandigheden bij 30 postmenopauzale vrouwen na dagelijkse toediening van één PROVERA 10 mg tablet gedurende 7 dagen. In beide onderzoeken werd MPA in serum gekwantificeerd met behulp van een gevalideerde gaschromatografie-massaspectrometrie (GC-MS) methode. Schattingen van de farmacokinetische parameters van MPA na enkelvoudige en meervoudige doses PROVERA-tabletten waren zeer variabel en zijn samengevat in Tabel 1.
Absorptie
Er is geen specifiek onderzoek gedaan naar de absolute biologische beschikbaarheid van MPA bij mensen. MPA wordt snel geabsorbeerd uit het maagdarmkanaal en maximale MPA-concentraties worden bereikt tussen 2 en 4 uur na orale toediening.
Toediening van PROVERA met voedsel verhoogt de biologische beschikbaarheid van MPA. Een dosis van 10 mg PROVERA 10 mg, onmiddellijk voor of na een maaltijd ingenomen, verhoogde de MPA Cmax (50 tot 70%) en de AUC (18 tot 33%). De halfwaardetijd van MPA veranderde niet met voedsel.
Verdeling
MPA is voor ongeveer 90% aan eiwit gebonden, voornamelijk aan albumine; er vindt geen MPA-binding plaats met geslachtshormoonbindend globuline.
Metabolisme
Na orale toediening wordt MPA uitgebreid gemetaboliseerd in de lever via hydroxylering, met daaropvolgende conjugatie en eliminatie in de urine.
uitscheiding
De meeste MPA-metabolieten worden in de urine uitgescheiden als glucuronideconjugaten en slechts kleine hoeveelheden worden uitgescheiden als sulfaten.
Specifieke populaties
Leverinsufficiëntie
MPA wordt bijna uitsluitend geëlimineerd via levermetabolisme. Bij 14 patiënten met gevorderde leverziekte was de MPA-dispositie significant veranderd (verminderde eliminatie). Bij patiënten met leververvetting was het gemiddelde percentage dat in de 24-uurs urine als intact MPA werd uitgescheiden na een dosis van 10 mg of 100 mg respectievelijk 7,3% en 6,4%.
Nierinsufficiëntie
Het effect van nierinsufficiëntie op de farmacokinetiek van PROVERA 5 mg is niet onderzocht.
Geneesmiddelinteracties
Medroxyprogesteronacetaat (MPA) wordt in vitro voornamelijk gemetaboliseerd door hydroxylering via het CYP3A4. Er zijn geen specifieke onderzoeken naar geneesmiddelinteracties uitgevoerd om de klinische effecten van CYP3A4-inductoren of -remmers op MPA te evalueren. Inductoren en/of remmers van CYP3A4 kunnen het metabolisme van MPA beïnvloeden.
Klinische studies
Effecten op het endometrium
In een 3 jaar durende, dubbelblinde, placebogecontroleerde studie van 356 niet-gehysterectomiseerde, postmenopauzale vrouwen tussen de 45 en 64 jaar, gerandomiseerd naar placebo (n=19), 0,625 mg alleen geconjugeerd oestrogeen (n=19) of 0,625 mg geconjugeerd oestrogeen plus cyclisch PROVERA (n=118), toonden de resultaten een verminderd risico op endometriumhyperplasie in de behandelingsgroep die 10 mg PROVERA 5 mg plus 0,625 mg geconjugeerde oestrogenen kreeg in vergelijking met de groep die alleen 0,625 mg geconjugeerde oestrogenen kreeg. Zie Tabel 2.
In een tweede 1-jarige studie werden 832 postmenopauzale vrouwen tussen de 45 en 65 jaar behandeld met dagelijks 0,625 mg geconjugeerd oestrogeen (dag 1-28) plus 5 mg cyclische PROVERA of 10 mg cyclische PROVERA (dag 15-28), of dagelijks 0,625 mg geconjugeerd oestrogeen alleen. De behandelingsgroepen die 5 of 10 mg cyclische PROVERA (dag 15-28) plus dagelijkse geconjugeerde oestrogenen kregen, vertoonden een significant lagere mate van hyperplasie in vergelijking met de groep met alleen geconjugeerde oestrogenen. Zie Tabel 3.
Onderzoek naar gezondheidsinitiatieven voor vrouwen
De WHI nam ongeveer 27.000 overwegend gezonde postmenopauzale vrouwen op in twee substudies om de risico's en voordelen van dagelijkse orale CE (0,625 mg)-alleen of in combinatie met MPA (2,5 mg) in vergelijking met placebo bij de preventie van bepaalde chronische ziekten te beoordelen. Het primaire eindpunt was de incidentie van coronaire hartziekte (CHD) (gedefinieerd als niet-fataal MI, stil MI en overlijden door CHD), met invasieve borstkanker als de primaire ongunstige uitkomst. Een "globale index" omvatte het vroegste optreden van CHD, invasieve borstkanker, beroerte, PE, endometriumkanker (alleen in de CE plus MPA-substudie), colorectale kanker, heupfractuur of overlijden door een andere oorzaak. Deze substudies evalueerden niet de effecten van CE-alone of CE plus MPA op symptomen van de menopauze.
WHI Oestrogeen Plus Progestageen Substudie
De WHI-substudie oestrogeen plus progestageen werd vroegtijdig stopgezet. Volgens de vooraf gedefinieerde stopregel overtrof na een gemiddelde follow-up van 5,6 jaar behandeling het verhoogde risico op invasieve borstkanker en cardiovasculaire gebeurtenissen de gespecificeerde voordelen die zijn opgenomen in de 'globale index'. Het absolute extra risico op gebeurtenissen opgenomen in de “globale index” was 19 per 10.000 vrouwjaren.
Voor die uitkomsten opgenomen in de WHI “global index” die statistische significantie bereikten na 5,6 jaar follow-up, waren de absolute extra risico’s per 10.000 vrouwjaren in de groep behandeld met CE plus MPA 7 extra CHD-voorvallen, 8 extra beroertes, 10 meer PE's en 8 meer invasieve borstkankers, terwijl de absolute risicoreductie per 10.000 vrouwjaren 6 minder colorectale kankers en 5 heupfracturen minder was.
De resultaten van de CE plus MPA-substudie, waaraan 16.608 vrouwen deelnamen (gemiddeld 63 jaar, variërend van 50 tot 79; 83,9 procent blank, 6,8 procent zwart, 5,4 procent Spaans, 3,9 procent overig) worden weergegeven in tabel 4. Deze resultaten weerspiegelen centraal beoordeelde gegevens na een gemiddelde follow-up van 5,6 jaar.
Het tijdstip van de start van de behandeling met oestrogeen plus progestageen ten opzichte van het begin van de menopauze kan het algehele risico-batenprofiel beïnvloeden. Het WHI oestrogeen plus progestageen-subonderzoek, gestratificeerd naar leeftijd, toonde bij vrouwen van 50 tot 59 jaar een niet-significante trend in de richting van een verminderd risico op totale mortaliteit [hazard ratio (HR) 0,69 (95 procent BI, 0,44-1,07)].
Geheugenonderzoek van het gezondheidsinitiatief voor vrouwen
De WHIMS oestrogeen plus progestageen aanvullende studie van WHI omvatte 4.532 overwegend gezonde postmenopauzale vrouwen van 65 jaar en ouder (47 procent was 65 tot 69 jaar oud, 35 procent was 70 tot 74 jaar oud en 18 procent was 75 jaar oud). leeftijd en ouder) om de effecten van dagelijkse CE (0,625 mg) plus MPA (2,5 mg) op de incidentie van waarschijnlijke dementie (primaire uitkomst) te evalueren in vergelijking met placebo.
Na een gemiddelde follow-up van 4 jaar was het relatieve risico op waarschijnlijke dementie voor CE plus MPA versus placebo 2,05 (95 procent BI, 1,21-3,48). Het absolute risico op waarschijnlijke dementie voor CE plus MPA versus placebo was 45 versus 33 per 10.000 vrouwjaren. Waarschijnlijke dementie zoals gedefinieerd in deze studie omvatte de ziekte van Alzheimer (AD), vasculaire dementie (VaD) en gemengd type (met kenmerken van zowel AD als VaD). De meest voorkomende classificatie van waarschijnlijke dementie in de behandelingsgroep en de placebogroep was AD. Aangezien het aanvullende onderzoek werd uitgevoerd bij vrouwen van 65 tot 79 jaar, is het niet bekend of deze bevindingen van toepassing zijn op jongere postmenopauzale vrouwen. (Zien WAARSCHUWINGEN , Waarschijnlijke dementie en PREVENTIEVE MAATREGELEN , Geriatrisch gebruik ).
PATIËNT INFORMATIE
PROVERA (pro-VE-rah) (medroxyprogesteronacetaat) tabletten, USP
Lees deze patiënteninformatie voordat u begint met het innemen van PROVERA en lees wat u krijgt elke keer dat u uw PROVERA-recept bijvult. Mogelijk is er nieuwe informatie. Deze informatie vervangt niet het praten met uw zorgverlener over uw medische toestand of uw behandeling.
Wat is de belangrijkste informatie die ik moet weten over PROVERA (een progestageen hormoon)?
- Gebruik geen oestrogenen met progestagenen om hartaandoeningen, hartaanvallen, beroertes of dementie (achteruitgang van de hersenfunctie) te voorkomen.
- Het gebruik van oestrogenen met progestagenen kan uw kans op hartaanvallen, beroertes, borstkanker en bloedstolsels vergroten.
- Het gebruik van oestrogenen met progestagenen kan uw kans op dementie vergroten, zo blijkt uit een onderzoek bij vrouwen van 65 jaar of ouder.
- U en uw zorgverlener moeten regelmatig overleggen of u nog steeds met PROVERA moet worden behandeld.
Wat is PROVERA 10 mg?
PROVERA is een geneesmiddel dat medroxyprogesteronacetaat, een progestageenhormoon, bevat.
Waar wordt PROVERA 5 mg voor gebruikt?
PROVERA wordt gebruikt om:
- Behandel menstruaties die zijn gestopt of om abnormale baarmoederbloedingen te behandelen. Vrouwen met een baarmoeder die niet zwanger zijn, die niet meer regelmatig menstrueren of die onregelmatige menstruaties beginnen te krijgen, kunnen een daling van hun progesteronspiegel hebben. Praat met uw zorgverlener over de vraag of PROVERA 10 mg geschikt voor u is.
- Verminder uw kansen om kanker van de baarmoeder (baarmoeder) te krijgen. Bij postmenopauzale vrouwen met een baarmoeder die oestrogenen gebruiken, zal het gebruik van progestageen in combinatie met oestrogeen uw kans op het krijgen van baarmoederkanker (baarmoeder) verminderen.
Wie mag PROVERA niet gebruiken?
Begin niet met het innemen van PROVERA als u:
- ongewone vaginale bloedingen hebben
- momenteel bepaalde vormen van kanker heeft of heeft gehad Oestrogeen plus progestageen kan uw kans op het krijgen van bepaalde soorten kanker vergroten, waaronder borstkanker. Als u kanker heeft of heeft gehad, overleg dan met uw zorgverlener of u PROVERA moet gebruiken.
- een beroerte of een hartaanval heeft gehad
- momenteel bloedstolsels heeft of heeft gehad
- momenteel leverproblemen heeft of heeft gehad
- zijn allergisch voor PROVERA 10 mg of een van de ingrediënten ervan Zie de lijst van ingrediënten in PROVERA aan het einde van deze bijsluiter.
- denk dat je zwanger bent PROVERA is niet voor zwangere vrouwen. Als u denkt dat u zwanger bent, moet u een zwangerschapstest ondergaan en de resultaten kennen. Gebruik PROVERA niet als de test positief is en overleg met uw zorgverlener. Er kan een verhoogd risico zijn op lichte geboorteafwijkingen bij kinderen van wie de moeder PROVERA gebruikt tijdens de eerste 4 maanden van de zwangerschap. PROVERA mag niet worden gebruikt als test voor zwangerschap.
Wat moet ik mijn zorgverlener vertellen voordat ik PROVERA 10 mg inneem? Vertel uw zorgverlener voordat u PROVERA 5 mg inneemt als u:
- andere medische problemen heeft Uw zorgverlener moet u mogelijk nauwkeuriger controleren als u bepaalde aandoeningen heeft, zoals astma (piepende ademhaling), epilepsie (aanvallen), diabetes, migraine, endometriose (ernstige bekkenpijn), lupus of problemen met uw hart, lever, schildklier, nieren of een hoog calciumgehalte in uw bloed.
- een operatie moeten ondergaan of op bedrust gaan liggen Uw zorgverlener zal u laten weten of u moet stoppen met het gebruik van PROVERA.
- geven borstvoeding Het hormoon in PROVERA kan in uw moedermelk terechtkomen.
Vertel uw zorgverlener over alle medicijnen die u gebruikt waaronder geneesmiddelen op recept en zonder recept, vitamines en kruidensupplementen. Sommige geneesmiddelen kunnen de werking van PROVERA beïnvloeden. PROVERA kan ook de werking van andere geneesmiddelen beïnvloeden.
Hoe moet ik PROVERA 10 mg innemen?
Begin met de laagste dosis en praat met uw zorgverlener over hoe goed die dosis voor u werkt. De laagste effectieve dosis PROVERA is niet vastgesteld. U en uw zorgverlener moeten regelmatig (elke 3 tot 6 maanden) praten over de dosis die u neemt en of u nog steeds behandeling met PROVERA nodig heeft.
Wat zijn de mogelijke bijwerkingen van PROVERA?
De volgende bijwerkingen zijn gemeld bij het gebruik van alleen PROVERA 10 mg:
- gevoelige borsten
- afscheiding van moedermelk
- doorbraakbloeding
- spotting (lichte vaginale bloeding)
- onregelmatige menstruatie
- amenorroe (afwezigheid van menstruatie)
- vaginale afscheidingen
- hoofdpijn
- nervositeit
- duizeligheid
- depressie
- slapeloosheid, slaperigheid, vermoeidheid
- premenstrueel syndroom-achtige symptomen
- tromboflebitis (ontstoken aderen)
- bloedstolsel
- jeuk, netelroos, huiduitslag
- acne
- haaruitval, haargroei
- buikpijn
- misselijkheid
- opgeblazen gevoel
- koorts
- toename in gewicht
- zwelling
- veranderingen in zicht en gevoeligheid voor contactlenzen
Bel onmiddellijk uw zorgverlener als u netelroos, problemen met ademhalen, zwelling van het gezicht, de mond, de tong of de nek krijgt
De volgende bijwerkingen zijn gemeld bij het gebruik van PROVERA 5 mg met een oestrogeen.
Bijwerkingen zijn gegroepeerd op hoe ernstig ze zijn en hoe vaak ze optreden wanneer u wordt behandeld.
Ernstige, maar minder vaak voorkomende bijwerkingen zijn onder meer:
- hartaanval
- hartinfarct
- bloedproppen
- Dementie
- borstkanker
- kanker van de baarmoeder
- kanker van de eierstok
- hoge bloeddruk
- hoge bloedsuikerspiegel
- Galblaas ziekte
- leverproblemen
- veranderingen in uw schildklierhormoonspiegels
- vergrotingen van goedaardige tumoren (“fibromen”)
Bel onmiddellijk uw zorgverlener als u een van de volgende waarschuwingssignalen of andere ongewone symptomen krijgt die u zorgen baren:
- nieuwe borstknobbels
- ongebruikelijk vaginaal bloedverlies
- veranderingen in visie en spraak
- plotselinge nieuwe ernstige hoofdpijn
- hevige pijn in uw borst of benen met of zonder kortademigheid, zwakte en vermoeidheid
- geheugenverlies of verwarring
Minder ernstige, maar vaak voorkomende bijwerkingen zijn:
- hoofdpijn
- Borstpijn
- onregelmatige vaginale bloedingen of spotting
- maag- of buikkrampen, opgeblazen gevoel
- misselijkheid en overgeven
- haaruitval
- vochtretentie
- vaginale schimmelinfectie
Dit zijn niet alle mogelijke bijwerkingen van PROVERA met of zonder oestrogeen. Vraag voor meer informatie uw zorgverlener of apotheker om advies over bijwerkingen. Vertel het uw zorgverlener als u een bijwerking heeft die u hindert of niet weggaat. U kunt bijwerkingen melden aan Pfizer op 1-800-438-1985 of FDA op 1-800-FDA-1088.
Wat kan ik doen om mijn kans op een ernstige bijwerking met PROVERA 10 mg te verkleinen?
- Praat regelmatig met uw zorgverlener over de vraag of u door moet gaan met het gebruik van PROVERA. De toevoeging van een progestageen wordt over het algemeen aanbevolen voor vrouwen met een baarmoeder om de kans op het krijgen van baarmoederkanker (baarmoeder) te verkleinen.
- Raadpleeg onmiddellijk uw zorgverlener als u vaginale bloedingen krijgt terwijl u PROVERA gebruikt.
- Laat elk jaar een bekkenonderzoek, borstonderzoek en mammogram (borströntgenfoto) uitvoeren, tenzij uw zorgverlener u iets anders vertelt. Als leden van uw familie borstkanker hebben gehad of als u ooit borstknobbels of een abnormaal mammogram heeft gehad, moet u mogelijk vaker borstonderzoeken ondergaan.
- Als u een hoge bloeddruk, een hoog cholesterolgehalte (vet in het bloed), diabetes, overgewicht heeft of als u tabak gebruikt, heeft u mogelijk een grotere kans op het krijgen van een hartaandoening. Vraag uw zorgverlener naar manieren om uw kans op het krijgen van een hartaandoening te verkleinen.
Algemene informatie over veilig en effectief gebruik van PROVERA
- Soms worden medicijnen voorgeschreven voor aandoeningen die niet in de patiëntenbijsluiter staan.
- Gebruik PROVERA niet voor aandoeningen waarvoor het niet is voorgeschreven.
- Geef PROVERA niet aan andere mensen, ook niet als zij dezelfde symptomen hebben als u. Het kan hen schaden.
Bewaar PROVERA 10 mg buiten het bereik van kinderen.
Deze folder geeft een samenvatting van de belangrijkste informatie over PROVERA. Als u meer informatie wilt, neem dan contact op met uw zorgverzekeraar of apotheker. U kunt informatie opvragen over PROVERA 10 mg die is geschreven voor gezondheidswerkers. U kunt meer informatie krijgen door het gratis nummer 1-800-438-1985 te bellen.
Wat zijn de ingrediënten in PROVERA?
Elke PROVERA 5 mg tablet voor orale toediening bevat 2,5 mg, 5 mg of 10 mg medroxyprogesteronacetaat.
Inactieve ingrediënten: calciumstearaat, maïszetmeel, lactose, minerale olie, sorbinezuur, sucrose, talk. De tablet van 2,5 mg bevat FD&C Geel nr. 6.
Het label van dit product is mogelijk bijgewerkt. Ga voor actuele volledige voorschrijfinformatie naar www.pfizer.com
