Danazol 50mg, 100mg, 200mg Gebruik, bijwerkingen en dosering. Prijs in online apotheek. Generieke medicijnen zonder recept.
Wat is Danazol 100 mg en hoe wordt het gebruikt?
Danazol 50 mg is een receptgeneesmiddel dat wordt gebruikt voor de behandeling van de symptomen van endometriose, erfelijk angio-oedeem en fibrocystische borstziekte. Danazol kan alleen of in combinatie met andere medicijnen worden gebruikt.
Danazol behoort tot een klasse geneesmiddelen die androgenen worden genoemd.
Het is niet bekend of Danazol veilig en effectief is bij kinderen.
Wat zijn de mogelijke bijwerkingen van Danazol?
Danazol 100 mg kan ernstige bijwerkingen veroorzaken, waaronder:
- zwelling van uw handen en voeten,
- menstruatieveranderingen (spotting, gemiste menstruatie),
- stemmingswisselingen,
- nervositeit,
- stemmingswisselingen,
- uitslag,
- jeuk,
- zwelling van het gezicht, de tong of de keel,
- ernstige duizeligheid en
- moeite met ademhalen
Roep meteen medische hulp in als u een van de bovenstaande symptomen heeft.
De meest voorkomende bijwerkingen van Danazol 200 mg zijn:
- gewichtstoename,
- acne,
- vette huid of haar,
- blozen,
- zweten,
- haaruitval,
- stemveranderingen (heesheid, veranderingen in toonhoogte),
- keelpijn,
- abnormale groei van lichaamshaar (bij vrouwen),
- vaginale droogheid, irritatie, branderig gevoel of jeuk,
- verminderde borstomvang,
- water afstotend,
- depressie,
- opgeblazen gevoel,
- prikkelbaarheid,
- veranderingen in de menstruatiecyclus (spotting, onregelmatige bloeding, gemiste menstruatie),
- nervositeit, en
- stemmingswisselingen
Vertel het uw arts als u een bijwerking heeft die u hindert of die niet weggaat.
Dit zijn niet alle mogelijke bijwerkingen van Danazol. Vraag uw arts of apotheker om meer informatie.
Bel uw arts voor medisch advies over bijwerkingen. U kunt bijwerkingen melden aan de FDA op 1-800-FDA-1088.
OMSCHRIJVING
Danazol 50 mg is een synthetische steroïde afgeleid van ethisteron. Het is een wit tot lichtgeel kristallijn poeder, praktisch onoplosbaar of onoplosbaar in water en matig oplosbaar in alcohol. Chemisch gezien is danazol 100 mg 17α-Pregna-2,4-dien-20-yno [2,3-d]-isoxazol-17-ol. De molecuulformule is C22H27NO2. Het heeft een molecuulgewicht van 337,46 en de volgende structuurformule:
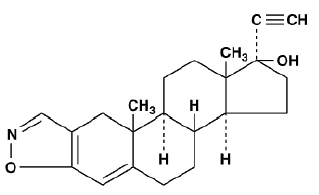
Danazol capsules voor orale toediening bevatten 50 mg, 100 mg of 200 mg danazol.
inactieve ingredienten
watervrije lactose, lactosemonohydraat, magnesiumstearaat, gepregelatiniseerd zetmeel, natriumlaurylsulfaat, talk. Capsuleomhulsels voor 200 mg danazol bevatten D&C Yellow #10, FD&C Red #40, D&C Red #28, gelatine en titaniumdioxide. Capsuleomhulsels voor 50 mg en 100 mg danazol 50 mg bevatten D&C Yellow #10, FD&C Red # 40, gelatine en titaniumdioxide. De afdrukinkt van de capsule bevat: schellakglazuur in ethanol, zwart ijzeroxide, n-butylalcohol, propyleenglycol, ethanol, methanol, FD&C Blue No. 2 Aluminium Lake, FD&C Red No. 40 Aluminium Lake, FD&C Blue No. 1 Aluminium Lake , en D&C Yellow No. 10 Aluminium Lake.
INDICATIES
Endometriose
Danazol 100 mg capsules zijn geïndiceerd voor de behandeling van endometriose die vatbaar is voor hormonale behandeling.
Erfelijk angio-oedeem
Danazol-capsules zijn geïndiceerd voor de preventie van aanvallen van alle soorten angio-oedeem (cutaan, abdominaal, larynx) bij mannen en vrouwen.
DOSERING EN ADMINISTRATIE
Endometriose
Bij matige tot ernstige ziekte, of bij patiënten die onvruchtbaar zijn als gevolg van endometriose, wordt een startdosis van 800 mg aanbevolen, verdeeld over twee doses. Amenorroe en een snelle reactie op pijnlijke symptomen worden het best bereikt bij deze dosering. Afhankelijk van de respons van de patiënt kan geleidelijke neerwaartse titratie worden overwogen tot een dosis die voldoende is om amenorroe in stand te houden. Voor milde gevallen wordt een initiële dagelijkse dosis van 200 mg tot 400 mg, verdeeld over twee doses, aanbevolen en deze kan worden aangepast afhankelijk van de respons van de patiënt. De therapie moet tijdens de menstruatie beginnen. Anders moeten geschikte tests worden uitgevoerd om er zeker van te zijn dat de patiënte niet zwanger is tijdens de behandeling met danazol 50 mg capsules (zie: CONTRA-INDICATIES en WAARSCHUWINGEN ). Het is essentieel dat de therapie 3 tot 6 maanden ononderbroken wordt voortgezet, maar kan indien nodig worden verlengd tot 9 maanden. Als de symptomen na beëindiging van de therapie terugkeren, kan de behandeling worden hervat .
Erfelijk angio-oedeem
De doseringsvereisten voor continue behandeling van erfelijk angio-oedeem met danazol-capsules moeten individueel worden bepaald op basis van de klinische respons van de patiënt. Het wordt aanbevolen om de patiënt te starten met 200 mg, twee of drie keer per dag. Nadat een gunstige initiële respons is verkregen in termen van preventie van episodes van oedemateuze aanvallen, dient de juiste continue dosering te worden bepaald door de dosering te verlagen met 50% of minder met tussenpozen van één tot drie maanden of langer als de frequentie van aanvallen voorafgaand aan de behandeling dit vereist. . Als er een aanval optreedt, kan de dagelijkse dosering worden verhoogd met maximaal 200 mg. Tijdens de dosisaanpassingsfase is nauwlettende controle van de respons van de patiënt geïndiceerd, vooral als de patiënt een voorgeschiedenis heeft van luchtwegbetrokkenheid.
HOE GELEVERD
Danazol 50 mg capsules USP, 50 mg zijn verkrijgbaar als ondoorzichtige maïs/witte ondoorzichtige capsules bedrukt met het logo "LANNETT" op de dop en "1392" op de romp en worden geleverd in:
Flessen van 100 ( NDC 0527-1392-01)
Danazol-capsules USP, 100 mg zijn verkrijgbaar als ondoorzichtige maïs/maïs ondoorzichtige capsules bedrukt met het logo "LANNETT" op de dop en "1368" op de romp en worden geleverd in:
Flessen van 100 ( NDC 0527-1368-01)
Danazol-capsules USP, 200 mg zijn verkrijgbaar als oranje ondoorzichtige/oranje ondoorzichtige capsules bedrukt met het logo "LANNETT" op de dop en "1369" op de romp en worden geleverd in:
Flessen van 60 ( NDC 0527-1369-06) Flessen van 100 ( NDC 0527-1369-01)
Bewaren bij 20 ° tot 25 ° C (68 ° tot 77 ° F) (zie USP-gecontroleerde kamertemperatuur).
Doseer in een goed gesloten container met een kindveilige sluiting zoals gedefinieerd in de USP.
Gedistribueerd door: Lannett Company, Inc. Philadelphia, PA 19154. Herzien: mei 2018
BIJWERKINGEN
De volgende gebeurtenissen zijn gemeld in verband met het gebruik van danazol 100 mg capsules:
Androgeenachtige effecten zijn onder meer gewichtstoename, acne en seborroe. Licht hirsutisme, oedeem, haaruitval, stemverandering, die de vorm kan aannemen van heesheid, keelpijn of van instabiliteit of verdieping van de toonhoogte, kan optreden en kan aanhouden na stopzetting van de therapie. Hypertrofie van de clitoris is zeldzaam.
Andere mogelijke endocriene effecten zijn menstruatiestoornissen, waaronder spotting, verandering van de timing van de cyclus en amenorroe. Hoewel cyclische bloedingen en ovulaties gewoonlijk terugkeren binnen 60-90 dagen na stopzetting van de behandeling met danazol-capsules, is af en toe aanhoudende amenorroe gemeld.
Blozen, zweten, vaginale droogheid en irritatie en vermindering van de borstomvang, kunnen wijzen op een verlaging van oestrogeen. Nervositeit en emotionele labiliteit zijn gemeld. Bij de man kan tijdens de behandeling een bescheiden afname van de spermatogenese zichtbaar zijn. Afwijkingen in het spermavolume, de viscositeit, het aantal zaadcellen en de beweeglijkheid kunnen optreden bij patiënten die langdurig worden behandeld.
Leverdisfunctie, zoals blijkt uit reversibele verhoogde serumenzymen en/of geelzucht, is gemeld bij patiënten die een dagelijkse dosis danazol-capsules van 400 mg of meer kregen. Het wordt aanbevolen dat patiënten die danazol-capsules krijgen, worden gecontroleerd op leverdisfunctie door laboratoriumtests en klinische observatie. Ernstige levertoxiciteit, waaronder cholestatische geelzucht, peliosis hepatis, leveradenoom, hepatocellulair letsel, hepatocellulaire geelzucht en leverfalen zijn gemeld (zie WAARSCHUWINGEN en PREVENTIEVE MAATREGELEN ).
Afwijkingen in laboratoriumtests kunnen optreden tijdens therapie met danazol 50 mg capsules, waaronder CPK, glucosetolerantie, glucagon, schildklierbindend globuline, geslachtshormoonbindend globuline, andere plasma-eiwitten, lipiden en lipoproteïnen.
De volgende reacties zijn gemeld, een oorzakelijk verband met de toediening van danazol-capsules is niet bevestigd of weerlegd;
Allergisch: urticaria, pruritus en zelden verstopte neus;
CZS-effecten: hoofdpijn, nervositeit en emotionele labiliteit, duizeligheid en flauwvallen, depressie, vermoeidheid, slaapstoornissen, tremor, paresthesieën, zwakte, visusstoornissen en zelden goedaardige intracraniële hypertensie, angst, veranderingen in eetlust, koude rillingen en zelden convulsies, Guillain-Barre-syndroom ;
Gastro-intestinaal: gastro-enteritis, misselijkheid, braken, constipatie en zelden pancreatitis en miltpeliose;
Musculoskeletaal: spierkrampen of -spasmen, of pijn, gewrichtspijn, gewrichtsblokkering, gewrichtszwelling, pijn in rug, nek of ledematen, en zelden, carpaaltunnelsyndroom dat secundair kan zijn aan vochtretentie;
Urogenitaal: hematurie, langdurige posttherapie amenorroe;
Hematologische: een toename van het aantal rode bloedcellen en bloedplaatjes. Reversibele erythrocytose, leukocytose of polycytemie kan worden veroorzaakt. Eosinofilie, leukopenie en trombocytopenie zijn ook opgemerkt.
Huid: huiduitslag (maculopapulair, vesiculair, papulair, purpurisch, petechiaal), en zelden, gevoeligheid voor de zon, Stevens-Johnson-syndroom en erythema multiforme;
Ander: verhoogde insulinebehoefte bij diabetespatiënten, verandering in libido, myocardinfarct, hartkloppingen, tachycardie, verhoging van de bloeddruk, interstitiële pneumonitis en in zeldzame gevallen cataract, bloedend tandvlees, koorts, bekkenpijn, afscheiding uit de tepels. Maligne levertumoren zijn in zeldzame gevallen gemeld na langdurig gebruik.
DRUG-INTERACTIES
Verlenging van de protrombinetijd treedt op bij patiënten die gestabiliseerd zijn op warfarine.
Therapie met danazol 50 mg kan een verhoging van de carbamazepinespiegels veroorzaken bij patiënten die beide geneesmiddelen gebruiken.

Danazol 50 mg kan insulineresistentie veroorzaken. Voorzichtigheid is geboden bij gebruik met antidiabetica.
Danazol 100 mg kan de plasmaspiegels van ciclosporine en tacrolimus verhogen, wat leidt tot een toename van de niertoxiciteit van deze geneesmiddelen. Controle van de systemische concentraties van deze geneesmiddelen en geschikte dosisaanpassingen kunnen nodig zijn bij gelijktijdig gebruik met danazol.
Danazol 100 mg kan de calcemische respons op synthetische vitamine D-analogen bij primaire hypoparathyreoïdie verhogen.
Het risico op myopathie en rabdomyolyse wordt verhoogd door gelijktijdige toediening van danazol 50 mg met statines zoals simvastatine, atorvastatine en lovastatine. Voorzichtigheid is geboden bij gelijktijdig gebruik. Raadpleeg de productetikettering van statinegeneesmiddelen voor specifieke informatie over dosisbeperkingen in aanwezigheid van danazol.
WAARSCHUWINGEN
Het gebruik van danazol 100 mg tijdens de zwangerschap is gecontra-indiceerd. Een gevoelige test (bijv. bèta-subeenheidtest indien beschikbaar) die vroege zwangerschap kan bepalen, wordt aanbevolen onmiddellijk vóór het begin van de therapie. Bovendien moet tijdens de behandeling een niet-hormonale anticonceptiemethode worden gebruikt. Als een patiënte zwanger wordt tijdens het gebruik van danazol 200 mg, moet de toediening van het geneesmiddel worden gestaakt en moet de patiënt worden geïnformeerd over het mogelijke risico voor de foetus. Blootstelling aan danazol 200 mg in utero kan leiden tot androgene effecten op de vrouwelijke foetus; meldingen van clitorale hypertrofie, labiale fusie, urogenitaal sinusdefect, vaginale atresie en ambigue genitaliën zijn ontvangen (zie PREVENTIEVE MAATREGELEN : Zwangerschap, Teratogene effecten).
Trombo-embolie, trombotische en tromboflebitische voorvallen, waaronder sagittale sinustrombose en levensbedreigende of fatale beroertes, zijn gemeld.
Ervaring met langdurige therapie met danazol 100 mg is beperkt. Peliosis hepatis en goedaardig leveradenoom zijn waargenomen bij langdurig gebruik. Peliosis hepatis en leveradenoom kunnen stil zijn totdat ze gecompliceerd worden door acute, mogelijk levensbedreigende intra-abdominale bloeding. De arts dient daarom alert te zijn op deze mogelijkheid. Er moeten pogingen worden ondernomen om de laagste dosis te bepalen die voldoende bescherming biedt. Als met het geneesmiddel werd begonnen in een tijd van verergering van erfelijk angioneurotisch oedeem als gevolg van trauma, stress of een andere oorzaak, moeten periodieke pogingen worden overwogen om de therapie te verminderen of stop te zetten.
Danazol 100 mg is in verband gebracht met verschillende gevallen van goedaardige intracraniële hypertensie, ook bekend als pseudotumor cerebri. Vroege tekenen en symptomen van goedaardige intracraniële hypertensie zijn onder meer papiloedeem, hoofdpijn, misselijkheid en braken, en visuele stoornissen. Patiënten met deze symptomen moeten worden gescreend op papiloedeem en, indien aanwezig, moeten de patiënten worden geadviseerd om onmiddellijk te stoppen met danazol 100 mg en te worden doorverwezen naar een neuroloog voor verdere diagnose en zorg.
Een tijdelijke verandering van lipoproteïnen in de vorm van verminderde lipoproteïnen met hoge dichtheid en mogelijk verhoogde lipoproteïnen met lage dichtheid is gemeld tijdens behandeling met danazol. Deze veranderingen kunnen opvallend zijn en voorschrijvers dienen de mogelijke impact op het risico op atherosclerose en coronaire hartziekte in overweging te nemen in overeenstemming met het mogelijke voordeel van de therapie voor de patiënt.
Patiënten moeten nauwlettend worden gecontroleerd op tekenen van androgene effecten, waarvan sommige mogelijk niet reversibel zijn, zelfs niet wanneer de toediening van het geneesmiddel wordt stopgezet.
PREVENTIEVE MAATREGELEN
Omdat danazol-capsules enige mate van vochtretentie kunnen veroorzaken, vereisen aandoeningen die door deze factor kunnen worden beïnvloed, zoals epilepsie, migraine of hart- of nierdisfunctie, polycytemie en hypertensie, zorgvuldige observatie. Voorzichtig gebruiken bij patiënten met diabetes mellitus.
Aangezien een leverfunctiestoornis die zich manifesteert door bescheiden verhogingen van de serumtransaminasenspiegels is gemeld bij patiënten die werden behandeld met danazol-capsules, moeten periodieke leverfunctietesten worden uitgevoerd (zie WAARSCHUWINGEN en ONGEWENSTE REACTIES ).
Van toediening van danazol 50 mg is gemeld dat het de manifestaties van acute intermitterende porfyrie verergert (zie CONTRA-INDICATIES ).
Laboratoriumcontrole van de hematologische toestand moet worden overwogen.
Laboratorium testen
Behandeling met danazol kan de laboratoriumbepalingen van testosteron, androstenedion en dehydroepiandrosteron verstoren. Andere metabole gebeurtenissen zijn onder meer een afname van schildklierbindend globuline en T4 met verhoogde opname van T3, maar zonder verstoring van het thyroïdstimulerend hormoon of van de vrije thyroxine-index.
Carcinogenese, mutagenese, verminderde vruchtbaarheid
De huidige gegevens zijn onvoldoende om de carcinogeniteit van danazol te beoordelen.
Zwangerschap Teratogene effecten
(zien CONTRA-INDICATIES .) Danazol 50 mg oraal toegediend aan drachtige ratten van de 6e tot de 15e dag van de dracht in doses tot 250 mg/kg/dag (7-15 maal de dosis voor de mens) resulteerde niet in geneesmiddelgeïnduceerde embryotoxiciteit of teratogeniteit, noch verschil in worp grootte, levensvatbaarheid of gewicht van het nageslacht in vergelijking met controles. Bij konijnen resulteerde de toediening van danazol 200 mg op dag 6-18 van de dracht in doses van 60 mg/kg/dag en hoger (2-4 maal de dosis voor de mens) in remming van de ontwikkeling van de foetus.
Moeders die borstvoeding geven
(zien CONTRA-INDICATIES .)
Pediatrisch gebruik
De veiligheid en werkzaamheid bij pediatrische patiënten zijn niet vastgesteld.
Geriatrisch gebruik
Klinische onderzoeken met danazol-capsules omvatten niet voldoende aantallen proefpersonen van 65 jaar en ouder om de veiligheid en werkzaamheid van Danocrine bij oudere patiënten te bepalen.
OVERDOSERING
Geen informatie verstrekt
CONTRA-INDICATIES
Danazol 50 mg capsules mogen niet worden toegediend aan patiënten met:
KLINISCHE FARMACOLOGIE
Danazol onderdrukt de hypofyse-ovarium-as. Deze onderdrukking is waarschijnlijk een combinatie van een depressieve hypothalamus-hypofyse-respons op een verlaagde oestrogeenproductie, de verandering van het geslachtssteroïdemetabolisme en de interactie van danazol met geslachtshormoonreceptoren. Het enige andere aantoonbare hormonale effect is een zwakke androgene activiteit. Danazol 50 mg onderdrukt de productie van zowel follikelstimulerend hormoon (FSH) als luteïniserend hormoon (LH).
Recent bewijs suggereert een direct remmend effect op gonadale plaatsen en een binding van danazol aan receptoren van gonadale steroïden op doelorganen. Bovendien is aangetoond dat danazol 50 mg de IgG-, IgM- en IgA-spiegels significant verlaagt, evenals de fosfolipide- en IgG-isotoop-auto-antilichamen bij patiënten met endometriose en geassocieerde verhogingen van auto-antilichamen, wat suggereert dat dit een ander mechanisme zou kunnen zijn waarmee het regressie van de ziekte vergemakkelijkt. .
Bij de behandeling van endometriose verandert danazol het normale en ectopische endometriumweefsel zodat het inactief en atrofisch wordt. Volledige resolutie van endometriumlaesies treedt in de meeste gevallen op.
Veranderingen in vaginale cytologie en baarmoederhalsslijm weerspiegelen het onderdrukkende effect van danazol op de hypofyse-ovarium-as.
Veranderingen in het menstruatiepatroon kunnen optreden.
Over het algemeen is de hypofyse-onderdrukkende werking van danazol 200 mg omkeerbaar. Ovulatie en cyclische bloeding keren gewoonlijk binnen 60 tot 90 dagen terug wanneer de behandeling met danazol 100 mg wordt stopgezet.
Bij de behandeling van erfelijk angio-oedeem voorkomt danazol in effectieve doses aanvallen van de ziekte die wordt gekenmerkt door episodisch oedeem van de buikorganen, extremiteiten, gezicht en luchtwegen, die invaliderend kunnen zijn en, als de luchtweg erbij betrokken is, fataal kunnen zijn. Bovendien corrigeert danazol 100 mg gedeeltelijk of volledig de primaire biochemische afwijking van erfelijk angio-oedeem door de niveaus van de deficiënte C1-esteraseremmer (C1El) te verhogen. Als gevolg van deze actie worden ook de serumspiegels van de C4-component van het complementsysteem verhoogd.
Farmacokinetiek
Absorptie
Na orale toediening van een dosis van 400 mg aan gezonde mannelijke vrijwilligers, worden piekplasmaconcentraties van danazol bereikt tussen 2 en 8 uur, met een mediane Tmax-waarde van 4 uur. Steady-state-omstandigheden worden waargenomen na 6 dagen van tweemaal daagse dosering van danazol 100 mg capsules.
De farmacokinetische parameters van danazol 100 mg capsules na toediening van een orale dosis van 400 mg aan gezonde mannen zijn samengevat in de volgende tabel:
De farmacokinetische parameters van danazol-capsules na orale toediening van enkelvoudige doses van 100, 200 en 400 mg aan gezonde vrouwelijke vrijwilligers zijn samengevat in de volgende tabel:
Dosisproportionaliteit
Onderzoeken naar biologische beschikbaarheid geven aan dat de bloedspiegels niet proportioneel toenemen met verhogingen van de toegediende dosis.
Toediening van een enkele dosis danazolcapsules bij gezonde vrouwelijke vrijwilligers vond dat een 4-voudige dosisverhoging in nuchtere en gevoede toestand slechts een 1,6- en 2,5-voudige toename van de AUC en een 1,3- en 2,2-voudige toename van de Cmax opleverde. Een vergelijkbare mate van niet-dosisproportionaliteit werd waargenomen bij steady-state.
Voedseleffect
Toediening van een enkelvoudige dosis van 100 mg en 200 mg capsules danazol aan vrouwelijke vrijwilligers toonde aan dat zowel de mate van beschikbaarheid als de maximale plasmaconcentratie respectievelijk 3 tot 4 keer stegen na een maaltijd (> 30 gram vet), in vergelijking met de nuchtere toestand. Verder vertraagde voedsel ook de gemiddelde tijd tot de piekconcentratie van danazol met ongeveer 30 minuten. Zelfs na meerdere doseringen onder minder extreme voedsel/nuchtere omstandigheden, bleef er een ongeveer 2- tot 2,5-voudig verschil in biologische beschikbaarheid tussen de gevoede en nuchtere toestand.
Verdeling
Danazol 100 mg is lipofiel en kan zich in celmembranen verdelen, wat de waarschijnlijkheid van verspreiding in diepe weefselcompartimenten aangeeft.
Metabolisme en uitscheiding
Danazol 200 mg lijkt te worden gemetaboliseerd en de metabolieten worden geëlimineerd via renale en fecale routes. De twee primaire metabolieten die in de urine worden uitgescheiden, zijn 2-hydroxymethyldanazol 50 mg en ethisteron. In de ontlasting werden minstens tien verschillende producten geïdentificeerd.
De gerapporteerde eliminatiehalfwaardetijd van danazol 100 mg varieert tussen onderzoeken. De gemiddelde halfwaardetijd van danazol bij gezonde mannen is 9,7 uur. Na 6 maanden dosering van 200 mg driemaal daags bij endometriosepatiënten, werd de halfwaardetijd van danazol gerapporteerd als 23,7 uur.
PATIËNT INFORMATIE
Geen informatie verstrekt. Raadpleeg de WAARSCHUWINGEN en PREVENTIEVE MAATREGELEN secties.
