Imdur 40mg, 20mg, 30mg, 60mg Isosorbide Gebruik, bijwerkingen en dosering. Prijs in online apotheek. Generieke medicijnen zonder recept.
Wat is Imdur 30 mg en hoe wordt het gebruikt?
Imdur 30 mg is een receptgeneesmiddel dat wordt gebruikt om de symptomen van pijn op de borst (angina pectoris) te behandelen. Imdur 30 mg kan alleen of in combinatie met andere medicijnen worden gebruikt.
Imdur 20 mg behoort tot een klasse geneesmiddelen die nitraten, angina pectoris wordt genoemd.
Het is niet bekend of Imdur 60 mg veilig en effectief is bij kinderen.
Wat zijn mogelijke bijwerkingen van Imdur?
Bijwerkingen van Imdur zijn onder meer:
- flauwvallen,
- snelle, onregelmatige of bonzende hartslagen,
- uitslag,
- jeuk,
- zwelling in het gezicht, de tong en de keel,
- ernstige duizeligheid, en
- moeite met ademhalen
Roep meteen medische hulp in als u een van de bovenstaande symptomen heeft.
De meest voorkomende bijwerkingen van Imdur 30 mg zijn:
- hoofdpijn,
- duizeligheid,
- duizeligheid, en
- misselijkheid
Vertel het uw arts als u een bijwerking heeft die u hindert of die niet weggaat.
Dit zijn niet alle mogelijke bijwerkingen van Imdur. Vraag uw arts of apotheker om meer informatie.
Bel uw arts voor medisch advies over bijwerkingen. U kunt bijwerkingen melden aan de FDA op 1-800-FDA-1088.
OMSCHRIJVING
Isosorbide-mononitraat (ISMN), een organisch nitraat en de belangrijkste biologisch actieve metaboliet van isosorbidedinitraat (ISDN), is een vasodilatator met effecten op zowel slagaders als aders.
IMDUR®-tabletten, voor orale toediening, bevatten 30 mg, 60 mg of 120 mg isosorbidemononitraat in een formulering met verlengde afgifte. Bovendien bevat elke tablet de volgende inactieve ingrediënten: colloïdaal siliciumdioxide, gehydrogeneerde ricinusolie, hypromellose, lactosemonohydraat, magnesiumstearaat, microkristallijne cellulose en talk.
De molecuulformule van ISMN is C6H9NO6 en het molecuulgewicht is 191,14. De chemische naam voor ISMN is 1,4:3,6-dianhydro-,D-glucitol 5-nitraat; de verbinding heeft de volgende structuurformule:
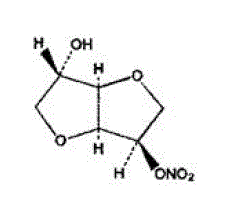
ISMN is een witte, kristallijne, geurloze verbinding die stabiel is in lucht en in oplossing, een smeltpunt heeft van ongeveer 90°C en een optische rotatie van +144° (2% in water, 20°C).
Isosorbide-mononitraat is vrij oplosbaar in water, ethanol, methanol, chloroform, ethylacetaat en dichloormethaan.
INDICATIES
IMDUR-tabletten zijn geïndiceerd voor de preventie van angina pectoris als gevolg van coronaire hartziekte. Het begin van de werking van oraal isosorbide-mononitraat is niet snel genoeg om dit product nuttig te laten zijn bij het afbreken van een acute angina-episode.
DOSERING EN ADMINISTRATIE
De aanbevolen startdosering van IMDUR-tabletten is 30 mg (toegediend als een enkele tablet van 30 mg of als 1/2 van een tablet van 60 mg) of 60 mg (toegediend als een enkele tablet) eenmaal daags. Na enkele dagen kan de dosering worden verhoogd tot 120 mg (gegeven als een enkele tablet van 120 mg of als twee tabletten van 60 mg) eenmaal daags. In zeldzame gevallen kan 240 mg nodig zijn. De dagelijkse dosis IMDUR-tabletten moet 's ochtends bij het opstaan worden ingenomen. IMDUR-tabletten met verlengde afgifte mogen niet worden gekauwd of fijngemaakt en moeten samen met een half glas vloeistof worden doorgeslikt. Breek de tablet van 30 mg niet.
HOE GELEVERD
IMDUR tabletten met verlengde afgifte 30 mg zijn witte, capsulevormige tabletten met een breukstreep aan één kant en de inscriptie "IMDUR" aan de kant zonder breukgleuf. Ze worden als volgt geleverd:
Flessen van 100 NDC 0085-1374-01
IMDUR tabletten met verlengde afgifte 60 mg zijn witte, capsulevormige tabletten met een breukstreep aan één kant met quot;60-60" en gegraveerd "IMDUR" aan de niet-gestreepte kant. Ze worden als volgt geleverd:
Flessen van 100 NDC 0085-2028-01
IMDUR 30 mg tabletten met verlengde afgifte 120 mg zijn witte, capsulevormige tabletten met de inscriptie "IMDUR" aan de ene kant en "120" aan de andere kant. Ze worden als volgt geleverd:
Flessen van 100 NDC 0085-0091-01
Bewaren bij een gecontroleerde kamertemperatuur van 20 ° - 25 ° C (68 ° -77 ° F) [Zie USP].
Gefabriceerd door: Kremers urban Pharmaceuticals inc, seymour,IN47274,USA. Herzien: december 2010
BIJWERKINGEN
De onderstaande tabel toont de frequenties van de bijwerkingen die optraden bij> 5% van de proefpersonen in drie placebogecontroleerde Noord-Amerikaanse onderzoeken waarin patiënten in de actieve behandelingsarm 30 mg, 60 mg, 120 mg of 240 mg isosorbide kregen. mononitraat als IMDUR 60 mg tabletten eenmaal daags. Tussen haakjes toont dezelfde tabel de frequenties waarmee deze bijwerkingen in verband werden gebracht met het staken van de behandeling. In totaal stopte 8% van de patiënten die 30 mg, 60 mg, 120 mg of 240 mg isosorbidemononitraat kregen in de drie placebogecontroleerde Noord-Amerikaanse onderzoeken de behandeling vanwege bijwerkingen. De meeste hiervan stopten vanwege hoofdpijn. Duizeligheid werd zelden geassocieerd met terugtrekking uit deze onderzoeken. Aangezien hoofdpijn een dosisgerelateerde bijwerking lijkt te zijn en de neiging heeft te verdwijnen bij voortzetting van de behandeling, wordt aanbevolen de IMDUR-behandeling te starten met lage doses gedurende enkele dagen voordat deze tot het gewenste niveau wordt verhoogd.
FREQUENTIE EN ONGEWENSTE GEBEURTENISSEN (GESTOPT) *
Bovendien werden de drie Noord-Amerikaanse onderzoeken samengevoegd met 11 gecontroleerde onderzoeken die in Europa werden uitgevoerd. Van de 14 gecontroleerde onderzoeken werden in totaal 711 patiënten gerandomiseerd naar IMDUR-tabletten. Toen de gepoolde gegevens werden beoordeeld, waren hoofdpijn en duizeligheid de enige bijwerkingen die door >5% van de patiënten werden gemeld. Andere bijwerkingen, elk gemeld door ≤ 5% van de blootgestelde patiënten, en in veel gevallen met een onzeker verband met de medicamenteuze behandeling, waren:
Autonome zenuwstelselaandoeningen : Droge mond, opvliegers.
Lichaam als geheel : Asthenie, rugpijn, pijn op de borst, oedeem, vermoeidheid, koorts, griepachtige symptomen, malaise, rigors.
Cardiovasculaire aandoeningen, algemeen : Hartfalen, hypertensie, hypotensie.
Aandoeningen van het centrale en perifere zenuwstelsel : Duizeligheid, hoofdpijn, hypesthesie, migraine, neuritis, parese, paresthesie, ptosis, tremor, duizeligheid.
Maagdarmstelselaandoeningen Buikpijn, constipatie, diarree, dyspepsie, winderigheid, maagzweer, gastritis, glossitis, hemorragische maagzweer, aambeien, dunne ontlasting, melena, misselijkheid, braken.
Gehoor- en vestibulaire aandoeningen : Oorpijn, oorsuizen, trommelvliesperforatie.
Hartslag- en ritmestoornissen : Aritmie, aritmie atriale, atriale fibrillatie, bradycardie, bundeltakblok, extrasystole, palpitatie, tachycardie, ventriculaire tachycardie.
Lever- en galwegenaandoeningen : SGOT-verhoging, SGPT-verhoging.
Metabole en voedingsstoornissen : Hyperurikemie, hypokaliëmie.
Aandoeningen van het bewegingsapparaat : Artralgie, frozen shoulder, spierzwakte, musculoskeletale pijn, myalgie, myositis, peesaandoening, torticollis.
Myo-, endo-, pericardiale en klepaandoeningen : Angina pectoris verergerd, hartgeruis, abnormaal hartgeluid, myocardinfarct, Q-golfafwijking.
Bloedplaatjes-, bloedings- en stollingsstoornissen : Purpura, trombocytopenie.
Psychische stoornissen Angst, concentratiestoornissen, verwardheid, verminderd libido, depressie, impotentie, slapeloosheid, nervositeit, paroniria, slaperigheid.
Rode bloedcellen stoornis : Hypochrome bloedarmoede.
Voortplantingsstoornissen, vrouwen : Atrofische vaginitis, pijn in de borst.
Weerstandsmechanisme-stoornissen : Bacteriële infectie, moniliasis, virale infectie.
Ademhalingsstelselaandoeningen : Bronchitis, bronchospasme, hoesten, kortademigheid, toegenomen sputum, verstopte neus, faryngitis, pneumonie, longinfiltratie, reutjes, rhinitis, sinusitis.
Huid- en aanhangselsaandoeningen : Acne, abnormale haartextuur, toegenomen transpiratie, pruritus, huiduitslag, huidknobbeltje.
Urinewegaandoeningen : Polyurie, niersteen, urineweginfectie.
Vasculaire (extracardiale) aandoeningen : Blozen, claudicatio intermittens, beenulcus, spatader.
Visiestoornissen : Conjunctivitis, fotofobie, abnormaal zicht.
Bovendien is de volgende spontane bijwerking gemeld tijdens het op de markt brengen van isosorbidemononitraat: syncope.

DRUG-INTERACTIES
De vaatverwijdende effecten van isosorbidemononitraat kunnen additief zijn met die van andere vaatverwijders. Vooral alcohol blijkt additieve effecten van deze variëteit te vertonen.
Duidelijke symptomatische orthostatische hypotensie is gemeld wanneer calciumkanaalblokkers en organische nitraten in combinatie werden gebruikt. Dosisaanpassingen van beide klasse middelen kunnen nodig zijn.
Geneesmiddel-/laboratoriumtestinteracties
Nitraten en nitrieten kunnen de Zlatkis-Zak-kleurreactie verstoren, waardoor vals lage waarden bij de serumcholesterolbepalingen ontstaan.
WAARSCHUWINGEN
Versterking van de vaatverwijdende effecten van IMDUR door sildenafil kan leiden tot ernstige hypotensie. Het tijdsverloop en de dosisafhankelijkheid van deze interactie zijn niet onderzocht. Geschikte ondersteunende zorg is niet onderzocht, maar het lijkt redelijk om dit te behandelen als een nitraatoverdosis, met elevatie van de extremiteiten en met centrale volume-expansie.
De voordelen van ISMN bij patiënten met een acuut myocardinfarct of congestief hartfalen zijn niet vastgesteld; omdat de effecten van isosorbidemononitraat moeilijk snel te beëindigen zijn, wordt dit medicijn in deze situaties niet aanbevolen.
Als isosorbidemononitraat in deze omstandigheden wordt gebruikt, moet zorgvuldige klinische of hemodynamische monitoring worden gebruikt om de gevaren van hypotensie en tachycardie te voorkomen.
PREVENTIEVE MAATREGELEN
Algemeen
Ernstige hypotensie, vooral bij een rechtopstaande houding, kan optreden bij zelfs kleine doses isosorbidemononitraat. Dit geneesmiddel moet daarom met voorzichtigheid worden gebruikt bij patiënten die mogelijk een volumedepletie hebben of die, om welke reden dan ook, al hypotensief zijn. Hypotensie veroorzaakt door isosorbidemononitraat kan gepaard gaan met paradoxale bradycardie en verhoogde angina pectoris.
Nitraattherapie kan de angina verergeren die wordt veroorzaakt door hypertrofische cardiomyopathie.
Bij industriële werknemers die langdurig zijn blootgesteld aan onbekende (vermoedelijk hoge) doses organische nitraten, treedt duidelijk tolerantie op. Pijn op de borst, acuut myocardinfarct en zelfs plotselinge dood zijn opgetreden tijdens tijdelijke onttrekking van nitraten bij deze werknemers, wat het bestaan van echte fysieke afhankelijkheid aantoont. Het belang van deze waarnemingen voor het routinematige, klinische gebruik van oraal isosorbidemononitraat is niet bekend.
Carcinogenese, mutagenese, verminderde vruchtbaarheid
Er is geen bewijs van carcinogeniteit waargenomen bij ratten die werden blootgesteld aan isosorbidemononitraat in hun voeding in doses tot 900 mg/kg/dag gedurende de eerste 6 maanden en 500 mg/kg/dag gedurende de resterende duur van een onderzoek waarin mannetjes werden gedoseerd tot 121 weken en vrouwen kregen een dosis tot 137 weken. Er zijn geen aanwijzingen voor carcinogeniteit waargenomen bij muizen die gedurende maximaal 104 weken in hun dieet aan isosorbidemononitraat werden blootgesteld bij doses tot 900 mg/kg/dag.
Isosorbidemononitraat veroorzaakte geen genmutaties (Ames-test, muislymfoomtest) of chromosoomafwijkingen (menselijke lymfocyten en micronucleustests bij muizen) bij biologisch relevante concentraties.
Er werden geen effecten op de vruchtbaarheid waargenomen in een onderzoek waarin mannelijke en vrouwelijke ratten doses tot 750 mg/kg/dag kregen toegediend, beginnend bij mannetjes 9 weken voor het paren en bij vrouwtjes 2 weken voor het paren.
Zwangerschap
Teratogene effecten
Zwangerschap Categorie B
In onderzoeken die waren opgezet om effecten van isosorbidemononitraat op de embryo-foetale ontwikkeling te detecteren, waren doses tot 240 of 248 mg/kg/dag, toegediend aan drachtige ratten en konijnen, niet geassocieerd met bewijs van dergelijke effecten. Deze dierdoses zijn ongeveer 100 keer de maximaal aanbevolen dosis voor de mens (120 mg bij een vrouw van 50 kg) wanneer de vergelijking is gebaseerd op lichaamsgewicht; wanneer de vergelijking is gebaseerd op het lichaamsoppervlak, is de dosis voor ratten ongeveer 17 keer de dosis voor de mens en de dosis voor konijnen ongeveer 38 keer de dosis voor de mens. Er zijn echter geen adequate en goed gecontroleerde onderzoeken bij zwangere vrouwen. Omdat reproductiestudies bij dieren niet altijd voorspellend zijn voor de respons van de mens, mogen IMDUR-tabletten alleen tijdens de zwangerschap worden gebruikt als dit duidelijk nodig is.
Nietteratogene effecten
Neonatale overleving en ontwikkeling en incidentie van doodgeborenen werden nadelig beïnvloed wanneer zwangere ratten orale doses van 750 (maar niet 300) mg isosorbidemononitraat/kg/dag kregen tijdens de late dracht en lactatie. Deze dosis (ongeveer 312 keer de dosis voor de mens wanneer de vergelijking is gebaseerd op lichaamsgewicht en 54 keer de dosis voor de mens wanneer de vergelijking is gebaseerd op het lichaamsoppervlak) ging gepaard met een afname van de gewichtstoename en motorische activiteit van de moeder en tekenen van verminderde lactatie.
Moeders die borstvoeding geven
Het is niet bekend of dit geneesmiddel wordt uitgescheiden in de moedermelk. Omdat veel geneesmiddelen in de moedermelk worden uitgescheiden, is voorzichtigheid geboden wanneer ISMN wordt toegediend aan een zogende moeder.
Pediatrisch gebruik
De veiligheid en werkzaamheid van ISMN bij pediatrische patiënten zijn niet vastgesteld.
Geriatrisch gebruik
Klinische onderzoeken met IMDUR 60 mg tabletten bevatten onvoldoende informatie over patiënten van 65 jaar en ouder om te bepalen of zij anders reageren dan jongere patiënten. Andere gerapporteerde klinische ervaring met IMDUR 20 mg heeft geen verschillen in respons tussen oudere en jongere patiënten aangetoond. Klinische ervaring met in de literatuur gerapporteerde organische nitraten wees op een potentieel voor ernstige hypotensie en verhoogde gevoeligheid voor nitraten bij ouderen. Over het algemeen moet de dosiskeuze voor een oudere patiënt voorzichtig zijn, meestal beginnend aan het lage uiteinde van het doseringsbereik, als gevolg van de grotere frequentie van verminderde lever-, nier- of hartfunctie en van gelijktijdige ziekte of andere medicamenteuze behandeling.
Oudere patiënten kunnen een verminderde baroreceptorfunctie hebben en kunnen ernstige orthostatische hypotensie ontwikkelen wanneer vaatverwijders worden gebruikt. IMDUR 60 mg moet daarom met voorzichtigheid worden gebruikt bij oudere patiënten die mogelijk een volumedepletie hebben, meerdere medicijnen gebruiken of die, om welke reden dan ook, al hypotensief zijn. Hypotensie veroorzaakt door isosorbidemononitraat kan gepaard gaan met paradoxale bradycardie en verhoogde angina pectoris.
Oudere patiënten kunnen vatbaarder zijn voor hypotensie en lopen mogelijk een groter risico om te vallen bij therapeutische doses nitroglycerine.
Nitraattherapie kan de angina, veroorzaakt door hypertrofische cardiomyopathie, verergeren, vooral bij ouderen.
OVERDOSERING
Hemodynamische effecten
De nadelige effecten van een overdosis isosorbidemononitraat zijn over het algemeen het gevolg van het vermogen van isosorbidemononitraat om vasodilatatie, veneuze pooling, verminderde hartminuutvolume en hypotensie te induceren. Deze hemodynamische veranderingen kunnen proteïsche manifestaties hebben, waaronder verhoogde intracraniale druk, met enige of alle aanhoudende kloppende hoofdpijn, verwardheid en matige koorts; duizeligheid, hartkloppingen; visuele stoornissen; misselijkheid en braken (mogelijk met koliek en zelfs bloederige diarree); syncope (vooral in de rechtopstaande houding); luchthonger en kortademigheid, later gevolgd door verminderde ademhalingsinspanning; diaforese, met de huid rood of koud en klam; hartblok en bradycardie; verlamming; coma; toevallen en overlijden.
Laboratoriumbepalingen van serumspiegels van isosorbidemononitraat en zijn metabolieten zijn niet algemeen beschikbaar, en dergelijke bepalingen hebben in ieder geval geen vastgestelde rol bij de behandeling van een overdosis isosorbidemononitraat.
Er zijn geen gegevens die suggereren welke dosis isosorbidemononitraat waarschijnlijk levensbedreigend is bij de mens. Bij ratten en muizen is er een significante letaliteit bij doses van respectievelijk 2000 mg/kg en 3000 mg/kg.
Er zijn geen gegevens beschikbaar die fysiologische manoeuvres suggereren (bijv. manoeuvres om de pH van de urine te veranderen) die de eliminatie van isosorbidemononitraat zouden kunnen versnellen. In het bijzonder is bekend dat dialyse niet effectief is bij het verwijderen van isosorbidemononitraat uit het lichaam.
Er is geen specifieke antagonist van de vaatverwijdende effecten van isosorbidemononitraat bekend en er is geen interventie bekend. Er is geen specifieke antagonist van de vaatverwijdende effecten van isosorbidemononitraat bekend en er is geen enkele interventie onderworpen aan gecontroleerd onderzoek als behandeling van overdosering met isosorbidemononitraat. Omdat de hypotensie die gepaard gaat met een overdosis isosorbidemononitraat het gevolg is van venodilatatie en arteriële hypovolemie, moet een voorzichtige behandeling in deze situatie worden gericht op een toename van het centrale vloeistofvolume. Passieve verhoging van de benen van de patiënt kan voldoende zijn, maar intraveneuze infusie van een normale zoutoplossing of soortgelijke vloeistof kan ook nodig zijn.
Het gebruik van epinefrine of andere arteriële vasoconstrictoren in deze setting zal waarschijnlijk meer kwaad dan goed doen.
Bij patiënten met nierziekte of congestief hartfalen is therapie die leidt tot centrale volumeexpansie niet zonder gevaar. Behandeling van overdosering met isosorbidemononitraat bij deze patiënten kan subtiel en moeilijk zijn, en invasieve controle kan nodig zijn.
methemoglobinemie
Methemoglobinemie is gemeld bij patiënten die andere organische nitraten kregen, en het kan waarschijnlijk ook optreden als bijwerking van isosorbidemononitraat. Nitraationen die vrijkomen tijdens het metabolisme van isosorbidemononitraat kunnen hemoglobine oxideren tot methemoglobine. Zelfs bij patiënten die totaal geen cytochroom-b-reductaseactiviteit hebben, en zelfs aangenomen dat het nitraatgedeelte van isosorbidemononitraat kwantitatief wordt toegepast op de oxidatie van hemoglobine, zou echter ongeveer 2 mg/kg isosorbidemononitraat nodig moeten zijn voordat een van deze patiënten zich klinisch significant manifesteert ( ≥10%) methemoglobinemie. Bij patiënten met een normale reductasefunctie zou voor een significante productie van methemoglobine zelfs grotere doses isosorbidemononitraat nodig zijn. In één onderzoek waarbij 36 patiënten 2-4 weken continue nitroglycerinetherapie kregen van 3,1 tot 4,4 mg/uur (equivalent, in de totale toegediende dosis nitraationen, aan 7,8-11,1 mg isosorbidemononitraat per uur), was het gemiddelde methemoglobinegehalte gemeten was 0,2%; dit was vergelijkbaar met wat werd waargenomen bij parallelle patiënten die placebo kregen.
Niettegenstaande deze waarnemingen zijn er casusrapporten van significante methemoglobinemie in combinatie met matige overdoses van organische nitraten. Van geen van de getroffen patiënten werd gedacht dat ze ongewoon vatbaar waren.
Methemoglobineniveaus zijn verkrijgbaar bij de meeste klinische laboratoria. De diagnose moet worden vermoed bij patiënten die tekenen van verminderde zuurstoftoevoer vertonen ondanks voldoende hartminuutvolume en voldoende arteriële pO2. Klassiek wordt methemoglobinemisch bloed beschreven als chocoladebruin zonder kleurverandering bij blootstelling aan lucht. Wanneer methemoglobinemie wordt gediagnosticeerd, is de voorkeursbehandeling methyleenblauw, 1-2 mg/kg intraveneus.
CONTRA-INDICATIES
IMDUR 20 mg tabletten zijn gecontra-indiceerd bij patiënten die overgevoeligheid of idiosyncratische reacties op andere nitraten of nitrieten hebben vertoond.
KLINISCHE FARMACOLOGIE
Werkingsmechanisme
Het IMDUR-product is een orale formulering met verlengde afgifte van ISMN, de belangrijkste actieve metaboliet van isosorbidedinitraat; het grootste deel van de klinische activiteit van het dinitraat is toe te schrijven aan het mononitraat.
De belangrijkste farmacologische werking van ISMN en alle organische nitraten in het algemeen is relaxatie van vasculaire gladde spieren, waardoor verwijding van perifere slagaders en aders wordt veroorzaakt, vooral de laatste. Verwijding van de aderen bevordert perifere pooling van bloed, vermindert de veneuze terugkeer naar het hart, waardoor de linker ventriculaire einddiastolische druk en pulmonale capillaire wiggedruk (preload) verminderen. Arteriolaire relaxatie vermindert de systemische vaatweerstand, de systolische arteriële druk en de gemiddelde arteriële druk (afterload). Verwijding van de kransslagaders komt ook voor. Het relatieve belang van preload-reductie, afterload-reductie en coronaire dilatatie blijft ongedefinieerd.
farmacodynamiek
Doseringsschema's voor de meeste chronisch gebruikte geneesmiddelen zijn ontworpen om plasmaconcentraties te verschaffen die continu hoger zijn dan een minimaal effectieve concentratie. Deze strategie is niet geschikt voor organische nitraten. Verschillende goed gecontroleerde klinische onderzoeken hebben inspanningstesten gebruikt om de anti-angineuze werkzaamheid van continu toegediende nitraten te beoordelen. In de grote meerderheid van deze onderzoeken waren actieve middelen niet te onderscheiden van placebo na 24 uur (of minder) continue therapie. Pogingen om tolerantie te overwinnen door dosisescalatie, zelfs tot doses die ver boven de acuut gebruikte doses liggen, zijn consequent mislukt. Pas nadat nitraten enkele uren uit het lichaam zijn verdwenen, is hun anti-angineuze werkzaamheid hersteld. IMDUR-tabletten, bij langdurig gebruik gedurende 42 dagen, gedoseerd met 120 mg eenmaal daags, bleven de trainingsprestaties verbeteren na 4 uur en 12 uur na toediening, maar de effecten (hoewel beter dan placebo) zijn minder dan of op zijn best gelijk aan de effecten van de eerste dosis van 60 mg.
Farmacokinetiek en metabolisme
Na orale toediening van ISMN als oplossing of tabletten met onmiddellijke afgifte, worden maximale plasmaconcentraties van ISMN bereikt in 30 tot 60 minuten, met een absolute biologische beschikbaarheid van ongeveer 100%. Na intraveneuze toediening wordt ISMN in ongeveer 9 minuten in het totale lichaamswater gedistribueerd met een distributievolume van ongeveer 0,6-0,7 l/kg. Isosorbide-mononitraat is voor ongeveer 5% gebonden aan humane plasma-eiwitten en wordt gedistribueerd naar bloedcellen en speeksel. Isosorbidemononitraat wordt voornamelijk gemetaboliseerd door de lever, maar in tegenstelling tot oraal isosorbidedinitraat is het niet onderhevig aan first-pass-metabolisme. Isosorbide-mononitraat wordt geklaard door denitratie tot isosorbide en glucuronidering als het mononitraat, waarbij 96% van de toegediende dosis binnen 5 dagen in de urine wordt uitgescheiden en slechts ongeveer 1% wordt uitgescheiden in de feces. Er zijn ten minste zes verschillende verbindingen in de urine aangetroffen, waarbij ongeveer 2% van de dosis als onveranderd geneesmiddel werd uitgescheiden en ten minste vijf metabolieten. De metabolieten zijn niet farmacologisch actief. Nierklaring is goed voor slechts ongeveer 4% van de totale lichaamsklaring. De gemiddelde plasma-eliminatiehalfwaardetijd van ISMN is ongeveer 5 uur.
De dispositie van ISMN bij patiënten met verschillende gradaties van nierinsufficiëntie, levercirrose of hartdisfunctie werd geëvalueerd en bleek vergelijkbaar te zijn met die waargenomen bij gezonde proefpersonen. De eliminatiehalfwaardetijd van ISMN was niet verlengd en er was geen accumulatie van het geneesmiddel bij patiënten met chronisch nierfalen na meervoudige orale toediening.
De farmacokinetiek en/of biologische beschikbaarheid van IMDUR 40 mg tabletten is onderzocht bij zowel normale vrijwilligers als patiënten na toediening van enkelvoudige en meervoudige doses. Gegevens uit deze onderzoeken suggereren dat de farmacokinetiek van ISMN, toegediend als IMDUR-tabletten, vergelijkbaar is tussen normale gezonde vrijwilligers en patiënten met angina pectoris. In onderzoeken met enkelvoudige en meervoudige doses was de farmacokinetiek van ISMN dosisproportioneel tussen 30 mg en 240 mg.
In een onderzoek met meerdere doses werd het effect van leeftijd op het farmacokinetische profiel van IMDUR 60 mg en 120 mg (2 × 60 mg) geëvalueerd bij proefpersonen 45 jaar. De resultaten van dat onderzoek geven aan dat er geen significante verschillen zijn in de farmacokinetische variabelen van ISMN tussen ouderen (≥65 jaar) en jongere personen (45-64 jaar) voor de dosis IMDUR 60 mg. De toediening van IMDUR-tabletten 120 mg (2 x 60 mg tabletten elke 24 uur gedurende 7 dagen) veroorzaakte een dosisproportionele toename van de Cmax en AUC, zonder veranderingen in Tmax of de terminale halfwaardetijd. De oudere groep (65-74 jaar) vertoonde 30% lagere schijnbare orale klaring (Cl/F) na de hogere dosis, dwz 120 mg, vergeleken met de jongere groep (45-64 jaar); Cl/F was niet verschillend tussen de twee groepen na het regime van 60 mg. Terwijl de Cl/F onafhankelijk was van de dosis in de jongere groep, vertoonde de oudere groep een iets lagere Cl/F na het 120 mg-regime in vergelijking met het 60 mg-regime. Verschillen tussen de twee leeftijdsgroepen waren echter niet statistisch significant. In hetzelfde onderzoek vertoonden vrouwen een lichte (15%) afname van de klaring wanneer de dosis werd verhoogd. Vrouwen vertoonden hogere AUC's en Cmax in vergelijking met mannen, maar deze verschillen werden verklaard door verschillen in lichaamsgewicht tussen de twee groepen. Toen de gegevens werden geanalyseerd met behulp van leeftijd als variabele, gaven de resultaten aan dat er geen significante verschillen waren in een van de farmacokinetische variabelen van ISMN tussen oudere (≥65 jaar) en jongere personen (45-64 jaar). De resultaten van deze studie moeten echter met de nodige voorzichtigheid worden bekeken vanwege het kleine aantal proefpersonen in elke leeftijdssubgroep en bijgevolg het gebrek aan voldoende statistische power.
De volgende tabel geeft een overzicht van de belangrijkste farmacokinetische parameters van ISMN na toediening van een enkelvoudige en meervoudige dosis van ISMN als drank of IMDUR-tabletten:
Voedseleffecten
De invloed van voedsel op de biologische beschikbaarheid van ISMN na toediening van een enkelvoudige dosis IMDUR-tabletten 60 mg werd geëvalueerd in drie verschillende onderzoeken met ofwel een "licht" ontbijt of een hoogcalorisch, vetrijk ontbijt. De resultaten van deze onderzoeken geven aan dat gelijktijdige inname van voedsel de snelheid (verhoging van Tmax) kan verlagen, maar niet de mate (AUC) van absorptie van ISMN.
Klinische proeven
Gecontroleerde onderzoeken met IMDUR-tabletten hebben anti-angineuze activiteit aangetoond na acute en chronische dosering. Toediening van IMDUR 40 mg tabletten eenmaal daags, vroeg in de ochtend bij het opstaan, leverde ten minste 12 uur angineuze activiteit op.
In een placebogecontroleerd parallel onderzoek werden 30, 60, 120 en 240 mg IMDUR 60 mg tabletten eenmaal daags gedurende maximaal 6 weken toegediend. Voorafgaand aan randomisatie voltooiden alle patiënten een enkelblinde placebofase van 1 tot 3 weken om de nitraatrespons en de reproduceerbaarheid van de totale trainingstijd op de loopband aan te tonen. Inspanningstolerantietests met behulp van het Bruce-protocol werden uitgevoerd vóór en op 4 en 12 uur na de ochtenddosis op dag 1, 7, 14, 28 en 42 van de dubbelblinde periode. IMDUR 60 mg tabletten 30 en 60 mg (alleen doses die acuut werden beoordeeld) vertoonden een significante toename van de totale loopbandtijd ten opzichte van de uitgangswaarde ten opzichte van placebo op 4 en 12 uur na de toediening van de eerste dosis. Op dag 42 vertoonden de doses van 120 en 240 mg IMDUR 40 mg tabletten een significante toename van de totale loopbandtijd op 4 en 12 uur na toediening, maar op dag 42 waren de doses van 30 en 60 mg niet langer te onderscheiden van placebo. Tijdens de chronische dosering werd in geen enkele IMDUR-behandelingsgroep een rebound waargenomen.
Gepoolde gegevens van twee andere onderzoeken, waarbij IMDUR 40 mg tabletten 60 mg eenmaal daags, ISDN 30 mg QID en placebo QID werden vergeleken bij patiënten met chronische stabiele angina met behulp van een gerandomiseerd, dubbelblind, drieweg-crossover-ontwerp, vonden statistisch significante verhogingen in inspanningstolerantie tijden voor IMDUR 20 mg-tabletten vergeleken met placebo op uur 4, 8 en 12 en met ISDN op uur 4. De toename van de inspanningstolerantie op dag 14, hoewel statistisch significant in vergelijking met placebo, was ongeveer de helft van die op dag 1 van het onderzoek .
PATIËNT INFORMATIE
Patiënten moeten worden verteld dat de anti-angineuze werkzaamheid van IMDUR 60 mg tabletten behouden kan blijven door het voorgeschreven doseringsschema zorgvuldig te volgen. Voor de meeste patiënten kan dit worden bereikt door de dosis in te nemen bij het opstaan.
Net als bij andere nitraten gaat soms dagelijkse hoofdpijn gepaard met de behandeling met isosorbidemononitraat. Bij patiënten die deze hoofdpijn krijgen, is de hoofdpijn een marker van de activiteit van het medicijn. Patiënten moeten de verleiding weerstaan om hoofdpijn te vermijden door het schema van hun behandeling met isosorbidemononitraat te wijzigen, aangezien verlies van hoofdpijn gepaard kan gaan met gelijktijdig verlies van anti-angineuze werkzaamheid. Aspirine of paracetamol verlicht vaak met succes isosorbide-mononitraat-geïnduceerde hoofdpijn zonder schadelijk effect op de anti-angineuze werkzaamheid van isosorbide-mononitraat.
Behandeling met isosorbidemononitraat kan gepaard gaan met een licht gevoel in het hoofd bij het staan, vooral vlak na het opstaan vanuit een liggende of zittende positie. Dit effect kan vaker voorkomen bij patiënten die ook alcohol hebben gedronken.
