Celebrex 100mg, 200mg Celecoxib Gebruik, bijwerkingen en dosering. Prijs in online apotheek. Generieke medicijnen zonder recept.
Wat is Celebrex 100 mg en hoe wordt het gebruikt?
Celebrex 200 mg is een receptgeneesmiddel dat wordt gebruikt om de symptomen van acute pijn of ontsteking te behandelen. Celebrex kan alleen of in combinatie met andere medicijnen worden gebruikt.
Celebrex 100 mg behoort tot een klasse geneesmiddelen die niet-steroïde anti-inflammatoire geneesmiddelen (NSAID's) worden genoemd.
Het is niet bekend of Celebrex veilig en effectief is bij kinderen jonger dan 2 jaar.
Wat zijn de mogelijke bijwerkingen van Celebrex 100 mg?
Celebrex 200 mg kan ernstige bijwerkingen veroorzaken, waaronder:
- zwelling,
- snelle gewichtstoename,
- kortademigheid,
- bloederige of teerachtige ontlasting,
- bloed ophoesten of braaksel dat op koffiedik lijkt,
- misselijkheid,
- maagpijn rechtsboven,
- jeuk,
- vermoeidheid,
- donkere urine,
- geel worden van de huid of ogen (geelzucht),
- weinig of geen plassen,
- zwelling in uw voeten of enkels,
- zich moe voelen,
- bleke huid,
- duizeligheid, en
- koude handen en voeten
Roep meteen medische hulp in als u een van de bovenstaande symptomen heeft.
De meest voorkomende bijwerkingen van Celebrex zijn:
- buikpijn,
- maagzuur,
- gas,
- diarree,
- constipatie,
- misselijkheid,
- braken,
- zwelling in uw handen of voeten,
- duizeligheid, en
- d
- verkoudheidsverschijnselen (verstopte neus, niezen, keelpijn)
Vertel het uw arts als u een bijwerking heeft die u hindert of die niet weggaat.
Dit zijn niet alle mogelijke bijwerkingen van Celebrex. Vraag uw arts of apotheker om meer informatie.
Bel uw arts voor medisch advies over bijwerkingen. U kunt bijwerkingen melden aan de FDA op 1-800-FDA-1088.
WAARSCHUWING
RISICO OP ERNSTIGE CARDIOVASCULAIRE EN GASTRO-INTESTINALE GEBEURTENISSEN
Cardiovasculaire trombotische gebeurtenissen
- Niet-steroïde anti-inflammatoire geneesmiddelen (NSAID's) veroorzaken een verhoogd risico op ernstige cardiovasculaire trombotische voorvallen, waaronder myocardinfarct en beroerte, die fataal kunnen zijn. Dit risico kan vroeg in de behandeling optreden en kan toenemen met de duur van het gebruik. [zie WAARSCHUWINGEN EN VOORZORGSMAATREGELEN]
- CELEBREX is gecontra-indiceerd bij coronaire bypassoperaties (CABG). [zie CONTRA-INDICATIES en WAARSCHUWINGEN EN VOORZORGSMAATREGELEN]
Gastro-intestinale bloeding, ulceratie en perforatie
- NSAID's veroorzaken een verhoogd risico op ernstige gastro-intestinale (GI) bijwerkingen, waaronder bloedingen, ulceratie en perforatie van de maag of darmen, die fataal kunnen zijn. Deze gebeurtenissen kunnen op elk moment tijdens het gebruik en zonder waarschuwingssymptomen optreden. Oudere patiënten en patiënten met een voorgeschiedenis van ulcus pepticum en/of gastro-intestinale bloeding lopen een groter risico op ernstige (GI) voorvallen. [zie WAARSCHUWINGEN EN VOORZORGSMAATREGELEN]
OMSCHRIJVING
CELEBREX (celecoxib) capsule is een niet-steroïde anti-inflammatoir geneesmiddel, verkrijgbaar als capsules met 50 mg, 100 mg, 200 mg en 400 mg celecoxib voor orale toediening. De chemische naam is 4-[5-(4-methylfenyl)-3-(trifluormethyl)-1H-pyrazol-1-yl] benzeensulfonamide en is een door een diaryl gesubstitueerd pyrazool. Het molecuulgewicht is 381,38. De moleculaire formule is C17H14F3N3O2S en heeft de volgende chemische structuur:
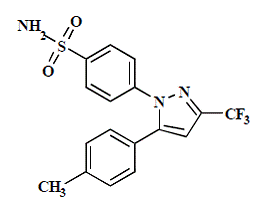
Celecoxib is een wit tot gebroken wit poeder met een pKa van 11,1 (sulfonamidegroep). Celecoxib is hydrofoob (log P is 3,5) en is praktisch onoplosbaar in waterige media bij een fysiologisch pH-bereik.
De inactieve ingrediënten in CELEBREX 200 mg zijn: croscarmellosenatrium, eetbare inkten, gelatine, lactosemonohydraat, magnesiumstearaat, povidon en natriumlaurylsulfaat.
INDICATIES
CELEBREX is aangegeven
Artrose (OA)
Voor de behandeling van de tekenen en symptomen van artrose [zie Klinische studies ].
Reumatoïde artritis (RA)
Voor de behandeling van de tekenen en symptomen van RA [zie Klinische studies ].
Juveniele reumatoïde artritis (JRA)
Voor de behandeling van de tekenen en symptomen van JRA bij patiënten van 2 jaar en ouder [zie: Klinische studies ].
Spondylitis ankylopoetica (AS)
Voor de behandeling van de tekenen en symptomen van AS [zie Klinische studies ].
Acute pijn
Voor de behandeling van acute pijn bij volwassenen [zie Klinische studies ].
Primaire dysmenorroe
Voor de behandeling van primaire dysmenorroe [zie Klinische studies ].
DOSERING EN ADMINISTRATIE
Algemene doseringsinstructies
Overweeg zorgvuldig de mogelijke voordelen en risico's van CELEBREX en andere behandelingsopties voordat u besluit CELEBREX te gebruiken. Gebruik de laagste effectieve dosering voor de kortste duur in overeenstemming met de individuele behandeldoelen van de patiënt [zie WAARSCHUWINGEN EN VOORZORGSMAATREGELEN ].
Deze doses kunnen worden gegeven zonder rekening te houden met het tijdstip van maaltijden.
artrose
Voor artrose is de dosering 200 mg per dag, toegediend als een enkele dosis of als 100 mg tweemaal daags.
Reumatoïde artritis
Voor RA is de dosering 100 mg tot 200 mg tweemaal daags.
Juveniele reumatoïde artritis
Voor JRA is de dosering voor pediatrische patiënten (leeftijd 2 jaar en ouder) gebaseerd op gewicht. Voor patiënten ≥10 kg tot ≤25 kg is de aanbevolen dosis 50 mg tweemaal daags. Voor patiënten >25 kg is de aanbevolen dosis 100 mg tweemaal daags.
Voor patiënten die moeite hebben met het doorslikken van capsules, kan de inhoud van een CELEBREX-capsule worden toegevoegd aan appelmoes. De volledige inhoud van de capsule wordt voorzichtig geleegd op een afgestreken theelepel koele of kamertemperatuur appelmoes en onmiddellijk ingenomen met water. De besprenkelde capsule-inhoud op appelmoes is tot 6 uur houdbaar onder gekoelde omstandigheden (2 °C tot 8 °C/35°F tot 45 °F).
Spondylitis ankylopoetica
Voor AS is de dosering van CELEBREX 200 mg per dag in enkelvoudige (eenmaal daags) of verdeelde (tweemaal daags) doses. Als er na 6 weken geen effect wordt waargenomen, kan een proef van 400 mg per dag de moeite waard zijn. Als er na 6 weken bij 400 mg per dag geen effect wordt waargenomen, is een respons niet waarschijnlijk en moeten alternatieve behandelingsopties worden overwogen.
Beheer van acute pijn en behandeling van primaire dysmenorroe
Voor de behandeling van acute pijn en de behandeling van primaire dysmenorroe is de dosering aanvankelijk 400 mg, indien nodig op de eerste dag gevolgd door een extra dosis van 200 mg. Op de volgende dagen is de aanbevolen dosis 200 mg tweemaal daags naar behoefte.
Speciale populaties
Leverfunctiestoornis
Bij patiënten met een matige leverfunctiestoornis (Child-Pugh-klasse B) de dosis met 50% verlagen. Het gebruik van CELEBREX 100 mg bij patiënten met een ernstige leverfunctiestoornis wordt niet aanbevolen [zie: WAARSCHUWINGEN EN VOORZORGSMAATREGELEN , Gebruik bij specifieke populaties , en KLINISCHE FARMACOLOGIE ].
Slechte metaboliseerders van CYP2C9-substraten
Bij volwassen patiënten van wie bekend is of vermoed wordt dat ze slechte CYP2C9-metaboliseerders zijn op basis van het genotype of voorgeschiedenis/ervaring met andere CYP2C9-substraten (zoals warfarine, fenytoïne), start u de behandeling met de helft van de laagst aanbevolen dosis.
Overweeg bij patiënten met JRA van wie bekend is of vermoed wordt dat ze slechte CYP2C9-metaboliseerders zijn, alternatieve behandelingen [zie Gebruik in specifieke populaties en KLINISCHE FARMACOLOGIE ].
HOE GELEVERD
Doseringsvormen en sterke punten
CELEBREX (celecoxib)-capsules:
50 mg wit, met omgekeerd wit bedrukt op de rode band van het lichaam en de dop met markeringen van 7767 op de dop en 50 op de romp.
100 mg wit, met omgekeerd wit gedrukt op de blauwe band van het lichaam en de dop met markeringen van 7767 op de dop en 100 op het lichaam.
200 mg wit, met omgekeerd bedrukt wit op gouden band met markeringen van 7767 op de dop en 200 op het lichaam.
400 mg wit, met omgekeerd gedrukt wit op groene band met markeringen van 7767 op de dop en 400 op het lichaam.
Opslag en behandeling
CELEBREX (celecoxib) 50 mg capsules zijn wit, met omgekeerd wit bedrukt op de rode band van het lichaam en de dop met markeringen van 7767 op de dop en 50 op de romp, geleverd als:
CELEBREX (celecoxib) 100 mg capsules zijn wit, met omgekeerd wit bedrukt op de blauwe band van het lichaam en de dop met markeringen van 7767 op de dop en 100 op de romp, geleverd als:
CELEBREX (celecoxib) 200 mg capsules zijn wit, met omgekeerd bedrukt wit op gouden band met markeringen van 7767 op de dop en 200 op de romp, geleverd als:
CELEBREX (celecoxib) 400 mg capsules zijn wit, met omgekeerd bedrukt wit op groene band met markeringen van 7767 op theca en 400 op het lichaam, geleverd als:
Opslag
Bewaren bij kamertemperatuur 20°C tot 25°C (68°F tot 77°F); excursies toegestaan tussen 15°C en 30°C (59°F tot 86°F) [zie USP-gecontroleerde kamertemperatuur ].
Gedistribueerd door: GD Searle LLC, Division of Pfizer Inc, NY, NY 10017. Herzien: april 2021
BIJWERKINGEN
De volgende bijwerkingen worden in andere secties van de etikettering in meer detail besproken:
- Cardiovasculaire trombotische gebeurtenissen [zie WAARSCHUWINGEN EN VOORZORGSMAATREGELEN ]
- GI-bloeding, ulceratie en perforatie [zie WAARSCHUWINGEN EN VOORZORGSMAATREGELEN ]
- Hepatotoxiciteit [zie WAARSCHUWINGEN EN VOORZORGSMAATREGELEN ]
- Hypertensie [zie WAARSCHUWINGEN EN VOORZORGSMAATREGELEN ]
- Hartfalen en oedeem [zie WAARSCHUWINGEN EN VOORZORGSMAATREGELEN ]
- Niertoxiciteit en hyperkaliëmie [zie WAARSCHUWINGEN EN VOORZORGSMAATREGELEN ]
- Anafylactische reacties [zie WAARSCHUWINGEN EN VOORZORGSMAATREGELEN ]
- Ernstige huidreacties [zie WAARSCHUWINGEN EN VOORZORGSMAATREGELEN ]
- Hematologische toxiciteit [zie WAARSCHUWINGEN EN VOORZORGSMAATREGELEN ]
Ervaring met klinische proeven
Omdat klinische onderzoeken onder sterk uiteenlopende omstandigheden worden uitgevoerd, kunnen de bijwerkingen die in de klinische onderzoeken van een geneesmiddel zijn waargenomen niet direct worden vergeleken met de percentages in de klinische onderzoeken van een ander geneesmiddel en komen mogelijk niet overeen met de percentages die in de praktijk worden waargenomen. De informatie over bijwerkingen uit klinische onderzoeken biedt echter een basis voor het identificeren van de bijwerkingen die verband lijken te houden met drugsgebruik en voor het benaderen van de percentages.
Van de met CELEBREX behandelde patiënten in de pre-marketing gecontroleerde klinische onderzoeken waren ongeveer 4.250 patiënten met artrose, ongeveer 2.100 patiënten met RA en ongeveer 1.050 patiënten met postoperatieve pijn. Meer dan 8.500 patiënten kregen een totale dagelijkse dosis CELEBREX 200 mg van 200 mg (100 mg tweemaal daags of 200 mg eenmaal daags) of meer, waaronder meer dan 400 die werden behandeld met 800 mg (400 mg tweemaal daags). Ongeveer 3.900 patiënten kregen CELEBREX in deze doses gedurende 6 maanden of langer; ongeveer 2.300 van hen hebben het voor 1 jaar of langer ontvangen en 124 van hen hebben het voor 2 jaar of langer ontvangen.
Pre-marketing onderzoek naar gecontroleerde artritis
Tabel 1 geeft een overzicht van alle bijwerkingen, ongeacht de causaliteit, die voorkwamen bij ≥2% van de patiënten die CELEBREX 100 mg kregen uit 12 gecontroleerde onderzoeken die werden uitgevoerd bij patiënten met artrose of RA met een placebo en/of een positieve controlegroep. Aangezien deze 12 onderzoeken een verschillende duur hadden en patiënten in de onderzoeken mogelijk niet voor dezelfde tijdsduur zijn blootgesteld, geven deze percentages geen cumulatieve frequenties van voorkomen weer.
In placebo- of actief-gecontroleerde klinische onderzoeken was het stopzettingspercentage als gevolg van bijwerkingen 7,1% voor patiënten die CELEBREX kregen en 6,1% voor patiënten die placebo kregen. Een van de meest voorkomende redenen voor stopzetting vanwege bijwerkingen in de CELEBREX-behandelingsgroepen waren dyspepsie en buikpijn (aangehaald als redenen voor stopzetting bij respectievelijk 0,8% en 0,7% van de CELEBREX-patiënten). Van de patiënten die placebo kregen, stopte 0,6% vanwege dyspepsie en stopte 0,6% vanwege buikpijn.
De volgende bijwerkingen traden op bij 0,1% tot 1,9% van de patiënten die werden behandeld met CELEBREX (100 mg tot 200 mg tweemaal daags of 200 mg eenmaal daags):
Gastro-intestinaal: Constipatie, diverticulitis, dysfagie, oprisping, oesofagitis, gastritis, gastro-enteritis, gastro-oesofageale reflux, aambeien, hiatale hernia, melena, droge mond, stomatitis, tenesmus, braken
Cardiovasculair: Verergerde hypertensie, angina pectoris, coronaire hartziekte, myocardinfarct
Algemeen: Overgevoeligheid, allergische reactie, pijn op de borst, cyste NOS, gegeneraliseerd oedeem, gezichtsoedeem, vermoeidheid, koorts, opvliegers, griepachtige symptomen, pijn, perifere pijn
Centraal, perifeer zenuwstelsel: Krampen in de benen, hypertonie, hypesthesie, migraine, paresthesie, duizeligheid
Horen en vestibulair: Doofheid, tinnitus
Hartslag en ritme: Hartkloppingen, tachycardie
Lever en gal: Leverenzym verhoogd (inclusief SGOT verhoogd, SGPT verhoogd)
Metabolisch en nutritioneel: bloedureumstikstof (BUN) verhoogd, creatinefosfokinase (CPK) verhoogd, hypercholesterolemie, hyperglykemie, hypokaliëmie, NPN verhoogd, creatinine verhoogd, alkalische fosfatase verhoogd, gewicht verhoogd
Musculoskeletaal: Artralgie, artrose, myalgie, synovitis, tendinitis
Bloedplaatjes (bloeding of stolling): Ecchymose, epistaxis, trombocytemie,
Psychiatrisch: Anorexia, angst, toegenomen eetlust, depressie, nervositeit, slaperigheid
Hemisch: Bloedarmoede
Ademhaling: Bronchitis, bronchospasme, verergerde bronchospasmen, hoesten, dyspneu, laryngitis, longontsteking
Huid en aanhangsels: Alopecia, dermatitis, fotosensitiviteitsreactie, pruritus, erythemateuze uitslag, maculopapulaire uitslag, huidaandoening, droge huid, toegenomen zweten, urticaria
Aandoeningen op de toedieningsplaats: Cellulitis, dermatitis contact
Urine: Albuminurie, cystitis, dysurie, hematurie, mictiefrequentie, niersteen
De volgende ernstige bijwerkingen (causaliteit niet geëvalueerd) kwamen voor bij
Cardiovasculair: Syncope, congestief hartfalen, ventrikelfibrilleren, longembolie, cerebrovasculair accident, perifeer gangreen, tromboflebitis
Gastro-intestinaal: Darmobstructie, darmperforatie, gastro-intestinale bloeding, colitis met bloeding, slokdarmperforatie, pancreatitis, ileus
Algemeen: Sepsis, plotselinge dood
Lever en gal: cholelithiasis
Hemic en lymfatisch: Trombocytopenie
Zenuwachtig: Ataxie, zelfmoord [zie DRUG-INTERACTIES ]
nier: Acuut nierfalen
Het Celecoxib-onderzoek naar de veiligheid van artritis op de lange termijn
[zien Klinische studies ]
Hematologische gebeurtenissen: De incidentie van klinisch significante verlagingen van hemoglobine (>2 g/dl) was lager bij patiënten die CELEBREX 400 mg tweemaal daags (0,5%) kregen in vergelijking met patiënten die diclofenac 75 mg tweemaal daags (1,3%) of ibuprofen 800 mg driemaal daags gebruikten 1,9 %. De lagere incidentie van voorvallen met CELEBREX bleef behouden met of zonder aspirinegebruik [zie: KLINISCHE FARMACOLOGIE ].
Opnames/ernstige bijwerkingen: De cumulatieve percentages van Kaplan-Meier na 9 maanden voor stopzettingen als gevolg van bijwerkingen voor CELEBREX 100 mg, diclofenac en ibuprofen waren respectievelijk 24%, 29% en 26%. De percentages voor ernstige ongewenste voorvallen (dwz die ziekenhuisopname veroorzaken of die als levensbedreigend of anderszins medisch significant worden beschouwd), ongeacht de causaliteit, waren niet verschillend tussen de behandelingsgroepen (respectievelijk 8%, 7% en 8%).
Onderzoek naar juveniele reumatoïde artritis
In een 12 weken durende, dubbelblinde, actief-gecontroleerde studie werden 242 JRA-patiënten van 2 jaar tot 17 jaar oud behandeld met celecoxib of naproxen; 77 JRA-patiënten werden behandeld met celecoxib 3 mg/kg tweemaal daags, 82 patiënten werden behandeld met celecoxib 6 mg/kg tweemaal daags en 83 patiënten werden behandeld met naproxen 7,5 mg/kg tweemaal daags. De meest voorkomende (≥5%) bijwerkingen bij met celecoxib behandelde patiënten waren hoofdpijn, koorts (pyrexie), pijn in de bovenbuik, hoesten, nasofaryngitis, buikpijn, misselijkheid, artralgie, diarree en braken. De meest voorkomende (≥ 5%) bijwerkingen bij met naproxen behandelde patiënten waren hoofdpijn, misselijkheid, braken, koorts, pijn in de bovenbuik, diarree, hoesten, buikpijn en duizeligheid (tabel 2). Vergeleken met naproxen had celecoxib in doses van 3 en 6 mg/kg tweemaal daags geen waarneembaar schadelijk effect op groei en ontwikkeling tijdens de 12 weken durende dubbelblinde studie. Er was geen substantieel verschil in het aantal klinische exacerbaties van uveïtis of systemische kenmerken van JRA tussen de behandelingsgroepen.
In een 12 weken durende open-label verlenging van het hierboven beschreven dubbelblinde onderzoek werden 202 JRA-patiënten behandeld met celecoxib 6 mg/kg tweemaal daags. De incidentie van bijwerkingen was vergelijkbaar met die waargenomen tijdens de dubbelblinde studie; er kwamen geen onverwachte bijwerkingen van klinisch belang naar voren.
Andere onderzoeken voorafgaand aan goedkeuring
Bijwerkingen van onderzoeken naar spondylitis ankylopoetica
In totaal werden 378 patiënten behandeld met CELEBREX 200 mg in placebo- en actief-gecontroleerde AS-onderzoeken. Doses tot 400 mg eenmaal daags werden onderzocht. De soorten bijwerkingen die in de AS-onderzoeken werden gemeld, waren vergelijkbaar met de bijwerkingen die in de OA/RA-onderzoeken werden gemeld.
Bijwerkingen van onderzoeken naar analgesie en dysmenorroe
Ongeveer 1.700 patiënten werden behandeld met CELEBREX 200 mg in analgesie- en dysmenorroe-onderzoeken. Alle patiënten in pijnonderzoeken na orale chirurgie kregen een enkele dosis onderzoeksmedicatie. Doses tot 600 mg/dag CELEBREX 200 mg werden onderzocht in pijnstudies bij primaire dysmenorroe en post-orthopedische chirurgie. De soorten bijwerkingen in de analgesie- en dysmenorroe-onderzoeken waren vergelijkbaar met die gerapporteerd in artritis-onderzoeken. De enige bijkomende gemelde bijwerking was post-dentale extractie alveolaire osteïtis (droge socket) in de pijnstudies na orale chirurgie.
De APC- en PreSAP-proeven
Bijwerkingen van langdurige, placebo-gecontroleerde polieppreventiestudies
Blootstelling aan CELEBREX in de APC- en PreSAP-onderzoeken was 400 mg tot 800 mg per dag gedurende maximaal 3 jaar [zie Klinische studies ].
Sommige bijwerkingen traden op bij hogere percentages patiënten dan in de premarketingonderzoeken bij artritis (duur van de behandeling tot 12 weken; zie Bijwerkingen uit CELEBREX 200 mg premarketing gecontroleerde artritisonderzoeken hierboven). De bijwerkingen waarvoor deze verschillen bij patiënten die met CELEBREX werden behandeld groter waren in vergelijking met de premarketingonderzoeken bij artritis, waren als volgt:
De volgende aanvullende bijwerkingen traden op bij ≥ 0,1% en
Zenuwstelselaandoeningen: herseninfarct
Oogaandoeningen: Glasvocht drijvers, conjunctivale bloeding
Oor en labyrint: labyrintitis
Hartaandoeningen: Angina instabiel, incompetentie van de aortaklep, atherosclerose van de kransslagader, sinusbradycardie, ventriculaire hypertrofie
Bloedvataandoeningen: Diepe veneuze trombose
Voortplantingsstelsel- en borstaandoeningen: ovariumcyste
onderzoeken: Bloedkalium verhoogd, bloednatrium verhoogd, bloedtestosteron verlaagd
Letsel, vergiftiging en procedurele complicaties: Epicondylitis, peesruptuur
Postmarketingervaring
De volgende bijwerkingen zijn vastgesteld tijdens het gebruik van CELEBREX na goedkeuring. Omdat deze reacties vrijwillig worden gemeld door een populatie van onbekende grootte, is het niet altijd mogelijk om een betrouwbare schatting te maken van hun frequentie of een oorzakelijk verband te leggen met blootstelling aan geneesmiddelen.
Cardiovasculair: Vasculitis, diepe veneuze trombose
Algemeen: Anafylactoïde reactie, angio-oedeem
Lever en gal: Levernecrose, hepatitis, geelzucht, leverfalen
Hemic en lymfatisch: Agranulocytose, aplastische anemie, pancytopenie, leukopenie
Metabolisch: Hypoglykemie, hyponatriëmie
Zenuwachtig: Aseptische meningitis, ageusie, anosmie, fatale intracraniële bloeding
nier: Interstitiële nefritis
DRUG-INTERACTIES
Zie Tabel 3 voor klinisch significante geneesmiddelinteracties met celecoxib.
WAARSCHUWINGEN
Inbegrepen als onderdeel van de PREVENTIEVE MAATREGELEN sectie.
PREVENTIEVE MAATREGELEN
Cardiovasculaire trombotische gebeurtenissen
Klinische onderzoeken met verschillende cyclo-oxygenase-2 (COX-2) selectieve en niet-selectieve NSAID's met een duur tot drie jaar hebben een verhoogd risico aangetoond op ernstige cardiovasculaire (CV) trombotische voorvallen, waaronder myocardinfarct (MI) en beroerte, die fataal kunnen zijn. Op basis van beschikbare gegevens is het onduidelijk dat het risico op CV trombotische voorvallen gelijk is voor alle NSAID's. De relatieve toename van ernstige CV trombotische voorvallen ten opzichte van baseline, veroorzaakt door het gebruik van NSAID's, lijkt vergelijkbaar te zijn bij degenen met en zonder bekende CV ziekte of risicofactoren voor CV ziekte. Patiënten met bekende CV ziekte of risicofactoren hadden echter een hogere absolute incidentie van overmatige ernstige CV trombotische voorvallen, vanwege hun verhoogde baseline percentage. Sommige observationele studies vonden dat dit verhoogde risico op ernstige CV trombotische voorvallen al in de eerste weken van de behandeling begon. De toename van het cardiovasculaire trombotische risico is het meest consistent waargenomen bij hogere doses.
In het APC-onderzoek (adenoompreventie met celecoxib) was er ongeveer een drievoudig verhoogd risico op het samengestelde eindpunt van cardiovasculair overlijden, MI of beroerte voor de behandelarmen met CELEBREX 400 mg tweemaal daags en CELEBREX 200 mg tweemaal daags in vergelijking met placebo. De verhogingen in beide celecoxib-dosisgroepen versus met placebo behandelde patiënten waren voornamelijk te wijten aan een verhoogde incidentie van een myocardinfarct [zie Klinische studies ].
Een gerandomiseerde gecontroleerde studie, getiteld de Prospective Randomized Evaluation of Celecoxib Integrated Safety vs. Ibuprofen of Naproxen (PRECISION) werd uitgevoerd om het relatieve cardiovasculaire trombotische risico van een COX-2-remmer, celecoxib, te beoordelen in vergelijking met de niet-selectieve NSAID's naproxen en ibuprofen. Celecoxib 100 mg tweemaal daags was niet-inferieur aan naproxen375 tot 500 mg tweemaal daags en ibuprofen 600 tot 800 mg driemaal daags voor het samengestelde eindpunt van de Antiplatelet Trialists' Samenwerking (APTC), die bestaat uit cardiovasculaire sterfte (inclusief hemorragische sterfte), niet-fataal myocardinfarct en niet-fatale beroerte [zie Klinische studies ].
Gebruik de laagst effectieve dosis voor de kortst mogelijke duur om het potentiële risico op een ongunstige CV-gebeurtenis bij met NSAID behandelde patiënten te minimaliseren. Artsen en patiënten moeten alert blijven op de ontwikkeling van dergelijke gebeurtenissen, gedurende de gehele behandelingskuur, zelfs als er geen eerdere CV-symptomen zijn. Patiënten moeten worden geïnformeerd over de symptomen van ernstige CV-gebeurtenissen en de te nemen stappen als deze zich voordoen.
Er is geen consistent bewijs dat gelijktijdig gebruik van aspirine het verhoogde risico op ernstige CV trombotische voorvallen geassocieerd met NSAID-gebruik vermindert. Het gelijktijdig gebruik van aspirine en een NSAID, zoals celecoxib, verhoogt het risico op ernstige gastro-intestinale (GI) gebeurtenissen [zie WAARSCHUWINGEN EN VOORZORGSMAATREGELEN ].
Status Post coronaire bypassoperatie (CABG)
Twee grote, gecontroleerde klinische onderzoeken met een COX-2-selectieve NSAID voor de behandeling van pijn in de eerste 10 tot 14 dagen na CABG-chirurgie vonden een verhoogde incidentie van myocardinfarct en beroerte. NSAID's zijn gecontra-indiceerd bij CABG [zie CONTRA-INDICATIES ].
Post-MI-patiënten
Observationele studies uitgevoerd in het Deense Nationale Register hebben aangetoond dat patiënten die in de post-MI-periode met NSAID's werden behandeld een verhoogd risico hadden op een her-infarct, CV-gerelateerd overlijden en mortaliteit door alle oorzaken vanaf de eerste week van de behandeling. In hetzelfde cohort was de incidentie van overlijden in het eerste jaar na MI 20 per 100 persoonsjaren bij NSAID-behandelde patiënten vergeleken met 12 per 100 persoonsjaren bij niet-NSAID-blootgestelde patiënten. Hoewel het absolute sterftecijfer enigszins daalde na het eerste jaar na MI, bleef het verhoogde relatieve risico op overlijden bij NSAID-gebruikers gedurende ten minste de volgende vier jaar van follow-up bestaan.
Vermijd het gebruik van CELEBREX 100 mg bij patiënten met een recent MI, tenzij verwacht wordt dat de voordelen opwegen tegen het risico op terugkerende CV trombotische voorvallen. Als CELEBREX wordt gebruikt bij patiënten met een recent MI, controleer de patiënten dan op tekenen van cardiale ischemie.
Gastro-intestinale bloedingen, ulceraties en perforaties
NSAID's, waaronder celecoxib, veroorzaken ernstige gastro-intestinale (GI) bijwerkingen, waaronder ontsteking, bloeding, ulceratie en perforatie van de slokdarm, maag, dunne darm of dikke darm, die fataal kan zijn. Deze ernstige bijwerkingen kunnen op elk moment optreden, met of zonder waarschuwingssymptomen, bij patiënten die met CELEBREX worden behandeld. Slechts één op de vijf patiënten die een ernstige bijwerking van het bovenste deel van het maagdarmkanaal ontwikkelen bij behandeling met NSAID's, is symptomatisch. Zweren van het bovenste deel van het maagdarmkanaal, grove bloeding of perforatie veroorzaakt door NSAID's kwamen voor bij ongeveer 1% van de patiënten die gedurende 3 tot 6 maanden werden behandeld en bij ongeveer 2% tot 4% van de patiënten die gedurende een jaar werden behandeld. Zelfs kortdurende NSAID-therapie is echter niet zonder risico.
Risicofactoren voor GI-bloeding, ulceratie en perforatie
Patiënten met een voorgeschiedenis van ulcus pepticum en/of gastro-intestinale bloeding die NSAID's gebruikten, hadden een meer dan 10-voudig verhoogd risico op het ontwikkelen van een gastro-intestinale bloeding in vergelijking met patiënten zonder deze risicofactoren. Andere factoren die het risico op gastro-intestinale bloedingen verhogen bij patiënten die met NSAID's worden behandeld, zijn onder meer een langere behandeling met NSAID's; gelijktijdig gebruik van orale corticosteroïden, plaatjesaggregatieremmers (zoals aspirine), anticoagulantia; of selectieve serotonineheropnameremmers (SSRI's); roken; gebruik van alcohol; oudere leeftijd; en een slechte algemene gezondheidstoestand. De meeste postmarketingmeldingen van fatale GI-voorvallen kwamen voor bij oudere of verzwakte patiënten. Bovendien lopen patiënten met gevorderde leverziekte en/of coagulopathie een verhoogd risico op gastro-intestinale bloedingen.
Het aantal gecompliceerde en symptomatische ulcera was 0,78% na negen maanden voor alle patiënten in de CLASS-studie en 2,19% voor de subgroep met een lage dosis ASA. Patiënten van 65 jaar en ouder hadden een incidentie van 1,40% na negen maanden, 3,06% wanneer ze ook ASA gebruikten [zie: Klinische studies ].
Strategieën om de GI-risico's bij met NSAID's behandelde patiënten te minimaliseren
- Gebruik de laagste effectieve dosering voor de kortst mogelijke duur.
- Vermijd toediening van meer dan één NSAID tegelijk.
- Vermijd het gebruik bij patiënten met een hoger risico, tenzij verwacht wordt dat de voordelen opwegen tegen het verhoogde risico op bloedingen. Overweeg voor dergelijke patiënten, evenals voor patiënten met actieve gastro-intestinale bloedingen, andere alternatieve therapieën dan NSAID's.
- Blijf alert op tekenen en symptomen van gastro-intestinale ulceratie en bloeding tijdens NSAID-therapie.
- Als een ernstige GI-bijwerking wordt vermoed, start dan onmiddellijk met evaluatie en behandeling en stop met CELEBREX 200 mg totdat een ernstige GI-bijwerking is uitgesloten.
- In de setting van gelijktijdig gebruik van een lage dosis aspirine voor hartprofylaxe, moet u patiënten nauwlettender controleren op tekenen van gastro-intestinale bloeding [zie DRUG-INTERACTIES ].
Hepatotoxiciteit
Verhogingen van ALAT of ASAT (drie of meer keer de bovengrens van normaal [ULN]) zijn gemeld bij ongeveer 1% van de met NSAID behandelde patiënten in klinische onderzoeken. Daarnaast zijn zeldzame, soms fatale gevallen van ernstig leverletsel gemeld, waaronder fulminante hepatitis, levernecrose en leverfalen.
Verhogingen van ALAT of ASAT (minder dan driemaal de ULN) kunnen voorkomen bij maximaal 15% van de patiënten die worden behandeld met NSAID's, waaronder celecoxib.
In gecontroleerde klinische onderzoeken met CELEBREX 200 mg was de incidentie van borderline-verhogingen (groter dan of gelijk aan 1,2 keer en minder dan 3 keer de bovengrens van normaal) van lever-geassocieerde enzymen 6% voor CELEBREX en 5% voor placebo, en ongeveer 0,2 % van de patiënten die CELEBREX gebruikten en 0,3% van de patiënten die placebo gebruikten, had opmerkelijke verhogingen van ALAT en ASAT.
Informeer patiënten over de waarschuwingssignalen en symptomen van hepatotoxiciteit (bijv. misselijkheid, vermoeidheid, lethargie, diarree, jeuk, geelzucht, gevoeligheid van het rechter bovenste kwadrant en "griepachtige" symptomen). Als zich klinische tekenen en symptomen ontwikkelen die overeenkomen met een leverziekte, of als systemische verschijnselen optreden (bijv. eosinofilie, huiduitslag), stop dan onmiddellijk met CELEBREX en voer een klinische evaluatie van de patiënt uit.
Hypertensie
NSAID's, waaronder CELEBREX 200 mg, kunnen leiden tot het ontstaan van hypertensie of verergering van reeds bestaande hypertensie, die beide kunnen bijdragen aan de verhoogde incidentie van CV-voorvallen. Patiënten die angiotensine converting enzyme (ACE)-remmers, thiazidediuretica of lisdiuretica gebruiken, kunnen een verminderde respons op deze therapieën hebben wanneer ze NSAID's gebruiken (zie DRUG-INTERACTIES ].
Zien Klinische studies voor aanvullende bloeddrukgegevens voor CELEBREX.
Controleer de bloeddruk (BP) tijdens de start van de NSAID-behandeling en tijdens de behandeling.
Hartfalen en oedeem
De Coxib en traditionele NSAID-onderzoekers' Samenwerkingsmeta-analyse van gerandomiseerde gecontroleerde onderzoeken toonde een ongeveer tweevoudige toename van ziekenhuisopnames voor hartfalen aan bij met COX-2 selectief behandelde patiënten en niet-selectieve NSAID-behandelde patiënten in vergelijking met met placebo behandelde patiënten. In een Deense National Registry-studie van patiënten met hartfalen verhoogde het gebruik van NSAID's het risico op MI, ziekenhuisopname voor hartfalen en overlijden.
Bovendien zijn vochtretentie en oedeem waargenomen bij sommige patiënten die met NSAID's werden behandeld. Het gebruik van celecoxib kan de CV-effecten afzwakken van verschillende therapeutische middelen die worden gebruikt om deze medische aandoeningen te behandelen (bijv. diuretica, ACE-remmers of angiotensinereceptorblokkers [ARB's]) [zie DRUG-INTERACTIES ].
In de CLASS-studie [zie Klinische studies ], de cumulatieve Kaplan-Meier-percentages bij 9 maanden van perifeer oedeem bij patiënten die CELEBREX 400 mg tweemaal daags kregen (respectievelijk 4 maal en 2 maal de aanbevolen OA- en RA-doses), ibuprofen800 mg driemaal daags en diclofenac 75 mg tweemaal daags waren respectievelijk 4,5%, 6,9% en 4,7%.
Vermijd het gebruik van CELEBREX 200 mg bij patiënten met ernstig hartfalen, tenzij verwacht wordt dat de voordelen opwegen tegen het risico op verergering van hartfalen. Als CELEBREX 100 mg wordt gebruikt bij patiënten met ernstig hartfalen, controleer de patiënten dan op tekenen van verergering van hartfalen.
Niertoxiciteit en hyperkaliëmie
Niertoxiciteit
Langdurige toediening van NSAID's heeft geresulteerd in renale papillaire necrose en ander nierletsel.
Niertoxiciteit is ook waargenomen bij patiënten bij wie renale prostaglandines een compenserende rol spelen bij het in stand houden van de nierperfusie. Bij deze patiënten kan toediening van een NSAID een dosisafhankelijke vermindering van prostaglandinformatie veroorzaken en, in tweede instantie, van de renale bloedstroom, wat een duidelijke nierdecompensatie kan veroorzaken. Patiënten met het grootste risico op deze reactie zijn patiënten met een verminderde nierfunctie, uitdroging, hypovolemie, hartfalen, leverdisfunctie, patiënten die diuretica, ACE-remmers of de ARB's gebruiken, en ouderen. Stopzetting van de NSAID-therapie wordt meestal gevolgd door herstel naar de toestand van voor de behandeling.
Er is geen informatie beschikbaar uit gecontroleerde klinische onderzoeken over het gebruik van CELEBREX 100 mg bij patiënten met gevorderde nierziekte. De renale effecten van CELEBREX kunnen de progressie van nierdisfunctie versnellen bij patiënten met een reeds bestaande nierziekte.
Corrigeer de volumestatus bij gedehydrateerde of hypovolemische patiënten voordat CELEBREX wordt gestart. Controleer de nierfunctie bij patiënten met nier- of leverinsufficiëntie, hartfalen, uitdroging of hypovolemie tijdens het gebruik van CELEBREX (zie DRUG-INTERACTIES ]. Vermijd het gebruik van CELEBREX 200 mg bij patiënten met gevorderde nierziekte, tenzij verwacht wordt dat de voordelen opwegen tegen het risico op verslechtering van de nierfunctie. Als CELEBREX 200 mg wordt gebruikt bij patiënten met gevorderde nierziekte, controleer de patiënten dan op tekenen van verslechtering van de nierfunctie.
Hyperkaliëmie
Verhogingen van de serumkaliumconcentratie, waaronder hyperkaliëmie, zijn gemeld bij gebruik van NSAID's, zelfs bij sommige patiënten zonder nierfunctiestoornis. Bij patiënten met een normale nierfunctie zijn deze effecten toegeschreven aan de toestand van ahyporeninemisch-hypoaldosteronisme.
Anafylactische reacties
Celecoxib is in verband gebracht met anafylactische reacties bij patiënten met en zonder bekende overgevoeligheid voor celecoxib en bij patiënten met aspirinegevoelig astma. Celebrex 200 mg is een sulfonamide en zowel NSAID's als sulfonamiden kunnen allergische reacties veroorzaken, waaronder anafylactische symptomen en levensbedreigende of minder ernstige astmatische episodes bij bepaalde gevoelige mensen [zie CONTRA-INDICATIES en WAARSCHUWINGEN EN VOORZORGSMAATREGELEN ].
Zoek noodhulp als er een anafylactische reactie optreedt.
Exacerbatie van astma gerelateerd aan aspirinegevoeligheid
Een subpopulatie van patiënten met astma kan aspirinegevoelig astma hebben, waaronder chronische rhinosinusitis gecompliceerd door neuspoliepen; ernstige, mogelijk fatale bronchospasmen; en/of intolerantie voor aspirine en andere NSAID's. Omdat kruisreactiviteit tussen aspirine en andere NSAID's is gemeld bij dergelijke aspirinegevoelige patiënten, is CELEBREX gecontra-indiceerd bij patiënten met deze vorm van aspirinegevoeligheid [zie CONTRA-INDICATIES ]. Wanneer CELEBREX wordt gebruikt bij patiënten met reeds bestaand astma (zonder bekende gevoeligheid voor aspirine), moet u de patiënten controleren op veranderingen in de tekenen en symptomen van astma.
Ernstige huidreacties
Ernstige huidreacties zijn opgetreden na behandeling met Celebrex 200 mg, waaronder erythema multiforme, exfoliatieve dermatitis, Stevens-Johnson-syndroom (SJS), toxische epidermale necrolyse (TEN), geneesmiddelreactie met eosinofilie en systemische symptomen (DRESS) en acute gegeneraliseerde exanthemateuze pustulose ( AGEP). Deze ernstige voorvallen kunnen zonder waarschuwing optreden en kunnen fataal zijn.
Informeer patiënten over de tekenen en symptomen van ernstige huidreacties en stop met het gebruik van CELEBREX 100 mg bij het eerste optreden van huiduitslag of enig ander teken van overgevoeligheid. CELEBREX 200 mg is gecontra-indiceerd bij patiënten met eerdere ernstige huidreacties op NSAID's [zie: CONTRA-INDICATIES ].
Geneesmiddelreactie met eosinofilie en systemische symptomen (JURK)
Geneesmiddelreactie met eosinofilie en systemische symptomen (DRESS) is gemeld bij patiënten die NSAID's zoals CELEBREX gebruiken. Sommige van deze voorvallen waren fataal of levensbedreigend. DRESS presenteert zich meestal, maar niet uitsluitend, met koorts, huiduitslag, lymfadenopathie en/of zwelling van het gezicht. Andere klinische manifestaties kunnen zijn: hepatitis, nefritis, hematologische afwijkingen, myocarditis of myositis. Soms kunnen de symptomen van DRESS lijken op een acute virale infectie. Eosinofilie is vaak aanwezig. Omdat deze aandoening variabel is in zijn presentatie, kunnen andere orgaansystemen die hier niet zijn vermeld, bij betrokken zijn. Het is belangrijk op te merken dat vroege manifestaties van overgevoeligheid, zoals koorts of lymfadenopathie, aanwezig kunnen zijn, ook al is huiduitslag niet duidelijk. Als dergelijke tekenen of symptomen aanwezig zijn, stop dan met CELEBREX 200 mg en evalueer de patiënt onmiddellijk.
Foetale toxiciteit
Voortijdige sluiting van foetale ductus arteriosus
Vermijd het gebruik van NSAID's, inclusief CELEBREX 100 mg, bij zwangere vrouwen met een zwangerschapsduur van ongeveer 30 weken en later. NSAID's, waaronder CELEBREX, verhogen het risico op voortijdige sluiting van de foetale ductus arteriosus rond deze zwangerschapsduur.
Oligohydramnion/neonatale nierinsufficiëntie
Het gebruik van NSAID's, waaronder CELEBREX, bij een zwangerschapsduur van ongeveer 20 weken of later in de zwangerschap kan foetale nierdisfunctie veroorzaken, wat kan leiden tot oligohydramnion en, in sommige gevallen, neonatale nierfunctiestoornis. Deze nadelige resultaten worden gemiddeld gezien na dagen tot weken behandeling, hoewel oligohydramnion zelden al 48 uur na het starten van NSAID's is gemeld. Oligohydramnion is vaak, maar niet altijd, reversibel bij stopzetting van de behandeling. Complicaties van langdurige oligohydramnion kunnen bijvoorbeeld contracturen van ledematen en vertraagde longrijping omvatten. In sommige postmarketinggevallen van verminderde neonatale nierfunctie waren invasieve procedures zoals wisseltransfusie of dialyse vereist.
Als behandeling met NSAID's nodig is tussen ongeveer 20 weken en 30 weken zwangerschap, beperk dan het gebruik van CELEBREX tot de laagst mogelijke effectieve dosis en de kortst mogelijke duur. Overweeg echografie van het vruchtwater als de behandeling met CELEBREX langer duurt dan 48 uur. Beëindig CELEBREX als oligohydramnion optreedt en volg de klinische praktijk op [zie Gebruik bij specifieke populaties ].
Hematologische toxiciteit
Bloedarmoede is opgetreden bij met NSAID behandelde patiënten. Dit kan te wijten zijn aan occult of grof bloedverlies, vochtretentie of een onvolledig beschreven effect op erytropoëse. Als een met CELEBREX behandelde patiënt tekenen of symptomen van bloedarmoede heeft, controleer hemoglobine of hematocriet.
In gecontroleerde klinische onderzoeken was de incidentie van anemie 0,6% bij CELEBREX en 0,4% bij placebo. Patiënten die langdurig met CELEBREX 200 mg worden behandeld, moeten hun hemoglobine of hematocriet laten controleren als ze tekenen of symptomen van bloedarmoede of bloedverlies vertonen.
NSAID's, waaronder CELEBREX 100 mg, kunnen het risico op bloedingen verhogen. Comorbide aandoeningen zoals stollingsstoornissen of gelijktijdig gebruik van warfarine, andere anticoagulantia, antibloedplaatjesgeneesmiddelen (bijv. aspirine), SSRI's en serotonine-noradrenalineheropnameremmers (SNRI's) kunnen dit risico verhogen. Controleer deze patiënten op tekenen van bloeding [zie DRUG-INTERACTIES ].
Maskeren van ontsteking en koorts
De farmacologische activiteit van CELEBREX 100 mg bij het verminderen van ontstekingen en mogelijk koorts kan het nut van diagnostische symptomen bij het opsporen van infecties verminderen.
Laboratoriumbewaking
Omdat ernstige gastro-intestinale bloedingen, hepatotoxiciteit en nierbeschadiging kunnen optreden zonder waarschuwingssymptomen of tekenen, kunt u overwegen patiënten die een langdurige NSAID-behandeling ondergaan, periodiek te controleren met een CBC en een chemieprofiel [zie WAARSCHUWINGEN EN VOORZORGSMAATREGELEN ].
In gecontroleerde klinische onderzoeken kwam verhoogde BUN vaker voor bij patiënten die CELEBREX kregen in vergelijking met placebo bij de zoon van de patiënt. Deze laboratoriumafwijking werd ook gezien bij patiënten die in deze onderzoeken vergelijkende NSAID's kregen. De klinische betekenis van deze afwijking is niet vastgesteld.
Gedissemineerde intravasculaire stolling (DIC)
Vanwege het risico op gedissemineerde intravasculaire stolling bij gebruik van CELEBREX 200 mg bij pediatrische patiënten met systemische JRA, moet u patiënten controleren op tekenen en symptomen van abnormale stolling of bloeding, en patiënten en hun zorgverleners informeren om symptomen zo snel mogelijk te melden.
Informatie over patiëntbegeleiding
Adviseer de patiënt om de door de FDA goedgekeurde patiëntetikettering te lezen ( Medicatiegids ) bij elk verstrekt recept. Informeer patiënten, families of hun verzorgers over de volgende informatie voordat de behandeling met CELEBREX wordt gestart en periodiek tijdens de lopende therapie.
Cardiovasculaire trombotische gebeurtenissen
Adviseer patiënten alert te zijn op de symptomen van cardiovasculaire trombotische voorvallen, waaronder pijn op de borst, kortademigheid, zwakte of onduidelijke spraak, en om elk van deze symptomen onmiddellijk aan hun zorgverlener te melden [zie WAARSCHUWINGEN EN VOORZORGSMAATREGELEN ].
Gastro-intestinale bloedingen, ulceraties en perforaties
Adviseer patiënten om symptomen van ulceraties en bloedingen, waaronder epigastrische pijn, dyspepsie, melena en hematemesis, aan hun zorgverlener te melden. In de setting van gelijktijdig gebruik van een lage dosis aspirine voor hartprofylaxe, informeer patiënten over het verhoogde risico op en de tekenen en symptomen van gastro-intestinale bloeding [zie WAARSCHUWINGEN EN VOORZORGSMAATREGELEN ].
Hepatotoxiciteit
Informeer patiënten over de waarschuwingssignalen en symptomen van hepatotoxiciteit (bijv. misselijkheid, vermoeidheid, lethargie, jeuk, diarree, geelzucht, gevoeligheid van het rechter bovenste kwadrant en "griepachtige" symptomen). Als deze zich voordoen, instrueer patiënten dan om te stoppen met CELEBREX 200 mg en onmiddellijk medische therapie te zoeken [zie: WAARSCHUWINGEN EN VOORZORGSMAATREGELEN , Gebruik bij specifieke populaties ].
Hartfalen en oedeem
Adviseer patiënten alert te zijn op de symptomen van congestief hartfalen, waaronder kortademigheid, onverklaarbare gewichtstoename of oedeem, en om contact op te nemen met hun zorgverlener als dergelijke symptomen optreden [zie WAARSCHUWINGEN EN VOORZORGSMAATREGELEN ].
Anafylactische reacties
Informeer patiënten over de tekenen van een anafylactische reactie (bijv. ademhalingsmoeilijkheden, zwelling van het gezicht of de keel). Instrueer patiënten om onmiddellijk noodhulp te zoeken als deze zich voordoen [zie CONTRA-INDICATIES en WAARSCHUWINGEN EN VOORZORGSMAATREGELEN ].
Ernstige huidreacties, waaronder JURK
Adviseer patiënten om onmiddellijk te stoppen met het gebruik van CELEBREX 100 mg als ze huiduitslag of koorts krijgen en om zo snel mogelijk contact op te nemen met hun zorgverlener [zie WAARSCHUWINGEN EN VOORZORGSMAATREGELEN ].
Vrouwelijke vruchtbaarheid
Adviseer vrouwen in de vruchtbare leeftijd die zwanger willen worden dat NSAID's, waaronder CELEBREX 200 mg, in verband kunnen worden gebracht met een verteerbare ovulatievertraging [zie Gebruik bij specifieke populaties ].
Foetale toxiciteit
Informeer zwangere vrouwen om het gebruik van CELEBREX en andere NSAID's te vermijden vanaf 30 weken zwangerschap vanwege het risico op voortijdige sluiting van de foetale ductus arteriosus. Als behandeling met CELEBREX 200 mg nodig is voor een zwangere vrouw met een zwangerschapsduur van ongeveer 20 tot 30 weken, vertel haar dan dat ze mogelijk moet worden gecontroleerd op oligohydramnion als de behandeling langer dan 48 uur aanhoudt [zie WAARSCHUWINGEN EN VOORZORGSMAATREGELEN en Gebruik bij specifieke populaties ].
Vermijd gelijktijdig gebruik van NSAID's
Informeer patiënten dat gelijktijdig gebruik van CELEBREX met andere NSAID's of salicylaten (bijv. diflunisal, salsalaat) niet wordt aanbevolen vanwege het verhoogde risico op gastro-intestinale toxiciteit en weinig of geen toename van de werkzaamheid (zie WAARSCHUWINGEN EN VOORZORGSMAATREGELEN en DRUG-INTERACTIES ]. Waarschuw patiënten dat NSAID's aanwezig kunnen zijn in vrij verkrijgbare medicijnen voor de behandeling van verkoudheid, koorts of slapeloosheid.
Gebruik van NSAID's en een lage dosis aspirine
Informeer patiënten om geen lage dosis aspirine gelijktijdig met CELEBREX 200 mg te gebruiken totdat ze met hun zorgverlener hebben gesproken [zie DRUG-INTERACTIES ].
De etikettering van dit product is mogelijk bijgewerkt. Ga voor de meest recente voorschrijfinformatie naar www.pfizer.com.
Niet-klinische toxicologie
Carcinogenese, mutagenese, verminderde vruchtbaarheid
Carcinogenese
Celecoxib was niet carcinogeen bij Sprague-Dawley-ratten die orale doses kregen tot 200 mg/kg voor mannetjes en 10 mg/kg voor vrouwtjes (ongeveer 2 tot 4 keer de menselijke blootstelling zoals gemeten door de AUC0-24 bij 200 mg tweemaal daags ) of bij muizen die gedurende twee jaar orale doses tot 25 mg/kg voor mannetjes en 50 mg/kg voor vrouwtjes kregen (ongeveer gelijk aan menselijke blootstelling zoals gemeten door de AUC0-24 bij 200 mg tweemaal daags).
Mutagenese
Celecoxib was niet mutageen in een Ames-test en een mutatietest in ovariumcellen van de Chinese hamster (CHO), noch clastogeen in een chromosoomafwijkingstest in CHO-cellen en een in vivo micronucleustest in beenmerg van ratten.
Aantasting van de vruchtbaarheid
Celecoxib had geen effect op de mannelijke of vrouwelijke vruchtbaarheid of mannelijke voortplantingsfunctie bij ratten bij orale doses tot 600 mg/kg/dag (ongeveer 11 keer de menselijke blootstelling bij 200 mg tweemaal daags op basis van de AUC0-24). Bij ≥50 mg/kg/dag (ongeveer 6 maal de menselijke blootstelling gebaseerd op de AUC0-24 bij 200 mg tweemaal daags) was er een verhoogd pre-implantatieverlies.
Gebruik bij specifieke populaties
Zwangerschap
Risico Samenvatting
Het gebruik van NSAID's, waaronder CELEBREX 200 mg, kan voortijdige sluiting van de foetale ductus arteriosus en foetale nierdisfunctie veroorzaken, wat kan leiden tot oligohydramnion en, in sommige gevallen, neonatale nierfunctiestoornis. Vanwege deze risico's, beperk de dosis en de duur van CELEBREX 200 mg gebruik tussen ongeveer 20 en 30 weken zwangerschap en vermijd het gebruik van CELEBREX bij ongeveer 30 weken zwangerschap en later in de zwangerschap (zie Klinische overwegingen, gegevens ).
Voortijdige sluiting van foetale ductus arteriosus
Het gebruik van NSAID's, waaronder CELEBREX, bij een zwangerschapsduur van ongeveer 30 weken of later in de zwangerschap verhoogt het risico op voortijdige sluiting van de foetale ductus arteriosus.
Oligohydramnion/neonatale nierinsufficiëntie
Het gebruik van NSAID's bij een zwangerschapsduur van ongeveer 20 weken of later in de zwangerschap is in verband gebracht met gevallen van foetale nierfunctiestoornis die leidt tot oligohydramnion en in sommige gevallen tot neonatale nierfunctiestoornis.
Gegevens uit observationele onderzoeken met betrekking tot andere mogelijke embryofoetale risico's van NSAID-gebruik bij vrouwen in het eerste of tweede trimester van de zwangerschap zijn niet overtuigend. In reproductiestudies bij dieren werden embryo-foetale sterfte en een toename van hernia diafragmatica waargenomen bij ratten die gedurende de periode van organogenese dagelijks celecoxib kregen toegediend in orale doses van ongeveer 6 maal de maximaal aanbevolen dosis voor de mens (MRHD) van 200 mg tweemaal daags. Bovendien werden structurele afwijkingen (bijv. septumdefecten, gefuseerde ribben, gefuseerde sternebrae en misvormde sternebrae) waargenomen bij konijnen die dagelijkse orale doses celecoxib kregen gedurende de periode van organogenese met ongeveer 2 maal de MRHD (zie Gegevens ). Op basis van diergegevens is aangetoond dat prostaglandinen een belangrijke rol spelen bij de vasculaire permeabiliteit van het endometrium, de implantatie van blastocysten en de decidualisatie. In dierstudies resulteerde toediening van prostaglandinesyntheseremmers zoals celecoxib in verhoogd pre- en postimplantatieverlies. Van prostaglandinen is ook aangetoond dat ze een belangrijke rol spelen bij de ontwikkeling van de foetale nieren. In gepubliceerde dierstudies is gemeld dat remmers van de prostaglandinesynthese de nierontwikkeling schaden bij toediening in klinisch relevante doses.
Het geschatte achtergrondrisico van ernstige geboorteafwijkingen en miskraam voor de aangegeven populatie is niet bekend. Alle zwangerschappen hebben een achtergrondrisico op geboorteafwijking, verlies of andere nadelige gevolgen. In de algemene bevolking van de VS is het geschatte achtergrondrisico van ernstige geboorteafwijkingen en miskraam bij klinisch erkende zwangerschappen respectievelijk 2% tot 4% en 15% tot 20%.
Klinische overwegingen
Foetale/neonatale bijwerkingen
Voortijdige sluiting van foetale ductus arteriosus
Vermijd het gebruik van NSAID's bij vrouwen bij een zwangerschapsduur van ongeveer 30 weken en later in de zwangerschap, omdat NSAID's, waaronder CELEBREX 200 mg, voortijdige sluiting van de foetale ductus arteriosus kunnen veroorzaken (zie Gegevens ).
Oligohydramnion/neonatale nierfunctiestoornis:
Als een NSAID nodig is bij een zwangerschapsduur van ongeveer 20 weken of later in de zwangerschap, beperk het gebruik dan tot de laagst mogelijke effectieve dosis en de kortst mogelijke duur. Als de behandeling met CELEBREX langer duurt dan 48 uur, overweeg dan om te controleren met echografie op oligohydramnion. Als oligohydramnion optreedt, stop dan met CELEBREX en volg de klinische praktijk op (zie: Gegevens ).
Arbeid of levering
Er zijn geen onderzoeken naar de effecten van CELEBREX tijdens de bevalling of bevalling. In dierstudies remmen NSAID's, waaronder celecoxib, de prostaglandinesynthese, veroorzaken ze een vertraagde bevalling en verhogen ze de incidentie van doodgeboorte.
Gegevens
Menselijke gegevens
De beschikbare gegevens bewijzen niet de aan- of afwezigheid van ontwikkelingstoxiciteit gerelateerd aan het gebruik van CELEBREX.
Voortijdige sluiting van foetale ductus arteriosus
Gepubliceerde literatuur meldt dat het gebruik van NSAID's bij een zwangerschapsduur van ongeveer 30 weken en later in de zwangerschap voortijdige sluiting van de foetale ductus arteriosus kan veroorzaken.
Oligohydramnion/neonatale nierinsufficiëntie
Gepubliceerde onderzoeken en postmarketingrapporten beschrijven het gebruik van NSAID's door de moeder bij een zwangerschapsduur van ongeveer 20 weken of later in de zwangerschap, geassocieerd met foetale nierdisfunctie, leidend tot oligohydramnion en in sommige gevallen neonatale nierfunctiestoornis. Deze nadelige resultaten worden gemiddeld gezien na dagen tot weken behandeling, hoewel oligohydramnion zelden al 48 uur na het starten van NSAID's is gemeld. In veel gevallen, maar niet in alle, was de afname van het vruchtwater van voorbijgaande aard en reversibel na stopzetting van het medicijn. Er is een beperkt aantal gevallen gemeld van gebruik van NSAID's door de moeder en neonatale nierdisfunctie zonder oligohydramnion, waarvan sommige onomkeerbaar waren. Sommige gevallen van neonatale nierdisfunctie vereisten behandeling met invasieve procedures, zoals wisseltransfusie of dialyse.
Methodologische beperkingen van deze postmarketingonderzoeken en -rapporten omvatten het ontbreken van een controlegroep; beperkte informatie over dosis, duur en timing van blootstelling aan geneesmiddelen; en gelijktijdig gebruik van andere medicijnen. Deze beperkingen maken het niet mogelijk om een betrouwbare schatting te maken van het risico op nadelige foetale en neonatale uitkomsten bij gebruik van NSAID's door de moeder. Omdat de gepubliceerde veiligheidsgegevens over neonatale uitkomsten voornamelijk betrekking hadden op premature baby's, is de generaliseerbaarheid van bepaalde gerapporteerde risico's voor de voldragen baby die door gebruik door de moeder aan NSAID's is blootgesteld, onzeker.
Dierlijke gegevens
Celecoxib bij orale doses ≥150 mg/kg/dag (ongeveer 2 keer de menselijke blootstelling bij 200 mg tweemaal daags zoals gemeten door AUC0-24), veroorzaakte een verhoogde incidentie van ventrikelseptumdefecten, een zeldzame gebeurtenis en foetale veranderingen, zoals ribben gefuseerd, sternebrae gefuseerd en sternebrae misvormd wanneer konijnen gedurende de gehele organogenese werden behandeld. Een dosisafhankelijke toename van indiafragmatische hernia's werd waargenomen wanneer ratten celecoxib kregen in orale doses 30 mg/kg/dag (ongeveer 6 maal de menselijke blootstelling gebaseerd op de AUC 0-24 bij 200 mg tweemaal daags voor RA) gedurende de gehele organogenese. Bij ratten resulteerde blootstelling aan celecoxib tijdens de vroege embryonale ontwikkeling in pre-implantatie- en post-implantatieverliezen bij orale doses ≥ 50 mg/kg/dag (ongeveer 6 maal de menselijke blootstelling gebaseerd op de AUC 0-24 bij 200 mg tweemaal daags voor RA).
Celecoxib leverde geen bewijs van vertraagde bevalling of partus bij orale doses tot 100 mg/kg bij ratten (ongeveer 7 maal de menselijke blootstelling zoals gemeten door de AUC 0-24 bij 200 mg tweemaal daags). De effecten van CELEBREX op de bevalling en bevalling bij zwangere vrouwen zijn niet bekend.
Borstvoeding
Risico Samenvatting
Beperkte gegevens van 3 gepubliceerde rapporten met in totaal 12 vrouwen die borstvoeding gaven, vertoonden lage niveaus van CELEBREX in de moedermelk. De berekende gemiddelde dagelijkse zuigelingendosis was 10 tot 40 mcg/kg/dag, minder dan 1% van de op gewicht gebaseerde therapeutische dosis voor een tweejarig kind. Een melding van twee zuigelingen van 17 en 22 maanden die borstvoeding kregen, liet geen bijwerkingen zien. Voorzichtigheid is geboden wanneer CELEBREX 100 mg wordt toegediend aan een vrouw die borstvoeding geeft. De ontwikkelings- en gezondheidsvoordelen van borstvoeding moeten worden overwogen, samen met de klinische behoefte van de moeder aan CELEBREX en eventuele nadelige effecten op de zuigeling die borstvoeding krijgt van de CELEBREX 200 mg of van de onderliggende maternale aandoening.
Vrouwtjes en mannetjes met reproductief potentieel
Onvruchtbaarheid
vrouwen
Op basis van het werkingsmechanisme kan het gebruik van door prostaglandine gemedieerde NSAID's, waaronder CELEBREX, het scheuren van de eierstokfollikels vertragen of voorkomen, wat bij sommige vrouwen in verband is gebracht met omkeerbare onvruchtbaarheid. Gepubliceerde dierstudies hebben aangetoond dat toediening van prostaglandinesyntheseremmers het potentieel heeft om prostaglandine-gemedieerde folliculaire ruptuur die nodig is voor ovulatie te verstoren. Kleine studies bij vrouwen die werden behandeld met NSAID's hebben ook een omkeerbare vertraging van de eisprong aangetoond. Overweeg het stopzetten van NSAID's, waaronder CELEBREX 200 mg, bij vrouwen die moeite hebben om zwanger te worden of die een onvruchtbaarheidsonderzoek ondergaan.
Pediatrisch gebruik
CELEBREX 200 mg is goedgekeurd voor verlichting van de tekenen en symptomen van juveniele reumatoïde artritis bij patiënten van 2 jaar en ouder. De veiligheid en werkzaamheid zijn bij kinderen na zes maanden niet onderzocht. De cardiovasculaire toxiciteit op lange termijn bij kinderen die zijn blootgesteld aan CELEBREX 100 mg is niet geëvalueerd en het is niet bekend of de langetermijnrisico's vergelijkbaar kunnen zijn met die bij volwassenen die zijn blootgesteld aan CELEBREX of andere COX-2 selectieve en niet-selectieve NSAID's [zie GEVAARLIJKE WAARSCHUWING: , WAARSCHUWINGEN EN VOORZORGSMAATREGELEN , en Klinische studies ].
Het gebruik van celecoxib bij patiënten van 2 tot 17 jaar met pauciarticulaire, polyarticulaire JRA of bij patiënten met systemische aanvang van JRA werd onderzocht in een 12 weken durende, dubbelblinde, actief gecontroleerde farmacokinetische, veiligheids- en werkzaamheidsstudie met een 12 weken open label verlenging. Celecoxib is niet onderzocht bij patiënten jonger dan 2 jaar, bij patiënten met een lichaamsgewicht van minder dan 10 kg (22 lbs) en bij patiënten met actieve systemische kenmerken. Patiënten met systemische JRA (zonder actieve systemische kenmerken) lijken een risico te lopen op de ontwikkeling van abnormale stollingslaboratoriumtests. Bij sommige patiënten met systemische aanvang van JRA werden zowel celecoxib als naproxen geassocieerd met een lichte verlenging van de geactiveerde partiële tromboplastinetijd (APTT), maar niet met de protrombinetijd (PT). Als NSAID's, waaronder celecoxib, worden gebruikt bij patiënten met systemische JRA, moet u patiënten controleren op tekenen en symptomen van abnormale stolling of bloeding, vanwege het risico op gedissemineerde intravasculaire stolling. Patiënten met systemisch begin JRA moeten worden gecontroleerd op de ontwikkeling van abnormale stollingstesten [zie: DOSERING EN ADMINISTRATIE , WAARSCHUWINGEN EN VOORZORGSMAATREGELEN , ONGEWENSTE REACTIES , Dierlijke toxicologie , Klinische studies ].
Alternatieve therapieën voor de behandeling van JRA moeten worden overwogen bij pediatrische patiënten waarvan is vastgesteld dat ze trage CYP2C9-metaboliseerders zijn [zie Slechte metaboliseerders van CYP2C9-substraten ].
Geriatrisch gebruik
Oudere patiënten lopen, vergeleken met jongere patiënten, een groter risico op NSAID-gerelateerde ernstige cardiovasculaire, gastro-intestinale en/of renale bijwerkingen. Als het verwachte voordeel voor de oudere patiënt opweegt tegen deze mogelijke risico's, begin dan met de dosering aan de lage kant van het doseringsbereik en controleer de patiënten op bijwerkingen [zie WAARSCHUWINGEN EN VOORZORGSMAATREGELEN ].
Van het totale aantal patiënten dat CELEBREX 100 mg kreeg in klinische onderzoeken voorafgaand aan de goedkeuring, waren er meer dan 3.300 tussen 65 en 74 jaar oud, terwijl ongeveer 1.300 extra patiënten 75 jaar en ouder waren. Er werden geen substantiële verschillen in effectiviteit waargenomen tussen deze proefpersonen en jongere proefpersonen. In klinische onderzoeken waarin de nierfunctie werd vergeleken zoals gemeten door de GFR, BUN en creatinine, en de bloedplaatjesfunctie zoals gemeten door de bloedingstijd en de bloedplaatjesaggregatie, waren de resultaten niet verschillend tussen oudere en jonge vrijwilligers. Echter, net als bij andere NSAID's, waaronder NSAID's die COX-2 selectief remmen, zijn er meer spontane postmarketingmeldingen geweest van fatale GI-voorvallen en acuut nierfalen bij ouderen dan bij jongere patiënten [zie WAARSCHUWINGEN EN VOORZORGSMAATREGELEN ].
Leverfunctiestoornis
De dagelijks aanbevolen dosis CELEBREX-capsules bij patiënten met een matige leverfunctiestoornis (Child-Pugh-klasse B) moet met 50% worden verlaagd. Het gebruik van CELEBREX bij patiënten met een ernstige leverfunctiestoornis wordt niet aanbevolen [zie: DOSERING EN ADMINISTRATIE en KLINISCHE FARMACOLOGIE ].
Nierfunctiestoornis
CELEBREX wordt niet aanbevolen bij patiënten met ernstige nierinsufficiëntie [zie: WAARSCHUWINGEN EN VOORZORGSMAATREGELEN en KLINISCHE FARMACOLOGIE ].
Slechte metaboliseerders van CYP2C9-substraten
Bij patiënten van wie bekend is of vermoed wordt dat ze slechte CYP2C9-metaboliseerders zijn (dwz CYP2C9*3/*3), dient op basis van genotype of voorgeschiedenis/ervaring met andere CYP2C9-substraten (zoals warfarine, fenytoïne) CELEBREX 200 mg toe te dienen, te beginnen met de helft van de laagste aanbevolen dosis. Alternatieve behandeling moet worden overwogen bij JRA-patiënten waarvan is vastgesteld dat ze slechte CYP2C9-metaboliseerders zijn [zie: DOSERING EN ADMINISTRATIE en KLINISCHE FARMACOLOGIE ].
OVERDOSERING
Symptomen na acute overdosering met NSAID's waren doorgaans beperkt tot lethargie, slaperigheid, misselijkheid, braken en epigastrische pijn, die over het algemeen reversibel waren met ondersteunende zorg. Gastro-intestinale bloedingen zijn opgetreden. Hypertensie, acuut nierfalen, ademhalingsdepressie en coma zijn opgetreden, maar waren zeldzaam [zie: WAARSCHUWINGEN EN VOORZORGSMAATREGELEN ].
Tijdens klinische onderzoeken zijn geen overdoses van CELEBREX 200 mg gemeld. Doses tot 2400 mg/dag gedurende maximaal 10 dagen bij 12 patiënten leidden niet tot ernstige toxiciteit. Er is geen informatie beschikbaar over de verwijdering van celecoxib door hemodialyse, maar op basis van de hoge mate van plasma-eiwitbinding (>97%) is het onwaarschijnlijk dat dialyse nuttig is bij overdosering.
Beheer patiënten met symptomatische en ondersteunende zorg na een overdosering met NSAID's. Er zijn geen specifieke antidota. Overweeg braken en/of actieve kool (60 tot 100 gram bij volwassenen, 1 tot 2 gram per kg lichaamsgewicht bij pediatrische patiënten) en/of osmotische catharsis bij symptomatische patiënten die binnen vier uur na inname worden waargenomen of bij patiënten met een grote overdosering ( 5 tot 10 keer de aanbevolen dosering). Geforceerde diurese, alkalisering van urine, hemodialyse of hemoperfusie zijn mogelijk niet nuttig vanwege de hoge eiwitbinding.
Neem voor meer informatie over een behandeling met overdosering contact op met een antigifcentrum (1-800-222-1222).
CONTRA-INDICATIES
CELEBREX is gecontra-indiceerd bij de volgende patiënten:
- Bekende overgevoeligheid (bijv. anafylactische reacties en ernstige huidreacties) voor celecoxib, een bestanddeel van het geneesmiddel [zie WAARSCHUWINGEN EN VOORZORGSMAATREGELEN ].
- Voorgeschiedenis van astma, urticaria of andere allergische reacties na inname van aspirine of andere NSAID's. Ernstige, soms fatale, anafylactische reacties op NSAID's zijn gemeld bij dergelijke patiënten [zie: WAARSCHUWINGEN EN VOORZORGSMAATREGELEN ].
- In de setting van CABG-chirurgie [zie WAARSCHUWINGEN EN VOORZORGSMAATREGELEN ].
- Bij patiënten die allergische reacties op sulfonamiden hebben aangetoond [zie: WAARSCHUWINGEN EN VOORZORGSMAATREGELEN ].
KLINISCHE FARMACOLOGIE
Werkingsmechanisme
Celecoxib heeft pijnstillende, ontstekingsremmende en koortswerende eigenschappen.
Aangenomen wordt dat het werkingsmechanisme van CELEBREX 100 mg te wijten is aan remming van de prostaglandinesynthese, voornamelijk via remming van COX-2.
Celecoxib is een krachtige remmer van de prostaglandinesynthese in vitro. Celecoxib-concentraties die tijdens de behandeling worden bereikt, hebben in-vivo-effecten veroorzaakt. Prostaglandinen sensibiliseren afferente zenuwen en versterken de werking van bradykinine bij het induceren van pijn in diermodellen. Prostaglandinen zijn mediatoren van ontstekingen. Aangezien celecoxib een remmer is van de prostaglandinesynthese, kan het werkingsmechanisme het gevolg zijn van een afname van prostaglandinen in perifere weefsels.
farmacodynamiek
Bloedplaatjes
In klinische onderzoeken met normale vrijwilligers had CELEBREX in enkelvoudige doses tot 800 mg en meervoudige doses van 600 mg tweemaal daags gedurende maximaal 7 dagen (hoger dan de aanbevolen therapeutische doses) geen effect op de vermindering van de bloedplaatjesaggregatie of de toename van de bloedingstijd. Vanwege het ontbreken van bloedplaatjeseffecten, is CELEBREX 100 mg geen vervanging voor aspirine voor cardiovasculaire profylaxe. Het is niet bekend of er effecten zijn van CELEBREX op bloedplaatjes die kunnen bijdragen aan het verhoogde risico op ernstige cardiovasculaire trombotische bijwerkingen die verband houden met het gebruik van CELEBREX.
Vloeistofretentie
Remming van de PGE2-synthese kan leiden tot natrium- en waterretentie door verhoogde reabsorptie in de niermedullaire dikke oplopende lus van Henle en misschien andere segmenten van het distale nefron. In de verzamelbuizen lijkt PGE2 de heropname van water te remmen door de werking van het antidiuretisch hormoon tegen te gaan.
Farmacokinetiek
Celecoxib vertoont een dosisproportionele toename van de blootstelling na orale toediening tot 200 mg tweemaal daags en een minder dan proportionele toename bij hogere doses. Het heeft een uitgebreide distributie en een hoge eiwitbinding. Het wordt voornamelijk gemetaboliseerd door CYP2C9 met een halfwaardetijd van ongeveer 11 uur.
Absorptie
Piekplasmaspiegels van celecoxib treden ongeveer 3 uur na een orale dosis op. Onder nuchtere omstandigheden zijn zowel de piekplasmaspiegels (Cmax) als de oppervlakte onder de curve (AUC) ruwweg dosisproportioneel tot 200 mg tweemaal daags; bij hogere doses zijn er minder dan proportionele stijgingen in Cmax en AUC (zie: Voedseleffecten ). Er zijn geen onderzoeken naar absolute biologische beschikbaarheid uitgevoerd. Bij meervoudige doseringen worden steady-state-omstandigheden bereikt op of vóór dag 5. De farmacokinetische parameters van celecoxib bij een groep gezonde proefpersonen worden weergegeven in Tabel 4.
Voedseleffecten
Wanneer CELEBREX 200 mg capsules werden ingenomen met een vetrijke maaltijd, werden de piekplasmaspiegels ongeveer 1 tot 2 uur vertraagd met een toename van de totale absorptie (AUC) van 10% tot 20%. Onder nuchtere omstandigheden, bij doses boven 200 mg, is er een minder dan proportionele toename van Cmax en AUC, waarvan wordt gedacht dat dit het gevolg is van de lage oplosbaarheid van het geneesmiddel in waterige media.
Gelijktijdige toediening van CELEBREX met aluminium- en magnesiumbevattende antacida resulteerde in een verlaging van de celecoxib-plasmaconcentraties met een verlaging van 37% in Cmax en 10% in AUC. CELEBREX kan in doses tot 200 mg tweemaal daags worden toegediend zonder rekening te houden met het tijdstip van maaltijden. Hogere doses (400 mg tweemaal daags) moeten met voedsel worden toegediend om de absorptie te verbeteren.
Bij gezonde volwassen vrijwilligers was de totale systemische blootstelling (AUC) aan celecoxib gelijk wanneer celecoxib werd toegediend als intacte capsule of capsule-inhoud die op appelmoes werd gestrooid. Er waren geen significante veranderingen in Cmax, Tmax of t½ na toediening van de capsuleinhoud op appelmoes [zie DOSERING EN ADMINISTRATIE ].
Verdeling
Bij gezonde proefpersonen is celecoxib sterk eiwitgebonden (~97%) binnen het klinische dosisbereik. In vitro-onderzoeken geven aan dat celecoxib zich voornamelijk bindt aan albumine en, in mindere mate, aan α-zure glycoproteïne. Het schijnbare distributievolume bij steady-state (V/F) is ongeveer 400 l, wat wijst op een uitgebreide distributie in de weefsels. Celecoxib is niet preferentieel gebonden aan rode bloedcellen.
Eliminatie
Metabolisme
Het celecoxibmetabolisme wordt voornamelijk gemedieerd via CYP2C9. Drie metabolieten, een primaire alcohol, het overeenkomstige carbonzuur en zijn glucuronideconjugaat, zijn geïdentificeerd in menselijk plasma. Deze metabolieten zijn inactief als COX-1- of COX-2-remmers.
uitscheiding
Celecoxib wordt voornamelijk geëlimineerd door levermetabolisme, waarbij weinig (
Specifieke populaties
geriatrische
Bij steady-state hadden oudere proefpersonen (ouder dan 65 jaar) een 40% hogere Cmax en een 50% hogere AUC in vergelijking met jonge proefpersonen. Bij oudere vrouwen zijn de Cmax en AUC van celecoxib hoger dan die bij oudere mannen, maar deze stijgingen zijn voornamelijk te wijten aan een lager lichaamsgewicht bij oudere vrouwen. Dosisaanpassing bij ouderen is over het algemeen niet nodig. Start echter bij patiënten met een lichaamsgewicht van minder dan 50 kg de therapie met de laagst aanbevolen dosis [zie Gebruik bij specifieke populaties ].
pediatrisch
De steady-state farmacokinetiek van celecoxib toegediend als een orale suspensie voor onderzoek werd geëvalueerd bij 152 JRA-patiënten van 2 jaar tot 17 jaar met een gewicht ≥ 10 kg met pauciarticulaire of polyarticulaire JRA en bij patiënten met systemische aanvang van JRA. Farmacokinetische populatieanalyse gaf aan dat de orale klaring (niet aangepast voor lichaamsgewicht) van celecoxib minder dan evenredig toeneemt met het gewichtstoename, waarbij voorspeld wordt dat patiënten van 10 kg en 25 kg een respectievelijk 40% en 24% lagere klaring hebben in vergelijking met een volwassen RA van 70 kg. geduldig.
Bij tweemaal daagse toediening van capsules van 50 mg aan JRA-patiënten die ≥12 tot ≤25 kg wegen en capsules van 100 mg aan JRA-patiënten die >25 kg wegen, moeten plasmaconcentraties worden bereikt die vergelijkbaar zijn met die waargenomen in een klinische studie die de non-inferioriteit van celecoxib aantoonde naproxen 7,5 mg/kg tweemaal daags [zie DOSERING EN ADMINISTRATIE ]. Celecoxib is niet onderzocht bij JRA-patiënten jonger dan 2 jaar, bij patiënten met een lichaamsgewicht van minder dan 10 kg (22 lbs) of langer dan 24 weken.
Ras
Meta-analyse van farmacokinetische onderzoeken heeft een ongeveer 40% hogere AUC van celecoxib gesuggereerd bij negers in vergelijking met blanken. De oorzaak en klinische betekenis van deze bevinding is onbekend.
Leverfunctiestoornis
Een farmacokinetisch onderzoek bij proefpersonen met een lichte (Child-Pugh-klasse A) en matige (Child-Pugh-klasse B) leverfunctiestoornis heeft aangetoond dat de AUC van celecoxib bij steady-state respectievelijk ongeveer 40% en 180% hoger is dan waargenomen bij gezonde controlepersonen onderwerpen. Daarom moet de dagelijks aanbevolen dosis van CELEBREX-capsules met ongeveer 50% worden verlaagd bij patiënten met een matige (Child-Pugh-klasse B) leverfunctiestoornis. Patiënten met een ernstige leverfunctiestoornis (Child-Pugh-klasse C) zijn niet onderzocht. Het gebruik van CELEBREX bij patiënten met een ernstige leverfunctiestoornis wordt niet aanbevolen [zie DOSERING EN ADMINISTRATIE en Gebruik bij specifieke populaties ].
Nierfunctiestoornis
In een cross-studie vergelijking was de AUC van celecoxib ongeveer 40% lager bij patiënten met chronische nierinsufficiëntie (GFR35-60 ml/min) dan bij proefpersonen met een normale nierfunctie. Er werd geen significant verband gevonden tussen GFR en celecoxibklaring. Patiënten met ernstige nierinsufficiëntie zijn niet onderzocht. Net als andere NSAID's, wordt CELEBREX 200 mg niet aanbevolen bij patiënten met ernstige nierinsufficiëntie [zie WAARSCHUWINGEN EN VOORZORGSMAATREGELEN ].
Geneesmiddelinteractiestudies
In vitro-onderzoeken geven aan dat celecoxib geen remmer is van cytochroom P450 2C9, 2C19 of 3A4.
In vivo-onderzoeken hebben het volgende aangetoond:
Aspirine
Wanneer NSAID's werden toegediend met aspirine, was de eiwitbinding van NSAID's verminderd, hoewel de klaring van vrije NSAID's niet veranderde. De klinische betekenis van deze interactie is niet bekend. Zie Tabel 3 voor klinisch significante geneesmiddelinteracties van NSAID's met aspirine [zie: DRUG-INTERACTIES ].
Lithium
In een onderzoek bij gezonde proefpersonen stegen de gemiddelde steady-state lithiumplasmaspiegels met ongeveer 17% bij proefpersonen die tweemaal daags 450 mg lithium kregen met CELEBREX 200 mg tweemaal daags in vergelijking met proefpersonen die alleen lithium kregen [zie DRUG-INTERACTIES ].
Fluconazol
Gelijktijdige toediening van 200 mg fluconazol eenmaal daags resulteerde in een tweevoudige verhoging van de celecoxib-plasmaconcentratie. Deze toename is te wijten aan de remming van het celecoxibmetabolisme via P450 2C9 door fluconazol [zie DRUG-INTERACTIES ].
Andere medicijnen
De effecten van celecoxib op de farmacokinetiek en/of farmacodynamiek van glyburide, ketoconazol, [zie DRUG-INTERACTIES ], fenytoïne en tolbutamide zijn in vivo onderzocht en er zijn geen klinisch belangrijke interacties gevonden.
farmacogenomica
CYP2C9-activiteit is verminderd bij personen met genetische polymorfismen die leiden tot verminderde enzymactiviteit, zoals die welke homozygoot zijn voor de CYP2C9*2- en CYP2C9*3-polymorfismen. Beperkte gegevens van 4 gepubliceerde rapporten die in totaal 8 proefpersonen met het homozygote CYP2C9*3/*3-genotype omvatten, vertoonden systemische celecoxibspiegels die 3 tot 7 keer hoger waren bij deze proefpersonen vergeleken met proefpersonen met CYP2C9*1/*1 of * I/*3 genotypen. De farmacokinetiek van celecoxib is niet onderzocht bij proefpersonen met andere CYP2C9-polymorfismen, zoals *2, *5, *6, *9 en *11. Geschat wordt dat de frequentie van het homozygote *3/*3 genotype 0,3% tot 1,0% is in verschillende etnische groepen [zie DOSERING EN ADMINISTRATIE , Gebruik bij specifieke populaties ].
Dierlijke toxicologie
Een toename van de incidentie van achtergrondbevindingen van spermatocele met of zonder secundaire veranderingen zoals epididymalhy pospermie en minimale tot lichte verwijding van de tubuli seminiferi werd gezien bij de juveniele rat. Deze reproductieve bevindingen, hoewel schijnbaar behandelingsgerelateerd, namen niet toe in incidentie of ernst met de dosis en kunnen wijzen op een verergering van een spontane aandoening. Vergelijkbare reproductieve bevindingen werden niet waargenomen in onderzoeken met jonge of volwassen honden of bij volwassen ratten die werden behandeld met celecoxib. De klinische betekenis van deze waarneming is niet bekend.
Klinische studies
artrose
CELEBREX 200 mg heeft een significante vermindering van gewrichtspijn aangetoond in vergelijking met placebo. CELEBREX werd geëvalueerd voor de behandeling van de tekenen en symptomen van artrose van de knie en heup in placebo- en actief-gecontroleerde klinische onderzoeken met een duur van maximaal 12 weken. Bij patiënten met artrose resulteerde behandeling met CELEBREX 100 mg tweemaal daags of 200 mg eenmaal daags in een verbetering van de WOMAC (Western Ontario en McMaster Universities) osteoartritisindex, een samenstelling van pijn, stijfheid en functionele metingen bij artrose. In drie 12 weken durende onderzoeken naar pijn die gepaard ging met opflakkering van artrose, gaven CELEBREX 100 mg doses van 100 mg tweemaal daags en 200 mg tweemaal daags een significante vermindering van pijn binnen 24 tot 48 uur na aanvang van de dosering. Bij doses van tweemaal daags 100 mg of tweemaal daags 200 mg bleek de werkzaamheid van CELEBREX 200 mg vergelijkbaar te zijn met die van tweemaal daags 500 mg naproxen. Doses van 200 mg tweemaal daags leverden geen extra voordeel op boven het voordeel dat wordt gezien bij tweemaal daags 100 mg. Er is aangetoond dat een totale dagelijkse dosis van 200 mg even effectief is, ongeacht of deze wordt toegediend als 100 mg tweemaal daags of 200 mg eenmaal daags.
Reumatoïde artritis
CELEBREX heeft een significante vermindering van gevoeligheid/pijn en zwelling van de gewrichten aangetoond in vergelijking met placebo. CELEBREX 100 mg werd geëvalueerd voor de behandeling van de tekenen en symptomen van RA in placebo- en actief-gecontroleerde klinische onderzoeken met een duur van maximaal 24 weken. In deze onderzoeken bleek CELEBREX superieur te zijn aan placebo, met behulp van de ACR20 Responder Index, een samenstelling van klinische, laboratorium- en functionele metingen bij RA. CELEBREX-doses van 100 mg tweemaal daags en 200 mg tweemaal daags waren vergelijkbaar in effectiviteit en beide waren vergelijkbaar met naproxen 500 mg tweemaal daags.
Hoewel CELEBREX 100 mg tweemaal daags en 200 mg tweemaal daags een vergelijkbare algehele effectiviteit gaven, hadden sommige patiënten extra voordeel van de 200 mg tweemaal daagse dosis. Doses van tweemaal daags 400 mg gaven geen extra voordeel boven het voordeel dat wordt gezien bij tweemaal daags 100 mg tot 200 mg.
Juveniele reumatoïde artritis (NCT00652925)
In een 12 weken durende, gerandomiseerde, dubbelblinde actief-gecontroleerde, parallelle groep, multicenter, non-inferiority studie, werden patiënten van 2 jaar tot 17 jaar oud met pauciarticulaire, polyarticulaire JRA of systemische aanvang JRA (met momenteel inactieve systemische kenmerken ), kreeg een van de volgende behandelingen: celecoxib 3 mg/kg (tot een maximum van 150 mg) tweemaal daags; celecoxib 6 mg/kg (tot een maximum van 300 mg) tweemaal daags; of naproxen 7,5 mg/kg (tot een maximum van 500 mg) tweemaal daags. De responspercentages waren gebaseerd op het JRA-definitie van verbetering van meer dan of gelijk aan 30% (JRA DOI 30), dat een samenstelling is van klinische, laboratorium- en functionele metingen van JRA. De JRA DOI 30-responspercentages in week 12 waren respectievelijk 69%, 80% en 67% in de celecoxib 3 mg/kg tweemaal daags, celecoxib 6 mg/kg tweemaal daags en naproxen 7,5 mg/kg tweemaal daags.
De werkzaamheid en veiligheid van CELEBREX 100 mg voor JRA zijn niet langer dan zes maanden onderzocht. De cardiovasculaire toxiciteit op lange termijn bij kinderen die zijn blootgesteld aan CELEBREX 200 mg is niet onderzocht en het is niet bekend of het risico op lange termijn vergelijkbaar kan zijn met dat bij volwassenen die zijn blootgesteld aan CELEBREX 100 mg of andere COX-2 selectieve en niet-selectieve NSAID's [ zien GEVAARLIJKE WAARSCHUWING: , WAARSCHUWINGEN EN VOORZORGSMAATREGELEN ].
Spondylitis ankylopoetica
CELEBREX werd geëvalueerd bij AS-patiënten in twee placebo- en actief-gecontroleerde klinische onderzoeken met een duur van 6 en 12 weken. CELEBREX in doses van 100 mg tweemaal daags, 200 mg eenmaal daags en 400 mg eenmaal daags bleek in deze onderzoeken statistisch superieur te zijn aan placebo voor alle drie de co-primaire werkzaamheidsmaatregelen die de globale pijnintensiteit (visuele analoge schaal), de globale ziekteactiviteit beoordelen (Visual Analogue Scale) en functionele beperkingen (Bath Ankylosing Spondylitis Functional Index). In de 12 weken durende studie was er geen verschil in de mate van verbetering tussen de 200 mg en 400 mg CELEBREX 200 mg doses in een vergelijking van de gemiddelde verandering ten opzichte van baseline, maar er was een groter percentage patiënten dat reageerde op CELEBREX400 mg, 53 %, dan CELEBREX 200 mg, 44%, met behulp van de beoordelingscriteria voor spondylitis ankylopoetica (ASAS20). De ASAS 20 definieert een responder als een verbetering ten opzichte van baseline van ten minste 20% en een absolute verbetering van ten minste 10 mm, op een schaal van 0 mm tot 100 mm, in ten minste drie van de vier volgende domeinen: globale pijn van de patiënt, spondylitis ankylopoetica in bad Functionele Index en ontsteking. De responderanalyse toonde ook geen verandering in de responderpercentages na 6 weken.
Analgesie, inclusief primaire dysmenorroe
In acute analgetische modellen van pijn na orale chirurgie, post-orthopedische chirurgische pijn en primaire dysmenorroe verlichtte CELEBREX 100 mg pijn die door patiënten als matig tot ernstig werd beoordeeld. Enkele doses [zie DOSERING EN ADMINISTRATIE ] CELEBREX 200 mg zorgde voor pijnverlichting binnen 60 minuten.
Cardiovasculaire resultatenstudie: prospectieve gerandomiseerde evaluatie van geïntegreerde veiligheid van celecoxib versus ibuprofen of naproxen (PRECISION; NCT00346216)
Ontwerp
De PRECISION-studie was een dubbelblinde, gerandomiseerde, gecontroleerde studie naar cardiovasculaire veiligheid bij patiënten met artrose en RA met of met een hoog risico op cardiovasculaire aandoeningen, waarbij celecoxib werd vergeleken met naproxen en ibuprofen. Patiënten werden gerandomiseerd naar een startdosering van 100 mg celecoxib tweemaal daags, 600 mg ibuprofen driemaal daags of 375 mg naproxen tweemaal daags, met de mogelijkheid om de dosis indien nodig te verhogen voor pijnbestrijding. Op basis van de gelabelde doses konden OA-patiënten die gerandomiseerd waren naar celecoxib de dosis niet verhogen.
Het primaire eindpunt, de Antiplatelet Trialists' Samenstelling (APTC) was een onafhankelijk beoordeelde samenstelling van cardiovasculaire sterfte (inclusief hemorragische sterfte), niet-fataal myocardinfarct en niet-fatale beroerte met 80% power om non-inferioriteit te evalueren. Alle patiënten kregen open-label esomeprazol (20-40 mg) voorgeschreven voor maagbescherming. De randomisatie van de behandeling werd gestratificeerd naar baseline lage dosis aspirinegebruik.
Daarnaast was er een substudie van 4 maanden waarin de effecten van de drie geneesmiddelen op de bloeddruk werden beoordeeld, zoals gemeten door ambulante monitoring.
Resultaten
Van de proefpersonen met artrose escaleerde slechts 0,2% (17/7259) celecoxib tot de dosis van 200 mg tweemaal daags, terwijl 54,7% (3946/7208) ibuprofen escaleerde tot 800 mg driemaal daags en 54,8% (3937/7178) escaleerde naproxen tot de tweemaal daagse dosis van 500 mg. Van de proefpersonen met RA escaleerde 55,7% (453/813) celecoxib tot de dosis van 200 mg tweemaal daags, 56,5% (470/832) escaleerde ibuprofen tot 800 mg driemaal daags en 54,6% (432/791) escaleerde naproxen tot de 500 mg tweemaal daagse dosis; de RA-populatie maakte echter slechts 10% uit van de proefpopulatie.
Omdat relatief weinig celecoxib-patiënten in totaal (5,8% [470/8072]) de dosis verhoogden tot 200 mg tweemaal daags, zijn de resultaten van de PRECISION-studie niet geschikt om de relatieve CV-veiligheid van celecoxib bij 200 mg tweemaal daags te bepalen in vergelijking met ibuprofen en naproxen in de ingenomen doses.
Primair eindpunt
De studie had twee vooraf gespecificeerde analysepopulaties:
- Intent-to-treat-populatie (ITT): bestaat uit alle gerandomiseerde proefpersonen die gedurende maximaal 30 maanden worden gevolgd
- Gemodificeerde intent-to-treat-populatie (mITT): Bestaat uit alle gerandomiseerde proefpersonen die ten minste één dosis onderzoeksmedicatie hebben gekregen en die ten minste één post-baseline-bezoek hebben gevolgd tot de eerdere stopzetting van de behandeling plus 30 dagen of 43 maanden
Celecoxib voldeed aan alle vier de vooraf gespecificeerde non-inferioriteitscriteria (p
De primaire analyseresultaten voor ITT en mITT worden beschreven in Tabel 5.
In de ITT-analysepopulatie tot en met 30 maanden was de mortaliteit door alle oorzaken 1,6% in de celecoxib-groep, 1,8% in de ibuprofen-groep en 2,0% in de naproxen-groep.
Ambulante bloeddrukmeting (ABPM) Deelonderzoek
In de PRECISION-ABPM-substudie, van de in totaal 444 analyseerbare patiënten in maand 4, verlaagde celecoxib, gedoseerd met 100 mg tweemaal daags, de gemiddelde 24-uurs systolische bloeddruk (SBP) met 0,3 mmHg, terwijl ibuprofen en naproxen bij de ingenomen doses stegen. gemiddelde 24-uurs SBP met respectievelijk 3,7 en 1,6 mmHg. Deze veranderingen resulteerden in een statistisch significant en klinisch relevant verschil van 3,9 mmHg (p=0,0009) tussen celecoxib en ibuprofen en een niet-statistisch significant verschil van 1,8 (p=0,119) mmHg tussen celecoxib en naproxen.
Speciale studies
Adenomateuze polieppreventiestudies (NCT00005094 en NCT0014193)
De cardiovasculaire veiligheid werd geëvalueerd in twee gerandomiseerde, dubbelblinde, placebogecontroleerde, driejarige onderzoeken waarbij patiënten met sporadische adenomateuze poliepen werden behandeld met CELEBREX: het APC-onderzoek (adenoompreventie met celecoxib) en het PreSAP-onderzoek (preventie van spontane adenomateuze poliepen) . In het APC-onderzoek was er een dosisgerelateerde toename van het samengestelde eindpunt (beoordeeld) van cardiovasculair overlijden, myocardinfarct of beroerte met celecoxib vergeleken met placebo gedurende een behandeling van 3 jaar. De PreSAP-studie toonde geen statistisch significant verhoogd risico aan voor hetzelfde samengestelde eindpunt (beoordeeld):
- In het APC-onderzoek waren de hazardratio's vergeleken met placebo voor een samengesteld eindpunt (beoordeeld) van cardiovasculair overlijden, myocardinfarct of beroerte 3,4 (95% BI 1,4 – 8,5) met celecoxib 400 mg tweemaal daags en 2,8 (95% BI 1,4 – 8,5) CI 1.1 - 7.2) met celecoxib 200 mg tweemaal daags. De cumulatieve percentages voor dit samengestelde eindpunt over een periode van 3 jaar waren respectievelijk 3,0% (20/671 proefpersonen) en 2,5% (17/685 proefpersonen), vergeleken met 0,9% (6/679 proefpersonen) met placebobehandeling. De verhogingen in beide celecoxib-dosisgroepen versus met placebo behandelde patiënten waren voornamelijk te wijten aan een verhoogde incidentie van een myocardinfarct.
- In de PreSAP-studie was de hazard ratio voor ditzelfde samengestelde eindpunt (beoordeeld) 1,2 (95% BI 0,6 – 2,4) met celecoxib 400 mg eenmaal daags in vergelijking met placebo. De cumulatieve percentages voor dit samengestelde eindpunt over een periode van 3 jaar waren respectievelijk 2,3% (21/933 proefpersonen) en 1,9% (12/628 proefpersonen).
Klinische onderzoeken met andere COX-2-selectieve en niet-selectieve NSAID's met een duur tot drie jaar hebben een verhoogd risico aangetoond op ernstige cardiovasculaire trombotische voorvallen, myocardinfarct en beroerte, die fataal kunnen zijn. Als gevolg hiervan worden alle NSAID's beschouwd als potentieel geassocieerd met dit risico.
Celecoxib langetermijnartritis veiligheidsonderzoek (KLASSE)
Dit was een prospectief, langetermijnonderzoek naar veiligheidsuitkomsten dat postmarketing werd uitgevoerd bij ongeveer 5.800 OA-patiënten en 2.200 RA-patiënten. Patiënten kregen tweemaal daags 400 mg CELEBREX (respectievelijk 4 keer en 2 keer de aanbevolen OA- en RA-doses), ibuprofen 800 mg driemaal daags of diclofenac 75 mg tweemaal daags (gebruikelijke therapeutische doses). Mediane blootstellingen voor CELEBREX (n = 3.987) en diclofenac (n = 1.996) waren 9 maanden, terwijl ibuprofen (n = 1.985) 6 maanden was. Het primaire eindpunt van deze uitkomststudie was de incidentie van gecompliceerde ulcera (gastro-intestinale bloeding, perforatie of obstructie). Patiënten mochten gelijktijdig een lage dosis (≤ 325 mg/dag) aspirine (ASA) gebruiken voor cardiovasculaire profylaxe (ASA-subgroepen: CELEBREX, n = 882; diclofenac, n = 445; ibuprofen, n = 412). Verschillen in de incidentie van gecompliceerde zweren tussen CELEBREX 200 mg en de gecombineerde groep van ibuprofen en diclofenac waren niet statistisch significant.
Patiënten die CELEBREX kregen en gelijktijdig laaggedoseerde ASA (N=882) kregen een 4-voudig hogere frequentie van gecompliceerde ulcera in vergelijking met patiënten die geen ASA kregen (N=3105). Het Kaplan-Meier-percentage voor gecompliceerde ulcera na 9 maanden was 1,12% versus 0,32% voor respectievelijk degenen die een lage dosis ASA kregen en degenen die geen ASA kregen [zie WAARSCHUWINGEN EN VOORZORGSMAATREGELEN ].
De geschatte cumulatieve percentages na 9 maanden van gecompliceerde en symptomatische ulcera voor patiënten die worden behandeld met CELEBREX 400 mg tweemaal daags worden beschreven in Tabel 7. Tabel 7 geeft ook resultaten weer voor patiënten jonger dan of ouder dan 65 jaar. Het verschil in percentages tussen CELEBREX 200 mg alleen en CELEBREX 100 mg met ASA-groepen kan te wijten zijn aan het hogere risico op GI-gebeurtenissen bij ASA-gebruikers.
Bij een klein aantal patiënten met een voorgeschiedenis van ulcusziekte was het aantal gecompliceerde en symptomatische ulcera bij patiënten die CELEBREX 100 mg alleen of CELEBREX 100 mg met ASA gebruikten respectievelijk 2,56% (n=243) en 6,85% (n=91) bij 48 weken. Deze resultaten zijn te verwachten bij patiënten met een voorgeschiedenis van ulcusziekte [zie: WAARSCHUWINGEN EN VOORZORGSMAATREGELEN en ONGEWENSTE REACTIES ].
Cardiovasculaire veiligheidsresultaten werden ook geëvalueerd in de CLASS-studie. Kaplan-Meier cumulatieve percentages voor door de onderzoeker gerapporteerde ernstige cardiovasculaire trombo-embolische bijwerkingen (waaronder MI, longembolie, diepe veneuze trombose, onstabiele angina, transient ischemische aanvallen en ischemische cerebrovasculaire accidenten) toonden geen verschillen aan tussen de behandeling met CELEBREX 200 mg, diclofenac of ibuprofen groepen. De cumulatieve percentages bij alle patiënten na negen maanden voor CELEBREX, diclofenac en ibuprofen waren respectievelijk 1,2%, 1,4% en 1,1%. De cumulatieve percentages bij niet-ASA-gebruikers na negen maanden in elk van de drie behandelingsgroepen waren minder dan 1%. De cumulatieve percentages voor myocardinfarct bij niet-ASA-gebruikers na negen maanden in elk van de drie behandelingsgroepen waren minder dan 0,2%. Er was geen placebogroep in de CLASS-studie, wat het vermogen om te bepalen of de drie geteste geneesmiddelen geen verhoogd risico op CV events hadden of dat ze allemaal het risico in een vergelijkbare mate verhoogden, beperkt. In het CLASS-onderzoek waren de cumulatieve Kaplan-Meier-percentages bij 9 maanden perifeer oedeem bij patiënten die CELEBREX 400 mg tweemaal daags kregen (respectievelijk 4 keer en 2 keer de aanbevolen OA- en RA-doses), ibuprofen 800 mg driemaal daags en diclofenac 75 mg tweemaal daags waren respectievelijk 4,5%, 6,9% en 4,7%. De percentages van hypertensie uit het CLASS-onderzoek bij de met CELEBREX, ibuprofen en diclofenac behandelde patiënten waren respectievelijk 2,4%, 4,2% en 2,5%.
Endoscopische onderzoeken
De correlatie tussen bevindingen van kortdurende endoscopische onderzoeken met CELEBREX en de relatieve incidentie van klinisch significante ernstige bijwerkingen van het bovenste deel van het maagdarmkanaal bij langdurig gebruik is niet vastgesteld. Ernstige klinisch significante bloeding in het bovenste deel van het maagdarmkanaal is waargenomen bij patiënten die CELEBREX 100 mg kregen in gecontroleerde en open-label onderzoeken [zie WAARSCHUWINGEN EN VOORZORGSMAATREGELEN en Klinische studies ].
Er is een gerandomiseerde, dubbelblinde studie uitgevoerd bij 430 RA-patiënten waarin een endoscopisch onderzoek werd uitgevoerd na 6 maanden. De incidentie van endoscopische ulcera bij patiënten die CELEBREX 200 mg tweemaal daags gebruikten, was 4% versus 15% voor patiënten die diclofenac SR 75 mg tweemaal daags gebruikten. CELEBREX was echter niet statistisch verschillend van diclofenac voor klinisch relevante GI-uitkomsten in het CLASS-onderzoek [zie Klinische studies ].
De incidentie van endoscopische ulcera werd onderzocht in twee 12 weken durende, placebogecontroleerde onderzoeken bij 2157 OA- en RA-patiënten bij wie baseline-endoscopieën geen ulcera lieten zien. Er was geen dosisrelatie voor de incidentie van gastro-duodenale ulcera en de dosis CELEBREX (50 mg tot 400 mg tweemaal daags). De incidentie voor naproxen 500 mg tweemaal daags was 16,2% en 17,6% in de twee onderzoeken, voor placebo 2,0% en 2,3%, en voor alle doses CELEBREX varieerde de incidentie tussen 2,7%-5,9%. Er zijn geen grote klinische uitkomststudies geweest om klinisch relevante GI-uitkomsten te vergelijken met CELEBREX en naproxen.
In de endoscopische onderzoeken nam ongeveer 11% van de patiënten aspirine (≤ 325 mg/dag). In de CELEBREX-groepen bleek het aantal endoscopische ulcera hoger te zijn bij aspirinegebruikers dan bij niet-gebruikers. Het verhoogde percentage zweren bij deze aspirinegebruikers was echter minder dan het endoscopische ulcuspercentage dat werd waargenomen in de actieve vergelijkingsgroepen, met of zonder aspirine.
PATIËNT INFORMATIE
Medicatiegids voor niet-steroïde anti-inflammatoire geneesmiddelen (NSAID's)
Wat is de belangrijkste informatie die ik moet weten over geneesmiddelen die niet-steroïde anti-inflammatoire geneesmiddelen (NSAID's) worden genoemd?
NSAID's kunnen ernstige bijwerkingen veroorzaken, waaronder:
- Verhoogd risico op een hartaanval of beroerte die tot de dood kan leiden. Dit risico kan vroeg in de behandeling optreden en kan toenemen:
- met toenemende doses NSAID's
- bij langer gebruik van NSAID's
Gebruik geen NSAID's vlak voor of na een hartoperatie die een "coronaire bypass-transplantaat (CABG)" wordt genoemd. Vermijd het gebruik van NSAID's na een recente hartaanval, tenzij uw zorgverlener u dat zegt. U heeft mogelijk een verhoogd risico op een nieuwe hartaanval als u NSAID's gebruikt na een recente hartaanval.
- Verhoogd risico op bloedingen, zweren en tranen (perforatie) van de slokdarm (buis die van de mond naar de maag loopt), maag en darmen:
- op elk moment tijdens gebruik
- zonder waarschuwingssymptomen
- dat kan de dood veroorzaken
- Het risico op het krijgen van een maagzweer of bloeding neemt toe met:
- voorgeschiedenis van maagzweren, of maag- of darmbloedingen bij gebruik van NSAID's
- geneesmiddelen gebruiken die "corticosteroïden", "bloedplaatjesaggregatieremmers", "anticoagulantia", "SSRI's" of "SNRI's" worden genoemd
- toenemende doses NSAID's
- langer gebruik van NSAID's
- roken
- alcohol drinken
- oudere leeftijd
- slechte gezondheid
- gevorderde leverziekte
- bloedingsproblemen
- NSAID's mogen alleen worden gebruikt:
- precies zoals voorgeschreven
- in de laagst mogelijke dosis voor uw behandeling
- voor de kortst benodigde tijd
Wat zijn NSAID's?
NSAID's worden gebruikt voor de behandeling van pijn en roodheid, zwelling en hitte (ontsteking) door medische aandoeningen zoals verschillende soorten artritis, menstruatiekrampen en andere soorten kortdurende pijn.
Wie mag geen NSAID's gebruiken?
Gebruik geen NSAID's:
- als u een astma-aanval, netelroos of een andere allergische reactie heeft gehad met aspirine of andere NSAID's.
- vlak voor of na een bypassoperatie van het hart.
Vertel uw zorgverlener voordat u NSAID's gebruikt over al uw medische aandoeningen, ook als u:
- lever- of nierproblemen heeft
- hoge bloeddruk hebben
- astma hebben
- zwanger bent of van plan bent zwanger te worden. Het gebruik van NSAID's na ongeveer 20 weken zwangerschap of later kan schadelijk zijn voor uw ongeboren baby. Als u gedurende meer dan 2 dagen NSAID's moet gebruiken wanneer u tussen de 20 en 30 weken zwanger bent, moet uw zorgverlener mogelijk de hoeveelheid vocht in uw baarmoeder rond uw baby controleren. U mag geen NSAID's gebruiken na ongeveer 30 weken zwangerschap
- borstvoeding geeft of van plan bent borstvoeding te geven.
Vertel uw zorgverlener over alle geneesmiddelen die u gebruikt, inclusief geneesmiddelen op recept of vrij verkrijgbare medicijnen, vitamines of kruidensupplementen. NSAID's en sommige andere geneesmiddelen kunnen met elkaar interageren en ernstige bijwerkingen veroorzaken. Begin niet met het innemen van een nieuw geneesmiddel zonder eerst met uw zorgverlener te overleggen.
Wat zijn de mogelijke bijwerkingen van NSAID's?
NSAID's kunnen ernstige bijwerkingen veroorzaken, waaronder:
Zie "Wat is de belangrijkste informatie die ik moet weten over geneesmiddelen die niet-steroïde anti-inflammatoire geneesmiddelen (NSAID's) worden genoemd)?
- nieuwe of ergere hoge bloeddruk
- hartfalen
- leverproblemen waaronder leverfalen
- nierproblemen waaronder nierfalen
- lage rode bloedcellen (bloedarmoede)
- levensbedreigende huidreacties
- levensbedreigende allergische reacties
Andere bijwerkingen van NSAID's zijn onder meer: maagpijn, constipatie, diarree, gas, brandend maagzuur, misselijkheid, braken en duizeligheid.
Schakel onmiddellijk noodhulp in als u een van de volgende symptomen krijgt:
- kortademigheid of moeite met ademhalen
- pijn op de borst
- zwakte in een deel of zijkant van uw lichaam
- onduidelijke spraak
- zwelling van het gezicht of de keel
Stop met het gebruik van uw NSAID en bel onmiddellijk uw zorgverlener als u een van de volgende symptomen krijgt:
- misselijkheid
- vermoeider of zwakker dan normaal
- diarree
- jeuk
- je huid of ogen zien er geel uit
- indigestie of maagpijn
- griepachtige symptomen
- bloed overgeven
- er zit bloed in uw stoelgang of het is zwart en plakkerig als teer
- ongebruikelijke gewichtstoename
- huiduitslag of blaren met koorts
- zwelling van de armen, benen, handen en voeten
Als u te veel van uw NSAID heeft ingenomen, neem dan onmiddellijk contact op met uw zorgverlener of roep medische hulp in.
Dit zijn niet alle mogelijke bijwerkingen van NSAID's. Vraag uw zorgverlener of apotheker om meer informatie over NSAID's.
Bel uw arts voor medisch advies over bijwerkingen. U kunt bijwerkingen melden aan de FDA op 1-800-FDA-1088.
Overige informatie over NSAID's
- Aspirine is een NSAID maar verhoogt de kans op een hartaanval niet. Aspirine kan bloedingen in de hersenen, maag en darmen veroorzaken. Aspirine kan ook zweren in de maag en darmen veroorzaken.
- Sommige NSAID's worden zonder recept in lagere doses verkocht (zonder recept verkrijgbaar). Praat met uw zorgverlener voordat u vrij verkrijgbare NSAID's langer dan 10 dagen gebruikt.
Algemene informatie over veilig en effectief gebruik van NSAID's
Medicijnen worden soms voorgeschreven voor andere doeleinden dan die in een Medicatiewijzer vermeld staan. Gebruik NSAID's niet voor een aandoening waarvoor het niet is voorgeschreven. Geef geen NSAID's aan andere mensen, ook niet als zij dezelfde symptomen hebben als u. Het kan hen schaden.
Als u meer informatie wilt over NSAID's, neem dan contact op met uw zorgverlener. U kunt uw apotheker of zorgverlener om informatie vragen over NSAID's die zijn geschreven voor gezondheidswerkers.
Deze medicatiehandleiding is goedgekeurd door de Amerikaanse Food and Drug Administration.
