Ditropan 2.5mg, 5mg Oxybutynin Gebruik, bijwerkingen en dosering. Prijs in online apotheek. Generieke medicijnen zonder recept.
Wat is Ditropan en hoe wordt het gebruikt?
Ditropan is een receptgeneesmiddel dat wordt gebruikt om de symptomen van een overactieve blaas te behandelen. Ditropan 5 mg kan alleen of in combinatie met andere medicijnen worden gebruikt.
Ditropan behoort tot een klasse geneesmiddelen die krampstillende middelen, urinewegen, worden genoemd.
Het is niet bekend of Ditropan veilig en effectief is bij kinderen jonger dan 5 jaar.
Wat zijn de mogelijke bijwerkingen van Ditropan?
Ditropan kan ernstige bijwerkingen veroorzaken, waaronder:
- ernstige maagpijn,
- constipatie,
- wazig zien,
- tunnelvisie,
- oogpijn,
- halo's rond lichten zien,
- weinig of geen plassen,
- pijnlijk of moeilijk plassen,
- dorstig of warm voelen,
- niet kunnen plassen,
- zwaar zweten, en
- hete en droge huid
Roep meteen medische hulp in als u een van de bovenstaande symptomen heeft.
De meest voorkomende bijwerkingen van Ditropan zijn:
- duizeligheid,
- slaperigheid,
- wazig zien,
- droge mond,
- diarree, en
- constipatie
Vertel het uw arts als u een bijwerking heeft die u hindert of die niet weggaat.
Dit zijn niet alle mogelijke bijwerkingen van Ditropan. Vraag uw arts of apotheker om meer informatie.
Bel uw arts voor medisch advies over bijwerkingen. U kunt bijwerkingen melden aan de FDA op 1-800-FDA-1088.
OMSCHRIJVING
Elke biconvexe, gegraveerde blauwe DITROPAN® (oxybutyninechloride) tablet met breukstreep bevat 5 mg oxybutyninechloride. Chemisch gezien is oxybutyninechloride d,l (racemisch) 4-diethylamino-2-butynylfenylcyclohexylglycolaathydrochloride. De
empirische formule van oxybutyninechloride is C22H31NO3•HCl. De structuurformule verschijnt hieronder:
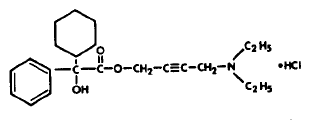
Oxybutyninechloride is een witte kristallijne vaste stof met een molecuulgewicht van 393,9. Het is gemakkelijk oplosbaar in water en zuren, maar relatief onoplosbaar in alkaliën.
DITROPAN-tabletten bevatten ook calciumstearaat, FD&C Blue #1 Lake, lactose en microkristallijne cellulose.
DITROPAN-tabletten zijn voor orale toediening.
Therapeutische categorie: Krampstillend, anticholinergisch.
INDICATIES
DITROPAN 2, 5 mg XL® (oxybutyninechloride) is een muscarine-antagonist die is geïndiceerd voor de behandeling van een overactieve blaas met symptomen van aandrangincontinentie, aandrang en frequentie.
DITROPAN XL® is ook geïndiceerd voor de behandeling van pediatrische patiënten van 6 jaar en ouder met symptomen van overactiviteit van de detrusor geassocieerd met een neurologische aandoening (bijv. spina bifida).
DOSERING EN ADMINISTRATIE
DITROPAN 2,5 mg XL® moet heel worden doorgeslikt met behulp van vloeistoffen en mag niet worden gekauwd, verdeeld of fijngemaakt.
DITROPAN XL® kan met of zonder voedsel worden toegediend.
volwassenen
De aanbevolen startdosering van DITROPAN 5 mg XL® is eenmaal daags 5 of 10 mg, elke dag op ongeveer hetzelfde tijdstip. De dosering kan worden aangepast in stappen van 5 mg om een evenwicht tussen werkzaamheid en verdraagbaarheid te bereiken (tot een maximum van 30 mg/dag). Over het algemeen kan de dosisaanpassing plaatsvinden met tussenpozen van ongeveer een week.
Pediatrische patiënten van 6 jaar en ouder
De aanbevolen startdosering van DITROPAN 5 mg XL® is eenmaal daags 5 mg, elke dag op ongeveer hetzelfde tijdstip. De dosering kan worden aangepast in stappen van 5 mg om een evenwicht tussen werkzaamheid en verdraagbaarheid te bereiken (tot een maximum van 20 mg/dag).
HOE GELEVERD
Doseringsvormen en sterke punten
DITROPAN 5 mg XL® tabletten met verlengde afgifte zijn verkrijgbaar als 5 en 10 mg tabletten voor oraal gebruik:
5 mg : Lichtgele, ronde tablet met “5 XL” aan één zijde bedrukt met zwarte inkt.
10 mg Roze, ronde tablet met aan één zijde “10 XL” bedrukt met zwarte inkt.
Opslag en behandeling
DITROPAN XL® tabletten met verlengde afgifte zijn verkrijgbaar in twee doseringssterkten, 5 mg (lichtgeel) en 10 mg (roze) en zijn aan één zijde bedrukt met “5 XL” of “10 XL” met zwarte inkt. DITROPAN XL® tabletten met verlengde afgifte worden geleverd in flessen van 100 tabletten.
Opslag
Bewaren bij 25°C (77°F); excursies toegestaan tot 15-30°C (59-86°F) [zie USP-gecontroleerde kamertemperatuur ]. Beschermen tegen vocht en vochtigheid.
Buiten bereik van kinderen houden.
Gefabriceerd door: ALZA Corporation, Vacaville, CA 95688, een ALZA OROS Technology Product. Gefabriceerd voor: Janssen Pharmaceuticals, Inc., Titusville, NJ 08560. Herzien: september 2019
BIJWERKINGEN
Ervaring met klinische proeven
Omdat klinische onderzoeken onder sterk uiteenlopende omstandigheden worden uitgevoerd, kunnen de bijwerkingen die in de klinische onderzoeken van een geneesmiddel zijn waargenomen niet direct worden vergeleken met de percentages in de klinische onderzoeken van een ander geneesmiddel en komen mogelijk niet overeen met de percentages die in de klinische praktijk worden waargenomen.
De veiligheid en werkzaamheid van DITROPAN 2, 5 mg XL® (5 tot 30 mg / dag) werd geëvalueerd bij 774 volwassen proefpersonen die deelnamen aan vijf dubbelblinde, gecontroleerde klinische onderzoeken. In vier van de vijf onderzoeken was Ditropan 5 mg IR (5 tot 20 mg/dag bij 199 proefpersonen) een actief vergelijkingsmiddel. Bijwerkingen gemeld door ≥ 1% van de proefpersonen worden weergegeven in tabel 1.
Het stopzettingspercentage als gevolg van bijwerkingen was 4, 4% met DITROPAN XL® vergeleken met 0% met Ditropan IR. De meest voorkomende bijwerking die het staken van de studiemedicatie veroorzaakte, was een droge mond (0,7%).
De volgende bijwerkingen werden gemeld door Metabolisme en voedingsstoornissen: anorexia, vochtretentie; Bloedvataandoeningen: opvliegers; Ademhalingsstelsel-, borstkas- en mediastinumaandoeningen: dysfonie; Maagdarmstelselaandoeningen: dysfagie, frequente stoelgang; Algemene aandoeningen en toedieningsplaatsstoornissen: ongemak op de borst, dorst.
Postmarketingervaring
De volgende aanvullende bijwerkingen zijn gemeld uit wereldwijde postmarketingervaring met DITROPAN 5 mg XL®. Omdat reacties na het in de handel brengen vrijwillig worden gemeld door een populatie van onbekende grootte, is het niet altijd mogelijk om een betrouwbare schatting van hun frequentie of een oorzakelijk verband met blootstelling aan geneesmiddelen vast te stellen.
Infecties en parasitaire aandoeningen: Urineweginfectie; Psychische stoornissen: psychotische stoornis, agitatie, verwardheid, hallucinaties, geheugenstoornis, abnormaal gedrag; Zenuwstelselaandoeningen: stuiptrekkingen; Oogaandoeningen: glaucoom; Ademhalingsstelsel-, borstkas- en mediastinumaandoeningen: verstopte neus; Hartaandoeningen: aritmie, tachycardie, hartkloppingen, verlenging van het QT-interval; Bloedvataandoeningen: blozen, hypertensie; Huid- en onderhuidaandoeningen: uitslag; Nier- en urinewegaandoeningen: impotentie; Algemene aandoeningen en toedieningsplaatsvoorwaarden: overgevoeligheidsreacties, waaronder angio-oedeem met luchtwegobstructie, urticaria en gezichtsoedeem; anafylactische reacties die ziekenhuisopname vereisen voor spoedbehandeling; Letsels, intoxicaties en verrichtingscomplicaties: vallen.
Bijkomende bijwerkingen die zijn gemeld bij sommige andere formuleringen van oxybutyninechloride zijn: cycloplegie, mydriasis en onderdrukking van borstvoeding. In één gemeld geval werd gelijktijdig gebruik van oxybutynine met carbamazepine en dantroleen geassocieerd met bijwerkingen als braken, slaperigheid, verwardheid, onvastheid, onduidelijke spraak en nystagmus, wat wijst op carbamazepine-toxiciteit.
DRUG-INTERACTIES
Gelijktijdig gebruik van oxybutynine met andere anticholinergica of met andere middelen die een droge mond, constipatie, slaperigheid (slaperigheid) en/of andere anticholinergica-achtige effecten veroorzaken, kan de frequentie en/of ernst van dergelijke effecten verhogen.
Anticholinergica kunnen mogelijk de absorptie van sommige gelijktijdig toegediende geneesmiddelen veranderen als gevolg van anticholinerge effecten op de gastro-intestinale motiliteit. Dit kan van belang zijn voor geneesmiddelen met een smalle therapeutische index. Anticholinergica kunnen ook de effecten van prokinetische middelen, zoals metoclopramide, tegenwerken.
De gemiddelde plasmaconcentraties van oxybutynine waren ongeveer 2 keer hoger wanneer DITROPAN 5 mg XL® werd toegediend met ketoconazol, een krachtige CYP3A4-remmer. Andere remmers van het cytochroom P450 3A4-enzymsysteem, zoals antimycotica (bijv. itraconazol en miconazol) of macrolide-antibiotica (bijv. erytromycine en claritromycine), kunnen de gemiddelde farmacokinetische parameters van oxybutynine (dwz Cmax en AUC) veranderen. De klinische relevantie van dergelijke mogelijke interacties is niet bekend. Voorzichtigheid is geboden wanneer dergelijke geneesmiddelen gelijktijdig worden toegediend.
WAARSCHUWINGEN
Inbegrepen als onderdeel van de PREVENTIEVE MAATREGELEN sectie.
PREVENTIEVE MAATREGELEN
Angio-oedeem
Angio-oedeem van het gezicht, de lippen, de tong en/of het strottenhoofd is gemeld met oxybutynine. In sommige gevallen trad angio-oedeem op na de eerste dosis. Angio-oedeem geassocieerd met zwelling van de bovenste luchtwegen kan levensbedreigend zijn. Als betrokkenheid van de tong, hypofarynx of strottenhoofd optreedt, moet oxybutynine onmiddellijk worden stopgezet en moet onmiddellijk worden voorzien in de juiste therapie en/of maatregelen die nodig zijn om een open luchtweg te verzekeren.
Effecten op het centrale zenuwstelsel
Oxybutynine wordt in verband gebracht met anticholinerge effecten op het centrale zenuwstelsel (CZS) [zie: ONGEWENSTE REACTIES ]. Er zijn verschillende anticholinerge effecten op het CZS gemeld, waaronder hallucinaties, agitatie, verwardheid en slaperigheid. Patiënten moeten worden gecontroleerd op tekenen van anticholinerge effecten op het centrale zenuwstelsel, vooral in de eerste paar maanden na het begin van de behandeling of na het verhogen van de dosis. Adviseer patiënten om niet te rijden of zware machines te bedienen totdat ze weten hoe DITROPAN XL® hen beïnvloedt. Als een patiënt anticholinerge effecten op het CZS ervaart, moet dosisverlaging of stopzetting van het geneesmiddel worden overwogen.
DITROPAN XL® moet met voorzichtigheid worden gebruikt bij patiënten met reeds bestaande dementie die worden behandeld met cholinesteraseremmers vanwege het risico op verergering van de symptomen.
DITROPAN XL® moet met voorzichtigheid worden gebruikt bij patiënten met de ziekte van Parkinson vanwege het risico op verergering van de symptomen.
Verergering van symptomen van Myasthenia Gravis
DITROPAN XL® moet met voorzichtigheid worden gebruikt bij patiënten met myasthenia gravis vanwege het risico op verergering van de symptomen.
Verergering van symptomen van verminderde gastro-intestinale motiliteit bij patiënten met autonome neuropathie
DITROPAN 2,5 mg XL® moet met voorzichtigheid worden gebruikt bij patiënten met autonome neuropathie vanwege het risico op verergering van symptomen van verminderde gastro-intestinale motiliteit.
Urineretentie
DITROPAN 5 mg XL® moet met voorzichtigheid worden toegediend aan patiënten met klinisch significante obstructie van de blaasafvoer vanwege het risico op urineretentie [zie CONTRA-INDICATIES ].
Gastro-intestinale bijwerkingen
DITROPAN 2,5 mg XL® moet met voorzichtigheid worden toegediend aan patiënten met gastro-intestinale obstructieve aandoeningen vanwege het risico op maagretentie [zie CONTRA-INDICATIES ].
DITROPAN XL® kan, net als andere anticholinergica, de gastro-intestinale motiliteit verminderen en moet met voorzichtigheid worden gebruikt bij patiënten met aandoeningen zoals colitis ulcerosa en intestinale atonie.
DITROPAN 2,5 mg XL® moet met voorzichtigheid worden gebruikt bij patiënten met gastro-oesofageale reflux en/of die gelijktijdig geneesmiddelen gebruiken (zoals bisfosfonaten) die oesofagitis kunnen veroorzaken of verergeren.
Zoals met elk ander niet-vervormbaar materiaal, is voorzichtigheid geboden bij het toedienen van DITROPAN XL® aan patiënten met reeds bestaande ernstige gastro-intestinale vernauwing (pathologisch of iatrogeen). Er zijn zeldzame meldingen geweest van obstructieve symptomen bij patiënten met bekende stricturen in verband met de inname van andere geneesmiddelen in niet-vervormbare formuleringen met gecontroleerde afgifte.
Niet-klinische toxicologie
Carcinogenese, mutagenese, verminderde vruchtbaarheid
Een studie van 24 maanden bij ratten met doseringen van oxybutyninechloride van 20, 80 en 160 mg/kg/dag toonde geen bewijs van carcinogeniteit. Deze doses zijn ongeveer 6, 25 en 50 keer de maximale menselijke blootstelling, gebaseerd op een humane equivalente dosis waarbij rekening wordt gehouden met normalisatie van het lichaamsoppervlak.
Oxybutyninechloride vertoonde geen toename van mutagene activiteit bij testen in de testsystemen Schizosaccharomyces pompholiciformis, Saccharomyces cerevisiae en Salmonella typhimurium.
Reproductieonderzoeken met oxybutyninechloride bij muizen, ratten, hamsters en konijnen toonden geen bewijs van verminderde vruchtbaarheid.
Gebruik bij specifieke populaties
Zwangerschap
Zwangerschap Categorie B
Er zijn geen adequate en goed gecontroleerde onderzoeken met DITROPAN 5 mg XL® bij zwangere vrouwen. DITROPAN XL® mag alleen tijdens de zwangerschap worden gebruikt als het mogelijke voordeel voor de patiënt opweegt tegen het risico voor de patiënt en de foetus. Vrouwen die zwanger worden tijdens de behandeling met DITROPAN XL® worden aangemoedigd om contact op te nemen met hun arts.
Risico Samenvatting
Op basis van diergegevens wordt voorspeld dat oxybutynine een lage kans heeft om het risico op nadelige ontwikkelingseffecten te verhogen boven het achtergrondrisico.
Dierlijke gegevens
Reproductieonderzoeken met oxybutyninechloride bij muizen, ratten, hamsters en konijnen toonden geen bewijs van verminderde vruchtbaarheid of schade aan de dierlijke foetus.
Moeders die borstvoeding geven
Het is niet bekend of oxybutynine wordt uitgescheiden in de moedermelk. Omdat veel geneesmiddelen worden uitgescheiden in de moedermelk, is voorzichtigheid geboden wanneer DITROPAN 5 mg XL® wordt toegediend aan een vrouw die borstvoeding geeft.
Pediatrisch gebruik
De veiligheid en werkzaamheid van DITROPAN XL® werden bestudeerd bij 60 kinderen in een 24 weken durende, open-label, niet-gerandomiseerde studie. De patiënten waren tussen de 6 en 15 jaar oud, hadden allemaal symptomen van overactiviteit van de detrusor in samenhang met een neurologische aandoening (bijv. spina bifida), ze gebruikten allemaal schone intermitterende katheterisatie en ze waren allemaal huidige gebruikers van oxybutyninechloride. Onderzoeksresultaten toonden aan dat toediening van DITROPAN 2,5 mg XL® 5 tot 20 mg/dag gepaard ging met een toename vanaf baseline van het gemiddelde urinevolume per katheterisatie van 108 ml tot 136 ml, een toename vanaf baseline van het gemiddelde urinevolume na het ontwaken van 148 ml tot 189 ml, en een stijging ten opzichte van de uitgangswaarde van het gemiddelde percentage katheterisaties zonder lekkende episode van 34% naar 51%.
De urodynamische resultaten waren consistent met de klinische resultaten. Toediening van DITROPAN XL® resulteerde in een toename vanaf baseline van de gemiddelde maximale cystometrische capaciteit van 185 ml tot 254 ml, een afname vanaf baseline van de gemiddelde detrusordruk bij maximale cystometrische capaciteit van 44 cm H2O tot 33 cm H2O en een verlaging van het percentage van de patiënten die ongeremde contracties van de detrusor vertoonden (van ten minste 15 cm H O) van 60% tot 28%.
De farmacokinetiek van DITROPAN 5 mg XL® bij deze patiënten was consistent met die gerapporteerd voor volwassenen [zie KLINISCHE FARMACOLOGIE ].
DITROPAN 5 mg XL® wordt niet aanbevolen bij pediatrische patiënten die de tablet niet in zijn geheel kunnen doorslikken zonder te kauwen, te verdelen of te pletten, of bij kinderen jonger dan 6 jaar.
Geriatrisch gebruik
De snelheid en ernst van de anticholinerge effecten die werden gemeld door patiënten jonger dan 65 jaar en die van 65 jaar en ouder waren vergelijkbaar. De farmacokinetiek van DITROPAN XL® was vergelijkbaar bij alle onderzochte patiënten (tot 78 jaar).
Nierfunctiestoornis
Er zijn geen onderzoeken uitgevoerd met DITROPAN XL® bij patiënten met een nierfunctiestoornis.
Leverfunctiestoornis
Er zijn geen onderzoeken uitgevoerd met DITROPAN 2, 5 mg XL® bij patiënten met leverinsufficiëntie.
OVERDOSERING
De continue afgifte van oxybutynine uit DITROPAN 5 mg XL® moet worden overwogen bij de behandeling van overdosering. Patiënten moeten gedurende ten minste 24 uur worden gecontroleerd. De behandeling moet symptomatisch en ondersteunend zijn. Een catharsis kan worden toegediend.
Overdosering met oxybutyninechloride is in verband gebracht met anticholinerge effecten, waaronder opwinding van het centrale zenuwstelsel, blozen, koorts, uitdroging, hartritmestoornissen, braken en urineretentie.
Inname van 100 mg oxybutyninechloride in combinatie met alcohol is gemeld bij een 13-jarige jongen met geheugenverlies en een 34-jarige vrouw die stupor ontwikkelde, gevolgd door desoriëntatie en opwinding bij het ontwaken, verwijde pupillen, droge huid, hartritmestoornissen en urineretentie. Beide patiënten herstelden volledig met symptomatische behandeling.
CONTRA-INDICATIES
DITROPAN 2,5 mg XL® is gecontra-indiceerd bij patiënten met urineretentie, maagretentie en andere ernstige verminderde gastro-intestinale motiliteitsaandoeningen, ongecontroleerd nauwekamerhoekglaucoom.
DITROPAN 2,5 mg XL® is ook gecontra-indiceerd bij patiënten die overgevoelig zijn gebleken voor de geneesmiddelsubstantie of andere componenten van het product. Er zijn meldingen geweest van overgevoeligheidsreacties, waaronder anafylaxie en angio-oedeem.
KLINISCHE FARMACOLOGIE
Werkingsmechanisme
Oxybutynine ontspant de gladde spieren van de blaas. Oxybutyninechloride oefent een direct krampstillend effect uit op gladde spieren en remt de muscarinewerking van acetylcholine op gladde spieren. Er treden geen blokkerende effecten op bij skeletale neuromusculaire verbindingen of autonome ganglia (antinicotinische effecten).
Antimuscarine-activiteit bevindt zich voornamelijk in het R-isomeer. Een metaboliet, desethyloxybutynine, heeft in in vitro-onderzoeken een farmacologische activiteit die vergelijkbaar is met die van oxybutynine.
farmacodynamiek
Bij patiënten met aandoeningen die worden gekenmerkt door onwillekeurige blaascontracties, hebben cystometrische onderzoeken aangetoond dat oxybutynine de blaascapaciteit (vesicale) verhoogt, de frequentie van ongeremde contracties van de detrusorspier vermindert en de aanvankelijke wens om te plassen vertraagt.
Farmacokinetiek
Absorptie
Na de eerste dosis DITROPAN XL® stijgen de plasmaconcentraties van oxybutynine gedurende 4 tot 6 uur; daarna worden stabiele concentraties gedurende maximaal 24 uur gehandhaafd, waardoor fluctuaties tussen piek- en dalconcentraties geassocieerd met oxybutynine worden geminimaliseerd.
De relatieve biologische beschikbaarheid van R- en S-oxybutynine van DITROPAN XL® is respectievelijk 156% en 187% in vergelijking met oxybutynine. De gemiddelde farmacokinetische parameters voor R- en S-oxybutynine zijn samengevat in Tabel 2. De plasmaconcentratie-tijdprofielen voor R- en S-oxybutynine zijn vergelijkbaar in vorm; Figuur 1 toont het profiel voor R-oxybutynine.
Figuur 1: Gemiddelde R-oxybutynine plasmaconcentraties na een enkele dosis DITROPAN XL® 10 mg en oxybutynine 5 mg elke 8 uur toegediend (n=23 voor elke behandeling).
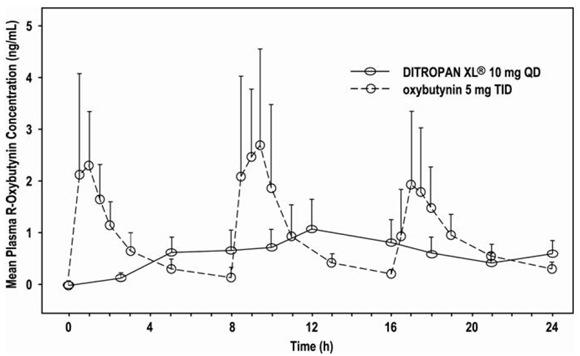
Steady-state oxybutynine-plasmaconcentraties worden bereikt op dag 3 van herhaalde DITROPAN XL®-dosering, zonder waargenomen accumulatie van het geneesmiddel of verandering in de farmacokinetische parameters van oxybutynine en desethyloxybutynine.
De farmacokinetiek van DITROPAN 5 mg XL® is onderzocht bij 19 kinderen in de leeftijd van 5-15 jaar met overactiviteit van de detrusor geassocieerd met een neurologische aandoening (bijv. spina bifida). De kinderen kregen DITROPAN 2,5 mg XL® totale dagelijkse dosis variërend van 5 tot 20 mg (0,10 tot 0,77 mg/kg). Er werd een spaarzame bemonsteringstechniek gebruikt om serummonsters te verkrijgen. Wanneer alle beschikbare gegevens zijn genormaliseerd naar een equivalent van 5 mg DITROPAN XL® per dag, worden de gemiddelde farmacokinetische parameters afgeleid voor R- en S-oxybutynine en R- en S-desethyloxybutynine samengevat in Tabel 3. De plasma-tijdconcentratieprofielen want R- en S-oxybutynine zijn vergelijkbaar van vorm; Figuur 2 toont het profiel voor R-oxybutynine wanneer alle beschikbare gegevens zijn genormaliseerd naar een equivalent van 5 mg per dag.
Figuur 2: Gemiddelde steady-state (± SD) R-oxybutynine plasmaconcentraties na toediening van 5 tot 20 mg DITROPAN 5 mg XL® eenmaal daags bij kinderen van 5-15 jaar. Plot geeft alle beschikbare gegevens weer, genormaliseerd naar een equivalent van DITROPAN XL® 5 mg eenmaal daags.
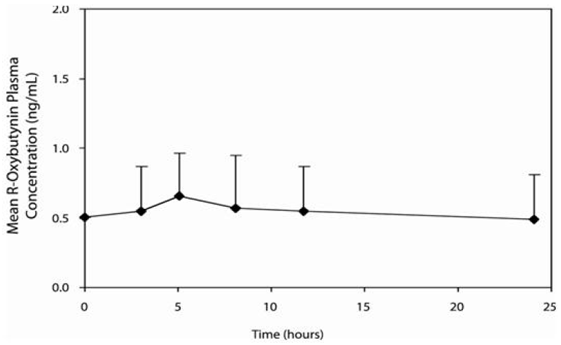
Voedseleffecten
De snelheid en mate van absorptie en het metabolisme van oxybutynine zijn vergelijkbaar onder gevoede en nuchtere omstandigheden.
Verdeling
Oxybutynine wordt wijd verspreid in lichaamsweefsels na systemische absorptie. Het distributievolume is 193 l na intraveneuze toediening van 5 mg oxybutyninechloride. Beide enantiomeren van oxybutynine zijn sterk gebonden (>99%) aan plasma-eiwitten. Beide enantiomeren van N-desethyloxybutynine zijn ook sterk gebonden (>97%) aan plasma-eiwitten. Het belangrijkste bindende eiwit is alfa-1-zuurglycoproteïne.
Metabolisme
Oxybutynine wordt voornamelijk gemetaboliseerd door de cytochroom P450-enzymsystemen, met name CYP3A4 dat voornamelijk in de lever en de darmwand wordt aangetroffen. Zijn stofwisselingsproducten omvatten fenylcyclohexylglycolzuur, dat farmacologisch inactief is, en desethyloxybutynine, dat farmacologisch actief is. Na toediening van DITROPAN 2, 5 mg XL® zijn de plasmaconcentraties van R- en S-desethyloxybutynine respectievelijk 73% en 92% van de concentraties die worden waargenomen met oxybutynine.
uitscheiding
Oxybutynine wordt uitgebreid gemetaboliseerd door de lever, waarbij minder dan 0,1% van de toegediende dosis onveranderd in de urine wordt uitgescheiden. Ook wordt minder dan 0,1% van de toegediende dosis uitgescheiden als de metaboliet desethyloxybutynine.
Evenredigheid van de dosis
Farmacokinetische parameters van oxybutynine en desethyloxybutynine (Cmax en AUC) na toediening van 5-20 mg DITROPAN 5 mg XL® zijn dosisproportioneel.
Gebruik bij specifieke populaties
pediatrisch
De farmacokinetiek van DITROPAN 2,5 mg XL® werd geëvalueerd bij 19 kinderen van 5-15 jaar met overactiviteit van de detrusor geassocieerd met een neurologische aandoening (bijv. spina bifida). De farmacokinetiek van DITROPAN 2, 5 mg XL® bij deze pediatrische patiënten was consistent met die gerapporteerd voor volwassenen (zie tabellen 2 en 3 en afbeeldingen 1 en 2 hierboven).
Geslacht
Er zijn geen significante verschillen in de farmacokinetiek van oxybutynine bij gezonde mannelijke en vrouwelijke vrijwilligers na toediening van DITROPAN 2,5 mg XL®.
Ras
Beschikbare gegevens suggereren dat er geen significante verschillen zijn in de farmacokinetiek van oxybutynine op basis van ras bij gezonde vrijwilligers na toediening van DITROPAN 2,5 mg XL®.
Klinische studies
DITROPAN 5 mg XL® werd geëvalueerd voor de behandeling van patiënten met een overactieve blaas met symptomen van aandrangincontinentie, aandrang en frequentie in drie gecontroleerde werkzaamheidsstudies. De meerderheid van de patiënten was blank (89,0%) en vrouw (91,9%) met een gemiddelde leeftijd van 59 jaar (bereik 18 tot 98 jaar). De toelatingscriteria vereisten dat patiënten aandrangincontinentie of gemengde incontinentie hadden (met een overwicht van aandrang), zoals blijkt uit ≥ 6 episoden van aandrangincontinentie per week en ≥ 10 micties per dag. Studie 1 was een escalatieontwerp met een vaste dosis, terwijl de andere twee onderzoeken een dosisaanpassingsontwerp gebruikten waarin de uiteindelijke dosis van elke patiënt werd aangepast aan een evenwicht tussen verbetering van incontinentiesymptomen en verdraagbaarheid van bijwerkingen. Alle drie de onderzoeken omvatten patiënten waarvan bekend was dat ze reageerden op oxybutynine of andere anticholinergica, en deze patiënten werden gedurende maximaal 2 weken op een laatste dosis gehouden.
De werkzaamheidsresultaten voor de drie gecontroleerde onderzoeken worden weergegeven in de volgende tabellen 4, 5 en 6 en figuren 3, 4 en 5.
Afbeelding 3: Gemiddelde verandering (±SD) in episoden van aandrang-urine-incontinentie per week vanaf baseline (onderzoek 1)
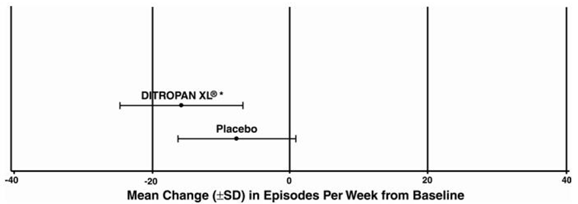
Afbeelding 4: Gemiddelde verandering (±SD) in episoden van aandrang-urine-incontinentie per week vanaf baseline (onderzoek 2)
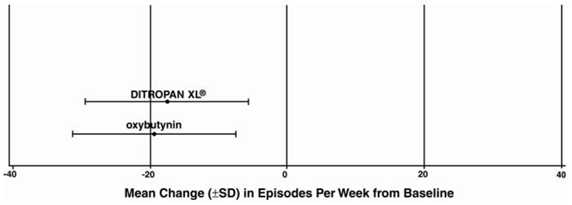
Afbeelding 5: Gemiddelde verandering (±SD) in episoden van aandrang-urine-incontinentie per week vanaf baseline (onderzoek 3)
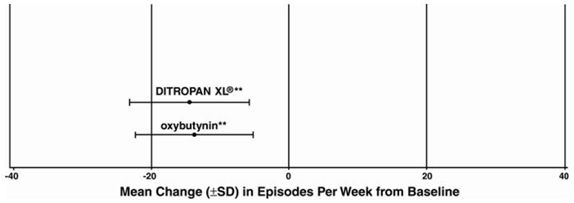
PATIËNT INFORMATIE
- Patiënten moeten worden geïnformeerd dat oxybutynine angio-oedeem kan veroorzaken dat kan leiden tot levensbedreigende luchtwegobstructie. Patiënten moeten het advies krijgen om de behandeling met oxybutynine onmiddellijk te staken en onmiddellijk medische hulp in te roepen als ze last krijgen van zwelling van de tong, oedeem van de laryngofarynx of ademhalingsmoeilijkheden.
- Patiënten moeten worden geïnformeerd dat anticholinerge (antimuscarine) middelen zoals DITROPAN XL® klinisch significante bijwerkingen kunnen veroorzaken die verband houden met anticholinerge activiteit, zoals:
- Urineretentie en constipatie
- Hitte-uitputting door verminderd zweten. Hitte-uitputting kan optreden wanneer anticholinergica worden toegediend in aanwezigheid van een hoge omgevingstemperatuur.
- Patiënten moeten erop worden gewezen dat anticholinergica zoals DITROPAN 5 mg XL slaperigheid (somnolentie), duizeligheid of wazig zien kunnen veroorzaken. Patiënten moeten worden geadviseerd om voorzichtig te zijn bij beslissingen om mogelijk gevaarlijke activiteiten uit te voeren totdat de effecten van DITROPAN XL® zijn vastgesteld.
- Patiënten moeten worden geïnformeerd dat alcohol de slaperigheid veroorzaakt door anticholinergica zoals DITROPAN XL® kan versterken.
- Patiënten moeten worden geïnformeerd dat DITROPAN 5 mg XL® in zijn geheel moet worden doorgeslikt met behulp van vloeistoffen. Patiënten mogen geen tabletten kauwen, verdelen of pletten. Het medicijn zit in een niet-resorbeerbare schaal die is ontworpen om het medicijn met een gecontroleerde snelheid af te geven. De tabletomhulling wordt uit het lichaam verwijderd; patiënten hoeven zich geen zorgen te maken als ze af en toe iets in hun ontlasting opmerken dat op een tablet lijkt.
- DITROPAN 5 mg XL® moet elke dag op ongeveer hetzelfde tijdstip worden ingenomen.
