Thorazine 50mg, 100mg Chlorpromazine Gebruik, bijwerkingen en dosering. Prijs in online apotheek. Generieke medicijnen zonder recept.
Wat is Thorazine 50 mg en hoe wordt het gebruikt?
Thorazine is een receptgeneesmiddel dat wordt gebruikt voor de behandeling van de symptomen van schizofrenie, psychotische stoornissen, misselijkheid en braken, angst voor de operatie, intraoperatieve sedatie, hardnekkige hik en acute intermitterende profyrie (jeuk en blaren op de huid). Thorazine kan alleen of in combinatie met andere medicijnen worden gebruikt.
Thorazine behoort tot een klasse geneesmiddelen die antipsychotica, fenothiazine, wordt genoemd.
Het is niet bekend of Thorazine 50 mg veilig en effectief is bij kinderen jonger dan 6 maanden.
Wat zijn de mogelijke bijwerkingen van Thorazine 100 mg?
Thorazine 100 mg kan ernstige bijwerkingen veroorzaken, waaronder:
- ongecontroleerde spierbewegingen in uw gezicht,
- stijfheid in je nek,
- beklemming in je keel,
- moeite met ademhalen of slikken,
- duizeligheid,
- verwardheid,
- agitatie,
- zenuwachtig voelen,
- Moeite met slapen
- zwakheid,
- zwelling van de borst of afscheiding,
- convulsies (toevallen),
- geel worden van de huid of ogen (geelzucht),
- koorts,
- rillingen,
- zweertjes in de mond,
- huidzweren,
- keelpijn,
- hoesten,
- zeer stijve (starre) spieren,
- hoge koorts,
- zweten,
- verwardheid,
- snelle of onregelmatige hartslagen, en
- trillingen
Roep meteen medische hulp in als u een van de bovenstaande symptomen heeft.
De meest voorkomende bijwerkingen van Thorazine zijn:
- slaperigheid,
- droge mond,
- verstopte neus,
- wazig zien,
- constipatie,
- impotentie, en
- moeite met een orgasme
Vertel het uw arts als u een bijwerking heeft die u hindert of die niet weggaat.
Dit zijn niet alle mogelijke bijwerkingen van Thorazine. Vraag uw arts of apotheker om meer informatie.
Bel uw arts voor medisch advies over bijwerkingen. U kunt bijwerkingen melden aan de FDA op 1-800-FDA-1088.
OMSCHRIJVING
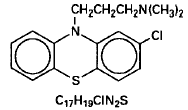
Thorazine (chloorpromazine) is 10-(3-dimethylaminopropyl)-2-chloorfenothiazine, een dimethylaminederivaat van fenothiazine. Het is aanwezig in orale en injecteerbare vormen als het hydrochloridezout en in de zetpillen als de basis.
— Elke ronde, oranje, omhulde tablet bevat chloorpromazinehydrochloride als volgt: 10 mg bedrukt met SKF en T73; 25 mg bedrukt met SKF en T74; 50 mg bedrukt met SKF en T76; 100 mg bedrukt met SKF en T77; 200 mg bedrukt met SKF en T79. Inactieve ingrediënten bestaan uit benzoëzuur, croscarmellosenatrium, D&C Yellow No. 10, FD&C Blue No. 2, FD&C Yellow No. 6, gelatine, hydroxypropylmethylcellulose, lactose, magnesiumstearaat, methylparaben, polyethyleenglycol, propylparaben, talk, titaniumdioxide en sporenhoeveelheden van andere inactieve ingrediënten.
Spansule® capsules met aanhoudende afgifte — Elke Thorazine (chloorpromazine) Spansule®-capsule is zo geprepareerd dat een eerste dosis onmiddellijk wordt afgegeven en de resterende medicatie geleidelijk over een langere periode wordt afgegeven.
Elke capsule, met ondoorzichtige oranje dop en natuurlijke romp, bevat chloorpromazinehydrochloride als volgt: 30 mg bedrukt met SKF en T63; 75 mg bedrukt met SKF en T64; 150 mg bedrukt met SKF en T66. Inactieve ingrediënten bestaan uit benzylalcohol, calciumsulfaat, cetylpyridiniumchloride, FD&C Yellow No. 6, gelatine, glyceryldistearaat, glycerylmonostearaat, ijzeroxide, povidon, siliciumdioxide, natriumlaurylsulfaat, zetmeel, sucrose, titaniumdioxide, was en sporenhoeveelheden van andere inactieve ingrediënten.
ampullen — Elke ml bevat, in waterige oplossing, chloorpromazinehydrochloride, 25 mg; ascorbinezuur, 2 mg; natriumbisulfiet, 1 mg; natriumchloride, 6 mg; natriumsulfiet, 1 mg.
Injectieflacons voor meerdere doses — Elke ml bevat, in waterige oplossing, chloorpromazinehydrochloride, 25 mg; ascorbinezuur, 2 mg; natriumbisulfiet, 1 mg; natriumchloride, 1 mg; natriumsulfiet, 1 mg; benzylalcohol, 2%, als conserveermiddel.
Siroop — Elke 5 ml (1 theelepel) heldere vloeistof met sinaasappelcustardsmaak bevat 10 mg chloorpromazinehydrochloride. Inactieve ingrediënten bestaan uit citroenzuur, smaakstoffen, natriumbenzoaat, natriumcitraat, sucrose en water.
zetpillen — Elke zetpil bevat chloorpromazine, 25 of 100 mg, glycerine, glycerylmonopalmitaat, glycerylmonostearaat, gehydrogeneerde kokosolievetzuren en gehydrogeneerde palmpitolievetzuren.
INDICATIES
Voor de behandeling van schizofrenie.
Om misselijkheid en braken onder controle te houden.
Voor verlichting van rusteloosheid en angst vóór de operatie.
Voor acute intermitterende porfyrie.
Als hulpmiddel bij de behandeling van tetanus.
Om de manifestaties van het manische type manisch-depressieve ziekte te beheersen.
Voor verlichting van hardnekkige hik.
Voor de behandeling van ernstige gedragsproblemen bij kinderen (1 tot 12 jaar) gekenmerkt door strijdlust en/of explosief hyperexciteerbaar gedrag (niet in verhouding tot onmiddellijke provocaties), en bij de kortdurende behandeling van hyperactieve kinderen die overmatige motoriek vertonen met bijbehorende gedragsstoornissen bestaande uit enkele of alle van de volgende symptomen: impulsiviteit, moeite om de aandacht vast te houden, agressiviteit, stemmingslabiliteit en slechte frustratietolerantie.
DOSERING EN ADMINISTRATIE
VOLWASSENEN
Pas de dosering aan de persoon en de ernst van zijn aandoening aan, in het besef dat de milligram-voor-milligram-potentierelatie tussen alle doseringsvormen niet nauwkeurig klinisch is vastgesteld. Het is belangrijk om de dosering te verhogen totdat de symptomen onder controle zijn. Bij verzwakte of uitgemergelde patiënten moet de dosering geleidelijker worden verhoogd. Bij voortgezette therapie de dosering geleidelijk verlagen tot het laagste effectieve onderhoudsniveau, nadat de symptomen gedurende een redelijke periode onder controle zijn geweest.
Over het algemeen kunnen doseringsaanbevelingen voor andere orale vormen van het medicijn worden toegepast op Spansule®-capsules met aanhoudende afgifte op basis van de totale dagelijkse dosering in milligram.
De tabletten van 100 mg en 200 mg zijn bestemd voor gebruik bij ernstige neuropsychiatrische aandoeningen.
Verhoog de parenterale dosering alleen als er geen hypotensie is opgetreden. Zie BELANGRIJKE OPMERKINGEN OVER INJECTIE voordat u IM gebruikt.
Oudere patiënten - Over het algemeen zijn doseringen in het lagere bereik voldoende voor de meeste oudere patiënten. Aangezien ze gevoeliger lijken te zijn voor hypotensie en neuromusculaire reacties, moeten dergelijke patiënten nauwlettend worden geobserveerd. De dosering moet worden aangepast aan het individu, de respons moet zorgvuldig worden gecontroleerd en de dosering moet dienovereenkomstig worden aangepast. Bij oudere patiënten moet de dosering geleidelijker worden verhoogd.
Psychotische stoornissen - Verhoog de dosering geleidelijk totdat de symptomen onder controle zijn. Maximale verbetering kan weken of zelfs maanden niet worden gezien. Ga door met optimale dosering gedurende 2 weken; verlaag vervolgens de dosering geleidelijk tot het laagste effectieve onderhoudsniveau. Een dagelijkse dosering van 200 mg is niet ongebruikelijk. Sommige patiënten hebben hogere doseringen nodig (bijv. 800 mg per dag is niet ongebruikelijk bij ontslagen psychiatrische patiënten).
GEHOSPITALISEERDE PATINTEN ACUTE SCHIZOFRENISCHE OF MANISCHE STATEN - IM: 25 mg (1 ml). Geef indien nodig een extra injectie van 25 tot 50 mg in 1 uur. Verhoog de volgende IM-doses geleidelijk over meerdere dagen - tot 400 mg elke 4 tot 6 uur in uitzonderlijk ernstige gevallen - totdat de patiënt onder controle is. Gewoonlijk wordt de patiënt binnen 24 tot 48 uur rustig en coöperatief en orale doses kunnen worden vervangen en verhoogd totdat de patiënt kalm is. 500 mg per dag is over het algemeen voldoende. Hoewel geleidelijke verhogingen tot 2.000 mg per dag of meer nodig kunnen zijn, is er gewoonlijk weinig therapeutische winst te behalen door 1.000 mg per dag gedurende langere perioden te overschrijden. Over het algemeen dienen de doseringen lager te zijn bij ouderen, uitgemergelde en verzwakte personen. MINDER acuut gestoord — Oraal: 25 mg driemaal daags Verhoog geleidelijk tot de effectieve dosis is bereikt - gewoonlijk 400 mg per dag. OUTPATINTEN— Oraal: 10 mg driemaal of driemaal, of 25 mg tweemaal daags of driemaal MEER ERNSTIGE GEVALLEN— Oraal: 25 mg driemaal daags Na 1 of 2 dagen kan de dagelijkse dosering worden verhoogd met 20 tot 50 mg met tussenpozen van een halve week totdat de patiënt kalm en coöperatief wordt . SNELLE CONTROLE VAN ERNSTIGE SYMPTOMEN - IM: 25 mg (1 ml). Herhaal indien nodig in 1 uur. Volgende doses moeten oraal zijn, 25 tot 50 mg driemaal daags
Misselijkheid en overgeven — Oraal: 10 tot 25 mg elke 4 tot 6 uur, prn, indien nodig verhoogd. IM: 25 mg (1 ml). Als er geen hypotensie optreedt, geef dan 25 tot 50 mg elke 3 tot 4 uur, prn, totdat het braken stopt. Schakel dan over op orale dosering. Rectaal: één zetpil van 100 mg elke 6 tot 8 uur, bij sommige patiënten is de helft van deze dosis voldoende.
TIJDENS CHIRURGIE — IM: 12,5 mg (0,5 ml). Herhaal indien nodig in 1 / 2 uur en als er geen hypotensie optreedt. IV: 2 mg per fractionele injectie, met tussenpozen van 2 minuten. Overschrijd niet 25 mg. Verdun tot 1 mg/ml, dwz 1 ml (25 mg) gemengd met 24 ml zoutoplossing.
preoperatieve vrees — Oraal: 25 tot 50 mg, 2 tot 3 uur voor de operatie. IM: 12,5 tot 25 mg (0,5 tot 1 ml), 1 tot 2 uur voor de operatie.
hardnekkige hik — Oraal: 25 tot 50 mg driemaal of driemaal daags Als de symptomen 2 tot 3 dagen aanhouden, geef dan 25 tot 50 mg (1 tot 2 ml) IM Als de symptomen aanhouden, gebruik dan een langzame IV-infusie met de patiënt plat in bed: 25 tot 50 mg ( 1 tot 2 ml) in 500 tot 1.000 ml zoutoplossing. Houd de bloeddruk nauwlettend in de gaten.
Acute intermitterende porfyrie — Oraal: 25 tot 50 mg driemaal daags of driemaal daags. Kan gewoonlijk na enkele weken worden stopgezet, maar voor sommige patiënten kan onderhoudstherapie nodig zijn. IM: 25 mg (1 ml) tid of qid totdat de patiënt orale therapie kan nemen.
Tetanus — IM: 25 tot 50 mg (1 tot 2 ml) 3 of 4 maal daags toegediend, meestal in combinatie met barbituraten. De totale doses en de frequentie van toediening moeten worden bepaald aan de hand van de respons van de patiënt, te beginnen met lage doses en geleidelijk te verhogen. IV: 25 tot 50 mg (1 tot 2 ml). Verdun tot ten minste 1 mg per ml en dien toe met een snelheid van 1 mg per minuut.
DOSERING EN TOEDIENING — PEDIATRISCHE PATINTEN (6 maanden tot 12 jaar)
Thorazine (chloorpromazine) mag over het algemeen niet worden gebruikt bij pediatrische patiënten jonger dan 6 maanden, behalve waar mogelijk levensreddend. Het mag niet worden gebruikt bij aandoeningen waarvoor geen specifieke pediatrische doseringen zijn vastgesteld.
Ernstige gedragsproblemen — OUTPATIENTEN — Selecteer de toedieningsweg op basis van de ernst van de toestand van de patiënt en verhoog de dosering geleidelijk indien nodig. Oraal: 1 / 4 mg/lb lichaamsgewicht elke 4 tot 6 uur, prn (bijv. voor een kind van 40 pond - 10 mg elke 4 tot 6 uur). Rectaal: 1/2 mg/lb lichaamsgewicht elke 6 tot 8 uur, prn (bijv. voor een kind van 20 tot 30 lb - een halve zetpil van 25 mg elke 6 tot 8 uur). IM: 1 / 4 mg/lb lichaamsgewicht q6 tot 8h, prn
GEHOSPITALISEERDE PATINTEN - Begin, net als bij poliklinische patiënten, met lage doses en verhoog de dosering geleidelijk. Bij ernstige gedragsstoornissen kunnen hogere doseringen (50 tot 100 mg per dag en bij oudere kinderen 200 mg per dag of meer) nodig zijn. Er is weinig bewijs dat gedragsverbetering bij ernstig gestoorde geestelijk gehandicapte patiënten verder wordt versterkt door doses van meer dan 500 mg per dag. Maximale IM-dosering: kinderen tot 5 jaar (of 50 lbs), niet meer dan 40 mg / dag; 5 tot 12 jaar (of 50 tot 100 lbs), niet meer dan 75 mg/dag behalve in onhandelbare gevallen.
Misselijkheid en overgeven — Dosering en frequentie van toediening moeten worden aangepast aan de ernst van de symptomen en de reactie van de patiënt. De duur van de activiteit na intramusculaire toediening kan tot 12 uur duren. Volgende doses kunnen indien nodig via dezelfde route worden toegediend. Oraal: 1 / 4 mg / lb lichaamsgewicht (bijv. 40 lb kind - 10 mg elke 4 tot 6 uur). Rectaal: 1/2 mg/lb lichaamsgewicht elke 6 tot 8 uur, prn (bijv. 20 tot 30 lb kind - de helft van een zetpil van 25 mg elke 6 tot 8 uur). IM: 1 / 4 mg/lb lichaamsgewicht elke 6 tot 8 uur, prn Maximale IM Dosering: Pediatrische patiënten 6 maanden tot 5 jaar. (of 50 lbs), niet meer dan 40 mg / dag; 5 tot 12 jaar. (of 50 tot 100 lbs), niet meer dan 75 mg / dag behalve in ernstige gevallen. TIJDENS CHIRURGIE — IM: 1/8 mg/lb lichaamsgewicht. Herhaal indien nodig in 1 / 2 uur en als er geen hypotensie optreedt. IV: 1 mg per fractionele injectie met tussenpozen van 2 minuten en de aanbevolen IM-dosering niet overschrijden. Verdun altijd tot 1 mg/ml, dwz 1 ml (25 mg) gemengd met 24 ml zoutoplossing.
preoperatieve vrees — 1 / 4 mg/lb lichaamsgewicht, ofwel oraal 2 tot 3 uur voor de operatie, of IM 1 tot 2 uur ervoor.
Tetanus — IM of IV: 1/4 mg/lb lichaamsgewicht elke 6 tot 8 uur. Indien IV gegeven, verdunnen tot ten minste 1 mg/ml en toedienen met een snelheid van 1 mg per 2 minuten. Bij patiënten tot 50 lbs, niet meer dan 40 mg per dag; 50 tot 100 lbs, niet meer dan 75 mg, behalve in ernstige gevallen.
Belangrijke opmerkingen over injectie:
Injecteer langzaam, diep in het bovenste buitenste kwadrant van de bil.
Vanwege mogelijke hypotensieve effecten, dient parenterale toediening gereserveerd te worden voor bedlegerige patiënten of voor acute ambulante gevallen, en laat de patiënt ten minste 1/2 uur na injectie liggen. Als irritatie een probleem is, verdun de injectie dan met zoutoplossing of 2% procaïne; mengen met andere middelen in de spuit wordt niet aanbevolen. Subcutane injectie wordt afgeraden. Vermijd het injecteren van onverdunde Thorazine (chloorpromazine) in een ader. IV-route is alleen voor ernstige hik, chirurgie en tetanus.
Vermijd het krijgen van oplossing op handen of kleding vanwege de mogelijkheid van contactdermatitis. Deze oplossing moet worden beschermd tegen licht. Dit is een heldere, kleurloze tot lichtgele oplossing; een lichte gelige verkleuring zal de potentie niet veranderen. Als de oplossing duidelijk verkleurd is, moet deze worden weggegooid. Voor informatie over sulfietgevoeligheid, zie de: WAARSCHUWINGEN deel van deze etikettering.
Opmerking over concentraat: Wanneer het concentraat moet worden gebruikt, voeg dan vlak voor toediening de gewenste dosering concentraat toe aan 60 ml (2 fl oz) of meer verdunningsmiddel. Dit zorgt voor smakelijkheid en stabiliteit. Voertuigen die worden voorgesteld voor verdunning zijn: tomaten- of vruchtensap, melk, eenvoudige siroop, sinaasappelsiroop, koolzuurhoudende dranken, koffie, thee of water. Halfvaste voedingsmiddelen (soepen, puddingen, enz.) kunnen ook worden gebruikt. Het concentraat is lichtgevoelig; het moet worden beschermd tegen licht en worden verstrekt in amberkleurige glazen flessen. Koeling is niet nodig.
HOE GELEVERD
Tabletten: 10 mg, in flessen van 100; 25 mg of 50 mg, in flessen van 100 en 1000. Voor gebruik bij ernstige neuropsychiatrische aandoeningen, 100 mg en 200 mg, in flessen van 100 en 1000.
NDC 0007-5073-20 10 mg 100's NDC 0007-5074-20 25 mg 100's NDC 0007-5074-30 25 mg 1000's NDC 0007-5076-20 50 mg 100's NDC 0007-5076-30 50 mg 1000's NDC 0007-5077- 20 100 mg 100's NDC 0007-5077-30 100 mg 1000's NDC 0007-5079-20 200 mg 100's NDC 0007-5079-30 200 mg 1000's
Spansule®-capsules met aanhoudende afgifte: 30 mg, 75 mg of 150 mg, in flessen van 50.
NDC 0007-5063-15 30 mg jaren 50 NDC 0007-5064-15 75 mg jaren 50 NDC 0007-5066-15 150 mg jaren 50
Ampulsen: 1 ml en 2 ml (25 mg/ml), in dozen van 10.
NDC 0007-5060-11 25 mg/ml in ampullen van 1 ml (doos van 10) NDC 0007-5061-11 25 mg/ml in ampullen van 2 ml (doos van 10)
Injectieflacons met meerdere doses: 10 ml (25 mg/ml), in dozen van 1.
NDC 0007-5062-01 25 mg / ml in injectieflacons met meerdere doses van 10 ml (doos van 1)
Siroop: 10 mg/5 ml, in flessen van 4 fl oz.
NDC 0007-5072-44 10 mg/5 ml 4 fl oz
Zetpillen: 25 mg of 100 mg, in dozen van 12.
NDC 0007-5070-03 25 mg (doos van 12) NDC 0007-5071-03 100 mg (doos van 12)
Alle doseringsvormen behalve Siroop moeten worden bewaard tussen 15° en 30°C (59° en 86°F). Siroop moet beneden 25°C (77°F) worden bewaard.
*fenytoïne, Parke-Davis. metrizamide, Sanofi Winthrop Pharmaceuticals. ‡ noradrenalinebitartraat, Sanofi Winthrop Pharmaceuticals. §fenylefrinehydrochloride, Sanofi Winthrop Pharmaceuticals. ||difenhydraminehydrochloride, Parke-Davis.
WAARSCHUWING : Thorazine® (chloorpromazine) Spansule-capsules worden vervaardigd met tetrachloorkoolstof en methylchloroform, stoffen die de volksgezondheid en het milieu schaden door ozon in de bovenste atmosfeer te vernietigen.
FDA-revisiedatum: 22-4-1998. Fabrikantinformatie: nvt
BIJWERKINGEN
Opmerking: sommige bijwerkingen van Thorazine (chloorpromazine) kunnen waarschijnlijker optreden of met grotere intensiteit optreden bij patiënten met speciale medische problemen, bijv. Patiënten met mitralisinsufficiëntie of feochromocytoom hebben ernstige hypotensie ervaren na de aanbevolen doses.
Slaperigheid , gewoonlijk licht tot matig, kan optreden, vooral tijdens de eerste of tweede week, waarna het meestal verdwijnt. Als het lastig is, kan de dosering worden verlaagd.
B De totale incidentie was laag, ongeacht de indicatie of dosering. De meeste onderzoekers concluderen dat het een overgevoeligheidsreactie is. De meeste gevallen treden op tussen de tweede en vierde week van de therapie. Het klinische beeld lijkt op infectieuze hepatitis, met laboratoriumkenmerken van obstructieve geelzucht, in plaats van die van parenchymale schade. Het is meestal onmiddellijk omkeerbaar na het stoppen van de medicatie; er is echter chronische geelzucht gemeld.
Er is geen sluitend bewijs dat een reeds bestaande leverziekte patiënten vatbaarder maakt voor geelzucht. Alcoholisten met cirrose zijn met succes behandeld met Thorazine (chloorpromazine) zonder complicaties. Desalniettemin moet het medicijn met voorzichtigheid worden gebruikt bij patiënten met een leveraandoening. Patiënten die geelzucht hebben gehad met een fenothiazine mogen, indien mogelijk, niet opnieuw worden blootgesteld aan Thorazine (chloorpromazine) of andere fenothiazinen.
Als koorts met grippe-achtige symptomen optreedt, moeten geschikte leveronderzoeken worden uitgevoerd. Als tests wijzen op een afwijking, stop dan met de behandeling.
Leverfunctietests bij geelzucht veroorzaakt door het medicijn kunnen extrahepatische obstructie nabootsen; wacht met verkennende laparotomie totdat extrahepatische obstructie is bevestigd.
Hematologische aandoeningen , waaronder agranulocytose, eosinofilie, leukopenie, hemolytische anemie, aplastische anemie, trombocytopenische purpura en pancytopenie zijn gemeld.
Agranulocytose Waarschuw patiënten om het plotselinge optreden van keelpijn of andere tekenen van infectie te melden. Als witte bloedcellen en differentiële tellingen wijzen op cellulaire depressie, stop dan met de behandeling en start met antibiotica en andere geschikte therapie.
De meeste gevallen hebben zich voorgedaan tussen de vierde en tiende week van de therapie; patiënten moeten gedurende die periode nauwlettend in de gaten worden gehouden.
Matige onderdrukking van witte bloedcellen is geen indicatie om de behandeling te stoppen, tenzij deze gepaard gaat met de hierboven beschreven symptomen.
Cardiovasculair
Hypotensieve effecten — Posturale hypotensie, eenvoudige tachycardie, kortstondig flauwvallen en duizeligheid kunnen optreden na de eerste injectie; af en toe na volgende injecties; zelden, na de eerste orale dosis. Meestal is herstel spontaan en verdwijnen de symptomen binnen 1/2 tot 2 uur. Af en toe kunnen deze effecten ernstiger en langduriger zijn, waardoor een schokachtige toestand ontstaat.
Om hypotensie na injectie tot een minimum te beperken, moet u de patiënt laten liggen en gedurende ten minste 1/2 uur observeren. Om hypotensie onder controle te houden, plaatst u de patiënt in een hoofd-lage positie met de benen omhoog. Als een vasoconstrictor nodig is, zijn Levophed® *** en Neo-Synephrine® § het meest geschikt. Andere bloeddrukverlagende middelen, waaronder epinefrine, mogen niet worden gebruikt omdat ze een paradoxale verdere verlaging van de bloeddruk kunnen veroorzaken.
ECG-wijzigingen - met name niet-specifieke, meestal reversibele Q- en T-golfverstoringen - zijn waargenomen bij sommige patiënten die fenothiazine-remmers kregen, waaronder Thorazine (chloorpromazine).
Opmerking: Plotselinge dood, blijkbaar als gevolg van een hartstilstand, is gemeld.
CNS-reacties
Neuromusculaire (extrapiramidale) reacties — Neuromusculaire reacties omvatten dystonieën, motorische rusteloosheid, pseudoparkinsonisme en tardieve dyskinesie, en lijken dosisgerelateerd te zijn. Ze worden besproken in de volgende paragrafen:
Dystonieën Symptomen kunnen zijn: spasmen van de nekspieren, die soms overgaan in acute, reversibele torticollis; strekstijfheid van de rugspieren, soms evoluerend naar opisthotonos; carpopedale spasmen, trismus, slikproblemen, oogcrisis en uitsteeksel van de tong.

Deze verdwijnen meestal binnen een paar uur en bijna altijd binnen 24 tot 48 uur nadat het medicijn is stopgezet.
In milde gevallen is geruststelling of een barbituraat vaak voldoende. In gematigde gevallen zullen barbituraten meestal snel verlichting brengen. In ernstigere gevallen bij volwassenen leidt de toediening van een middel tegen parkinsonisme, behalve levodopa, gewoonlijk tot een snelle omkering van de symptomen. Bij kinderen (1 tot 12 jaar) zullen geruststelling en barbituraten de symptomen gewoonlijk onder controle houden. (Of parenteraal Benadryl® ll kan nuttig zijn. Zie de voorschrijfinformatie van Benadryl voor de juiste dosering voor kinderen.) Als een geschikte behandeling met antiparkinsonmiddelen of Benadryl de tekenen en symptomen niet omkeert, moet de diagnose opnieuw worden beoordeeld.
Indien nodig moeten passende ondersteunende maatregelen worden genomen, zoals het vrijhouden van de luchtwegen en voldoende hydratatie. Als de therapie opnieuw wordt ingesteld, moet deze in een lagere dosering plaatsvinden. Als deze symptomen optreden bij kinderen of zwangere patiënten, mag het geneesmiddel niet opnieuw worden ingesteld.
Motorische rusteloosheid: Symptomen kunnen zijn: agitatie of zenuwachtigheid en soms slapeloosheid. Deze symptomen verdwijnen vaak spontaan. Soms kunnen deze symptomen lijken op de oorspronkelijke neurotische of psychotische symptomen. De dosering mag niet worden verhoogd totdat deze bijwerkingen zijn verdwenen.
Als deze symptomen te lastig worden, kunnen ze meestal onder controle worden gehouden door een verlaging van de dosering of een verandering van het medicijn. Behandeling met antiparkinsonmiddelen, benzodiazepinen of propranolol kan nuttig zijn.
Pseudo-parkinsonisme: Symptomen kunnen zijn: maskerachtig gelaat, kwijlen, trillen, rollende beweging, tandradstijfheid en schuifelend lopen. In de meeste gevallen zijn deze symptomen gemakkelijk onder controle te krijgen wanneer gelijktijdig een middel tegen parkinsonisme wordt toegediend. Middelen tegen parkinsonisme mogen alleen worden gebruikt als dat nodig is. Over het algemeen is een therapie van enkele weken tot 2 of 3 maanden voldoende. Na deze tijd moeten patiënten worden geëvalueerd om te bepalen of zij de behandeling moeten voortzetten. (Opmerking: Levodopa is niet effectief gebleken bij door antipsychotica geïnduceerd pseudoparkinsonisme.) Af en toe is het nodig om de dosering van Thorazine (chloorpromazine) te verlagen of het medicijn te staken.
Tardieve dyskinesie: Zoals met alle antipsychotica kan tardieve dyskinesie optreden bij sommige patiënten die langdurig worden behandeld of optreden nadat de medicamenteuze behandeling is stopgezet. Het syndroom kan zich ook ontwikkelen, hoewel veel minder vaak, na relatief korte behandelingsperioden met lage doses. Dit syndroom komt voor in alle leeftijdsgroepen. Hoewel de prevalentie ervan het hoogst lijkt te zijn bij oudere patiënten, met name oudere vrouwen, is het onmogelijk om te vertrouwen op prevalentieschattingen om bij aanvang van de antipsychotische behandeling te voorspellen welke patiënten het syndroom waarschijnlijk zullen ontwikkelen. De symptomen zijn aanhoudend en bij sommige patiënten lijken ze onomkeerbaar. Het syndroom wordt gekenmerkt door ritmische onwillekeurige bewegingen van de tong, het gezicht, de mond of de kaak (bijv. uitpuilende tong, puffende wangen, tuiten van de mond, kauwbewegingen). Soms kunnen deze gepaard gaan met onwillekeurige bewegingen van ledematen. In zeldzame gevallen zijn deze onwillekeurige bewegingen van de extremiteiten de enige manifestaties van tardieve dyskinesie. Een variant van tardieve dyskinesie, tardieve dystonie, is ook beschreven.
Er is geen effectieve behandeling bekend voor tardieve dyskinesie; middelen tegen parkinsonisme verlichten de symptomen van dit syndroom niet. Indien klinisch haalbaar, wordt aangeraden om alle antipsychotica stop te zetten als deze symptomen optreden. Mocht het nodig zijn de behandeling te hervatten, de dosering van het middel te verhogen of over te schakelen op een ander antipsychoticum, dan kan het syndroom worden gemaskeerd.
Er is gemeld dat fijne vermiculaire bewegingen van de tong een vroeg teken van het syndroom kunnen zijn en dat als de medicatie op dat moment wordt gestopt, het syndroom zich mogelijk niet ontwikkelt.
Nadelige gedragseffecten - Psychotische symptomen en catatonische toestanden zijn zelden gemeld.
Andere CZS-effecten — Maligne neurolepticasyndroom (MNS) is gemeld in verband met antipsychotica. (Zien WAARSCHUWINGEN .) Hersenoedeem is gemeld.
Convulsieve aanvallen (petit mal en grand mal) zijn gemeld, vooral bij patiënten met EEG-afwijkingen of een voorgeschiedenis van dergelijke aandoeningen.
Afwijkingen van de cerebrospinale vloeistofeiwitten zijn ook gemeld.
Allergische reacties van een mild urticaria-type of lichtgevoeligheid worden waargenomen. Vermijd overmatige blootstelling aan de zon. Ernstigere reacties, waaronder exfoliatieve dermatitis, zijn af en toe gemeld.
Contactdermatitis is gemeld bij verplegend personeel; daarom wordt het gebruik van rubberen handschoenen aanbevolen bij het toedienen van Thorazine (chloorpromazine) vloeistof of injecteerbaar.
Daarnaast zijn astma, larynxoedeem, angioneurotisch oedeem en anafylactoïde reacties gemeld.
Endocriene aandoeningen Borstvoeding en matige stuwing van de borsten kunnen optreden bij vrouwen bij hoge doses. Indien aanhoudend, de dosering verlagen of het medicijn stopzetten. Er zijn fout-positieve zwangerschapstesten gemeld, maar deze treden minder vaak op bij gebruik van een serumtest. Amenorroe en gynaecomastie zijn ook gemeld. Hyperglykemie, hypoglykemie en glycosurie zijn gemeld.
Autonome reacties : Af en toe een droge mond; verstopte neus; misselijkheid; obstipatie; constipatie; adynamische ileus; urineretentie; priapisme; miosis en mydriasis, atonische colon, ejaculatiestoornissen/impotentie.
Speciale overwegingen bij langdurige therapie: Huidpigmentatie en oculaire veranderingen zijn opgetreden bij sommige patiënten die gedurende langere perioden substantiële doses Thorazine (chloorpromazine) gebruikten.
Huidpigmentatie Zeldzame gevallen van huidpigmentatie zijn waargenomen bij gehospitaliseerde psychiatrische patiënten, voornamelijk vrouwen die het geneesmiddel gewoonlijk gedurende 3 jaar of langer hebben gekregen in doseringen variërend van 500 mg tot 1500 mg per dag. De pigmentveranderingen, beperkt tot blootgestelde delen van het lichaam, variëren van een bijna onmerkbare verdonkering van de huid tot een leisteengrijze kleur, soms met een violette tint. Histologisch onderzoek onthult een pigment, voornamelijk in de dermis, dat waarschijnlijk een melanine-achtig complex is. De pigmentatie kan vervagen na stopzetting van het medicijn.
Oculaire veranderingen Oculaire veranderingen zijn vaker voorgekomen dan huidpigmentatie en zijn waargenomen bij zowel gepigmenteerde als niet-gepigmenteerde patiënten die Thorazine (chloorpromazine) kregen, gewoonlijk gedurende 2 jaar of langer in doseringen van 300 mg per dag en hoger. Oogveranderingen worden gekenmerkt door afzetting van fijne deeltjes in de lens en het hoornvlies. In meer gevorderde gevallen zijn ook stervormige opaciteiten waargenomen in het voorste deel van de lens. De aard van de oogafzettingen is nog niet vastgesteld. Een klein aantal patiënten met ernstige oculaire veranderingen had een visuele beperking. Naast deze cornea- en lenticulaire veranderingen zijn epitheliale keratopathie en pigmentaire retinopathie gemeld. Rapporten suggereren dat de ooglaesies kunnen afnemen na het stoppen met het medicijn.
Aangezien het optreden van oogveranderingen verband lijkt te houden met de doseringsniveaus en/of de duur van de therapie, wordt gesuggereerd dat langdurige patiënten met matige tot hoge doseringen periodieke oogonderzoeken ondergaan.
Etiologie — De etiologie van beide reacties is niet duidelijk, maar blootstelling aan licht, samen met dosering/duur van de therapie, lijkt de belangrijkste factor te zijn. Als een van deze reacties wordt waargenomen, moet de arts de voordelen van voortzetting van de therapie afwegen tegen de mogelijke risico's en, op basis van het individuele geval, bepalen of de huidige therapie moet worden voortgezet, de dosering moet worden verlaagd of het geneesmiddel moet worden stopgezet.
Andere bijwerkingen: Lichte koorts kan optreden na grote IM-doses. Hyperpyrexie is gemeld. Toename van eetlust en gewicht komen soms voor. Perifeer oedeem en een systemisch lupus erythematosus-achtig syndroom zijn gemeld.
Opmerking: er zijn af en toe meldingen geweest van plotseling overlijden bij patiënten die fenothiazinen kregen. In sommige gevallen bleek de oorzaak een hartstilstand of verstikking te zijn door het uitvallen van de hoestreflex.
DRUG-INTERACTIES
Geen informatie verstrekt.
WAARSCHUWINGEN
De extrapiramidale symptomen die secundair aan Thorazine (chloorpromazine) kunnen optreden, kunnen worden verward met de tekenen van het centrale zenuwstelsel van een niet-gediagnosticeerde primaire ziekte die verantwoordelijk is voor het braken, bijvoorbeeld het syndroom van Reye of andere encefalopathie. Het gebruik van Thorazine (chloorpromazine) en andere mogelijke hepatotoxinen moet worden vermeden bij kinderen en adolescenten van wie de tekenen en symptomen wijzen op het syndroom van Reye.
Tardieve dyskinesie: Tardieve dyskinesie, een syndroom dat bestaat uit mogelijk onomkeerbare, onwillekeurige, dyskinetische bewegingen, kan optreden bij patiënten die worden behandeld met antipsychotica. Hoewel de prevalentie van het syndroom het hoogst lijkt te zijn bij ouderen, vooral bij oudere vrouwen, is het onmogelijk om te vertrouwen op prevalentieschattingen om bij aanvang van de antipsychotische behandeling te voorspellen welke patiënten het syndroom waarschijnlijk zullen ontwikkelen. Of antipsychotica verschillen in hun potentieel om tardieve dyskinesie te veroorzaken, is niet bekend.
Aangenomen wordt dat zowel het risico op het ontwikkelen van het syndroom als de kans dat het onomkeerbaar wordt, toeneemt naarmate de duur van de behandeling en de totale cumulatieve dosis antipsychotica die aan de patiënt worden toegediend, toenemen. Het syndroom kan zich echter ontwikkelen, hoewel veel minder vaak, na relatief korte behandelingsperioden met lage doses.
Er is geen behandeling bekend voor vastgestelde gevallen van tardieve dyskinesie, hoewel het syndroom gedeeltelijk of volledig kan verdwijnen als de behandeling met antipsychotica wordt stopgezet. Behandeling met antipsychotica zelf kan echter de tekenen en symptomen van het syndroom onderdrukken (of gedeeltelijk) en kan daardoor mogelijk het onderliggende ziekteproces maskeren. Het effect dat symptomatische onderdrukking heeft op het lange termijn beloop van het syndroom is onbekend.
Gezien deze overwegingen moeten antipsychotica zo worden voorgeschreven dat de kans op tardieve dyskinesie het grootst is. Chronische behandeling met antipsychotica dient in het algemeen te worden voorbehouden aan patiënten die lijden aan een chronische ziekte waarvan, 1) bekend is dat ze reageren op antipsychotica, en 2) voor wie alternatieve, even effectieve, maar mogelijk minder schadelijke behandelingen niet beschikbaar of geschikt zijn. Bij patiënten die wel een chronische behandeling nodig hebben, moet worden gestreefd naar de kleinste dosis en de kortste behandelingsduur die een bevredigende klinische respons oplevert. De noodzaak van voortzetting van de behandeling moet periodiek opnieuw worden beoordeeld.
Als er tekenen en symptomen van tardieve dyskinesie optreden bij een patiënt die antipsychotica gebruikt, dient te worden overwogen het gebruik van het geneesmiddel te staken. Sommige patiënten kunnen echter behandeling nodig hebben ondanks de aanwezigheid van het syndroom.
Voor meer informatie over de beschrijving van tardieve dyskinesie en de klinische detectie ervan, verwijzen wij u naar de secties over: PREVENTIEVE MAATREGELEN en ONGEWENSTE REACTIES .
Maligne neurolepticasyndroom (MNS): Een potentieel fataal symptoomcomplex dat soms wordt aangeduid als maligne neurolepticasyndroom (MNS) is gemeld in verband met antipsychotica. Klinische manifestaties van MNS zijn hyperpyrexie, spierstijfheid, veranderde mentale toestand en tekenen van autonome instabiliteit (onregelmatige pols of bloeddruk, tachycardie, diaforese en hartritmestoornissen).
De diagnostische evaluatie van patiënten met dit syndroom is gecompliceerd. Om tot een diagnose te komen, is het belangrijk om gevallen te identificeren waarin de klinische presentatie zowel een ernstige medische aandoening (bijv. longontsteking, systemische infectie, enz.) als onbehandelde of onvoldoende behandelde extrapiramidale tekenen en symptomen (EPS) omvat. Andere belangrijke overwegingen bij de differentiële diagnose zijn centrale anticholinerge toxiciteit, hitteberoerte, medicijnkoorts en primaire pathologie van het centrale zenuwstelsel (CZS).
De behandeling van MNS dient te omvatten 1) onmiddellijke stopzetting van antipsychotica en andere geneesmiddelen die niet essentieel zijn voor gelijktijdige therapie, 2) intensieve symptomatische behandeling en medische controle, en 3) behandeling van alle bijkomende ernstige medische problemen waarvoor specifieke behandelingen beschikbaar zijn. Er is geen algemene overeenstemming over specifieke farmacologische behandelingsregimes voor ongecompliceerde MNS.
Als een patiënt behandeling met antipsychotica nodig heeft na herstel van MNS, moet de mogelijke herintroductie van medicamenteuze therapie zorgvuldig worden overwogen. De patiënt moet zorgvuldig worden gecontroleerd, aangezien recidieven van MNS zijn gemeld.
Een encefalopathisch syndroom (gekenmerkt door zwakte, lethargie, koorts, trillen en verwardheid, extrapiramidale symptomen, leukocytose, verhoogde serumenzymen, BUN en FBS) is opgetreden bij enkele patiënten die werden behandeld met lithium plus een antipsychoticum. In sommige gevallen werd het syndroom gevolgd door onomkeerbare hersenbeschadiging. Vanwege een mogelijk causaal verband tussen deze gebeurtenissen en de gelijktijdige toediening van lithium en antipsychotica, moeten patiënten die een dergelijke combinatietherapie krijgen, nauwlettend worden gecontroleerd op vroege tekenen van neurologische toxiciteit en de behandeling moet onmiddellijk worden stopgezet als dergelijke symptomen optreden. Dit encefalopathisch syndroom kan vergelijkbaar zijn met of hetzelfde zijn als het maligne neurolepticasyndroom (MNS).
Thorazine (chloorpromazine) ampullen en flacons met meerdere doses bevatten natriumbisulfiet en natriumsulfiet, sulfieten die allergische reacties kunnen veroorzaken, waaronder anafylactische symptomen en levensbedreigende of minder ernstige astmatische episodes bij bepaalde gevoelige personen. De algemene prevalentie van sulfietgevoeligheid in de algemene bevolking is onbekend en waarschijnlijk laag. Sulfietgevoeligheid wordt vaker gezien bij astmatische dan bij niet-astmatische mensen.
Patiënten met beenmergdepressie of die eerder een overgevoeligheidsreactie hebben vertoond (bijv. bloeddyscrasieën, geelzucht) met een fenothiazine mogen geen fenothiazine krijgen, inclusief Thorazine (chloorpromazine), tenzij naar het oordeel van de arts de mogelijke voordelen van de behandeling opwegen tegen de mogelijk gevaar.
Thorazine (chloorpromazine) kan de mentale en/of fysieke vermogens aantasten, vooral tijdens de eerste paar dagen van de behandeling. Waarschuw patiënten daarom voor activiteiten die alertheid vereisen (bijv. het bedienen van voertuigen of machines).
Het gebruik van alcohol met dit medicijn moet worden vermeden vanwege mogelijke additieve effecten en hypotensie. Thorazine (chloorpromazine) kan het antihypertensieve effect van guanethidine en verwante verbindingen tegengaan.
Gebruik tijdens de zwangerschap: De veiligheid voor het gebruik van Thorazine (chloorpromazine) tijdens de zwangerschap is niet vastgesteld. Daarom wordt het niet aanbevolen om het medicijn aan zwangere patiënten te geven, behalve wanneer het, naar het oordeel van de arts, essentieel is. De potentiële voordelen moeten duidelijk opwegen tegen de mogelijke gevaren. Er zijn gevallen gemeld van langdurige geelzucht, extrapiramidale verschijnselen, hyperreflexie of hyporeflexie bij pasgeboren baby's van wie de moeder fenothiazinen kreeg.
Reproductiestudies bij knaagdieren hebben potentieel voor embryotoxiciteit, verhoogde neonatale mortaliteit en overdracht van het geneesmiddel door borstvoeding aangetoond. Tests bij de nakomelingen van de met geneesmiddel behandelde knaagdieren tonen verminderde prestaties aan. De mogelijkheid van blijvende neurologische schade kan niet worden uitgesloten.
Moeders die borstvoeding geven: Er zijn aanwijzingen dat chloorpromazine wordt uitgescheiden in de moedermelk van moeders die borstvoeding geven. Vanwege het potentieel voor ernstige bijwerkingen van chloorpromazine bij zuigelingen, moet worden besloten of de borstvoeding moet worden gestaakt of dat het geneesmiddel moet worden gestaakt, rekening houdend met het belang van het geneesmiddel voor de moeder.
PREVENTIEVE MAATREGELEN
Algemeen
Gezien de waarschijnlijkheid dat sommige patiënten die chronisch aan antipsychotica worden blootgesteld, tardieve dyskinesie zullen ontwikkelen, wordt geadviseerd alle patiënten bij wie chronisch gebruik wordt overwogen, indien mogelijk, volledige informatie over dit risico te krijgen. Bij de beslissing om patiënten en/of hun voogden te informeren, moet uiteraard rekening worden gehouden met de klinische omstandigheden en de competentie van de patiënt om de verstrekte informatie te begrijpen.
Thorazine (chloorpromazine) moet met voorzichtigheid worden toegediend aan personen met cardiovasculaire, lever- of nieraandoeningen. Er zijn aanwijzingen dat patiënten met een voorgeschiedenis van hepatische encefalopathie als gevolg van cirrose een verhoogde gevoeligheid hebben voor de CZS-effecten van Thorazine (chloorpromazine) (dwz verminderde cerebratie en abnormale vertraging van het EEG).
Vanwege het CZS-onderdrukkende effect moet Thorazine (chloorpromazine) met voorzichtigheid worden gebruikt bij patiënten met chronische luchtwegaandoeningen zoals ernstige astma, emfyseem en acute luchtweginfecties, vooral bij kinderen (1 tot 12 jaar).
Omdat Thorazine (chloorpromazine) de hoestreflex kan onderdrukken, is aspiratie van braaksel mogelijk.
Thorazine (chloorpromazine) verlengt en intensiveert de werking van CZS-depressiva zoals anesthetica, barbituraten en narcotica. Wanneer Thorazine (chloorpromazine) gelijktijdig wordt toegediend, is ongeveer 1/4 tot 1/2 van de gebruikelijke dosering van dergelijke middelen vereist. Wanneer Thorazine (chloorpromazine) niet wordt toegediend om de behoefte aan CZS-depressiva te verminderen, is het het beste om dergelijke depressiva te stoppen voordat de behandeling met Thorazine (chloorpromazine) wordt gestart. Deze middelen kunnen vervolgens worden hersteld in lage doses en indien nodig worden verhoogd.
Opmerking: Thorazine (chloorpromazine) versterkt de anticonvulsieve werking van barbituraten niet. Daarom mag de dosering van anticonvulsiva, inclusief barbituraten, niet worden verlaagd als Thorazine (chloorpromazine) wordt gestart. Start in plaats daarvan Thorazine (chloorpromazine) in lage doses en verhoog indien nodig.
Wees voorzichtig bij personen die worden blootgesteld aan extreme hitte, organofosforinsecticiden en bij personen die atropine of verwante geneesmiddelen krijgen.
Antipsychotica verhogen de prolactinespiegels; de verhoging houdt aan tijdens chronische toediening. Weefselkweekexperimenten geven aan dat ongeveer 1/3 van de menselijke borstkankers in vitro prolactine-afhankelijk is, een factor van potentieel belang als het voorschrijven van deze geneesmiddelen wordt overwogen bij een patiënt met een eerder gedetecteerde borstkanker. Hoewel stoornissen zoals galactorroe, amenorroe, gynaecomastie en impotentie zijn gemeld, is de klinische betekenis van verhoogde serumprolactinespiegels voor de meeste patiënten onbekend. Een toename van borstneoplasmata is gevonden bij knaagdieren na chronische toediening van antipsychotica. Noch klinische noch epidemiologische studies die tot nu toe zijn uitgevoerd, hebben echter een verband aangetoond tussen chronische toediening van deze geneesmiddelen en borsttumorvorming; het beschikbare bewijs wordt op dit moment te beperkt geacht om sluitend te zijn.
Chromosomale afwijkingen in spermatocyten en abnormaal sperma zijn aangetoond bij knaagdieren die werden behandeld met bepaalde antipsychotica.
Zoals met alle geneesmiddelen die een anticholinergisch effect uitoefenen en/of mydriasis veroorzaken, dient chloorpromazine met voorzichtigheid te worden gebruikt bij patiënten met glaucoom.
Chloorpromazine vermindert het effect van orale anticoagulantia.
Fenothiazinen kunnen alfa-adrenerge blokkades veroorzaken.
Chloorpromazine kan de convulsieve drempel verlagen; dosisaanpassingen van anti-epileptica kunnen nodig zijn. Versterking van de anticonvulsieve effecten treedt niet op. Er is echter gemeld dat chloorpromazine het metabolisme van Dilantin® * kan verstoren en zo de toxiciteit van Dilantin kan versnellen.
Gelijktijdige toediening met propranolol resulteert in verhoogde plasmaspiegels van beide geneesmiddelen.
Thiazidediuretica kunnen de orthostatische hypotensie die kan optreden bij fenothiazinen, versterken.
De aanwezigheid van fenothiazinen kan vals-positieve testresultaten voor fenylketonurie (PKU) opleveren.
Geneesmiddelen die de aanvalsdrempel verlagen, waaronder fenothiazinederivaten, mogen niet worden gebruikt met Amipaque®†. Zoals met andere fenothiazinederivaten, moet Thorazine (chloorpromazine) ten minste 48 uur vóór myelografie worden stopgezet, mag het niet worden hervat gedurende ten minste 24 uur na de procedure en mag het niet worden gebruikt voor de controle van misselijkheid en braken die optreden vóór myelografie of postprocedure met Amipak.
Langdurige therapie: Om de kans op bijwerkingen gerelateerd aan het cumulatieve geneesmiddeleffect te verkleinen, moeten patiënten met een voorgeschiedenis van langdurige therapie met Thorazine (chloorpromazine) en / of andere antipsychotica periodiek worden geëvalueerd om te beslissen of de onderhoudsdosering kan worden verlaagd of de medicamenteuze behandeling kan worden stopgezet.
Anti-emetisch effect: De anti-emetische werking van Thorazine (chloorpromazine) kan de tekenen en symptomen van overdosering van andere geneesmiddelen maskeren en kan de diagnose en behandeling van andere aandoeningen zoals darmobstructie, hersentumor en het syndroom van Reye verdoezelen. (Zien WAARSCHUWINGEN .)
Wanneer Thorazine (chloorpromazine) wordt gebruikt met chemotherapeutische geneesmiddelen tegen kanker, kan braken als teken van de toxiciteit van deze middelen worden verdoezeld door het anti-emetische effect van Thorazine (chloorpromazine).
Abrupte terugtrekking: Net als andere fenothiazinen is het niet bekend dat Thorazine (chloorpromazine) psychische afhankelijkheid veroorzaakt en veroorzaakt het geen tolerantie of verslaving. Na abrupt staken van de behandeling met hoge doses kunnen echter symptomen optreden die lijken op lichamelijke afhankelijkheid, zoals gastritis, misselijkheid en braken, duizeligheid en trillen. Deze symptomen kunnen gewoonlijk worden vermeden of verminderd door geleidelijke verlaging van de dosering of door gelijktijdig gebruik van antiparkinsonmiddelen gedurende enkele weken nadat Thorazine (chloorpromazine) is stopgezet.
OVERDOSERING
(Zie ook ONGEWENSTE REACTIES .)
SYMPTOMEN— Voornamelijk symptomen van depressie van het centrale zenuwstelsel tot slaperigheid of coma toe. Hypotensie en extrapiramidale symptomen.
Andere mogelijke verschijnselen zijn agitatie en rusteloosheid, convulsies, koorts, autonome reacties zoals droge mond en ileus, ECG-veranderingen en hartritmestoornissen.
BEHANDELING— Het is belangrijk om vast te stellen welke andere medicijnen de patiënt neemt, aangezien meervoudige medicamenteuze behandeling gebruikelijk is in situaties van overdosering. De behandeling is in wezen symptomatisch en ondersteunend. Vroege maagspoeling is nuttig. Houd de patiënt onder observatie en houd de luchtwegen open, aangezien betrokkenheid van het extrapiramidale mechanisme bij ernstige overdosering dysfagie en ademhalingsmoeilijkheden kan veroorzaken. Probeer geen braken op te wekken omdat zich een dystonische reactie van het hoofd of de nek kan ontwikkelen die kan leiden tot aspiratie van braaksel. Extrapiramidale symptomen kunnen worden behandeld met geneesmiddelen tegen parkinsonisme, barbituraten of Benadryl. Zie voorschrijfinformatie voor deze producten. Voorzichtigheid is geboden om toenemende ademhalingsdepressie te voorkomen.
Als toediening van een stimulerend middel wenselijk is, wordt amfetamine, dextroamfetamine of cafeïne met natriumbenzoaat aanbevolen. Stimulerende middelen die convulsies kunnen veroorzaken (bijv. picrotoxine of pentyleentetrazol) moeten worden vermeden.
Als hypotensie optreedt, moeten de standaardmaatregelen voor het beheersen van circulatoire shock worden gestart. Als het wenselijk is om een vasoconstrictor toe te dienen, zijn Levophed en Neo-Synephrine het meest geschikt. Andere bloeddrukverhogende middelen, waaronder epinefrine, worden niet aanbevolen omdat fenothiazinederivaten de gebruikelijke verhogende werking van deze middelen kunnen omkeren en een verdere verlaging van de bloeddruk kunnen veroorzaken.
Beperkte ervaring geeft aan dat fenothiazinen niet dialyseerbaar zijn.
Speciale opmerking over Spansule®-capsules - Aangezien een groot deel van de medicatie van de Spansule-capsule is gecoat voor geleidelijke afgifte, moet de therapie die gericht is op het omkeren van de effecten van het ingenomen geneesmiddel en op het ondersteunen van de patiënt worden voortgezet zolang de symptomen van overdosering aanhouden. Kathartica met zoutoplossing zijn nuttig voor het versnellen van de evacuatie van pellets die nog geen medicatie hebben afgegeven.
CONTRA-INDICATIES
Niet gebruiken bij patiënten met een bekende overgevoeligheid voor fenothiazinen.
Niet gebruiken in comateuze toestand of in aanwezigheid van grote hoeveelheden middelen die het centrale zenuwstelsel onderdrukken (alcohol, barbituraten, verdovende middelen, enz.).
KLINISCHE FARMACOLOGIE
ACTIES
Het precieze mechanisme waardoor de therapeutische effecten van chloorpromazine worden geproduceerd, is niet bekend. De belangrijkste farmacologische acties zijn psychotroop. Het oefent ook een kalmerende en anti-emetische activiteit uit.
Chloorpromazine werkt op alle niveaus van het centrale zenuwstelsel, voornamelijk op subcorticale niveaus, evenals op meerdere orgaansystemen. Chloorpromazine heeft een sterke anti-adrenerge en zwakkere perifere anticholinerge activiteit; ganglionblokkering is relatief gering. Het bezit ook een lichte antihistaminische en antiserotonine-activiteit.
PATIËNT INFORMATIE
Geen informatie verstrekt. Raadpleeg de WAARSCHUWINGEN en PREVENTIEVE MAATREGELEN secties.
