Mellaril 10mg, 25mg, 50mg, 100mg Thioridazine Gebruik, bijwerkingen en dosering. Prijs in online apotheek. Generieke medicijnen zonder recept.
Wat is Mellaril Topper en hoe wordt het gebruikt?
Mellaril Topper is een receptgeneesmiddel dat wordt gebruikt om de symptomen van schizofrenie en depressieve stoornissen te behandelen. Mellaril 25 mg Topper kan alleen of in combinatie met andere medicijnen worden gebruikt.
- Mellaril 50 mg Topper behoort tot een klasse geneesmiddelen die antipsychotica, fenothiazine, wordt genoemd.
- Het is niet bekend of Mellaril Topper veilig en effectief is bij kinderen jonger dan 2 jaar.
Wat zijn de mogelijke bijwerkingen van Mellaril Topper?
Mellaril 100 mg Topper kan ernstige bijwerkingen veroorzaken, waaronder:
- netelroos,
- moeite met ademhalen,
- zwelling van uw gezicht, lippen, tong of keel,
- ongecontroleerde spierbewegingen in uw armen, benen of gezicht (kauwen, smakken op de lippen, fronsende tongbeweging, knipperen of oogbeweging),
- snelle of bonzende hartslagen,
- fladderend in je borst,
- kortademigheid,
- plotselinge duizeligheid,
- agitatie,
- verwardheid,
- hartinfarct,
- verminderd nachtzicht,
- tunnelvisie,
- waterige ogen,
- verhoogde gevoeligheid voor licht,
- weinig of niet plassen,
- koorts,
- rillingen,
- zweertjes in de mond,
- huidzweren,
- keelpijn,
- hoesten,
- duizeligheid,
- zeer stijve (starre) spieren,
- hoge koorts,
- zweten, en
- trillingen
Roep meteen medische hulp in als u een van de bovenstaande symptomen heeft.
De meest voorkomende bijwerkingen van Mellaril Topper zijn:
- slaperigheid,
- droge mond,
- wazig zien,
- misselijkheid,
- braken,
- constipatie,
- diarree,
- zwelling van de borst of afscheiding,
- veranderingen in uw menstruatie, en
- zwelling in uw handen of voeten
Vertel het uw arts als u een bijwerking heeft die u hindert of die niet weggaat.
Dit zijn niet alle mogelijke bijwerkingen van Mellaril 10mg Topper. Vraag uw arts of apotheker om meer informatie.
Bel uw arts voor medisch advies over bijwerkingen. U kunt bijwerkingen melden aan de FDA op 1-800-FDA-1088.
WAARSCHUWING
MELLARIL® (THIORIDAZINE HCl) IS GETOOND OM HET QTc-INTERVAL OP DOSISGERELATEERDE WIJZE TE VERLENGEN, EN DRUGS MET DIT POTENTIEEL, INCLUSIEF MELLARIL (thioridazine hcl), ZIJN IN VERBAND MET TORSADE DE POINTES-TYPE ARRHYTHMIAS EN DRUGS-TYPE ARRHYTHMIAS. DOOR ZIJN POTENTIEEL VOOR AANZIENLIJKE, MOGELIJK LEVENSbedreigende, PRO-ARITMISCHE EFFECTEN, MOET MELLARIL (thioridazine hcl) WORDEN GERESERVEERD VOOR GEBRUIK BIJ DE BEHANDELING VAN SCHIZOFRENIE PATINTEN DIE GEEN AANVAARDBARE ANTWOORDEN KUNNEN TONEN. VAN ONVOLDOENDE DOELTREFFENDHEID OF HET ONVERMOGEN OM EEN EFFECTIEVE DOSIS TE BEREIKEN DOOR ONDRAAGBARE BIJWERKINGEN VAN DIE DRUGS. (ZIEN WAARSCHUWINGEN, CONTRA-INDICATIES, EN INDICATIES ).
OMSCHRIJVING
Mellaril® (thioridazine HCl) is 2-methylmercapto-10-[2-(N-methyl-2-piperidyl)ethyl]fenothiazine.
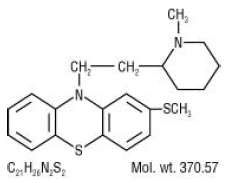
10 mg, 15 mg, 25 mg, 50 mg, 100 mg, 150 mg en 200 mg tabletten
Actief ingrediënt: thioridazine HCl, USP
10 mg-tabletten
Inactieve ingredienten: acacia, calciumsulfaatdihydraat, carnaubawas, D&C Yellow #10, FD&C Blue #1, FD&C Yellow #6, gelatine, lactose, methylparaben, povidon, propylparaben, natriumbenzoaat, zetmeel, stearinezuur, sucrose, synthetisch zwart ijzeroxide, talk , titaniumdioxide en andere ingrediënten.
15 mg tabletten
Inactieve ingredienten: acacia, calciumsulfaatdihydraat, carnaubawas, D&C Red #7, gelatine, lactose, methylparaben, povidon, propylparaben, zetmeel, stearinezuur, sucrose, synthetisch zwart ijzeroxide, talk, titaniumdioxide en andere ingrediënten.
25 mg tabletten
Inactieve ingredienten: acacia, calciumsulfaatdihydraat, carnaubawas, gelatine, lactose, methylparaben, povidon, propylparaben, natriumbenzoaat, zetmeel, stearinezuur, sucrose, synthetisch zwart ijzeroxide, synthetisch ijzeroxide, talk, titaniumdioxide en andere ingrediënten.
50 mg tabletten
Inactieve ingredienten: acacia, calciumsulfaatdihydraat, carnaubawas, gelatine, lactose, natriumbenzoaat, zetmeel, stearinezuur, sucrose, synthetisch zwart ijzeroxide, talk, titaniumdioxide en andere ingrediënten.
100 mg tabletten
Inactieve ingredienten: acacia, calciumsulfaatdihydraat, carnaubawas, D&C Yellow #10, FD&C Blue #1, FD&C Blue #2, FD&C Yellow #6, lactose, methylparaben, povidon, propylparaben, natriumbenzoaat, sorbitol, zetmeel, stearinezuur, sucrose, synthetisch zwart ijzeroxide, talk, titaniumdioxide en andere ingrediënten.
150 mg tabletten
Inactieve ingredienten: acacia, calciumsulfaatdihydraat, carnaubawas, D&C Geel #10, FD&C Groen #3, FD&C Geel #6, lactose, methylparaben, povidon, propylparaben, natriumbenzoaat, zetmeel, stearinezuur, sucrose, synthetisch zwart ijzeroxide, talk, titanium dioxide en andere ingrediënten.
200 mg tabletten
Inactieve ingredienten: acacia, ammoniumcalciumalginaat, calciumsulfaatdihydraat, carnaubawas, colloïdaal siliciumdioxide, D&C Red #7, lactose, magnesiumstearaat, methylparaben, povidon, propylparaben, natriumbenzoaat, zetmeel, stearinezuur, sucrose, synthetisch zwart ijzeroxide, talk, titaniumdioxide en andere ingrediënten.
30 mg/ml en 100 mg/ml drank (concentraat)
Actief ingrediënt: thioridazine HCl, USP
30 mg/ml orale oplossing (concentraat)
Inactieve ingredienten: alcohol, 3,0%, smaakstof, methylparaben, propylparaben, gezuiverd water en sorbitoloplossing. Kan natriumhydroxide of zoutzuur bevatten om de pH aan te passen.
100 mg/ml orale oplossing (concentraat)
Inactieve ingredienten: alcohol, 4,2%, aroma, glycerine, methylparaben, propylparaben, gezuiverd water, sorbitoloplossing en sucrose. Kan natriumhydroxide of zoutzuur bevatten om de pH aan te passen.
5 mg/ml en 20 mg/ml orale suspensie
Actief ingrediënt: elke ml bevat thioridazine, USP, overeenkomend met respectievelijk 5 mg en 20 mg thioridazine HCl, USP.
5 mg/ml orale suspensie
Inactieve ingredienten: carbomeer 934, smaakstof, polysorbaat 80, gezuiverd water, natriumhydroxide en sucrose.
20 mg/ml orale suspensie
Inactieve ingredienten: carbomeer 934, D&C Yellow #10, FD&C Yellow #6, smaakstof, polysorbaat 80, gezuiverd water, natriumhydroxide en sucrose.
INDICATIES
Mellaril® (thioridazine HCl) is geïndiceerd voor de behandeling van schizofrene patiënten die niet adequaat reageren op behandeling met andere antipsychotica. Vanwege het risico op significante, mogelijk levensbedreigende, pro-aritmische effecten bij behandeling met Mellaril (thioridazine hcl), mag Mellaril (thioridazine hcl) alleen worden gebruikt bij patiënten die niet adequaat hebben gereageerd op behandeling met geschikte kuren met andere antipsychotica, ofwel vanwege onvoldoende effectiviteit of
het onvermogen om een effectieve dosis te bereiken als gevolg van ondraaglijke bijwerkingen van die geneesmiddelen. Daarom wordt het ten zeerste aanbevolen dat een patiënt, voordat de behandeling met mellaril (thioridazine hcl) wordt gestart, ten minste 2 onderzoeken krijgt, elk met een ander antipsychoticum, in een adequate dosis en voor een adequate duur (zie WAARSCHUWINGEN en CONTRA-INDICATIES ).
De voorschrijver moet zich er echter van bewust zijn dat Mellaril (thioridazine hcl) niet systematisch is geëvalueerd in gecontroleerde onderzoeken bij therapieresistente schizofrene patiënten en dat de werkzaamheid ervan bij dergelijke patiënten onbekend is.
DOSERING EN ADMINISTRATIE
Aangezien Mellaril (thioridazine HCl) geassocieerd is met een dosisgerelateerde verlenging van het QTc-interval, wat een potentieel levensbedreigende gebeurtenis is, moet het gebruik ervan worden gereserveerd voor schizofrene patiënten die niet adequaat reageren op behandeling met andere antipsychotica. De dosering moet individueel worden bepaald en de kleinste effectieve dosering moet voor elke patiënt worden bepaald (zie: INDICATIES en WAARSCHUWINGEN ).
volwassenen
De gebruikelijke startdosering voor volwassen schizofrene patiënten is driemaal daags 50-100 mg, indien nodig geleidelijk te verhogen tot maximaal 800 mg per dag. Zodra de symptomen effectief onder controle zijn, kan de dosering geleidelijk worden verlaagd om de minimale onderhoudsdosis te bepalen. De totale dagelijkse dosering varieert van 200-800 mg, verdeeld over twee tot vier doses.
Pediatrische patiënten
Voor pediatrische patiënten met schizofrenie die niet reageren op andere middelen, is de aanbevolen aanvangsdosis 0,5 mg/kg/dag verdeeld over verschillende doses. De dosering kan geleidelijk worden verhoogd totdat een optimaal therapeutisch effect is bereikt of de maximale dosis van 3 mg/kg/dag is bereikt.
HOE GELEVERD
Mellaril® (thioridazine HCl) tabletten
10 mg
Heldere chartreuse, omhulde tabletten; "S" bedrukt aan de ene kant, "78-2'' bedrukt aan de andere kant, in zwart.
Fles van 100 .......................................... NDC 0078-0002-05 Fles van 1000 ........................................ NDC 0078-0002-09 Eenheidsdosisverpakking van 100 ............ NDC 0078-0002-06
15 mg
Roze, omhulde tabletten; "S" bedrukt aan de ene kant, "78-8'' bedrukt aan de andere kant, in zwart.
Fles van 100 .......................................... NDC 0078-0008-05
25 mg
Lichtbruine, omhulde tabletten; "S" bedrukt aan de ene kant, "MELLARIL (thioridazine hcl) 25'' bedrukt aan de andere kant, in zwart.
Fles van 100 .......................................... NDC 0078-0003-05 Fles van 1000 ........................................ NDC 0078-0003-09 Eenheidsdosisverpakking van 100 ............ NDC 0078-0003-06
50 mg
Witte, omhulde tabletten; "S" bedrukt aan de ene kant, "MELLARIL (thioridazine hcl) 50'' bedrukt aan de andere kant, in zwart.
Fles van 100 .......................................... NDC 0078-0004-05 Fles van 1000 ........................................ NDC 0078-0004-09 Eenheidsdosisverpakking van 100 ............ NDC 0078-0004-06
100 mg
Lichtgroene, omhulde tabletten; "^4&" bedrukt aan de ene kant, "MELLARIL (thioridazine hcl) 100'' bedrukt aan de andere kant, in zwart.
Fles van 100 .......................................... NDC 0078-0005-05 Fles van 1000 ........................................ NDC 0078-0005-09 Eenheidsdosisverpakking van 100 ............ NDC 0078-0005-06
150 mg
Gele, omhulde tabletten; "S" bedrukt aan de ene kant, "MELLARIL (thioridazine hcl) 150'' bedrukt aan de andere kant, in zwart.
Fles van 100 .......................................... NDC 0078-0006-05
200 mg
Roze, omhulde tabletten, "^4&" bedrukt aan de ene kant, "MELLARIL (thioridazine hcl) 200'' bedrukt aan de andere kant, in zwart.
Fles van 100 .......................................... NDC 0078-0007-05 Eenheidsdosisverpakking van 100 ............ NDC 0078-0007-06
Opslaan en afgeven
Beneden 86 ° F (30 ° C); strakke bak.
Mellaril® (thioridazine HCl) orale oplossing (concentraat)
30 mg/ml
Een heldere, strogele vloeistof met een kersachtige geur. Elke ml bevat 30 mg thioridazine-hydrochloride, USP, alcohol, 3,0 vol.%. Onmiddellijke container: amberkleurige glazen flessen van 4 fl. oz. (118 ml) als volgt: 4 fl. oz. flessen, in dozen van 12 flessen, met een bijbehorende druppelaar met schaalverdeling om 10 mg, 25 mg en 50 mg thioridazine-hydrochloride, USP ( NDC 0078-0001-31).
100 mg/ml
Een heldere, lichtgele vloeistof met een aardbeiachtige geur. Elke ml bevat 100 mg thioridazine-hydrochloride, USP, alcohol, 4,2 vol.%. Onmiddellijke container: amberkleurige glazen flessen van 4 fl. oz. (118 ml), in dozen van 12 flessen, met een bijbehorende druppelaar met schaalverdeling voor het afleveren van 100 mg, 150 mg en 200 mg thioridazine-hydrochloride, USP ( NDC 0078-0009-31).
Opslaan en afgeven
Beneden 86 ° F (30 ° C); strakke, amberkleurige glazen fles.
De drank (concentraat) kan worden verdund met gedestilleerd water, aangezuurd kraanwater of geschikte sappen. Elke dosis moet zo worden verdund net voor toediening - bereiding en opslag van bulkverdunningen wordt niet aanbevolen.
Mellaril (thioridazine hcl) -S® (thioridazine) orale suspensie
5 mg/ml
Een gebroken witte suspensie met een botermuntsmaak en een pepermuntgeur. Elke ml bevat thioridazine, USP, overeenkomend met 5 mg thioridazine-hydrochloride, USP. Met botersmaak in pintflessen (NDC 0078-0068-33).
20 mg/ml
Een gele suspensie met een botermuntsmaak en een pepermuntgeur. Elke ml bevat thioridazine, USP, overeenkomend met 20 mg thioridazine-hydrochloride, USP. Met botersmaak in pintflessen (NDC 0078-0069-33).
Opslaan en afgeven
Beneden 77 ° F (25 ° C); strakke, amberkleurige glazen fles.
Aanvullende informatie beschikbaar voor artsen. Novartis Pharmaceuticals Corporation, East Hanover, New Jersey 07936. Herzien: juni 2000.
BIJWERKINGEN
In de aanbevolen doseringsbereiken met Mellaril® (thioridazine HCl) zijn de meeste bijwerkingen mild en van voorbijgaande aard.
Centraal zenuwstelsel: Soms kan slaperigheid optreden, vooral wanneer grote doses vroeg in de behandeling worden gegeven. Over het algemeen heeft dit effect de neiging om af te nemen bij voortzetting van de therapie of een verlaging van de dosering. Pseudoparkinsonisme en andere extrapiramidale symptomen kunnen voorkomen, maar komen zelden voor. Nachtelijke verwardheid, hyperactiviteit, lethargie, psychotische reacties, rusteloosheid en hoofdpijn zijn gemeld, maar zijn uiterst zeldzaam.
Autonoom zenuwstelsel: Een droge mond, wazig zien, constipatie, misselijkheid, braken, diarree, verstopte neus en bleekheid zijn waargenomen.
Endocrien systeem: Galactorroe, stuwing van de borst, amenorroe, remming van de ejaculatie en perifeer oedeem zijn beschreven.
Huid: Dermatitis en huiduitslag van het urticariële type zijn zelden waargenomen. Lichtgevoeligheid is uiterst zeldzaam.
Cardiovasculair systeem: Mellaril (thioridazine hcl) veroorzaakt een dosisgerelateerde verlenging van het QTc-interval, wat geassocieerd is met het vermogen om torsade de pointes-type aritmieën, een mogelijk fatale polymorfe ventriculaire tachycardie en plotselinge dood te veroorzaken (zie WAARSCHUWINGEN ). Zowel torsade de pointes-achtige aritmieën en plotselinge dood zijn gemeld in verband met Mellaril (thioridazine hcl). Een causaal verband tussen deze gebeurtenissen en de behandeling met Mellaril (thioridazine hcl) is niet vastgesteld, maar gezien het vermogen van Mellaril (thioridazine hcl) om het QTc-interval te verlengen, is een dergelijke relatie mogelijk. Andere ECG-veranderingen zijn gemeld (zie Fenothiazinederivaten: cardiovasculaire effecten ).

Ander: Zeldzame gevallen beschreven als parotiszwelling zijn gemeld na toediening van mellaril (thioridazine hcl).
Post Introductie Rapporten
Dit zijn vrijwillige meldingen van bijwerkingen die tijdelijk zijn geassocieerd met Mellaril (thioridazine hcl) die zijn ontvangen sinds het op de markt brengen, en er is mogelijk geen causaal verband tussen het gebruik van Mellaril (thioridazine hcl) en deze gebeurtenissen: priapisme.
Fenothiazinederivaten
Opgemerkt moet worden dat de werkzaamheid, indicaties en ongewenste effecten variëren met de verschillende fenothiazinen. Er is gemeld dat ouderdom de tolerantie voor fenothiazinen verlaagt. De meest voorkomende neurologische bijwerkingen bij deze patiënten zijn parkinsonisme en acathisie. Er lijkt een verhoogd risico op agranulocytose en leukopenie te zijn bij de geriatrische populatie. De arts moet zich ervan bewust zijn dat het volgende is opgetreden met een of meer fenothiazinen en moet worden overwogen wanneer een van deze geneesmiddelen wordt gebruikt:
Autonome reacties: Miosis, obstipatie, anorexia, paralytische ileus.
Huidreacties: Erytheem, exfoliatieve dermatitis, contactdermatitis.
Bloeddyscrasieën: Agranulocytose, leukopenie, eosinofilie, trombocytopenie, bloedarmoede, aplastische anemie, pancytopenie.
Allergische reacties: Koorts, larynxoedeem, angioneurotisch oedeem, astma.
Levertoxiciteit: Geelzucht, galstasis.
Cardiovasculaire effecten: Veranderingen in het terminale gedeelte van het elektrocardiogram, waaronder verlenging van het QT-interval, depressie en inversie van de T-golf, en het verschijnen van een golf die voorlopig wordt geïdentificeerd als een gespleten T-golf of een U-golf, zijn waargenomen bij patiënten die fenothiazinen kregen, waaronder Mellaril (thioridazine hcl). Tot op heden lijken deze te wijten te zijn aan veranderde repolarisatie, niet gerelateerd aan myocardiale schade, en omkeerbaar. Niettemin is een significante verlenging van het QT-interval in verband gebracht met ernstige ventriculaire aritmieën en plotselinge dood (zie WAARSCHUWINGEN ). Hypotensie, zelden resulterend in hartstilstand, is gemeld.
Extrapiramidale symptomen: Acathisie, agitatie, motorische rusteloosheid, dystonische reacties, trismus, torticollis, opisthotonus, oculogyrische crises, tremor, spierstijfheid, akinesie.
Tardieve dyskinesie: Chronisch gebruik van neuroleptica kan in verband worden gebracht met de ontwikkeling van tardieve dyskinesie. De meest opvallende kenmerken van dit syndroom worden beschreven in de WAARSCHUWINGEN sectie en vervolgens.
Het syndroom wordt gekenmerkt door onwillekeurige choreoathetotische bewegingen waarbij de tong, het gezicht, de mond, de lippen of de kaak op verschillende manieren betrokken zijn (bijv. uitsteeksel van de tong, puffende wangen, tuiten van de mond, kauwbewegingen), romp en ledematen. De ernst van het syndroom en de mate van stoornis die wordt veroorzaakt, lopen sterk uiteen.
Het syndroom kan klinisch herkenbaar worden tijdens de behandeling, bij verlaging van de dosering of bij stopzetting van de behandeling. Bewegingen kunnen in intensiteit afnemen en kunnen helemaal verdwijnen als verdere behandeling met neuroleptica wordt onthouden. Over het algemeen wordt aangenomen dat reversibiliteit waarschijnlijker is na korte in plaats van langdurige blootstelling aan neuroleptica. Daarom is vroege detectie van tardieve dyskinesie belangrijk. Om de kans op detectie van het syndroom zo vroeg mogelijk te vergroten, moet de dosering van het neurolepticum periodiek worden verlaagd (indien klinisch mogelijk) en moet de patiënt worden geobserveerd op tekenen van de aandoening. Deze manoeuvre is van cruciaal belang, want neuroleptica kunnen de tekenen van het syndroom maskeren.
Maligne neurolepticasyndroom (MNS): Chronisch gebruik van neuroleptica kan in verband worden gebracht met de ontwikkeling van maligne neurolepticasyndroom. De meest opvallende kenmerken van dit syndroom worden beschreven in de WAARSCHUWINGEN sectie en vervolgens. Klinische manifestaties van MNS zijn hyperpyrexie, spierstijfheid, veranderde mentale toestand en tekenen van autonome instabiliteit (onregelmatige pols of bloeddruk, tachycardie, diaforese en hartritmestoornissen).
Endocriene stoornissen: Onregelmatige menstruatie, veranderd libido, gynaecomastie, borstvoeding, gewichtstoename, oedeem. Er zijn fout-positieve zwangerschapstesten gemeld.
Urine stoornissen: Retentie, incontinentie.
anderen: Hyperpyrexie. Er zijn gedragseffecten gemeld die wijzen op een paradoxale reactie. Deze omvatten opwinding, bizarre dromen, verergering van psychosen en giftige verwarde toestanden. Meer recentelijk is een eigenaardig huid-oogsyndroom erkend als bijwerking na langdurige behandeling met fenothiazinen. Deze reactie wordt gekenmerkt door progressieve pigmentatie van delen van de huid of conjunctiva en/of vergezeld van verkleuring van de blootgestelde sclera en het hoornvlies. Opaciteiten van de voorste lens en het hoornvlies beschreven als onregelmatig of stervormig van vorm zijn ook gemeld. Systemisch lupus erythematosus-achtig syndroom.
DRUG-INTERACTIES
Verminderde cytochroom P450 2D6 isozymactiviteit, geneesmiddelen die dit isozym remmen (bijv. fluoxetine en paroxetine) en bepaalde andere geneesmiddelen (bijv. fluvoxamine, propranolol en pindolol) lijken het metabolisme van thioridazine aanzienlijk te remmen. De resulterende verhoogde niveaus van thioridazine zullen naar verwachting de verlenging van het QTc-interval in verband met mellaril (thioridazine hcl) vergroten en kunnen het risico op ernstige, mogelijk fatale hartritmestoornissen, zoals torsade de pointes-achtige aritmieën, verhogen. Een dergelijk verhoogd risico kan ook het gevolg zijn van het additieve effect van gelijktijdige toediening van mellaril (thioridazine hcl) met andere middelen die het QTc-interval verlengen. Daarom is Mellaril (thioridazine hcl) gecontra-indiceerd bij deze geneesmiddelen en bij patiënten, die ongeveer 7% van de normale populatie uitmaken, van wie bekend is dat ze een genetisch defect hebben dat leidt tot verminderde activiteit van P450 2D6 (zie WAARSCHUWINGEN en CONTRA-INDICATIES ).
Geneesmiddelen die cytochroom P450 2D6 remmen
In een onderzoek onder 19 gezonde mannelijke proefpersonen, waaronder 6 langzame en 13 snelle hydroxylatoren van puinoquin, veroorzaakte een enkele orale dosis van 25 mg thioridazine een 2,4 keer hogere Cmax en een 4,5 keer hogere AUC voor thioridazine in de langzame hydroxylatoren vergeleken met snelle hydroxylatoren. Men denkt dat de snelheid van hydroxylering van debrisoquin afhangt van het niveau van cytochroom P450 2D6-isozymactiviteit. Deze studie suggereert dus dat geneesmiddelen die P450 2D6 remmen of de aanwezigheid van verminderde activiteitsniveaus van dit isozym verhoogde plasmaspiegels van thioridazine zullen produceren. Daarom is de gelijktijdige toediening van geneesmiddelen die P450 2D6 remmen met Mellaril (thioridazine hcl) en het gebruik van Mellaril (thioridazine hcl) bij patiënten waarvan bekend is dat ze een verminderde activiteit van P450 2D6 hebben, gecontra-indiceerd.
Geneesmiddelen die de klaring van Mellaril® (thioridazine hcl) via andere mechanismen verminderen
Fluvoxamine: Het effect van fluvoxamine (25 mg tweemaal daags gedurende één week) op de steady-state-concentratie van thioridazine werd geëvalueerd bij 10 mannelijke ziekenhuispatiënten met schizofrenie. De concentraties van thioridazine en zijn twee actieve metabolieten, mesoridazine en sulforidazine, namen drievoudig toe na gelijktijdige toediening van fluvoxamine. Fluvoxamine en mellaril (thioridazine hcl) mogen niet gelijktijdig worden toegediend.
Propranolol: Er is gemeld dat gelijktijdige toediening van propranolol (100-800 mg per dag) verhogingen van de plasmaspiegels van thioridazine (ongeveer 50%-400%) en zijn metabolieten (ongeveer 80%-300%) veroorzaakt. Propranolol en mellaril (thioridazine hcl) mogen niet gelijktijdig worden toegediend.
Pindolol: Gelijktijdige toediening van pindolol en thioridazine heeft geleid tot matige, dosisgerelateerde verhogingen van de serumspiegels van thioridazine en twee van zijn metabolieten, evenals tot hoger dan verwachte serumpindololspiegels. Pindolol en mellaril (thioridazine hcl) mogen niet gelijktijdig worden toegediend.
Geneesmiddelen die het QTc-interval verlengen
Er zijn geen onderzoeken naar de gelijktijdige toediening van mellaril (thioridazine hcl) en andere geneesmiddelen die het QTc-interval verlengen. Er wordt echter verwacht dat een dergelijke gelijktijdige toediening een additieve verlenging van het QTc-interval zal veroorzaken en daarom is dergelijk gebruik gecontra-indiceerd.
WAARSCHUWINGEN
Potentieel voor pro-aritmische effecten
WEGENS HET POTENTIEEL OP AANZIENLIJKE, MOGELIJK LEVENSBEDRIJVENDE, PRO-ARRITMISCHE EFFECTEN BIJ DE BEHANDELING MET MELLARIL® (THIORIDAZINE HCl), MOET CQUARIL (thioridazine hcl) WORDEN GERESERVEERD VOOR GEBRUIK BIJ DE BEHANDELING VAN SCHIZOPHRENISCHE SCHIZOPHRENISCHE PA TOATIENTEN BEHANDELING MET ANDERE ANTIPSYCHOTISCHE DRUGS, OFWEL DOOR ONVOLDOENDE DOELTREFFENDHEID OF HET ONVERMOGEN OM EEN EFFECTIEVE DOSIS TE BEREIKEN DOOR ONDRAAGBARE BIJWERKINGEN VAN DIE DRUGS. DAAROM WORDT HET STERK AANBEVOLEN DAT AAN EEN PATINT TEN MINSTE TWEE PROEVEN, ELK MET EEN VERSCHILLEND ANTIPSYCHOTISCH DRUGSPRODUCT, BIJ EEN VOLDOENDE DOSERING WORDT GEGEVEN. MELLARIL (thioridazine hcl) IS NIET SYSTEMATISCH GEVALUEERD IN GECONTROLEERDE PROEVEN BIJ DE BEHANDELING VAN REFRACTORY SCHIZOFRENISCHE PATINTEN EN DE WERKZAAMHEID BIJ DERGELIJKE PATINTEN IS ONBEKEND.
Een cross-overstudie bij negen gezonde mannen waarin enkelvoudige doses thioridazine 10 mg en 50 mg werden vergeleken met placebo, toonde een dosisgerelateerde verlenging van het QTc-interval aan. De gemiddelde maximale toename van het QTc-interval na de dosis van 50 mg was ongeveer 23 msec; een grotere verlenging kan worden waargenomen bij de klinische behandeling van niet-gescreende patiënten.
Verlenging van het QTc-interval is in verband gebracht met het vermogen om torsade de pointes-achtige aritmieën, een mogelijk fatale polymorfe ventriculaire tachycardie en plotselinge dood te veroorzaken. Er zijn verschillende gepubliceerde casusrapporten van torsade de pointes en plotselinge dood in verband met behandeling met thioridazine. Een causaal verband tussen deze gebeurtenissen en de behandeling met Mellaril (thioridazine hcl) is niet vastgesteld, maar gezien het vermogen van Mellaril (thioridazine hcl) om het QTc-interval te verlengen, is een dergelijke relatie mogelijk.
Bepaalde omstandigheden kunnen het risico op torsade de pointes en/of plotseling overlijden verhogen in verband met het gebruik van geneesmiddelen die het QTc-interval verlengen, waaronder 1) bradycardie, 2) hypokaliëmie, 3) gelijktijdig gebruik van andere geneesmiddelen die het QTc-interval verlengen, 4) aanwezigheid van aangeboren verlenging van het QT-interval, en 5) voor thioridazine in het bijzonder, het gebruik ervan bij patiënten met verminderde activiteit van P450 2D6 of de gelijktijdige toediening ervan met geneesmiddelen die P450 2D6 kunnen remmen of door een ander mechanisme de klaring verstoren van thioridazine (zie CONTRA-INDICATIES en PREVENTIEVE MAATREGELEN ).
Het wordt aanbevolen dat patiënten die in aanmerking komen voor behandeling met Mellaril (thioridazine hcl) een baseline-ECG laten uitvoeren en serumkaliumspiegels laten meten. Serumkalium moet worden genormaliseerd voordat de behandeling wordt gestart en patiënten met een QTc-interval van meer dan 450 msec mogen geen behandeling met mellaril (thioridazine hcl) krijgen. Het kan ook nuttig zijn om ECG's en serumkalium periodiek te controleren tijdens de behandeling met Mellaril (thioridazine hcl), vooral tijdens een periode van dosisaanpassing. Mellaril (thioridazine hcl) moet worden gestaakt bij patiënten met een QTc-interval van meer dan 500 msec.
Patiënten die Mellaril (thioridazine hcl) gebruiken en symptomen ervaren die geassocieerd kunnen zijn met het optreden van torsade de pointes (bijv. Duizeligheid, hartkloppingen of syncope) kunnen verdere hartevaluatie rechtvaardigen; in het bijzonder moet Holter-monitoring worden overwogen.
Tardieve dyskinesie
Tardieve dyskinesie, een syndroom dat bestaat uit mogelijk onomkeerbare, onwillekeurige, dyskinetische bewegingen, kan optreden bij patiënten die worden behandeld met neuroleptica (antipsychotica). Hoewel de prevalentie van het syndroom het hoogst lijkt te zijn bij ouderen, vooral bij oudere vrouwen, is het onmogelijk om te vertrouwen op prevalentieschattingen om bij aanvang van de neuroleptische behandeling te voorspellen welke patiënten het syndroom waarschijnlijk zullen ontwikkelen. Of neuroleptische geneesmiddelen verschillen in hun potentieel om tardieve dyskinesie te veroorzaken, is onbekend.
Aangenomen wordt dat zowel het risico op het ontwikkelen van het syndroom als de kans dat het onomkeerbaar wordt, toeneemt naarmate de duur van de behandeling en de totale cumulatieve dosis van de aan de patiënt toegediende neuroleptica toeneemt. Het syndroom kan zich echter ontwikkelen, hoewel veel minder vaak, na relatief korte behandelingsperioden met lage doses.
Er is geen behandeling bekend voor vastgestelde gevallen van tardieve dyskinesie, hoewel het syndroom gedeeltelijk of volledig kan verdwijnen als de neuroleptische behandeling wordt stopgezet. Neuroleptische behandeling zelf kan echter de tekenen en symptomen van het syndroom onderdrukken (of gedeeltelijk onderdrukken) en daardoor mogelijk het onderliggende ziekteproces maskeren. Het effect dat symptomatische onderdrukking heeft op het lange termijn beloop van het syndroom is onbekend.
Gezien deze overwegingen moeten neuroleptica zo worden voorgeschreven dat de kans op tardieve dyskinesie het grootst is. Chronische neuroleptische behandeling dient over het algemeen te worden voorbehouden aan patiënten die lijden aan een chronische ziekte waarvan, 1) bekend is dat ze reageren op neuroleptica, en 2) voor wie alternatieve, even effectieve, maar mogelijk minder schadelijke behandelingen niet beschikbaar of geschikt zijn. Bij patiënten die wel een chronische behandeling nodig hebben, moet worden gestreefd naar de kleinste dosis en de kortste behandelingsduur die een bevredigende klinische respons oplevert. De noodzaak van voortzetting van de behandeling moet periodiek opnieuw worden beoordeeld.
Als er tekenen en symptomen van tardieve dyskinesie optreden bij een patiënt die neuroleptica gebruikt, moet het stoppen van het geneesmiddel worden overwogen. Sommige patiënten kunnen echter behandeling nodig hebben ondanks de aanwezigheid van het syndroom.
(Voor meer informatie over de beschrijving van tardieve dyskinesie en de klinische detectie ervan, verwijzen wij u naar de secties over informatie voor patiënten en ONGEWENSTE REACTIES. )
Met betrekking tot fenothiazinen in het algemeen is gesuggereerd dat mensen die een overgevoeligheidsreactie (bijv. bloeddyscrasieën, geelzucht) op de ene hebben vertoond, meer vatbaar kunnen zijn om een reactie op anderen te vertonen. Er moet aandacht worden besteed aan het feit dat fenothiazinen in staat zijn om depressiva van het centrale zenuwstelsel (bijv. anesthetica, opiaten, alcohol, enz.) evenals atropine- en fosforinsecticiden te versterken. Artsen dienen de voordelen en risico's zorgvuldig af te wegen bij de behandeling van minder ernstige aandoeningen.
Voortplantingsstudies bij dieren en klinische ervaring tot nu toe hebben geen teratogeen effect met mellaril (thioridazine hcl) aangetoond. Met het oog op de wenselijkheid om de toediening van alle geneesmiddelen tijdens de zwangerschap tot een minimum te beperken, mag mellaril (thioridazine hcl) echter alleen worden gegeven als de voordelen van de behandeling groter zijn dan de mogelijke risico's voor moeder en foetus.
Maligne neurolepticasyndroom (NMS)
Een potentieel fataal symptoomcomplex dat soms wordt aangeduid als maligne neurolepticasyndroom (MNS) is gemeld in verband met antipsychotica. Klinische manifestaties van MNS zijn hyperpyrexie, spierstijfheid, veranderde mentale toestand en tekenen van autonome instabiliteit (onregelmatige pols of bloeddruk, tachycardie, diaforese en hartritmestoornissen).
De diagnostische evaluatie van patiënten met dit syndroom is gecompliceerd. Om tot een diagnose te komen, is het belangrijk om gevallen te identificeren waarin de klinische presentatie zowel een ernstige medische aandoening (bijv. longontsteking, systemische infectie, enz.) als onbehandelde of onvoldoende behandelde extrapiramidale tekenen en symptomen (EPS) omvat. Andere belangrijke overwegingen bij de differentiële diagnose zijn centrale anticholinerge toxiciteit, hitteberoerte, medicijnkoorts en primaire pathologie van het centrale zenuwstelsel (CZS).
De behandeling van MNS moet het volgende omvatten: 1) onmiddellijke stopzetting van antipsychotica en andere geneesmiddelen die niet essentieel zijn voor gelijktijdige therapie, 2) intensieve symptomatische behandeling en medische controle, en 3) behandeling van alle bijkomende ernstige medische problemen waarvoor specifieke behandelingen beschikbaar zijn. Er is geen algemene overeenstemming over specifieke farmacologische behandelingsregimes voor ongecompliceerde MNS.
Als een patiënt behandeling met antipsychotica nodig heeft na herstel van MNS, moet de mogelijke herintroductie van medicamenteuze therapie zorgvuldig worden overwogen. De patiënt moet zorgvuldig worden gecontroleerd, aangezien recidieven van MNS zijn gemeld.
Depressiva van het centrale zenuwstelsel
Zoals in het geval van andere fenothiazinen, is Mellaril (thioridazine hcl) in staat depressiva van het centrale zenuwstelsel (bijv. alcohol, anesthetica, barbituraten, narcotica, opiaten, andere psychoactieve drugs, enz.) evenals atropine- en fosforinsecticiden te versterken. Ernstige ademhalingsdepressie en ademstilstand zijn gemeld wanneer een patiënt een fenothiazine en een gelijktijdige hoge dosis barbituraat kreeg.
PREVENTIEVE MAATREGELEN
Leukopenie en/of agranulocytose en convulsieve aanvallen zijn gemeld, maar komen niet vaak voor. Van Mellaril® (thioridazine HCl) is aangetoond dat het nuttig is bij de behandeling van gedragsstoornissen bij epileptische patiënten, maar anticonvulsieve medicatie moet ook worden gehandhaafd. Pigmentaire retinopathie, die voornamelijk is waargenomen bij patiënten die grotere dan de aanbevolen doses innamen, wordt gekenmerkt door vermindering van de gezichtsscherpte, bruinachtige verkleuring van het gezichtsvermogen en verslechtering van het nachtzicht; onderzoek van de fundus onthult afzettingen van pigment. De mogelijkheid van deze complicatie kan worden verminderd door binnen de aanbevolen doseringslimieten te blijven.
Wanneer patiënten deelnemen aan activiteiten die volledige mentale alertheid vereisen (bijv. autorijden), is het raadzaam om de fenothiazinen voorzichtig toe te dienen en de dosering geleidelijk te verhogen. Vrouwelijke patiënten lijken een grotere neiging tot orthostatische hypotensie te hebben dan mannelijke patiënten. De toediening van epinefrine moet worden vermeden bij de behandeling van door geneesmiddelen veroorzaakte hypotensie, aangezien fenothiazinen af en toe een omgekeerd epinefrine-effect kunnen veroorzaken. Als een vasoconstrictor nodig is, zijn levarterenol en fenylefrine het meest geschikt.
Neuroleptica verhogen de prolactinespiegels; de verhoging houdt aan tijdens chronische toediening. Weefselkweekexperimenten geven aan dat ongeveer een derde van de menselijke borstkankers in vitro afhankelijk is van prolactine, een factor van potentieel belang als het voorschrijven van deze geneesmiddelen wordt overwogen bij een patiënt met een eerder gedetecteerde borstkanker. Hoewel stoornissen zoals galactorroe, amenorroe, gynaecomastie en impotentie zijn gemeld, is de klinische betekenis van verhoogde serumprolactinespiegels voor de meeste patiënten onbekend. Een toename van borstneoplasmata is gevonden bij knaagdieren na chronische toediening van neuroleptica. Noch klinische studies noch epidemiologische studies die tot nu toe zijn uitgevoerd, hebben echter een verband aangetoond tussen chronische toediening van deze geneesmiddelen en borsttumorvorming; het beschikbare bewijs wordt op dit moment te beperkt geacht om sluitend te zijn.
Pediatrisch gebruik
Zien DOSERING sectie Pediatrische patiënten .
OVERDOSERING
Veel van de waargenomen symptomen zijn uitbreidingen van de hieronder beschreven bijwerkingen ONGEWENSTE REACTIES. Mellaril® (thioridazine hcl) (thioridazine HCl) kan giftig zijn bij overdosering, waarbij cardiale toxiciteit van bijzonder belang is. Frequente ECG-controle en controle van de vitale functies van patiënten met een overdosis wordt aanbevolen. Observatie gedurende meerdere dagen kan nodig zijn vanwege het risico van vertraagde effecten.
Tekenen en symptomen
Effecten en klinische complicaties van acute overdosering met fenothiazinen kunnen zijn:
Cardiovasculair: Hartritmestoornissen, hypotensie, shock, ECG-veranderingen, verhoogde QT- en PR-intervallen, niet-specifieke ST- en T-golfveranderingen, bradycardie, sinustachycardie, atrioventriculair blok, ventriculaire tachycardie, ventriculaire fibrillatie, torsade de pointes, myocardiale depressie.
Centraal zenuwstelsel: Sedatie, extrapiramidale effecten, verwardheid, opwinding, hypothermie, hyperthermie, rusteloosheid, toevallen, areflexie, coma.
Autonoom zenuwstelsel: Mydriasis, miosis, droge huid, droge mond, verstopte neus, urineretentie, wazig zien.
Ademhaling: Ademhalingsdepressie, apneu, longoedeem.
Gastro-intestinaal: Hypomotiliteit, constipatie, ileus.
nier: Oligurie, uremie.
Toxische dosis- en bloedconcentratiebereiken voor de fenothiazinen zijn niet stevig vastgesteld. Er is gesuggereerd dat het bereik van de toxische bloedconcentratie voor thioridazine begint bij 1,0 mg/dl en dat 2-8 mg/dl het dodelijke concentratiebereik is.
Behandeling
Er moet een luchtweg worden aangelegd en onderhouden. Er moet worden gezorgd voor voldoende zuurstofvoorziening en ventilatie.
Cardiovasculaire monitoring moet onmiddellijk beginnen en moet continue elektrocardiografische monitoring omvatten om mogelijke aritmieën te detecteren. De behandeling kan een of meer van de volgende therapeutische interventies omvatten: correctie van elektrolytafwijkingen en zuur-base-evenwicht, lidocaïne, fenytoïne, isoproterenol, ventriculaire stimulatie en defibrillatie. Disopyramide, procaïnamide en kinidine kunnen additieve QT-verlengende effecten veroorzaken bij toediening aan patiënten met acute overdosering van mellaril en moeten worden vermeden (zie WAARSCHUWINGEN en CONTRA-INDICATIES ). Voorzichtigheid is geboden bij het toedienen van lidocaïne, omdat dit het risico op het ontwikkelen van aanvallen kan verhogen.
Voor de behandeling van hypotensie kunnen intraveneuze vloeistoffen en vasopressoren nodig zijn. Fenylefrine, levarterenol of metaraminol zijn de geschikte pressormiddelen voor gebruik bij de behandeling van refractaire hypotensie. De krachtige -adrenerge blokkerende eigenschappen van de fenothiazinen maken het gebruik van vasopressoren met gemengde α- en β-adrenerge agonistische eigenschappen ongepast, waaronder epinefrine en dopamine. Paradoxale vasodilatatie kan het gevolg zijn. Bovendien is het redelijk om te verwachten dat de α-adrenerge blokkerende eigenschappen van bretylium additief kunnen zijn aan die van mellaril (thioridazine hcl), wat resulteert in problematische hypotensie.
Bij het behandelen van overdosering moet de arts altijd de mogelijkheid van betrokkenheid van meerdere geneesmiddelen in overweging nemen. Maagspoeling en herhaalde doses actieve kool moeten worden overwogen. Inductie van braken heeft minder de voorkeur boven maagspoeling vanwege het risico op dystonie en de kans op aspiratie van braaksel. Emesis mag niet worden opgewekt bij patiënten waarvan wordt verwacht dat ze snel verslechteren, of bij patiënten met een verminderd bewustzijn.
Acute extrapiramidale symptomen kunnen worden behandeld met difenhydraminehydrochloride of benztropinemesylaat.
Vermijd het gebruik van barbituraten bij de behandeling van aanvallen, omdat deze door fenothiazine geïnduceerde ademhalingsdepressie kunnen versterken.
Geforceerde diurese, hemoperfusie, hemodialyse en manipulatie van de urine-pH zijn van onwaarschijnlijk voordeel bij de behandeling van een overdosis fenothiazine vanwege hun grote distributievolume en uitgebreide plasma-eiwitbinding.
Actuele informatie over de behandeling van overdosering kan vaak worden verkregen bij een gecertificeerd Regionaal Antigifcentrum. Telefoonnummers van gecertificeerde Regionale Antigifcentra staan vermeld in de Physicians' Desk Reference®**.
CONTRA-INDICATIES
Het gebruik van Mellaril® (thioridazine HCl) moet worden vermeden in combinatie met andere geneesmiddelen waarvan bekend is dat ze het QTc-interval verlengen en bij patiënten met een aangeboren lang QT-syndroom of een voorgeschiedenis van hartritmestoornissen.
Verminderde cytochroom P450 2D6 isozymactiviteit Geneesmiddelen die dit isozym remmen (bijv. fluoxetine en paroxetine) en bepaalde andere geneesmiddelen (bijv. fluvoxamine, propranolol en pindolol) lijken het metabolisme van thioridazine aanzienlijk te remmen. De resulterende verhoogde niveaus van thioridazine zullen naar verwachting de verlenging van het QTc-interval in verband met mellaril (thioridazine hcl) vergroten en kunnen het risico op ernstige, mogelijk fatale hartritmestoornissen, zoals torsade de pointes-achtige aritmieën, verhogen. Een dergelijk verhoogd risico kan ook het gevolg zijn van het additieve effect van gelijktijdige toediening van mellaril (thioridazine hcl) met andere middelen die het QTc-interval verlengen. Daarom is Mellaril (thioridazine hcl) gecontra-indiceerd bij deze geneesmiddelen en bij patiënten, die ongeveer 7% van de normale populatie uitmaken, van wie bekend is dat ze een genetisch defect hebben dat leidt tot verminderde activiteit van P450 2D6 (zie WAARSCHUWINGEN en PREVENTIEVE MAATREGELEN ).
Net als bij andere fenothiazinen is mellaril (thioridazine hcl) gecontra-indiceerd bij ernstige depressie van het centrale zenuwstelsel of comateuze toestanden van welke oorzaak dan ook, waaronder door geneesmiddelen geïnduceerde depressie van het centrale zenuwstelsel (zie WAARSCHUWINGEN ). Er moet ook worden opgemerkt dat hypertensieve of hypotensieve hartziekte in extreme mate een contra-indicatie is voor toediening van fenothiazine.
KLINISCHE FARMACOLOGIE
De farmacologische basisactiviteit van Mellaril® (thioridazine HCl) is vergelijkbaar met die van andere fenothiazinen, maar gaat gepaard met minimale extrapiramidale stimulatie.
Het is echter aangetoond dat thioridazine het QTc-interval op een dosisafhankelijke manier verlengt. Dit effect kan het risico op ernstige, mogelijk fatale ventriculaire aritmieën, zoals torsade de pointes-type aritmieën, verhogen. Vanwege dit risico is mellaril (thioridazine hcl) alleen geïndiceerd voor schizofrene patiënten die niet hebben gereageerd op andere antipsychotica of deze niet kunnen verdragen (zie WAARSCHUWINGEN en CONTRA-INDICATIES ). De voorschrijver moet zich er echter van bewust zijn dat Mellaril (thioridazine hcl) niet systematisch is geëvalueerd in gecontroleerde onderzoeken bij therapieresistente schizofrene patiënten en dat de werkzaamheid ervan bij dergelijke patiënten onbekend is.
PATIËNT INFORMATIE
Patiënten moeten worden geïnformeerd dat mellaril (thioridazine hcl) in verband is gebracht met mogelijk fatale hartritmestoornissen. Het risico op dergelijke gebeurtenissen kan verhoogd zijn wanneer bepaalde geneesmiddelen samen met mellaril (thioridazine hcl) worden gegeven. Daarom moeten patiënten de voorschrijver informeren dat ze een behandeling met mellaril (thioridazine hcl) krijgen voordat ze een nieuw medicijn nemen.
Gezien de waarschijnlijkheid dat sommige patiënten die chronisch aan neuroleptica worden blootgesteld, tardieve dyskinesie zullen ontwikkelen, wordt geadviseerd alle patiënten bij wie chronisch gebruik wordt overwogen, indien mogelijk, volledige informatie over dit risico te krijgen. Bij de beslissing om patiënten en/of hun voogden te informeren, moet uiteraard rekening worden gehouden met de klinische omstandigheden en de competentie van de patiënt om de verstrekte informatie te begrijpen.
