Reglan 10mg Metoclopramide Gebruik, bijwerkingen en dosering. Prijs in online apotheek. Generieke medicijnen zonder recept.
Wat is Reglan 10 mg en hoe wordt het gebruikt?
Reglan 10 mg is een receptgeneesmiddel dat wordt gebruikt voor de behandeling van symptomen van gastro-oesofageale refluxziekte (GERD), misselijkheid en braken veroorzaakt door chemotherapie, diabetische gastroparese en tijdens radiologie van het bovenste maagdarmkanaal. Reglan 10 mg kan alleen of in combinatie met andere medicijnen worden gebruikt.
Reglan 10 mg behoort tot een klasse geneesmiddelen die anti-emetische middelen worden genoemd; Prokinetische middelen.
Wat zijn de mogelijke bijwerkingen van Reglan 10 mg?
Reglan kan ernstige bijwerkingen veroorzaken, waaronder:
- trillen of trillen in uw armen of benen,
- verwardheid,
- depressie,
- gedachten aan zelfmoord of jezelf pijn doen,
- langzame of schokkerige spierbewegingen in uw gezicht,
- convulsies (toevallen),
- ongerustheid,
- agitatie,
- zenuwachtig gevoel,
- moeite om stil te blijven,
- slaapproblemen (slapeloosheid),
- zwelling,
- kortademigheid,
- snelle gewichtstoename,
- zeer stijve of stijve spieren,
- hoge koorts,
- zweten,
- verwardheid,
- snelle of onregelmatige hartslagen, en
- duizeligheid
Roep meteen medische hulp in als u een van de bovenstaande symptomen heeft.
De meest voorkomende bijwerkingen van Reglan 10 mg zijn:
- rusteloosheid,
- slaperigheid,
- gebrek aan energie,
- misselijkheid,
- braken,
- hoofdpijn,
- verwarring, en
- slaapproblemen (slapeloosheid)
Vertel het uw arts als u een bijwerking heeft die u hindert of die niet weggaat.
Dit zijn niet alle mogelijke bijwerkingen van Reglan. Vraag uw arts of apotheker om meer informatie.
Bel uw arts voor medisch advies over bijwerkingen. U kunt bijwerkingen melden aan de FDA op 1-800-FDA-1088.
WAARSCHUWING
TARDIEVE DYSKINESI
Behandeling met metoclopramide kan tardieve dyskinesie veroorzaken, een ernstige bewegingsstoornis die vaak onomkeerbaar is. Het risico op het ontwikkelen van tardieve dyskinesie neemt toe met de duur van de behandeling en de totale cumulatieve dosis.
De behandeling met metoclopramide moet worden stopgezet bij patiënten die tekenen of symptomen van tardieve dyskinesie ontwikkelen. Er is geen behandeling bekend voor tardieve dyskinesie. Bij sommige patiënten kunnen de symptomen verminderen of verdwijnen nadat de behandeling met metoclopramide is stopgezet.
Behandeling met metoclopramide langer dan 12 weken moet worden vermeden in alle, maar zeldzame gevallen waarin wordt aangenomen dat het therapeutische voordeel opweegt tegen het risico op het ontwikkelen van tardieve dyskinesie.
Zie WAARSCHUWINGEN
OMSCHRIJVING
Voor orale toediening zijn reglan®-tabletten (metoclopramide-tabletten, USP) 10 mg witte, ingekerfde, capsulevormige tabletten met de inscriptie "REGLAN" aan de ene kant en "ANI 10" aan de andere kant.
Elke pil bevat:
Metoclopramidebase 10 mg (als het monohydrochloride-monohydraat)
inactieve ingredienten
Magnesiumstearaat, mannitol, microkristallijne cellulose, stearinezuur.
reglan®-tabletten (metoclopramide-tabletten, USP) 5 mg zijn groene, elliptische tabletten met de inscriptie "REGLAN" boven "5" aan de ene kant en "ANI" aan de andere kant.
Elke pil bevat:
Metoclopramidebase 5 mg (als het monohydrochloride-monohydraat)
inactieve ingredienten
Maïszetmeel, D&C Geel 10 Aluminium Lake, FD&C Blauw 1 Aluminium Lake, Lactose, Microkristallijne Cellulose, Siliciumdioxide, Stearinezuur.
Metoclopramidehydrochloride is een witte kristallijne, geurloze stof, goed oplosbaar in water. Chemisch gezien is het 4-amino-5-chloor-N-[2-(diethylamino)ethyl]-2-methoxybenzamide-monohydrochloride-monohydraat. De molecuulformule is C14H22ClN3O2 • HCl • H2O. Het molecuulgewicht is 354,3.
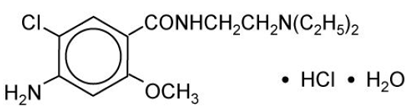
INDICATIES
Het gebruik van reglan® tabletten wordt alleen aanbevolen voor volwassenen. De therapie mag niet langer duren dan 12 weken.
Symptomatische gastro-oesofageale reflux
reglan®-tabletten zijn geïndiceerd als kortdurende (4 tot 12 weken) therapie voor volwassenen met symptomatische, gedocumenteerde gastro-oesofageale reflux die niet reageren op conventionele therapie.
Het belangrijkste effect van metoclopramide is op symptomen van postprandiaal en overdag brandend maagzuur, met minder waargenomen effect op nachtelijke symptomen. Als de symptomen beperkt blijven tot bepaalde situaties, zoals na het avondeten, moet het gebruik van metoclopramide als enkelvoudige dosis voorafgaand aan de provocerende situatie worden overwogen, in plaats van het geneesmiddel gedurende de dag te gebruiken. Genezing van slokdarmzweren en erosies is endoscopisch aangetoond aan het einde van een 12 weken durende studie met doses van 15 mg per dag. Aangezien er geen gedocumenteerde correlatie is tussen symptomen en genezing van slokdarmlaesies, moeten patiënten met gedocumenteerde laesies endoscopisch worden gecontroleerd.
Diabetische gastroparese (diabetische maagstasis)
reglan®-tabletten (metoclopramide-tabletten, USP) zijn geïndiceerd voor de verlichting van symptomen die gepaard gaan met acute en terugkerende diabetische maagstasis. De gebruikelijke verschijnselen van vertraagde maaglediging (bijv. misselijkheid, braken, brandend maagzuur, aanhoudende volheid na de maaltijd en anorexia) lijken binnen verschillende tijdsintervallen op reglan® te reageren. Aanzienlijke verlichting van misselijkheid treedt vroeg op en blijft gedurende een periode van drie weken verbeteren. Verlichting van braken en anorexia kan een week of langer voorafgaan aan de verlichting van een vol gevoel in de buik.
DOSERING EN ADMINISTRATIE
Therapie met reglan®-tabletten mag niet langer duren dan 12 weken.
Voor de verlichting van symptomatische gastro-oesofageale reflux
Dien 10 mg tot 15 mg reglan® (metoclopramide hydrochloride, USP) oraal toe tot driemaal 30 minuten voor elke maaltijd en voor het slapengaan, afhankelijk van de symptomen die worden behandeld en de klinische respons (zie KLINISCHE FARMACOLOGIE en AANWIJZINGEN EN GEBRUIK ). Als de symptomen slechts met tussenpozen of op specifieke tijdstippen van de dag optreden, kan het gebruik van metoclopramide in enkelvoudige doses tot 20 mg voorafgaand aan de uitlokkende situatie de voorkeur hebben boven continue behandeling. Af en toe hebben patiënten (zoals oudere patiënten) die gevoeliger zijn voor de therapeutische of nadelige effecten van metoclopramide slechts 5 mg per dosis nodig.
De ervaring met oesofageale erosies en ulceraties is beperkt, maar genezing is tot dusver gedocumenteerd in één gecontroleerd onderzoek met een QID-therapie van 15 mg/dosis, en dit regime moet worden gebruikt wanneer laesies aanwezig zijn, zolang het wordt verdragen (zie ONGEWENSTE REACTIES ). Vanwege de slechte correlatie tussen symptomen en endoscopisch uiterlijk van de slokdarm, wordt therapie gericht op slokdarmlaesies het best geleid door endoscopische evaluatie.
Therapie langer dan 12 weken is niet geëvalueerd en kan niet worden aanbevolen.
Voor de verlichting van de symptomen In overeenstemming met diabetische gastropares is (diabetische gastric stas) Dien 10 mg metoclopramide 30 minuten vóór elke maaltijd en voor het slapengaan toe gedurende twee tot acht weken, afhankelijk van de respons en de waarschijnlijkheid van aanhoudend welzijn bij stopzetting van het geneesmiddel.
De initiële toedieningsweg moet worden bepaald aan de hand van de ernst van de symptomen die zich voordoen. Als alleen de vroegste manifestaties van diabetische maagstasis aanwezig zijn, kan orale toediening van reglan® worden gestart. Als er echter ernstige symptomen aanwezig zijn, moet de therapie beginnen met een injectie met metoclopramide (raadpleeg de etikettering van de injectie voordat u met parenterale toediening begint).
Toediening van metoclopramide-injectie tot 10 dagen kan nodig zijn voordat de symptomen verdwijnen, waarna orale toediening kan worden ingesteld. Aangezien diabetische maagstasis vaak terugkeert, moet de behandeling met reglan® zo snel mogelijk worden hervat.
Gebruik bij patiënten met nier- of leverinsufficiëntie
Aangezien metoclopramide voornamelijk via de nieren wordt uitgescheiden, moet bij patiënten bij wie de creatinineklaring lager is dan 40 ml/min, de behandeling worden gestart met ongeveer de helft van de aanbevolen dosering. Afhankelijk van de klinische werkzaamheid en veiligheidsoverwegingen kan de dosering naar behoefte worden verhoogd of verlaagd.
Zien OVERDOSERING voor informatie over dialyse.
Metoclopramide ondergaat minimaal levermetabolisme, behalve eenvoudige conjugatie. Het veilige gebruik ervan is beschreven bij patiënten met gevorderde leverziekte bij wie de nierfunctie normaal was.
HOE GELEVERD
Elke witte, capsulevormige reglan®-tablet met breukgleuf (metoclopramide-tabletten, USP) bevat 10 mg metoclopramidebase (als het monohydrochloride-monohydraat). Beschikbaar in:
Flessen van 100 tabletten ( NDC 62559-166-01)
Elke groene, elliptische reglan®-tablet (metoclopramide-tabletten, USP) bevat 5 mg metoclopramidebase (als het monohydrochloride-monohydraat). Beschikbaar in:
Flessen van 100 tabletten ( NDC 62559-165-01)
Doseer tabletten in een strakke, lichtbestendige container.
Tabletten moeten worden bewaard bij een gecontroleerde kamertemperatuur, tussen 20°C en 25°C (68°F en 77°F).
Gefabriceerd door: ANI Pharmaceuticals, Inc. Baudette, MN 56623. Herzien: december 2014
BIJWERKINGEN
Over het algemeen correleert de incidentie van bijwerkingen met de dosis en duur van de toediening van metoclopramide. De volgende reacties zijn gemeld, hoewel de gegevens in de meeste gevallen geen schatting van de frequentie mogelijk maken:
CNS-effecten
Rusteloosheid, slaperigheid, vermoeidheid en lusteloosheid komen voor bij ongeveer 10% van de patiënten die de meest voorgeschreven dosering van 10 mg eenmaal per dag krijgen (zie PREVENTIEVE MAATREGELEN ). Slapeloosheid, hoofdpijn, verwardheid, duizeligheid of mentale depressie met zelfmoordgedachten (zie: WAARSCHUWINGEN komen minder vaak voor. De incidentie van slaperigheid is groter bij hogere doses. Er zijn geïsoleerde meldingen van convulsieve aanvallen zonder duidelijke relatie met metoclopramide. Zelden zijn hallucinaties gemeld.
Extrapiramidale reacties (EPS)
Acute dystonische reacties, het meest voorkomende type EPS geassocieerd met metoclopramide, komen voor bij ongeveer 0,2% van de patiënten (1 op 500) die worden behandeld met 30 tot 40 mg metoclopramide per dag. Symptomen zijn onder meer onwillekeurige bewegingen van ledematen, grimassen in het gezicht, torticollis, oculogyrische crisis, ritmisch uitpuilen van de tong, bulbaire spraak, trismus, opisthotonus (tetanus-achtige reacties), en, in zeldzame gevallen, stridor en dyspneu, mogelijk als gevolg van laryngospasme; normaal gesproken worden deze symptomen gemakkelijk ongedaan gemaakt door difenhydramine (zie: WAARSCHUWINGEN ).
Parkinsonachtige symptomen kunnen zijn: bradykinesie, tremor, tandradstijfheid, maskerachtig gelaat (zie WAARSCHUWINGEN ).
Tardieve dyskinesie wordt het vaakst gekenmerkt door onwillekeurige bewegingen van de tong, het gezicht, de mond of de kaak, en soms door onwillekeurige bewegingen van de romp en/of extremiteiten; bewegingen kunnen een choreoathetotisch uiterlijk hebben (zie: WAARSCHUWINGEN ).
Motorische rusteloosheid (akathisie) kan bestaan uit gevoelens van angst, opwinding, zenuwachtigheid en slapeloosheid, evenals onvermogen om stil te zitten, ijsberen, tikken met de voet. Deze symptomen kunnen spontaan verdwijnen of reageren op een verlaging van de dosering.
Maligne neurolepticasyndroom
Zeldzame gevallen van maligne neurolepticasyndroom (MNS) zijn gemeld. Dit potentieel fatale syndroom bestaat uit het symptoomcomplex hyperthermie, veranderd bewustzijn, spierstijfheid en autonome disfunctie (zie WAARSCHUWINGEN ).
Endocriene stoornissen
Galactorroe, amenorroe, gynaecomastie, impotentie secundair aan hyperprolactinemie (zie PREVENTIEVE MAATREGELEN ). Vochtretentie secundair aan voorbijgaande verhoging van aldosteron (zie: KLINISCHE FARMACOLOGIE ).
Cardiovasculair
Hypotensie, hypertensie, supraventriculaire tachycardie, bradycardie, vochtretentie, acuut congestief hartfalen en mogelijk AV-blok (zie CONTRA-INDICATIES en PREVENTIEVE MAATREGELEN ).
gastro-intestinaal
Misselijkheid en darmstoornissen, voornamelijk diarree.
lever
Zelden gevallen van hepatotoxiciteit, gekenmerkt door bevindingen als geelzucht en veranderde leverfunctietesten, wanneer metoclopramide werd toegediend met andere geneesmiddelen met een bekend hepatotoxisch potentieel.
nier
Urinefrequentie en incontinentie.
hematologisch
Enkele gevallen van neutropenie, leukopenie of agranulocytose, meestal zonder duidelijke relatie met metoclopramide. Methemoglobinemie, bij volwassenen en vooral bij overdosering bij pasgeborenen (zie: OVERDOSERING ). Sulfhemoglobinemie bij volwassenen.
Allergische reacties
Enkele gevallen van huiduitslag, urticaria of bronchospasmen, vooral bij patiënten met een voorgeschiedenis van astma. Zelden, angioneurotisch oedeem, inclusief glossaal of larynxoedeem.
Diversen
Visuele stoornissen. Porfyrie.
DRUG-INTERACTIES
De effecten van metoclopramide op de gastro-intestinale motiliteit worden tegengewerkt door anticholinergica en narcotische analgetica. Additieve sedatieve effecten kunnen optreden wanneer metoclopramide wordt gegeven met alcohol, sedativa, hypnotica, narcotica of kalmerende middelen.
De bevinding dat metoclopramide catecholamines afgeeft bij patiënten met essentiële hypertensie, suggereert dat het voorzichtig of helemaal niet moet worden gebruikt bij patiënten die monoamineoxidaseremmers krijgen.
De opname van geneesmiddelen uit de maag kan worden verminderd (bijv. digoxine) door metoclopramide, terwijl de snelheid en/of mate van absorptie van geneesmiddelen uit de dunne darm kan worden verhoogd (bijv. paracetamol, tetracycline, levodopa, ethanol, cyclosporine).
Gastroparese (maagstasis) kan bij sommige patiënten verantwoordelijk zijn voor een slechte diabetescontrole. Exogeen toegediende insuline kan beginnen te werken voordat voedsel de maag heeft verlaten en tot hypoglykemie leiden. Omdat de werking van metoclopramide de afgifte van voedsel aan de darmen en dus de absorptiesnelheid beïnvloedt, kan het nodig zijn de insulinedosering of het tijdstip van dosering aan te passen.
WAARSCHUWINGEN
Psychische depressie is opgetreden bij patiënten met en zonder voorgeschiedenis van depressie. De symptomen varieerden van mild tot ernstig en omvatten zelfmoordgedachten en zelfmoord. Metoclopramide mag alleen aan patiënten met een voorgeschiedenis van depressie worden gegeven als de verwachte voordelen opwegen tegen de mogelijke risico's.
Extrapiramidale symptomen, die zich voornamelijk manifesteren als acute dystonische reacties, komen voor bij ongeveer 1 op de 500 patiënten die worden behandeld met de gebruikelijke doseringen voor volwassenen van 30 tot 40 mg/dag metoclopramide. Deze treden meestal op tijdens de eerste 24 tot 48 uur van de behandeling met metoclopramide, komen vaker voor bij pediatrische patiënten en volwassen patiënten jonger dan 30 jaar en komen zelfs vaker voor bij hogere doses. Deze symptomen kunnen zijn: onwillekeurige bewegingen van ledematen en grimassen in het gezicht, torticollis, oculogyrische crisis, ritmisch uitpuilen van de tong, bulbaire spraak, trismus of dystonische reacties die op tetanus lijken. In zeldzame gevallen kunnen dystonische reacties optreden als stridor en dyspneu, mogelijk als gevolg van laryngospasme. Als deze symptomen optreden, injecteer dan 50 mg difenhydraminehydrochloride intramusculair, en ze zullen meestal verdwijnen. Benztropinemesylaat, 1 tot 2 mg intramusculair, kan ook worden gebruikt om deze reacties om te keren.
Parkinsonachtige symptomen zijn opgetreden, vaker binnen de eerste 6 maanden na het begin van de behandeling met metoclopramide, maar soms na langere perioden. Deze symptomen verdwijnen over het algemeen binnen 2 tot 3 maanden na stopzetting van metoclopramide. Patiënten met een reeds bestaande ziekte van Parkinson dienen metoclopramide met voorzichtigheid of helemaal niet te worden toegediend, aangezien dergelijke patiënten bij gebruik van metoclopramide verergering van parkinsonsymptomen kunnen ervaren.
Tardieve dyskinesie
(Zie DOOS WAARSCHUWING)
Behandeling met metoclopramide kan tardieve dyskinesie (TD) veroorzaken, een potentieel onomkeerbare en ontsierende aandoening die wordt gekenmerkt door onwillekeurige bewegingen van het gezicht, de tong of de ledematen. Het risico op het ontwikkelen van tardieve dyskinesie neemt toe met de duur van de behandeling en de totale cumulatieve dosis. Een analyse van gebruikspatronen toonde aan dat ongeveer 20% van de patiënten die metoclopramide gebruikten het langer dan 12 weken gebruikte. Behandeling met metoclopramide langer dan de aanbevolen 12 weken moet worden vermeden in alle, maar zeldzame gevallen waarin wordt aangenomen dat het therapeutische voordeel opweegt tegen het risico op het ontwikkelen van TD.
Hoewel het risico op het ontwikkelen van TD in de algemene bevolking verhoogd kan zijn bij ouderen, vrouwen en diabetici, is het niet mogelijk om te voorspellen welke patiënten door metoclopramide geïnduceerde TD zullen ontwikkelen. Zowel het risico op het ontwikkelen van TD als de waarschijnlijkheid dat TD onomkeerbaar zal worden, nemen toe met de duur van de behandeling en de totale cumulatieve dosis.
Metoclopramide moet worden gestaakt bij patiënten die tekenen of symptomen van TD ontwikkelen. Er is geen effectieve behandeling bekend voor vastgestelde gevallen van TD, hoewel bij sommige patiënten TD binnen enkele weken tot maanden na stopzetting van metoclopramide kan verdwijnen, gedeeltelijk of volledig.
Metoclopramide zelf kan de tekenen van TD onderdrukken of gedeeltelijk onderdrukken, waardoor het onderliggende ziekteproces wordt gemaskeerd. Het effect van deze symptomatische onderdrukking op het lange termijn beloop van TD is niet bekend. Daarom mag metoclopramide niet worden gebruikt voor de symptomatische controle van TD.
Maligne neurolepticasyndroom (NMS)
Er zijn zeldzame meldingen geweest van een ongewoon maar potentieel fataal symptoomcomplex dat soms wordt aangeduid als maligne neurolepticasyndroom (MNS), geassocieerd met metoclopramide. Klinische manifestaties van MNS omvatten hyperthermie, spierstijfheid, veranderd bewustzijn en tekenen van autonome instabiliteit (onregelmatige pols of bloeddruk, tachycardie, diaforese en hartritmestoornissen).
De diagnostische evaluatie van patiënten met dit syndroom is gecompliceerd. Om tot een diagnose te komen, is het belangrijk om gevallen te identificeren waarin de klinische presentatie zowel een ernstige medische aandoening (bijv. longontsteking, systemische infectie, enz.) als onbehandelde of onvoldoende behandelde extrapiramidale tekenen en symptomen (EPS) omvat. Andere belangrijke overwegingen bij de differentiële diagnose zijn centrale anticholinerge toxiciteit, hitteberoerte, maligne hyperthermie, medicijnkoorts en primaire pathologie van het centrale zenuwstelsel (CZS).
De behandeling van MNS dient te omvatten 1) onmiddellijke stopzetting van metoclopramide en andere geneesmiddelen die niet essentieel zijn voor gelijktijdige therapie, 2) intensieve symptomatische behandeling en medische controle, en 3) behandeling van alle bijkomende ernstige medische problemen waarvoor specifieke behandelingen beschikbaar zijn. Bromocriptine en natrium dantroleen zijn gebruikt bij de behandeling van MNS, maar hun werkzaamheid is niet vastgesteld (zie ONGEWENSTE REACTIES ).
PREVENTIEVE MAATREGELEN
Algemeen
In één onderzoek bij hypertensieve patiënten bleek intraveneus toegediend metoclopramide catecholamines af te geven; daarom is voorzichtigheid geboden wanneer metoclopramide wordt gebruikt bij patiënten met hypertensie.
Omdat metoclopramide een voorbijgaande toename van plasma-aldosteron veroorzaakt, kunnen bepaalde patiënten, vooral die met cirrose of congestief hartfalen, het risico lopen vochtretentie en volumeoverbelasting te ontwikkelen. Als deze bijwerkingen op enig moment tijdens de behandeling met metoclopramide optreden, moet het medicijn worden stopgezet.
Bijwerkingen, vooral die met betrekking tot het zenuwstelsel, kunnen optreden na het stoppen met het gebruik van reglan®. Een klein aantal patiënten kan een wachttijd ervaren na het stoppen met reglan®, die duizeligheid, nervositeit en/of hoofdpijn kan omvatten.
Informatie voor patiënten
Het gebruik van reglan® wordt alleen aanbevolen voor volwassenen. Metoclopramide kan de mentale en/of fysieke vermogens aantasten die nodig zijn voor het uitvoeren van gevaarlijke taken zoals het bedienen van machines of het besturen van een motorvoertuig. De ambulante patiënt moet dienovereenkomstig worden gewaarschuwd.
Voor aanvullende informatie moeten patiënten worden geïnstrueerd om de medicatiehandleiding voor reglan®-tabletten te raadplegen.

Carcinogenese, mutagenese, verminderde vruchtbaarheid
Een onderzoek van 77 weken werd uitgevoerd bij ratten met orale doses tot ongeveer 40 maal de maximaal aanbevolen dagelijkse dosis voor de mens. Metoclopramide verhoogt de prolactinespiegels en de verhoging houdt aan tijdens chronische toediening. Weefselkweekexperimenten geven aan dat ongeveer een derde van de menselijke borstkankers in vitro prolactine-afhankelijk is, een factor van potentieel belang als het voorschrijven van metoclopramide wordt overwogen bij een patiënt met eerder gedetecteerde borstkanker. Hoewel stoornissen zoals galactorroe, amenorroe, gynaecomastie en impotentie zijn gemeld bij prolactineverhogende geneesmiddelen, is de klinische betekenis van verhoogde serumprolactinespiegels voor de meeste patiënten niet bekend. Een toename van borstneoplasmata is gevonden bij knaagdieren na chronische toediening van prolactinestimulerende neuroleptica en metoclopramide. Noch klinische studies noch epidemiologische studies die tot nu toe zijn uitgevoerd, hebben echter een verband aangetoond tussen chronische toediening van deze geneesmiddelen en borsttumorvorming; het beschikbare bewijs is op dit moment te beperkt om overtuigend te zijn.
Een Ames-mutageniteitstest uitgevoerd op metoclopramide was negatief.
Zwangerschap Categorie B
Reproductieonderzoeken uitgevoerd bij ratten, muizen en konijnen via de IV, IM, SC en orale routes bij maximale niveaus variërend van 12 tot 250 maal de dosis voor de mens hebben geen verminderde vruchtbaarheid of significante schade aan de foetus aangetoond als gevolg van metoclopramide. Er zijn echter geen adequate en goed gecontroleerde onderzoeken bij zwangere vrouwen. Omdat reproductiestudies bij dieren niet altijd voorspellend zijn voor de respons van de mens, mag dit medicijn alleen tijdens de zwangerschap worden gebruikt als dit duidelijk nodig is.
Moeders die borstvoeding geven
Metoclopramide wordt uitgescheiden in de moedermelk. Voorzichtigheid is geboden wanneer metoclopramide wordt toegediend aan een zogende moeder.
Pediatrisch gebruik
De veiligheid en werkzaamheid bij pediatrische patiënten zijn niet vastgesteld (zie: OVERDOSERING ).
Voorzichtigheid is geboden bij het toedienen van metoclopramide aan pasgeborenen, aangezien langdurige klaring kan leiden tot te hoge serumconcentraties (zie: KLINISCHE FARMACOLOGIE - Farmacokinetiek ). Bovendien hebben pasgeborenen verlaagde NADH-cytochroom-b5-reductasespiegels die, in combinatie met de bovengenoemde farmacokinetische factoren, pasgeborenen vatbaarder maken voor methemoglobinemie (zie OVERDOSERING ).
Het veiligheidsprofiel van metoclopramide bij volwassenen kan niet worden geëxtrapoleerd naar pediatrische patiënten. Dystonieën en andere extrapiramidale reacties geassocieerd met metoclopramide komen vaker voor bij pediatrische patiënten dan bij volwassenen. (Zien WAARSCHUWINGEN en ONGEWENSTE REACTIES - Extrapiramidale reacties. )
Geriatrisch gebruik
Klinische onderzoeken met reglan® omvatten niet voldoende aantallen proefpersonen van 65 jaar en ouder om te bepalen of oudere proefpersonen anders reageren dan jongere proefpersonen.
Het risico op het ontwikkelen van Parkinson-achtige bijwerkingen neemt toe met toenemende dosis. Geriatrische patiënten moeten de laagste dosis reglan® krijgen die effectief is. Als zich parkinsonachtige symptomen ontwikkelen bij een geriatrische patiënt die reglan® krijgt, moet reglan® in het algemeen worden stopgezet voordat met specifieke antiparkinsonmiddelen wordt begonnen (zie WAARSCHUWINGEN en DOSERING EN ADMINISTRATIE – Voor de verlichting van symptomatische gastro-intestinale reflux ).
Ouderen lopen mogelijk een groter risico op tardieve dyskinesie (zie: WAARSCHUWINGEN – Tardieve dyskinesie ).
Sedatie is gemeld bij gebruikers van reglan®. Sedatie kan verwarring veroorzaken en zich manifesteren als oversedatie bij ouderen (zie: KLINISCHE FARMACOLOGIE , PREVENTIEVE MAATREGELEN – Informatie voor patiënten en ONGEWENSTE REACTIES – CZS-effecten ).
Van reglan® is bekend dat het grotendeels door de nieren wordt uitgescheiden en het risico op toxische reacties op dit geneesmiddel kan groter zijn bij patiënten met een verminderde nierfunctie (zie DOSERING EN ADMINISTRATIE – Gebruik bij patiënten met nier- of leverfunctiestoornissen ).
Om deze redenen moet de dosiskeuze voor een oudere patiënt voorzichtig zijn, meestal beginnend aan het lage uiteinde van het doseringsbereik, als gevolg van de grotere frequentie van verminderde nierfunctie, gelijktijdige ziekte of andere medicamenteuze behandeling bij ouderen (zie DOSERING EN ADMINISTRATIE – Voor de verlichting van symptomatische gastro-oesofageale reflux en gebruik bij patiënten met nier- of leverinsufficiëntie ).
Andere speciale populaties
Patiënten met NADH-cytochroom-b5-reductasedeficiëntie lopen een verhoogd risico op het ontwikkelen van methemoglobinemie en/of sulfhemoglobinemie wanneer metoclopramide wordt toegediend. Bij patiënten met G6PD-deficiëntie die metoclopramide-geïnduceerde methemoglobinemie ervaren, wordt behandeling met methyleenblauw niet aanbevolen (zie OVERDOSERING ).
OVERDOSERING
Symptomen van overdosering kunnen slaperigheid, desoriëntatie en extrapiramidale reacties zijn. Anticholinergica of antiparkinsongeneesmiddelen of antihistaminica met anticholinerge eigenschappen kunnen nuttig zijn bij het beheersen van de extrapiramidale reacties. Symptomen zijn zelfbeperkend en verdwijnen meestal binnen 24 uur.
Hemodialyse verwijdert relatief weinig metoclopramide, waarschijnlijk vanwege de kleine hoeveelheid van het geneesmiddel in het bloed ten opzichte van weefsels. Evenzo verwijdert continue ambulante peritoneale dialyse geen significante hoeveelheden geneesmiddel. Het is onwaarschijnlijk dat de dosering moet worden aangepast om verliezen door dialyse te compenseren. Dialyse is waarschijnlijk geen effectieve methode voor het verwijderen van geneesmiddelen in situaties van overdosering.
Onbedoelde overdosering als gevolg van verkeerde toediening is gemeld bij zuigelingen en kinderen bij het gebruik van metoclopramide drank. Hoewel er geen consistent patroon was in de meldingen die verband hielden met deze overdoses, omvatten de voorvallen toevallen, extrapiramidale reacties en lethargie.
Methemoglobinemie is opgetreden bij premature en voldragen pasgeborenen die een overdosis metoclopramide kregen (1 tot 4 mg/kg/dag oraal, intramusculair of intraveneus gedurende 1 tot 3 of meer dagen). Methemoglobinemie kan worden teruggedraaid door de intraveneuze toediening van methyleenblauw. Methyleenblauw kan echter hemolytische anemie veroorzaken bij patiënten met G6PD-deficiëntie, die fataal kan zijn (zie: PREVENTIEVE MAATREGELEN – Andere speciale populaties ).
CONTRA-INDICATIES
Metoclopramide mag niet worden gebruikt wanneer stimulatie van de gastro-intestinale motiliteit gevaarlijk kan zijn, bijv. in de aanwezigheid van gastro-intestinale bloeding, mechanische obstructie of perforatie.
Metoclopramide is gecontra-indiceerd bij patiënten met feochromocytoom omdat het geneesmiddel een hypertensieve crisis kan veroorzaken, waarschijnlijk als gevolg van het vrijkomen van catecholamines uit de tumor. Dergelijke hypertensieve crises kunnen worden gecontroleerd door fentolamine.
Metoclopramide is gecontra-indiceerd bij patiënten met een bekende gevoeligheid of intolerantie voor het geneesmiddel. Metoclopramide mag niet worden gebruikt bij epileptica of bij patiënten die andere geneesmiddelen krijgen die extrapiramidale reacties kunnen veroorzaken, aangezien de frequentie en ernst van aanvallen of extrapiramidale reacties kunnen toenemen.
KLINISCHE FARMACOLOGIE
Metoclopramide stimuleert de beweeglijkheid van het bovenste deel van het maagdarmkanaal zonder de maag-, gal- of pancreasafscheiding te stimuleren. De werking ervan is onduidelijk. Het lijkt weefsels gevoelig te maken voor de werking van acetylcholine. Het effect van metoclopramide op de beweeglijkheid is niet afhankelijk van intacte vagale innervatie, maar kan worden opgeheven door anticholinergica.
Metoclopramide verhoogt de tonus en amplitude van maagcontracties (vooral antrale), ontspant de pylorussfincter en de bulbus duodeni en verhoogt de peristaltiek van de twaalfvingerige darm en jejunum, wat resulteert in een versnelde maaglediging en darmtransit. Het verhoogt de rusttoon van de onderste slokdarmsfincter. Het heeft weinig of geen effect op de beweeglijkheid van de dikke darm of galblaas.
Bij patiënten met gastro-oesofageale reflux en lage LESP (lagere druk van de slokdarmsfincter), veroorzaken enkelvoudige orale doses metoclopramide dosisgerelateerde verhogingen van LESP. De effecten beginnen bij ongeveer 5 mg en nemen toe tot 20 mg (de grootste geteste dosis). De toename van LESP vanaf een dosis van 5 mg duurt ongeveer 45 minuten en die van 20 mg duurt tussen de 2 en 3 uur. Verhoogde maaglediging is waargenomen bij enkelvoudige orale doses van 10 mg.
De anti-emetische eigenschappen van metoclopramide lijken het gevolg te zijn van het antagonisme van de centrale en perifere dopaminereceptoren. Dopamine veroorzaakt misselijkheid en braken door stimulatie van de medullaire chemoreceptortriggerzone (CTZ), en metoclopramide blokkeert de stimulatie van de CTZ door middelen zoals ldopa of apomorfine waarvan bekend is dat ze de dopaminegehalten verhogen of dopamine-achtige effecten hebben. Metoclopramide maakt ook een einde aan de vertraging van de maaglediging veroorzaakt door apomorfine.
Net als de fenothiazinen en verwante geneesmiddelen, die ook dopamine-antagonisten zijn, veroorzaakt metoclopramide sedatie en kan het extrapiramidale reacties veroorzaken, hoewel deze relatief zeldzaam zijn (zie WAARSCHUWINGEN ). Metoclopramide remt de centrale en perifere effecten van apomorfine, induceert de afgifte van prolactine en veroorzaakt een voorbijgaande stijging van de circulerende aldosteronspiegels, wat in verband kan worden gebracht met voorbijgaande vochtretentie.
De farmacologische werking van metoclopramide begint 1 tot 3 minuten na een intraveneuze dosis, 10 tot 15 minuten na intramusculaire toediening en 30 tot 60 minuten na een orale dosis; farmacologische effecten houden 1 tot 2 uur aan.
Farmacokinetiek
Metoclopramide wordt snel en goed geabsorbeerd. Ten opzichte van een intraveneuze dosis van 20 mg is de absolute orale biologische beschikbaarheid van metoclopramide 80% ± 15,5%, zoals aangetoond in een cross-overonderzoek bij 18 proefpersonen. Piekplasmaconcentraties treden op ongeveer 1 tot 2 uur na een enkelvoudige orale dosis. Een vergelijkbare tijd tot piek wordt waargenomen na individuele doses bij steady-state.
In een onderzoek met een enkele dosis van 12 proefpersonen nam het gebied onder de geneesmiddelconcentratie-tijdcurve lineair toe met doses van 20 tot 100 mg. Piekconcentraties nemen lineair toe met de dosis; tijd tot piekconcentraties blijft hetzelfde; de lichaamsklaring is ongewijzigd; en het eliminatiepercentage blijft hetzelfde. De gemiddelde eliminatiehalfwaardetijd bij personen met een normale nierfunctie is 5 tot 6 uur. Lineaire kinetische processen beschrijven adequaat de absorptie en eliminatie van metoclopramide.
Ongeveer 85% van de radioactiviteit van een oraal toegediende dosis verschijnt binnen 72 uur in de urine. Van de 85% die via de urine wordt uitgescheiden, is ongeveer de helft aanwezig als vrij of geconjugeerd metoclopramide.
Het medicijn is niet uitgebreid gebonden aan plasma-eiwitten (ongeveer 30%). Het distributievolume over het hele lichaam is hoog (ongeveer 3,5 l/kg), wat wijst op een uitgebreide distributie van het geneesmiddel naar de weefsels.
Nierfunctiestoornis beïnvloedt de klaring van metoclopramide. In een onderzoek met patiënten met verschillende gradaties van nierinsufficiëntie was een verlaging van de creatinineklaring gecorreleerd met een verlaging van de plasmaklaring, renale klaring, niet-renale klaring en toename van de eliminatiehalfwaardetijd. De kinetiek van metoclopramide in aanwezigheid van nierinsufficiëntie bleef echter lineair. De verminderde klaring als gevolg van nierinsufficiëntie suggereert dat de onderhoudsdosering naar beneden moet worden bijgesteld om accumulatie van het geneesmiddel te voorkomen.
Volwassen farmacokinetische gegevens
Bij pediatrische patiënten is de farmacodynamiek van metoclopramide na orale en intraveneuze toediening zeer variabel en is er geen relatie tussen concentratie en effect vastgesteld.
Er zijn onvoldoende betrouwbare gegevens om te concluderen of de farmacokinetiek van metoclopramide bij volwassenen en de pediatrische populatie vergelijkbaar is. Hoewel er onvoldoende gegevens zijn om de werkzaamheid van metoclopramide te ondersteunen bij pediatrische patiënten met symptomatische gastro-oesofageale reflux (GER) of misselijkheid en braken door chemotherapie, is de farmacokinetiek ervan onderzocht bij deze patiëntenpopulaties.
In een open-label onderzoek kregen zes pediatrische patiënten (leeftijdscategorie 3,5 weken tot 5,4 maanden) met GER elke 6 uur metoclopramide 0,15 mg/kg drank voor 10 doses. De gemiddelde piekplasmaconcentratie van metoclopramide na de tiende dosis was 2-voudig (56,8 g/l) hoger in vergelijking met die waargenomen na de eerste dosis (29 g/l), wat wijst op accumulatie van het geneesmiddel bij herhaalde dosering. Na de tiende dosis waren de gemiddelde tijd tot het bereiken van piekconcentraties (2,2 uur), halfwaardetijd (4,1 uur), klaring (0,67 l/u/kg) en distributievolume (4,4 l/kg) van metoclopramide vergelijkbaar met die waargenomen na de eerste dosis. Bij de jongste patiënt (leeftijd 3,5 weken) was de halfwaardetijd van metoclopramide na de eerste en de tiende dosis (respectievelijk 23,1 en 10,3 uur) significant langer in vergelijking met andere zuigelingen vanwege een verminderde klaring. Dit kan worden toegeschreven aan onvolgroeide lever- en niersystemen bij de geboorte.
Eenmalige intraveneuze doses metoclopramide 0,22 tot 0,46 mg/kg (gemiddeld 0,35 mg/kg) werden gedurende 5 minuten toegediend aan 9 pediatrische kankerpatiënten die chemotherapie kregen (gemiddelde leeftijd 11,7 jaar; bereik 7 tot 14 jaar) voor profylaxe van cytotoxische opgewekt braken. De plasmaconcentraties van metoclopramide, geëxtrapoleerd naar tijd nul, varieerden van 65 tot 395 g/l (gemiddeld 152 g/l). De gemiddelde eliminatiehalfwaardetijd, klaring en distributievolume van metoclopramide waren 4,4 uur (bereik 1,7 tot 8,3 uur), 0,56 l/u/kg (bereik 0,12 tot 1,20 l/u/kg) en 3,0 l/ kg (bereik, respectievelijk 1,0 tot 4,8 L/kg).
In een ander onderzoek kregen negen pediatrische kankerpatiënten (leeftijdscategorie van 1 tot 9 jaar) 4 tot 5 intraveneuze infusies (gedurende 30 minuten) metoclopramide in een dosis van 2 mg/kg om het braken onder controle te houden. Na de laatste dosis varieerden de piekserumconcentraties van metoclopramide van 1060 tot 5680 g/l. De gemiddelde eliminatiehalfwaardetijd, klaring en distributievolume van metoclopramide waren 4,5 uur (bereik 2,0 tot 12,5 uur), 0,37 l/u/kg (bereik 0,10 tot 1,24 l/u/kg) en 1,93 l/ kg (bereik, respectievelijk 0,95 tot 5,50 L/kg).
PATIËNT INFORMATIE
REGLAN (REG-lan) (metoclopramide-tabletten) Tabletten
Lees de medicatiehandleiding die bij REGLAN wordt geleverd voordat u begint met het innemen ervan en elke keer dat u een nieuwe vulling krijgt. Mogelijk is er nieuwe informatie. Als u een ander product gebruikt dat metoclopramide bevat (zoals REGLAN 10 mg injectie, REGLAN ODT of metoclopramide drank), moet u de medicatiehandleiding lezen die bij dat product wordt geleverd. Sommige informatie kan afwijken. Deze medicatiehandleiding vervangt niet het praten met uw arts over uw medische toestand of uw behandeling.
Wat is de belangrijkste informatie die ik over REGLAN moet weten?
REGLAN kan ernstige bijwerkingen veroorzaken, waaronder:
Tardieve dyskinesie (abnormale spierbewegingen). Deze bewegingen gebeuren meestal in de gezichtsspieren. Je hebt geen controle over deze bewegingen. Ze gaan misschien niet weg, zelfs niet na het stoppen van REGLAN. Er is geen behandeling voor tardieve dyskinesie, maar de symptomen kunnen in de loop van de tijd verminderen of verdwijnen nadat u stopt met het innemen van REGLAN.
Uw kansen op het krijgen van tardieve dyskinesie gaan omhoog:
- hoe langer u REGLAN 10 mg inneemt en hoe meer REGLAN 10 mg u inneemt. U mag REGLAN 10 mg niet langer dan 12 weken gebruiken.
- als u ouder bent, vooral als u een vrouw bent
- als u suikerziekte heeft
Het is voor uw arts niet mogelijk om te weten of u tardieve dyskinesie krijgt als u REGLAN gebruikt.
Bel onmiddellijk uw arts als u bewegingen krijgt die u niet kunt stoppen of controleren, zoals:
- met je lippen smakken, kauwen of je mond tuiten
- fronsen of fronsen
- tong uitsteken
- knipperen en je ogen bewegen
- trillen van je armen en benen
Zie de rubriek "Wat zijn de mogelijke bijwerkingen van REGLAN 10 mg?" voor meer informatie over bijwerkingen.
Wat is REGLAN 10 mg?
REGLAN 10 mg is een receptgeneesmiddel dat wordt gebruikt:
- bij volwassenen gedurende 4 tot 12 weken om symptomen van brandend maagzuur te verlichten met gastro-oesofageale refluxziekte (GERD) wanneer bepaalde andere behandelingen niet werken. REGLAN verlicht brandend maagzuur en brandend maagzuur na de maaltijd. Het helpt ook zweren in de slokdarm te genezen.
- om symptomen van langzame maaglediging te verlichten bij mensen met diabetes. REGLAN helpt bij de behandeling van symptomen zoals misselijkheid, braken, brandend maagzuur, een vol gevoel lang na een maaltijd en verlies van eetlust. Niet al deze symptomen worden tegelijkertijd beter.
Het is niet bekend of REGLAN veilig is en werkt bij kinderen.
Wie mag REGLAN 10 mg niet gebruiken?
Gebruik REGLAN niet als u:
- maag- of darmproblemen heeft die met REGLAN erger kunnen worden, zoals een bloeding, verstopping of een scheur in de maag of darmwand
- een bijniertumor heeft die een feochromocytoom wordt genoemd;
- allergisch bent voor REGLAN 10 mg of iets daarin. Zie het einde van deze medicatiehandleiding voor een lijst met ingrediënten in REGLAN.
- medicijnen innemen die ongecontroleerde bewegingen kunnen veroorzaken, zoals medicijnen voor geestesziekten epileptische aanvallen hebben
Wat moet ik mijn arts vertellen voordat ik REGLAN inneem?
Vertel uw arts over al uw medische aandoeningen, ook als u:
- depressie
- ziekte van Parkinson
- hoge bloeddruk
- nierproblemen. Uw arts kan beginnen met een lagere dosis.
- leverproblemen of hartfalen. REGLAN kan ervoor zorgen dat uw lichaam vocht vasthoudt.
- suikerziekte. Uw dosis insuline moet mogelijk worden aangepast.
- borstkanker
- u zwanger bent of van plan bent zwanger te worden. Het is niet bekend of REGLAN 10 mg schadelijk is voor uw ongeboren baby.
- u geeft borstvoeding. REGLAN 10 mg kan in de moedermelk terechtkomen en kan schadelijk zijn voor uw baby. Praat met uw arts over de beste manier om uw baby te voeden als u REGLAN gebruikt.
Vertel uw arts over alle geneesmiddelen die u gebruikt, inclusief geneesmiddelen op recept en zonder recept, vitamines en kruidensupplementen. REGLAN en sommige andere geneesmiddelen kunnen met elkaar interageren en werken mogelijk niet zo goed, of veroorzaken mogelijke bijwerkingen. Start geen nieuwe geneesmiddelen terwijl u REGLAN 10 mg gebruikt totdat u met uw arts heeft gesproken.
Vertel het uw arts vooral als u:
- een ander geneesmiddel dat metoclopramide bevat, zoals REGLAN 10 mg ODT of metoclopramide drank
- een bloeddrukmedicijn
- een geneesmiddel tegen depressie, in het bijzonder een monoamineoxidaseremmer (MAOI)
- insuline
- een geneesmiddel dat u slaperig kan maken, zoals medicijnen tegen angst, slaapmiddelen en verdovende middelen.
Als u niet zeker weet of uw geneesmiddel hierboven vermeld staat, vraag het dan aan uw arts of apotheker.
Weet welke medicijnen u gebruikt. Houd er een lijst van bij en laat deze aan uw arts en apotheker zien als u een nieuw geneesmiddel krijgt.
Hoe moet ik REGLAN gebruiken?
- REGLAN 10 mg wordt geleverd als een tablet die u via de mond inneemt.
- Neem REGLAN precies in zoals uw arts u dat heeft verteld. Verander uw dosis niet tenzij uw arts u dat zegt.
- mag REGLAN niet langer dan 12 weken gebruiken.
- Als u te veel REGLAN 10 mg heeft ingenomen, neem dan onmiddellijk contact op met uw arts of het Antigifcentrum.
Wat moet ik vermijden tijdens het gebruik van REGLAN?
- Drink geen alcohol terwijl u REGLAN gebruikt. Alcohol kan sommige bijwerkingen van REGLAN 10 mg verergeren, zoals slaperigheid.
- Rijd niet, werk niet met machines of voer geen gevaarlijke taken uit totdat u weet welke invloed REGLAN op u heeft. REGLAN kan slaperigheid veroorzaken.
Wat zijn de mogelijke bijwerkingen van REGLAN?
Reglan kan ernstige bijwerkingen veroorzaken, waaronder:
- Tardieve dyskinesie (abnormale spierbewegingen). Zie "Wat is de belangrijkste informatie die ik moet weten over REGLAN?"
- Ongecontroleerde spasmen van uw gezichts- en nekspieren, of spieren van uw lichaam, armen en benen (dystonie). Deze spierspasmen kunnen abnormale bewegingen en lichaamshoudingen veroorzaken. Deze spasmen beginnen meestal binnen de eerste 2 dagen van de behandeling. Deze spasmen komen vaker voor bij kinderen en volwassenen onder de 30 jaar.
- Depressie, gedachten over zelfmoord en zelfmoord. Sommige mensen die REGLAN gebruiken, worden depressief. Je kunt gedachten hebben over jezelf pijn doen of doden. Sommige mensen die Reglan gebruiken, hebben een einde aan hun leven gemaakt (zelfmoord).
- Maligne neurolepticasyndroom (NMS). NMS is een zeer zeldzame maar zeer ernstige aandoening die kan optreden bij Reglan. NMS kan de dood veroorzaken en moet in een ziekenhuis worden behandeld. Symptomen van NMS zijn onder meer: hoge koorts, stijve spieren, problemen met denken, zeer snelle of onregelmatige hartslag en meer zweten.
- Parkinsonisme. Symptomen zijn onder meer licht beven, stijfheid van het lichaam, moeite met bewegen of het bewaren van uw evenwicht. Als u al de ziekte van Parkinson heeft, kunnen uw symptomen verergeren terwijl u REGLAN krijgt.
Bel uw arts en zoek meteen medische hulp als u:
- zich depressief voelen of gedachten hebben over zelfbeschadiging of zelfmoord
- hoge koorts, stijve spieren, problemen met denken, zeer snelle of onregelmatige hartslag en meer zweten
- spierbewegingen hebben die u niet kunt stoppen of beheersen
- spierbewegingen hebben die nieuw of ongebruikelijk zijn
Vaak voorkomende bijwerkingen van Reglan 10 mg zijn:
- zich rusteloos, slaperig, moe, duizelig of uitgeput voelen
- hoofdpijn
- verwardheid
- Moeite met slapen
U kunt meer bijwerkingen krijgen naarmate u REGLAN langer inneemt en hoe meer REGLAN u inneemt.
U kunt nog steeds bijwerkingen krijgen nadat u met REGLAN bent gestopt. U kunt symptomen krijgen van het stoppen (ontwenningsverschijnselen) van REGLAN 10 mg, zoals hoofdpijn en duizeligheid of zenuwachtigheid.
Vertel uw arts over eventuele bijwerkingen die u hinderen of die niet verdwijnen. Dit zijn niet alle mogelijke bijwerkingen van REGLAN.
Bel uw arts voor medisch advies over bijwerkingen. U kunt bijwerkingen melden aan de FDA op 1-800-FDA-1088.
Hoe moet ik REGLAN bewaren?
- Bewaar REGLAN bij kamertemperatuur tussen 20 °C en 25 °C (68 °F tot 77 °F).
- Bewaar REGLAN 10 mg in de fles waarin het wordt geleverd. Houd de fles goed gesloten.
Houd REGLAN 10 mg en alle geneesmiddelen buiten het bereik van kinderen.
Algemene informatie over REGLAN
Medicijnen worden soms voorgeschreven voor andere doeleinden dan die in een Medicatiewijzer vermeld staan. Gebruik REGLAN niet voor een aandoening waarvoor het niet is voorgeschreven. Geef REGLAN 10 mg niet aan andere mensen, ook niet als zij dezelfde symptomen hebben als u. Het kan hen schaden.
Deze medicatiehandleiding vat de belangrijkste informatie over REGLAN samen. Als u meer informatie wilt, neem dan contact op met uw arts. U kunt uw arts of apotheker om informatie vragen over REGLAN 10 mg dat is geschreven voor gezondheidswerkers. Ga voor meer informatie naar www.anipharmaceuticals.com of bel gratis op 1-800-308-6755.
Wat zijn de ingrediënten in REGLAN?
Actief ingrediënt: metoclopramide
Inactieve ingredienten :
REGLAN 10 mg tabletten : magnesiumstearaat, mannitol, microkristallijne cellulose, stearinezuur
REGLAN 5 mg tabletten: maïszetmeel, D&C geel 10 aluminiumlak, FD&C blauw 1 aluminiumlak, lactose, microkristallijne cellulose, siliciumdioxide, stearinezuur
