Proair Inhaler 100mcg Salbutamol Gebruik, bijwerkingen en dosering. Prijs in online apotheek. Generieke medicijnen zonder recept.
Wat is ProAir en hoe wordt het gebruikt?
ProAir is een receptgeneesmiddel dat wordt gebruikt voor de behandeling van de symptomen van acuut, ernstig of inspanningsastma (bronchospasme). ProAir kan alleen of in combinatie met andere medicijnen worden gebruikt.
ProAir behoort tot een klasse geneesmiddelen die PAH, PDE-5-remmers, fosfodiësterase-5-enzymremmers worden genoemd.
Het is niet bekend of ProAir veilig en effectief is bij kinderen jonger dan 4 jaar.
Wat zijn de mogelijke bijwerkingen van ProAir?
ProAir kan ernstige bijwerkingen veroorzaken, waaronder:
- piepende ademhaling,
- verstikking,
- andere ademhalingsproblemen,
- pijn op de borst,
- snelle hartslag,
- bonzende hartslagen of fladderen in uw borst,
- ernstige hoofdpijn,
- bonzen in je nek of oren,
- pijn of een branderig gevoel bij het plassen,
- verhoogde dorst,
- meer plassen,
- droge mond,
- fruitige ademgeur,
- beenkrampen,
- constipatie,
- onregelmatige hartslagen,
- verhoogde dorst of plassen,
- gevoelloosheid of tintelingen, en
- spierzwakte of slap gevoel
Roep meteen medische hulp in als u een van de bovenstaande symptomen heeft.
De meest voorkomende bijwerkingen van ProAir zijn:
- pijn op de borst,
- snelle of bonzende hartslagen,
- duizeligheid,
- zich wankel of nerveus voelen,
- hoofdpijn,
- rugpijn,
- pijn in het lichaam,
- maagklachten,
- keelpijn,
- sinuspijn, en
- loopneus of verstopte neus
Vertel het uw arts als u een bijwerking heeft die u hindert of die niet weggaat.
Dit zijn niet alle mogelijke bijwerkingen van ProAir. Vraag uw arts of apotheker om meer informatie.
Bel uw arts voor medisch advies over bijwerkingen. U kunt bijwerkingen melden aan de FDA op 1-800-FDA-1088.
OMSCHRIJVING
Het werkzame bestanddeel van ProAir HFA (albuterolsulfaat) Inhalatie-aerosol is albuterolsulfaat, een racemisch zout van albuterol. Albuterolsulfaat heeft de chemische naam α -[(tert-butylamino)methyl]-4-hydroxy-m-xyleen-α,α'-diolsulfaat (2:1) (zout) en heeft de volgende chemische structuur:
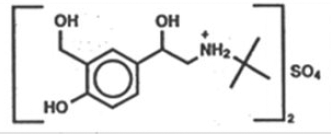
Het molecuulgewicht van albuterolsulfaat is 576,7 en de empirische formule is (C13H21NO3)2 •H2SO4. Albuterolsulfaat is een wit tot gebroken wit kristallijn poeder. Het is oplosbaar in water en slecht oplosbaar in ethanol. Albuterolsulfaat is de officiële generieke naam in de Verenigde Staten en salbutamolsulfaat is de door de Wereldgezondheidsorganisatie aanbevolen generieke naam. ProAir HFA Inhalatie-aerosol is een onder druk staande, afgemeten dosis-aërosoleenheid met een dosisteller. ProAir HFA is alleen bedoeld voor orale inhalatie. Het bevat een microkristallijne suspensie van albuterolsulfaat in drijfgas HFA-134a (1, 1, 1, 2- tetrafluorethaan) en ethanol.
Prime de inhalator voor het eerste gebruik en in gevallen waarin de inhalator meer dan 2 weken niet is gebruikt door drie verstuivingen in de lucht te verspreiden, weg van het gezicht. Na het primen levert elke activering 108 mcg albuterolsulfaat, uit het mondstuk van de actuator (equivalent aan 90 mcg albuterolbase). Elke bus levert 200 verstuivingen (inhalaties).
Dit product bevat geen chloorfluorkoolwaterstoffen (CFK's) als drijfgas.
INDICATIES
bronchospasme
PROAIR HFA-inhalatie-aerosol is geïndiceerd voor de behandeling of preventie van bronchospasmen bij patiënten van 4 jaar en ouder met reversibele obstructieve luchtwegaandoening.
Door inspanning geïnduceerde bronchospasme
PROAIR HFA-inhalatie-aerosol is geïndiceerd voor de preventie van door inspanning veroorzaakte bronchospasmen bij patiënten van 4 jaar en ouder.
DOSERING EN ADMINISTRATIE
bronchospasme
Voor de behandeling van acute episoden van bronchospasme of het voorkomen van symptomen die gepaard gaan met bronchospasme, is de gebruikelijke dosering voor volwassenen en kinderen van 4 jaar en ouder twee inhalaties die elke 4 tot 6 uur worden herhaald. Frequentere toediening of een groter aantal inhalaties wordt niet aanbevolen. Bij sommige patiënten kan één inhalatie om de 4 uur voldoende zijn.
Door inspanning geïnduceerde bronchospasme
De gebruikelijke dosering voor volwassenen en kinderen van 4 jaar of ouder is twee inhalaties 15 tot 30 minuten voor het sporten.
Administratie Informatie
Dien PROAIR HFA alleen toe via orale inhalatie. Goed schudden voor elke spray. Om het juiste gebruik van dit product te behouden en om ophoping en verstopping van medicijnen te voorkomen, is het belangrijk om de reinigingsinstructies nauwkeurig op te volgen.
Priming
Prime de inhalator voor het eerste gebruik en in gevallen waarin de inhalator meer dan 2 weken niet is gebruikt door drie verstuivingen in de lucht te verspreiden, weg van het gezicht.
Schoonmaak
Zoals bij alle HFA-bevattende albuterol-inhalatoren, is het belangrijk om het plastic mondstuk regelmatig schoon te maken om het juiste gebruik van dit product te behouden en om ophoping en verstopping van medicijnen te voorkomen. De inhalator geeft mogelijk geen medicatie meer af als het plastic mondstuk van de actuator niet goed wordt schoongemaakt en gedroogd. Reinigen: Was het plastic mondstuk met warm stromend water gedurende 30 seconden, schud overtollig water af en laat het minstens één keer per week grondig aan de lucht drogen. Als de patiënt meer dan één PROAIR HFA-inhalator heeft, moet de patiënt elk afzonderlijk wassen om te voorkomen dat de verkeerde bus op de verkeerde plastic actuator wordt bevestigd. Op deze manier weet de patiënt zeker dat hij altijd het juiste aantal resterende doses weet. Bevestig nooit een medicijnflesje van een andere inhalator aan de PROAIR HFA-actuator en bevestig de PROAIR HFA-container nooit aan een actuator van een andere inhalator. Als het mondstuk verstopt raakt, zal het wassen van het mondstuk de verstopping verwijderen. Als het nodig is om de inhalator te gebruiken voordat deze volledig droog is, schud dan overtollig water af, vervang de bus, spray tweemaal in de lucht weg van het gezicht en neem de voorgeschreven dosis. Na dergelijk gebruik moet het mondstuk opnieuw worden gewassen en moet het grondig aan de lucht worden gedroogd. [zien Door de FDA goedgekeurde etikettering van patiënten ].
Dosisteller
PROAIR HFA heeft een dosisteller die aan de actuator is bevestigd. Wanneer de patiënt de inhalator ontvangt, verschijnt er een zwarte stip in het kijkvenster totdat deze 3 keer is geprimed, waarna het nummer 200 wordt weergegeven. De dosisteller telt af elke keer dat er een spray wordt afgegeven. Wanneer de dosisteller 20 bereikt, verandert de kleur van de cijfers in rood om de patiënt eraan te herinneren om contact op te nemen met hun apotheker voor het bijvullen van medicatie of om hun arts te raadplegen voor een nieuw recept.
Wanneer de dosisteller 0 bereikt, verandert de achtergrond in ononderbroken rood. PROAIR HFA-inhalator moet worden weggegooid wanneer de dosisteller 0 aangeeft of na de vervaldatum op het product, afhankelijk van wat zich het eerst voordoet.
HOE GELEVERD
Doseringsvormen en sterke punten
PROAIR HFA is een inhalatie-aerosol. PROAIR HFA wordt geleverd als een 8,5 g/200 verstuivingen onder druk staande aluminium bus met een rode plastic actuator met een dosisteller en witte stofkap, elk in dozen van één. Elke activering levert 120 mcg albuterolsulfaat uit de busklep en 108 mcg albuterolsulfaat uit het mondstuk van de actuator (equivalent aan 90 mcg albuterolbasis).
Opslag en behandeling
PROAIR HFA (albuterolsulfaat) Inademing Aerosol wordt geleverd als een aluminium bus onder druk met een rode plastic actuator met een dosisteller en een witte stofkap, elk in dozen van één. Elke bus bevat 8,5 g van de formulering en biedt 200 verstuivingen ( NDC 59310-579-22). Elke activering levert 120 mcg albuterolsulfaat uit de busklep en 108 mcg albuterolsulfaat uit het mondstuk van de actuator (equivalent aan 90 mcg albuterolbasis).
GOED SCHUDDEN VOOR GEBRUIK. Bewaren tussen 15° en 25°C (59° en 77°F). Inhoud onder druk. Niet doorboren of verbranden. Beschermen tegen vriestemperaturen en langdurige blootstelling aan direct zonlicht. Blootstelling aan temperaturen boven 120 ° F kan barsten veroorzaken. Voor de beste resultaten moet de bus voor gebruik op kamertemperatuur zijn. Vermijd spuiten in de ogen. Buiten bereik van kinderen houden.
Zien Door de FDA goedgekeurde etikettering van patiënten voor instructies voor het vullen en reinigen.
De rode actuator die bij PROAIR HFA-inhalatie-aerosol wordt geleverd, mag niet worden gebruikt met de bus van andere inhalatie-aerosolproducten. De PROAIR HFA-inhalatie-aerosolbus mag niet worden gebruikt met de actuator van andere inhalatie-aerosolproducten.
PROAIR HFA-inhalator heeft een dosisteller die aan de actuator is bevestigd. Patiënten mogen nooit proberen de nummers voor de dosisteller te veranderen of te knoeien met het pinmechanisme in de actuator. Gooi de PROAIR HFA-inhalator weg wanneer de teller 0 aangeeft of na de vervaldatum op het product, afhankelijk van wat zich het eerst voordoet. De gelabelde hoeveelheid medicatie in elke verstuiving kan niet worden gegarandeerd nadat de teller 0 weergeeft, ook al is de canister niet helemaal leeg en zal hij blijven werken. Dompel de canister nooit onder in water om te bepalen hoe vol de canister is (“floattest”).
PROAIR HFA Inhalatie Aerosol bevat geen chloorfluorkoolwaterstoffen (CFK's) als drijfgas.
Mktd door: Teva Respiratory, LLC, Frazer, PA 19355. Mfd door: IVAX Pharmaceuticals Ireland Waterford, Ierland. Herzien: februari 2019
BIJWERKINGEN
Het gebruik van PROAIR HFA kan gepaard gaan met het volgende:
- Paradoxaal bronchospasme [zie WAARSCHUWINGEN EN VOORZORGSMAATREGELEN ]
- Cardiovasculaire effecten [zie WAARSCHUWINGEN EN VOORZORGSMAATREGELEN ]
- Onmiddellijke overgevoeligheidsreacties [zie WAARSCHUWINGEN EN VOORZORGSMAATREGELEN ]
- Hypokaliëmie [zie WAARSCHUWINGEN EN VOORZORGSMAATREGELEN ]
Ervaring met klinische proeven
In totaal werden 1090 proefpersonen behandeld met PROAIR HFA-inhalatie-aerosol, of met dezelfde formulering van albuterol als in PROAIR HFA-inhalatie-aerosol, tijdens het wereldwijde klinische ontwikkelingsprogramma.
Omdat klinische onderzoeken onder sterk uiteenlopende omstandigheden worden uitgevoerd, kunnen de bijwerkingen die in de klinische onderzoeken van een geneesmiddel zijn waargenomen niet direct worden vergeleken met de percentages in de klinische onderzoeken van een ander geneesmiddel en komen mogelijk niet overeen met de percentages die in de praktijk worden waargenomen.
Volwassenen en adolescenten van 12 jaar en ouder
De informatie over bijwerkingen in de onderstaande tabel met betrekking tot PROAIR HFA-inhalatie-aerosol is afgeleid van een 6 weken durend, geblindeerd onderzoek waarin PROAIR HFA-inhalatie-aerosol (180 mcg viermaal daags) werd vergeleken met een dubbelblinde gematchte placebo HFA-inhalatie-aerosol en een evaluator-geblindeerde op de markt gebrachte actieve comparator HFA-134a albuterol-inhalator bij 172 astmatische patiënten van 12 tot 76 jaar. De tabel geeft een overzicht van de incidentie van alle bijwerkingen (ongeacht of deze door de onderzoeker zijn gerelateerd aan het geneesmiddel of niet gerelateerd zijn aan het geneesmiddel) uit deze studie die optraden met een snelheid van 3% of meer in de PROAIR HFA-inhalatie-aerosolbehandelingsgroep en vaker in de PROAIR HFA Inhalatie Aerosol-behandelingsgroep dan in de gematchte placebogroep. Over het algemeen waren de incidentie en aard van de gemelde bijwerkingen voor PROAIR HFA-inhalatie-aerosol en de op de markt gebrachte actieve comparator HFA-134a albuterol-inhalator vergelijkbaar.
Incidentie van bijwerkingen (% van de patiënten) in een klinische studie van zes weken*
Bijwerkingen gemeld door minder dan 3% van de patiënten die PROAIR HFA-inhalatie-aerosol kregen, maar door een groter deel van de patiënten met PROAIR HFA-inhalatie-aerosol dan de gematchte placebopatiënten, die mogelijk verband houden met PROAIR HFA-inhalatie-aerosol, omvatten pijn op de borst, infectie, diarree, glossitis, accidenteel letsel (zenuwstelsel), angst, kortademigheid, ooraandoening, oorpijn en urineweginfectie.
In studies met kleine cumulatieve doses waren tremor, nervositeit en hoofdpijn de meest voorkomende bijwerkingen.
Pediatrische patiënten van 4 tot 11 jaar oud
Bijwerkingen gemeld in een pediatrisch klinisch onderzoek van 3 weken waarin dezelfde formulering van albuterol als in PROAIR HFA-inhalatie-aerosol (180 mcg albuterol viermaal daags) werd vergeleken met een overeenkomende placebo HFA-inhalatie-aerosol trad op met een lage incidentie (niet meer dan 2% in de actieve behandelingsgroep) en waren vergelijkbaar met die welke werden gezien in onderzoeken bij volwassenen en adolescenten.
Postmarketingervaring
De volgende bijwerkingen zijn vastgesteld tijdens het gebruik van PROAIR HFA na goedkeuring. Omdat deze reacties vrijwillig worden gemeld door een populatie van onbekende grootte, is het niet altijd mogelijk om op betrouwbare wijze hun frequentie te schatten of een oorzakelijk verband met blootstelling aan geneesmiddelen vast te stellen. Rapporten omvatten zeldzame gevallen van verergerde bronchospasmen, gebrek aan werkzaamheid, astma-exacerbatie (in één geval fataal gemeld), spierkrampen en verschillende orofaryngeale bijwerkingen zoals keelirritatie, veranderde smaak, glossitis, tongzweren en kokhalzen.
De volgende bijwerkingen zijn waargenomen bij het gebruik van geïnhaleerde albuterol na goedkeuring: urticaria, angio-oedeem, huiduitslag, bronchospasme, heesheid, orofaryngeaal oedeem en aritmieën (waaronder atriale fibrillatie, supraventriculaire tachycardie, extrasystolen). Bovendien kan albuterol, net als andere sympathicomimetica, bijwerkingen veroorzaken zoals: angina, hypertensie of hypotensie, hartkloppingen, stimulatie van het centrale zenuwstelsel, slapeloosheid, hoofdpijn, nervositeit, tremor, spierkrampen, uitdroging of irritatie van de orofarynx, hypokaliëmie, hyperglykemie en metabole acidose.
DRUG-INTERACTIES
Andere kortwerkende sympathicomimetische luchtwegverwijders in aërosols mogen niet gelijktijdig met PROAIR HFA-inhalatie-aerosol worden gebruikt. Als aanvullende adrenerge geneesmiddelen via welke route dan ook moeten worden toegediend, moeten deze met voorzichtigheid worden gebruikt om schadelijke cardiovasculaire effecten te voorkomen.
Bètablokkers
Bèta-adrenerge-receptorblokkers blokkeren niet alleen het pulmonale effect van bèta-agonisten, zoals PROAIR HFA-inhalatie-aerosol, maar kunnen bij astmapatiënten ernstige bronchospasmen veroorzaken. Daarom dienen patiënten met astma normaal gesproken niet met bètablokkers te worden behandeld. Onder bepaalde omstandigheden, bijvoorbeeld als profylaxe na een myocardinfarct, kunnen er echter geen aanvaardbare alternatieven zijn voor het gebruik van bèta-adrenerge blokkers bij patiënten met astma. Overweeg in deze setting cardioselectieve bètablokkers, hoewel ze met de nodige voorzichtigheid moeten worden toegediend.
diuretica
De ECG-veranderingen en/of hypokaliëmie die het gevolg kunnen zijn van de toediening van niet-kaliumsparende diuretica (zoals lis- of thiazidediuretica) kunnen acuut verergeren door bèta-agonisten, vooral wanneer de aanbevolen dosis van de bèta-agonist wordt overschreden. Hoewel de klinische significantie van deze effecten niet bekend is, is voorzichtigheid geboden bij gelijktijdige toediening van bèta-agonisten met niet-kaliumsparende diuretica. Overweeg de kaliumspiegels te controleren.
Digoxine
Gemiddelde verlagingen van 16% en 22% in serumdigoxinespiegels werden aangetoond na respectievelijk een enkelvoudige intraveneuze en orale toediening van albuterol aan normale vrijwilligers die gedurende 10 dagen digoxine hadden gekregen. De klinische betekenis van deze bevindingen voor patiënten met obstructieve luchtwegaandoeningen die chronisch albuterol en digoxine krijgen, is onduidelijk. Desalniettemin zou het verstandig zijn om de serumdigoxinespiegels zorgvuldig te evalueren bij patiënten die momenteel digoxine en PROAIR HFA-inhalatie-aerosol krijgen.
Monoamineoxidaseremmers of tricyclische antidepressiva
PROAIR HFA-inhalatie-aerosol moet met uiterste voorzichtigheid worden toegediend aan patiënten die worden behandeld met monoamineoxidaseremmers of tricyclische antidepressiva, of binnen 2 weken na stopzetting van dergelijke middelen, omdat de werking van albuterol op het cardiovasculaire systeem kan worden versterkt. Overweeg alternatieve therapie bij patiënten die MAO-remmers of tricyclische antidepressiva gebruiken.
WAARSCHUWINGEN
Inbegrepen als onderdeel van de PREVENTIEVE MAATREGELEN sectie.
PREVENTIEVE MAATREGELEN
Paradoxaal bronchospasme
PROAIR HFA Inademing Aerosol kan paradoxale bronchospasmen veroorzaken die levensbedreigend kunnen zijn. Als er paradoxale bronchospasmen optreden, moet de PROAIR HFA-inhalatie-aerosol onmiddellijk worden stopgezet en moet een alternatieve therapie worden ingesteld. Erkend moet worden dat paradoxaal bronchospasme, wanneer geassocieerd met inhalatiepreparaten, vaak optreedt bij het eerste gebruik van een nieuwe bus.
Verslechtering van astma
Astma kan acuut verslechteren over een periode van uren of chronisch over meerdere dagen of langer. Als de patiënt meer doses PROAIR HFA-inhalatie-aerosol nodig heeft dan normaal, kan dit een teken zijn van destabilisatie van astma en moet de patiënt en het behandelingsschema opnieuw worden beoordeeld, waarbij speciale aandacht moet worden besteed aan de mogelijke noodzaak van een ontstekingsremmende behandeling, bijv. corticosteroïden.
Gebruik van ontstekingsremmende middelen
Het gebruik van bèta-adrenerge-agonist-luchtwegverwijders alleen is bij veel patiënten mogelijk niet voldoende om astma onder controle te houden. Er moet in een vroeg stadium worden overwogen om ontstekingsremmende middelen, bijv. corticosteroïden, aan het therapeutische regime toe te voegen.
Cardiovasculaire effecten
PROAIR HFA-inhalatie-aerosol kan, net als andere bèta-adrenerge agonisten, bij sommige patiënten klinisch significante cardiovasculaire effecten veroorzaken, gemeten aan de hand van polsslag, bloeddruk en/of symptomen. Hoewel dergelijke effecten soms voorkomen na toediening van PROAIR HFA-inhalatie-aerosol in de aanbevolen doses, kan het nodig zijn om het geneesmiddel te staken als ze optreden. Bovendien is gemeld dat bèta-agonisten ECG-veranderingen veroorzaken, zoals afvlakking van de T-golf, verlenging van het QTc-interval en ST-segmentdepressie. De klinische betekenis van deze bevindingen is niet bekend. Daarom moet PROAIR HFA-inhalatie-aerosol, net als alle sympathomimetische amines, met voorzichtigheid worden gebruikt bij patiënten met cardiovasculaire aandoeningen, met name coronaire insufficiëntie, hartritmestoornissen en hypertensie.
Overschrijd de aanbevolen dosis niet
Er zijn sterfgevallen gemeld in verband met overmatig gebruik van sympathicomimetica via inhalatie bij patiënten met astma. De exacte doodsoorzaak is niet bekend, maar een hartstilstand als gevolg van een onverwachte ontwikkeling van een ernstige acute astmatische crisis en daaropvolgende hypoxie wordt vermoed.
Onmiddellijke overgevoeligheidsreacties
Onmiddellijke overgevoeligheidsreacties kunnen optreden na toediening van albuterolsulfaat, zoals blijkt uit zeldzame gevallen van urticaria, angio-oedeem, huiduitslag, bronchospasme, anafylaxie en orofaryngeaal oedeem. Er moet rekening worden gehouden met de mogelijkheid van overgevoeligheid bij de klinische evaluatie van patiënten die onmiddellijke overgevoeligheidsreacties ervaren tijdens het gebruik van PROAIR HFA-inhalatie-aerosol.
Naast elkaar bestaande voorwaarden
PROAIR HFA-inhalatie-aerosol moet, net als alle sympathicomimetische amines, met voorzichtigheid worden gebruikt bij patiënten met cardiovasculaire aandoeningen, met name coronaire insufficiëntie, hartritmestoornissen en hypertensie; bij patiënten met convulsieve aandoeningen, hyperthyreoïdie of diabetes mellitus; en bij patiënten die ongewoon reageren op sympathicomimetische amines. Klinisch significante veranderingen in de systolische en diastolische bloeddruk zijn waargenomen bij individuele patiënten en kunnen bij sommige patiënten worden verwacht na gebruik van een bèta-adrenerge bronchodilatator. Van hoge doses intraveneus albuterol is gemeld dat ze reeds bestaande diabetes mellitus en ketoacidose verergeren.
Hypokaliëmie
Net als bij andere bèta-agonisten kan PROAIR HFA-inhalatie-aerosol bij sommige patiënten aanzienlijke hypokaliëmie veroorzaken, mogelijk door intracellulaire shunting, wat mogelijk nadelige cardiovasculaire effecten kan veroorzaken. De afname is meestal van voorbijgaande aard en vereist geen suppletie.
Informatie over patiëntbegeleiding
Zien Door de FDA goedgekeurde etikettering van patiënten
Patiënten moeten de volgende informatie krijgen:
Gebruiksfrequentie
De werking van PROAIR HFA Inhalatie-aerosol zou 4 tot 6 uur moeten duren. Gebruik PROAIR HFA Inhalatie-aerosol niet vaker dan aanbevolen. Instrueer patiënten om de dosis of frequentie van doses PROAIR HFA-inhalatie-aerosol niet te verhogen zonder de arts te raadplegen. Als patiënten merken dat de behandeling met PROAIR HFA-inhalatie-aerosol minder effectief wordt voor symptomatische verlichting, de symptomen verergeren en/of ze het product vaker dan normaal moeten gebruiken, moeten ze onmiddellijk medische hulp inroepen.
Priming en reiniging
Priming
Primen is essentieel om te zorgen voor het juiste albuterolgehalte bij elke verstuiving. Instrueer patiënten om de inhalator voor het eerste gebruik te primen en in gevallen waarin de inhalator meer dan 2 weken niet is gebruikt, door drie verstuivingen in de lucht te verspreiden, weg van het gezicht.
Schoonmaak
Om een juiste dosering te garanderen en verstopping van de actuatoropening te voorkomen, instrueert u patiënten om het rode plastic mondstuk van de actuator ten minste eenmaal per week grondig te wassen en af te drogen. Instrueer patiënten dat als ze meer dan één PROAIR HFA-inhalator hebben, ze elke inhalator op verschillende tijdstippen moeten wassen om te voorkomen dat de verkeerde bus op de verkeerde plastic actuator wordt bevestigd. Zo weten ze zeker dat ze altijd het juiste aantal resterende doses weten. Patiënten moeten worden geïnstrueerd om nooit een bus met geneesmiddel van een andere inhalator aan de PROAIR HFA-actuator te bevestigen en de PROAIR HFA-canister nooit aan een actuator van een andere inhalator te bevestigen. Patiënten mogen de bus niet van de actuator verwijderen, behalve tijdens het reinigen, omdat er opnieuw een dosis in de lucht kan komen en de dosisteller aftelt telkens wanneer een spray wordt afgegeven. Gedetailleerde reinigingsinstructies zijn opgenomen in de geïllustreerde informatie voor de patiëntenbijsluiter.
Dosisteller
Patiënten moeten worden geïnformeerd dat PROAIR HFA een dosisteller heeft die aan de actuator is bevestigd. Wanneer de patiënt de inhalator ontvangt, verschijnt er een zwarte stip in het kijkvenster totdat deze 3 keer is geprimed, waarna het nummer 200 wordt weergegeven. De dosisteller telt af elke keer dat er een spray wordt afgegeven. Het dosistellervenster toont het aantal verstuivingen dat nog in de inhalator zit in eenheden van twee (bijv. 200, 198, 196, enz.). Wanneer de teller 20 weergeeft, verandert de kleur van de cijfers in rood om de patiënt eraan te herinneren om contact op te nemen met hun apotheker voor het bijvullen van medicatie of om hun arts te raadplegen voor een nieuw recept. Wanneer de dosisteller 0 bereikt, verandert de achtergrond in ononderbroken rood. Patiënten moeten worden geïnformeerd dat ze de PROAIR HFA-inhalator moeten weggooien wanneer de dosisteller 0 weergeeft of na de vervaldatum op het product, afhankelijk van wat zich het eerst voordoet.
Paradoxaal bronchospasme
Informeer patiënten dat PROAIR HFA-inhalatie-aerosol paradoxale bronchospasmen kan veroorzaken. Instrueer patiënten om te stoppen met PROAIR HFA-inhalatie-aerosol als paradoxale bronchospasmen optreden.
Gelijktijdig drugsgebruik
Terwijl patiënten PROAIR HFA-inhalatie-aerosol gebruiken, mogen andere inhalatiegeneesmiddelen en astmamedicatie alleen worden ingenomen zoals voorgeschreven door een arts.
Veelvoorkomende bijwerkingen
Vaak voorkomende bijwerkingen van behandeling met geïnhaleerde albuterol zijn hartkloppingen, pijn op de borst, snelle hartslag, tremor of nervositeit.
Zwangerschap
Patiënten die zwanger zijn of borstvoeding geven, dienen contact op te nemen met hun arts over het gebruik van PROAIR HFA Inhalatie-aerosol.
Er is een register voor blootstelling aan zwangerschap dat de zwangerschapsuitkomsten controleert bij vrouwen die tijdens de zwangerschap zijn blootgesteld aan astmamedicatie [zie Gebruik bij specifieke populaties ].
Algemene informatie over gebruik
Effectief en veilig gebruik van PROAIR HFA-inhalatie-aerosol omvat een begrip van de manier waarop het moet worden toegediend.
Goed schudden voor elke spray.
Gebruik PROAIR HFA-inhalatie-aerosol alleen met de actuator die bij het product is geleverd. Gooi de PROAIR HFA-inhalator weg wanneer de dosisteller 0 weergeeft of na de vervaldatum op het product, afhankelijk van wat zich het eerst voordoet. Dompel de canister nooit onder in water om te bepalen hoe vol de canister is (“float test”).
Over het algemeen is de techniek voor het toedienen van PROAIR HFA Inhalatie-aerosol aan kinderen vergelijkbaar met die voor volwassenen. Kinderen dienen PROAIR HFA-inhalatie-aerosol te gebruiken onder toezicht van een volwassene, volgens de instructies van de arts van de patiënt.
Door de FDA goedgekeurde etikettering van patiënten
Zie afscheuren geïllustreerd Informatie voor de patiënt brochure.
Niet-klinische toxicologie
Carcinogenese, mutagenese, verminderde vruchtbaarheid
In een 2 jaar durend onderzoek bij Sprague-Dawley-ratten veroorzaakte albuterolsulfaat een dosisgerelateerde toename van de incidentie van goedaardige leiomyomen van het mesovarium bij en boven een voedingsdosering van 2 mg/kg (ongeveer 15 maal en 6 maal de maximaal aanbevolen humane dagelijkse inhalatiedosis (MRHDID) voor respectievelijk volwassenen en kinderen, op basis van mg/m²). In een ander onderzoek werd dit effect geblokkeerd door gelijktijdige toediening van propranolol, een niet-selectieve bèta-adrenerge antagonist. In een 18 maanden durend onderzoek bij CD-1-muizen vertoonde albuterolsulfaat geen bewijs van tumorigeniteit bij voedingsdoses tot 500 mg/kg (respectievelijk ongeveer 1.900 keer en 740 keer de MRHDID voor volwassenen en kinderen op een mg/m² basis). In een 22 maanden durend onderzoek bij gouden hamsters vertoonde albuterolsulfaat geen bewijs van tumorigeniciteit bij dieetdoses tot 50 mg/kg (ongeveer 250 keer en 100 keer de MRHDID voor volwassenen en kinderen, respectievelijk op basis van mg/m²) .
Albuterolsulfaat was niet mutageen in de Ames-test of een mutatietest in gist. Albuterolsulfaat was niet clastogeen in een humane perifere lymfocytentest of in een AH1-stammuizenmicronucleustest.
Voortplantingsonderzoeken bij ratten hebben geen bewijs van verminderde vruchtbaarheid aangetoond bij orale doses tot 50 mg/kg (ongeveer 380 maal de MRHDID voor volwassenen op basis van mg/m²).
Gebruik bij specifieke populaties
Zwangerschap
Zwangerschapsblootstellingsregister
Er is een register voor blootstelling aan zwangerschap dat de zwangerschapsuitkomsten controleert bij vrouwen die tijdens de zwangerschap zijn blootgesteld aan astmamedicatie. Neem voor meer informatie contact op met de zwangerschapsstudies van Mothers To Baby, uitgevoerd door de Organization of Teratology Information Specialists op 1-877-311-8972 of bezoek http://mothertobaby.org/pregnancystudies/.
Risico Samenvatting
Er zijn geen gerandomiseerde klinische onderzoeken naar het gebruik van albuterol tijdens de zwangerschap. Beschikbare gegevens uit gepubliceerde epidemiologische onderzoeken en postmarketing-case-rapporten van zwangerschapsuitkomsten na gebruik van albuterol via inhalatie tonen niet consequent een risico op ernstige geboorteafwijkingen of miskraam aan. Er zijn klinische overwegingen bij het gebruik van albuterol bij zwangere vrouwen [zie: Klinische overwegingen ]. In reproductiestudies bij dieren, toen albuterolsulfaat subcutaan werd toegediend aan zwangere muizen, was er bewijs van een gespleten gehemelte bij minder dan en tot 9 keer de maximaal aanbevolen dagelijkse inhalatiedosis voor de mens (MRHDID) (zie Gegevens ].
Het geschatte achtergrondrisico van ernstige geboorteafwijkingen en miskraam voor de aangegeven populatie(s) is niet bekend. In de algemene bevolking van de VS is het geschatte risico op ernstige geboorteafwijkingen en miskraam bij klinisch erkende zwangerschappen respectievelijk 2 tot 4% en 15 tot 20%.
Klinische overwegingen
Ziekte-geassocieerd maternale en/of embryo-/foetale risico
Bij vrouwen met astma die slecht of matig onder controle is, is er een verhoogd risico op pre-eclampsie bij de moeder en vroeggeboorte, een laag geboortegewicht en een kleine zwangerschapsduur bij de pasgeborene. Zwangere vrouwen moeten nauwlettend worden gecontroleerd en de medicatie moet zo nodig worden aangepast om optimale controle te behouden.
Arbeid of levering
Vanwege het potentieel voor interferentie van bèta-agonisten met de contractiliteit van de baarmoeder, moet het gebruik van PROAIR HFA-inhalatie-aerosol voor verlichting van bronchospasme tijdens de bevalling worden beperkt tot die patiënten bij wie de voordelen duidelijk opwegen tegen het risico. PROAIR HFA-inhalatie-aerosol is niet goedgekeurd voor de behandeling van vroegtijdige bevalling. Ernstige bijwerkingen, waaronder longoedeem, zijn gemeld tijdens of na de behandeling van vroegtijdige bevalling met bèta2-agonisten, waaronder albuterol.
Gegevens
Dierlijke gegevens
In een reproductiestudie bij muizen veroorzaakte subcutaan toegediende albuterolsulfaat de vorming van gespleten gehemelte bij 5 van de 111 (4,5%) foetussen bij een blootstelling van negen tienden van de MRHDID voor volwassenen (op basis van mg/m² bij een maternale dosis van 0,25 mg/kg ) en bij 10 van de 108 (9,3%) foetussen bij ongeveer 9 keer de MRHDID (op basis van mg/m² bij een maternale dosis van 2,5 mg/kg). Soortgelijke effecten werden niet waargenomen bij ongeveer een elfde van de MRHDID voor volwassenen (op basis van mg/m² bij een maternale dosis van 0,025 mg/kg). Gespleten gehemelte kwam ook voor bij 22 van de 72 (30,5%) foetussen van vrouwen die subcutaan werden behandeld met isoproterenol (positieve controle).
In een reproductiestudie bij konijnen induceerde oraal toegediende albuterolsulfaat cranioschisis bij 7 van de 19 foetussen (37%) bij ongeveer 750 keer de MRHDID (op basis van mg/m² bij een maternale dosis van 50 mg/kg).
In een reproductiestudie bij ratten veroorzaakte een albuterolsulfaat/HFA-134a-formulering toegediend door inhalatie geen teratogene effecten bij blootstellingen van ongeveer 80 keer de MRHDID (op basis van mg/m² bij een maternale dosis van 10,5 mg/kg).
Een onderzoek waarbij zwangere ratten radioactief gelabeld albuterolsulfaat kregen toegediend, toonde aan dat geneesmiddelgerelateerd materiaal wordt overgedragen van de maternale circulatie naar de foetus.
Borstvoeding
Risico Samenvatting
Er zijn geen gegevens beschikbaar over de aanwezigheid van albuterol in moedermelk, de effecten op het kind dat borstvoeding krijgt of de effecten op de melkproductie. De plasmaspiegels van albuterol na therapeutische doses per inhalatie zijn echter laag bij de mens, en indien aanwezig in de moedermelk, heeft albuterol een lage orale biologische beschikbaarheid [zie KLINISCHE FARMACOLOGIE ].
De ontwikkelings- en gezondheidsvoordelen van borstvoeding moeten worden overwogen, samen met de klinische behoefte van de moeder aan albuterol en eventuele nadelige effecten op het kind dat borstvoeding krijgt van albuterol of van de onderliggende maternale aandoening.
Pediatrisch gebruik
De veiligheid en werkzaamheid van PROAIR HFA-inhalatie-aerosol voor de behandeling of preventie van bronchospasmen bij kinderen van 12 jaar en ouder met reversibele obstructieve luchtwegaandoening is gebaseerd op een klinisch onderzoek van 6 weken bij 116 patiënten van 12 jaar en ouder met astma ter vergelijking doses van 180 mcg viermaal daags met placebo, en één cross-over-onderzoek met een enkele dosis waarin doses van 90, 180 en 270 mcg werden vergeleken met placebo bij 58 patiënten [zie Klinische studies ]. De veiligheid en werkzaamheid van PROAIR HFA-inhalatie-aerosol voor de behandeling van door inspanning geïnduceerde bronchospasmen bij kinderen van 12 jaar en ouder is gebaseerd op een cross-over-onderzoek met een enkelvoudige dosis bij 24 volwassenen en adolescenten met door inspanning veroorzaakte bronchospasme, waarbij doses van 180 mcg werden vergeleken met placebo. [zien Klinische studies ].
De veiligheid van PROAIR HFA-inhalatie-aerosol bij kinderen van 4 tot 11 jaar is gebaseerd op een klinisch onderzoek van 3 weken bij 50 patiënten van 4 tot 11 jaar met astma, waarbij dezelfde formulering van albuterol werd gebruikt als in PROAIR HFA-inhalatie-aerosol, waarbij doses van 180 mcg viermaal daags met placebo. De werkzaamheid van PROAIR HFA-inhalatie-aerosol bij kinderen van 4 tot 11 jaar is geëxtrapoleerd uit klinische onderzoeken bij patiënten van 12 jaar en ouder met astma en door inspanning geïnduceerde bronchospasmen, op basis van gegevens uit een onderzoek met een enkele dosis waarin het bronchusverwijdende effect van PROAIR HFA 90 mcg en 180 mcg met placebo bij 55 patiënten met astma en een 3 weken durende klinische studie met dezelfde formulering van albuterol als in PROAIR HFA-inhalatie-aerosol bij 95 astmatische kinderen van 4 tot 11 jaar, waarbij een dosis van 180 mcg albuterol werd vergeleken viermaal daags met placebo [zie Klinische studies ].

De veiligheid en werkzaamheid van PROAIR HFA-inhalatie-aerosol bij pediatrische patiënten jonger dan 4 jaar zijn niet vastgesteld.
Geriatrisch gebruik
Klinische onderzoeken met PROAIR HFA-inhalatie-aerosol omvatten niet voldoende aantallen patiënten van 65 jaar en ouder om te bepalen of zij anders reageren dan jongere patiënten. Andere gerapporteerde klinische ervaringen hebben geen verschillen in respons tussen oudere en jongere patiënten aangetoond. Over het algemeen moet de dosiskeuze voor een oudere patiënt voorzichtig zijn, meestal beginnend aan het lage uiteinde van het doseringsbereik, als gevolg van de grotere frequentie van verminderde lever-, nier- of hartfunctie en van gelijktijdige ziekte of andere medicamenteuze behandeling [zie WAARSCHUWINGEN EN VOORZORGSMAATREGELEN ].
Van alle bèta-2-adrenerge agonisten, inclusief albuterol, is bekend dat ze grotendeels door de nieren worden uitgescheiden, en het risico op toxische reacties kan groter zijn bij patiënten met een verminderde nierfunctie. Omdat oudere patiënten een grotere kans hebben op een verminderde nierfunctie, moet voorzichtigheid worden betracht bij het kiezen van de dosering en kan het nuttig zijn om de nierfunctie te controleren.
OVERDOSERING
De verwachte symptomen bij overdosering zijn die van overmatige bèta-adrenerge stimulatie en/of het optreden of overdrijven van een van de symptomen vermeld onder ONGEWENSTE REACTIES, bijv. toevallen, angina, hypertensie of hypotensie, tachycardie met snelheden tot 200 slagen per minuut, aritmieën, nervositeit , hoofdpijn, tremor, droge mond, hartkloppingen, misselijkheid, duizeligheid, vermoeidheid, malaise en slapeloosheid.
Hypokaliëmie kan ook optreden. Zoals met alle sympathicomimetische medicatie, kunnen hartstilstand en zelfs overlijden in verband worden gebracht met misbruik van PROAIR HFA-inhalatie-aerosol.
De behandeling bestaat uit het staken van PROAIR HFA-inhalatie-aerosol samen met geschikte symptomatische therapie. Het oordeelkundig gebruik van een cardioselectieve bètablokker kan worden overwogen, rekening houdend met het feit dat dergelijke medicatie bronchospasmen kan veroorzaken. Er is onvoldoende bewijs om te bepalen of dialyse gunstig is voor overdosering van PROAIR HFA-inhalatie-aerosol.
De orale mediane dodelijke dosis albuterolsulfaat bij muizen is hoger dan 2.000 mg/kg (ongeveer 6.800 keer de maximaal aanbevolen dagelijkse inhalatiedosis voor volwassenen op basis van mg/m² en ongeveer 3.200 keer de maximaal aanbevolen dagelijkse inhalatiedosis voor kinderen op een mg /m² basis). Bij volwassen ratten is de subcutane mediane dodelijke dosis albuterolsulfaat ongeveer 450 mg/kg (ongeveer 3000 keer de maximaal aanbevolen dagelijkse inhalatiedosis voor volwassenen op basis van mg/m² en ongeveer 1400 keer de maximaal aanbevolen dagelijkse inhalatiedosis voor kinderen op een mg/m² basis). Bij jonge ratten is de subcutane mediane dodelijke dosis ongeveer 2.000 mg/kg (ongeveer 14.000 keer de maximaal aanbevolen dagelijkse inhalatiedosis voor volwassenen op basis van mg/m² en ongeveer 6.400 keer de maximaal aanbevolen dagelijkse inhalatiedosis voor kinderen op mg/m² basis). De mediane dodelijke dosis bij inademing is niet bepaald bij dieren.
CONTRA-INDICATIES
PROAIR HFA-inhalatie-aerosol is gecontra-indiceerd bij patiënten met een voorgeschiedenis van overgevoeligheid voor albuterol en andere PROAIR HFA-inhalatie-aerosol-componenten. Zeldzame gevallen van overgevoeligheidsreacties, waaronder urticaria, angio-oedeem en huiduitslag zijn gemeld na het gebruik van albuterolsulfaat (zie WAARSCHUWINGEN EN VOORZORGSMAATREGELEN ].
KLINISCHE FARMACOLOGIE
Werkingsmechanisme
Albuterolsulfaat is een bèta-2-adrenerge agonist. De farmacologische effecten van albuterolsulfaat zijn toe te schrijven aan activering van bèta-2-adrenerge receptoren op gladde spieren van de luchtwegen. Activering van bèta2-adrenerge receptoren leidt tot de activering van adenylcyclase en tot een verhoging van de intracellulaire concentratie van cyclisch-3',5'-adenosinemonofosfaat (cyclisch AMP). Deze toename van cyclisch AMP wordt geassocieerd met de activering van proteïnekinase A, dat op zijn beurt de fosforylering van myosine remt en de intracellulaire ionische calciumconcentraties verlaagt, wat resulteert in spierontspanning. Albuterol ontspant de gladde spieren van alle luchtwegen, van de luchtpijp tot de terminale bronchiolen. Albuterol werkt als een functionele antagonist om de luchtwegen te ontspannen, ongeacht het betrokken spasmogeen, en beschermt zo tegen alle bronchoconstrictieve uitdagingen. Verhoogde cyclische AMP-concentraties worden ook geassocieerd met de remming van de afgifte van mediatoren uit mestcellen in de luchtwegen. Hoewel wordt erkend dat bèta-2-adrenerge receptoren de belangrijkste receptoren zijn op bronchiale gladde spieren, geven gegevens aan dat er bèta-receptoren in het menselijk hart zijn, waarvan 10% tot 50% cardiale bèta-2-adrenerge receptoren zijn. De precieze functie van deze receptoren is niet vastgesteld [zie WAARSCHUWINGEN EN VOORZORGSMAATREGELEN ].
In de meeste gecontroleerde klinische onderzoeken is aangetoond dat albuterol meer effect heeft op de luchtwegen, in de vorm van bronchiale gladde spierontspanning, dan isoproterenol bij vergelijkbare doses, terwijl het minder cardiovasculaire effecten veroorzaakt. Echter, geïnhaleerde albuterol kan, net als andere bèta-adrenerge agonisten, bij sommige patiënten een significant cardiovasculair effect veroorzaken, zoals gemeten aan de hand van polsslag, bloeddruk, symptomen en/of elektrocardiografische veranderingen [zie WAARSCHUWINGEN EN VOORZORGSMAATREGELEN ].
Farmacokinetiek
De systemische niveaus van albuterol zijn laag na inhalatie van de aanbevolen doses. In een cross-overstudie uitgevoerd bij gezonde mannelijke en vrouwelijke vrijwilligers, gaven hoge cumulatieve doses PROAIR HFA-inhalatie-aerosol (1.080 mcg albuterolbase toegediend gedurende één uur) gemiddelde piekplasmaconcentraties (Cmax) en systemische blootstelling (AUCinf) van ongeveer 4.100 pg/ ml en 28.426 pg/ml*uur, vergeleken met respectievelijk ongeveer 3.900 pg/ml en 28.395 pg/ml*uur na dezelfde dosis van een actieve HFA-134a-albuterol-inhalator-comparator. De terminale plasmahalfwaardetijd van albuterol geleverd door PROAIR HFA-inhalatie-aerosol was ongeveer 6 uur. Vergelijking van de farmacokinetische parameters toonde geen verschillen tussen de producten.
Het farmacokinetische profiel van PROAIR HFA-inhalatie-aerosol werd geëvalueerd in een tweerichtings cross-over-onderzoek bij 11 gezonde pediatrische vrijwilligers in de leeftijd van 4 tot 11 jaar. Een enkelvoudige toediening van PROAIR HFA-inhalatie-aerosol (180 mcg albuterolbase) leverde een kleinste-kwadratengemiddelde (SE) Cmax en AUC0-∞ op van respectievelijk 1.100 (1,18) pg/ml en 5.120 (1,15) pg/ml*uur. De kleinste-kwadratengemiddelde (SE) terminale plasmahalfwaardetijd van albuterol geleverd door PROAIR HFA-inhalatie-aerosol was 166 (7,8) minuten.
Metabolisme en eliminatie
Informatie beschikbaar in de gepubliceerde literatuur suggereert dat het primaire enzym dat verantwoordelijk is voor het metabolisme van albuterol bij mensen SULTIA3 (sulfotransferase) is. Wanneer racemisch albuterol intraveneus of via inhalatie werd toegediend na orale toediening van houtskool, was er een 3- tot 4-voudig verschil in het gebied onder de concentratie-tijdcurves tussen de (R)- en (S)albuterol-enantiomeren, met (S) )-albuterolconcentraties constant hoger. Zonder voorbehandeling met houtskool waren de verschillen echter 8- tot 24-voudig, wat suggereert dat de (R)-albuterol bij voorkeur wordt gemetaboliseerd in het maagdarmkanaal, vermoedelijk door SULTIA3.
De primaire eliminatieroute van albuterol is via renale excretie (80% tot 100%) van ofwel de moederverbinding ofwel de primaire metaboliet. Minder dan 20% van het medicijn wordt gedetecteerd in de ontlasting. Na intraveneuze toediening van racemisch albuterol werd tussen 25% en 46% van de (R)-albuterolfractie van de dosis als onveranderd (R)-albuterol uitgescheiden in de urine.
Geriatrische, pediatrische, lever-/nierfunctiestoornissen
Er zijn geen farmacokinetische onderzoeken uitgevoerd voor PROAIR HFA-inhalatie-aerosol bij pasgeborenen of oudere proefpersonen.
Het effect van leverinsufficiëntie op de farmacokinetiek van PROAIR HFA-inhalatie-aerosol is niet geëvalueerd.
Het effect van nierinsufficiëntie op de farmacokinetiek van albuterol werd geëvalueerd bij 5 proefpersonen met een creatinineklaring van 7 tot 53 ml/min, en de resultaten werden vergeleken met die van gezonde vrijwilligers. Nierziekte had geen effect op de halfwaardetijd, maar er was een afname van 67% in de klaring van albuterol. Voorzichtigheid is geboden bij het toedienen van hoge doses PROAIR HFA-inhalatie-aerosol aan patiënten met nierinsufficiëntie [zie: Gebruik bij specifieke populaties ].
Dierlijke toxicologie en/of farmacologie
preklinisch
Intraveneuze studies bij ratten met albuterolsulfaat hebben aangetoond dat albuterol de bloed-hersenbarrière passeert en hersenconcentraties bereikt die ongeveer 5% van de plasmaconcentraties bedragen. In structuren buiten de bloed-hersenbarrière (pijnappelklier en hypofyse) bleken de albuterolconcentraties 100 keer zo hoog te zijn als die in de hele hersenen.
Studies bij laboratoriumdieren (minivarkens, knaagdieren en honden) hebben het optreden van hartritmestoornissen en plotselinge dood (met histologisch bewijs van myocardiale necrose) aangetoond wanneer β-agonisten en methylxanthinen gelijktijdig werden toegediend. De klinische betekenis van deze bevindingen is niet bekend.
Drijfgas HFA-134a heeft geen farmacologische activiteit, behalve bij zeer hoge doses bij dieren (380 - 1300 maal de maximale blootstelling bij de mens op basis van vergelijkingen van AUC-waarden), en veroorzaakt voornamelijk ataxie, tremoren, kortademigheid of speekselvloed. Deze zijn vergelijkbaar met effecten die worden geproduceerd door de structureel verwante chloorfluorkoolwaterstoffen (CFK's), die op grote schaal zijn gebruikt in inhalatoren voor afgemeten doses.
Bij dieren en mensen bleek drijfgas HFA-134a snel te worden geabsorbeerd en snel geëlimineerd, met een eliminatiehalfwaardetijd van 3-27 minuten bij dieren en 5-7 minuten bij mensen. De tijd tot de maximale plasmaconcentratie (Tmax) en de gemiddelde verblijftijd zijn beide extreem kort, wat leidt tot een voorbijgaande verschijning van HFA-134a in het bloed zonder bewijs van accumulatie.
Klinische studies
Bronchospasme geassocieerd met astma
Volwassen en adolescente patiënten van 12 jaar en ouder
In een 6 weken durende, gerandomiseerde, dubbelblinde, placebogecontroleerde studie werd PROAIR HFA-inhalatie-aerosol (58 patiënten) vergeleken met een gematchte placebo-HFA-inhalatie-aerosol (58 patiënten) bij astmatische patiënten van 12 tot 76 jaar oud bij een dosis van 180 mcg albuterol viermaal daags. Een evaluator-blind op de markt gebrachte actieve comparator HFA-134a albuterol-inhalator-arm (56 patiënten) werd opgenomen.
Seriële FEV1-metingen, hieronder weergegeven als procentuele verandering ten opzichte van de basislijn van de testdag op dag 1 en op dag 43, toonden aan dat twee inhalaties van PROAIR HFA-inhalatie-aerosol een significant grotere verbetering in FEV1 opleverden ten opzichte van de waarde voor de behandeling dan de overeenkomende placebo, evenals een vergelijkbaar bronchusverwijdend effect als de op de markt gebrachte actieve comparator HFA-134a albuterol-inhalator.
FEV1 als gemiddelde procentuele verandering ten opzichte van de testdag vóór de dosis in een 6 weken durende klinische proef Dag 1
PATIËNT INFORMATIE
PROAIR® HFA (pro'ar) (albuterolsulfaat) Inademing Aerosol
Lees deze patiënteninformatie voordat u PROAIR HFA gaat gebruiken en elke keer dat u een nieuwe vulling krijgt. Mogelijk is er nieuwe informatie. Deze informatie vervangt niet het praten met uw arts over uw medische toestand of uw behandeling.
Wat is PROAIR HFA?
PROAIR HFA is een receptgeneesmiddel dat wordt gebruikt bij mensen van 4 jaar en ouder om:
- behandelen of voorkomen van bronchospasmen bij mensen met een reversibele obstructieve luchtwegaandoening
- door inspanning veroorzaakte bronchospasmen voorkomen
Het is niet bekend of PROAIR HFA veilig en effectief is bij kinderen jonger dan 4 jaar.
Wie mag PROAIR HFA niet gebruiken?
Gebruik PROAIR HFA niet als u: zijn allergisch voor albuterolsulfaat of voor één van de ingrediënten in PROAIR HFA. Zie het einde van deze bijsluiter voor een volledige lijst van ingrediënten in PROAIR HFA.
Wat moet ik mijn arts vertellen voordat ik PROAIR HFA gebruik?
Vertel uw arts voordat u PROAIR HFA gebruikt als u:
- hartproblemen hebben
- hoge bloeddruk hebben (hypertensie)
- stuiptrekkingen hebben (toevallen)
- schildklierproblemen hebben
- diabetes hebben
- een laag kaliumgehalte in uw bloed heeft
- zwanger bent of van plan bent zwanger te worden. Het is niet bekend of PROAIR HFA schadelijk is voor uw ongeboren baby. Neem contact op met uw arts als u zwanger bent of van plan bent zwanger te worden.
- borstvoeding geeft of van plan bent borstvoeding te geven. Het is niet bekend of PROAIR HFA in uw moedermelk terechtkomt. Praat met uw arts over de beste manier om uw baby te voeden als u PROAIR HFA gebruikt.
Vertel uw arts over alle medicijnen die u gebruikt, waaronder geneesmiddelen op recept en zonder recept, vitamines en kruidensupplementen.
PROAIR HFA en andere geneesmiddelen kunnen elkaar beïnvloeden en bijwerkingen veroorzaken. PROAIR HFA kan de werking van andere geneesmiddelen beïnvloeden en andere geneesmiddelen kunnen de werking van PROAIR HFA beïnvloeden.
Vertel het uw arts vooral als u:
- andere geneesmiddelen voor inhalatie of astmamedicijnen
- bètablokker medicijnen
- diuretica
- digoxine
- monoamineoxidaseremmers
- tricyclische antidepressiva
Vraag uw arts of apotheker om een lijst van deze geneesmiddelen als u het niet zeker weet.
Weet welke medicijnen u gebruikt. Houd er een lijst van bij om uw arts en apotheker te laten zien wanneer u een nieuw geneesmiddel krijgt.
Hoe moet ik PROAIR HFA gebruiken?
- Voor gedetailleerde instructies, zie "Gebruiksaanwijzing" aan het einde van deze patiëntinformatie.
- Gebruik PROAIR HFA precies zoals uw arts u heeft verteld om het te gebruiken.
- Als uw kind PROAIR HFA moet gebruiken, let dan goed op uw kind om er zeker van te zijn dat uw kind de inhalator correct gebruikt. Uw arts zal u laten zien hoe uw kind PROAIR HFA moet gebruiken.
- Elke dosis PROAIR HFA moet maximaal 4 uur tot 6 uur duren.
- Niet doen verhoog uw dosis of neem extra doses PROAIR HFA in zonder eerst met uw arts te overleggen.
- Roep meteen medische hulp in als PROAIR HFA uw symptomen niet langer helpt.
- Roep meteen medische hulp in als uw symptomen verergeren of als u uw inhalator vaker moet gebruiken.
- Terwijl u PROAIR HFA gebruikt, mag u geen andere noodmedicatie voor inhalatie en astmamedicatie gebruiken, tenzij uw arts u dat zegt.
- Bel uw arts als uw astmasymptomen zoals piepende ademhaling en moeite met ademhalen over een paar uur of dagen erger worden. Het kan zijn dat uw arts u een ander geneesmiddel moet geven (bijvoorbeeld corticosteroïden) om uw symptomen te behandelen.
Wat zijn de mogelijke bijwerkingen van PROAIR HFA?
PROAIR HFA kan ernstige bijwerkingen veroorzaken, waaronder:
- verergering van ademhalingsproblemen, hoesten en piepende ademhaling (paradoxale bronchospasme). Als dit gebeurt, stop dan met het gebruik van PROAIR HFA en bel uw arts of schakel onmiddellijk noodhulp in. Paradoxaal bronchospasme is waarschijnlijker bij uw eerste gebruik van een nieuwe bus met geneesmiddel.
- hartproblemen, waaronder een snellere hartslag en een hogere bloeddruk
- mogelijk overlijden bij mensen met astma die te veel PROAIR HFA . gebruiken
- allergische reacties. Bel onmiddellijk uw arts als u de volgende symptomen van een allergische reactie heeft:
- Jeukende huid
- zwelling onder uw huid of in uw keel
- uitslag
- verergering van moeite met ademhalen
- lage kaliumspiegels in uw bloed
- verergering van andere medische problemen bij mensen die ook PROAIR HFA gebruiken, waaronder verhogingen van de bloedsuikerspiegel
De meest voorkomende bijwerkingen van PROAIR HFA zijn:
- je hart voelt alsof het bonkt of bonst (hartkloppingen)
- pijn op de borst
- snelle hartslag
- beverigheid
- nervositeit
- hoofdpijn
- duizeligheid
- keelpijn
- loopneus
Vertel het uw arts als u een bijwerking heeft die u hindert of die niet weggaat.
Dit zijn niet alle mogelijke bijwerkingen van PROAIR HFA. Vraag uw arts of apotheker om meer informatie.
Bel uw arts voor medisch advies over bijwerkingen. U kunt bijwerkingen melden aan de FDA op 1-800-FDA-1088.
Hoe moet ik PROAIR HFA bewaren?
- Bewaar PROAIR HFA bij kamertemperatuur tussen 59 ° F en 77 ° F (15 ° C en 25 ° C).
- Vermijd blootstelling aan extreme hitte en kou.
- Schud de PROAIR HFA-bus goed voor gebruik.
- Niet doen de PROAIR HFA-bus doorprikken.
- Niet doen bewaar de PROAIR HFA-bus in de buurt van hitte of een vlam. Temperaturen boven 120 ° F kunnen ervoor zorgen dat de bus barst.
- Niet doen gooi de PROAIR HFA-bus in het vuur of in een verbrandingsoven.
- Vermijd het spuiten van PROAIR HFA in uw ogen.
Houd PROAIR HFA en alle geneesmiddelen buiten het bereik van kinderen.
Algemene informatie over het veilige en effectieve gebruik van PROAIR HFA
Medicijnen worden soms voorgeschreven voor andere doeleinden dan die in een Medicatiewijzer vermeld staan. Gebruik PROAIR HFA niet voor een aandoening waarvoor het niet is voorgeschreven. Geef PROAIR HFA niet aan andere mensen, ook niet als zij dezelfde symptomen hebben als u. Het kan hen schaden.
Deze patiëntinformatie vat de belangrijkste informatie over PROAIR HFA samen. Als u meer informatie wilt, neem dan contact op met uw arts. U kunt uw apotheker of arts om informatie vragen over PROAIR HFA die is geschreven voor gezondheidswerkers.
Ga voor meer informatie naar www.ProAirHFA.com of bel 1-888-482-9522.
Wat zijn de ingrediënten in PROAIR HFA?
Actief bestanddeel: albuterolsulfaat
Inactieve ingrediënten: drijfgas HFA-134a en ethanol.
Gebruiksaanwijzing
PROAIR® HFA (pro'ar) (albuterolsulfaat) Inademing Aerosol
Lees deze gebruiksaanwijzing voordat u PROAIR HFA gaat gebruiken en elke keer dat u een navulling krijgt. Mogelijk is er nieuwe informatie. Deze informatie vervangt niet het praten met uw arts over uw medische toestand of uw behandeling.
De onderdelen van uw PROAIR HFA-inhalator:
Er zijn 2 hoofdonderdelen van uw PROAIR HFA-inhalator, waaronder een:
- rode plastic actuator die het medicijn uit de bus spuit. Zie afbeelding A.
- beschermende stofkap die het mondstuk van de actuator bedekt. Zie afbeelding A.
Er is ook een metalen bus die het medicijn bevat. Zie afbeelding A.
Er is ook een dosisteller bevestigd aan de achterkant van de actuator met een kijkvenster dat u laat zien hoeveel verstuivingen geneesmiddel u nog hebt. Zie afbeelding B.
U ziet een zwarte stip in het kijkvenster op de actuator totdat het apparaat 3 keer is geprimed. Zie Afbeelding B en "Uw PROAIR HFA-apparaat voorbereiden" hieronder.
Afbeelding A en Afbeelding B 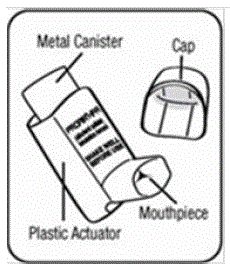
- Niet doen gebruik de PROAIR HFA-actuator met een medicijnflesje uit een andere inhalator.
- Niet doen gebruik een PROAIR HFA-bus met een actuator van een andere inhalator, inclusief een andere PROAIR HFA-inhalator.
Uw PROAIR HFA-apparaat voorbereiden:
Uw PROAIR-apparaat moet worden geprimed voordat u het voor de eerste keer gebruikt of als uw apparaat meer dan 14 dagen achter elkaar niet is gebruikt. Niet doen prime uw PROAIR HFA-apparaat elke dag.
- Haal uw PROAIR HFA-apparaat uit de verpakking.
- Verwijder de beschermende stofkap van het mondstuk.
- Schud de inhalator goed en spuit hem in de lucht, weg van uw gezicht. Zie afbeelding C.
Figuur C 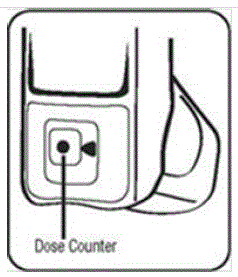
- Schud en spuit de inhalator nog 2 keer op deze manier om het vullen te voltooien. De dosisteller op de actuator moet het nummer 200 weergeven nadat u de actuator voor de eerste keer hebt gevuld. Zie afbeelding D.
Figuur D 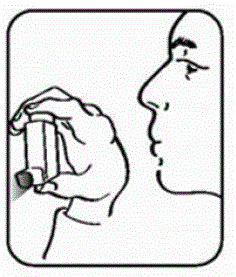
Elke keer dat u uw PROAIR HFA-apparaat gebruikt:
- Zorg ervoor dat de bus stevig in de plastic actuator past.
- Kijk in het mondstuk om er zeker van te zijn dat er geen vreemde voorwerpen zijn, vooral als de dop niet is gebruikt om het mondstuk af te dekken.
De dosisteller op uw PROAIR HFA-actuator aflezen
- De dosisteller telt af elke keer dat er een spray wordt afgegeven. Het dosistellervenster toont het aantal verstuivingen dat nog in uw inhalator zit in eenheden van 2 verstuivingen. Er zijn bijvoorbeeld nog 190 verstuivingen over als de pijl precies tegenover het getal 190 staat, of 189 verstuivingen als de pijl tussen 190 en 188 wijst. Zie figuur D.
- Wanneer de dosisteller 0 bereikt, blijft deze 0 aangeven en moet u uw PROAIR HFA-apparaat vervangen.
- De dosisteller kan niet worden gereset en is permanent aan de actuator bevestigd. Verander nooit de nummers voor de dosisteller en raak de pin in de actuator nooit aan.
- Niet doen verwijder de bus van de plastic actuator, behalve tijdens het reinigen. Als u de bus weer aan de actuator bevestigt, kan er per ongeluk een dosis PROAIR HFA in de lucht komen. De dosisteller telt af elke keer dat er een spray wordt afgegeven.
Uw PROAIR HFA-apparaat gebruiken:
Stap 1. Schud de inhalator goed voor elke verstuiving. Neem de dop van het mondstuk van de actuator.
Stap 2. Houd de inhalator vast met het mondstuk naar beneden. Zie afbeelding E.
Figuur E 
Stap 3. Adem uit door je mond en duw zoveel mogelijk lucht uit je longen als je kunt. Plaats het mondstuk in uw mond en sluit uw lippen eromheen. Zie afbeelding F.
Stap 4. Duw de bovenkant van de bus helemaal naar beneden terwijl u diep en langzaam door uw mond inademt. Zie afbeelding F.
Figuur F 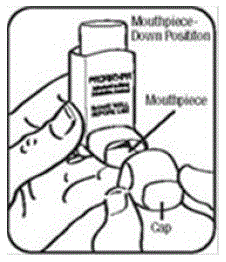
Stap 5. Direct nadat de spray naar buiten komt, haal je je vinger van de bus. Nadat u helemaal heeft ingeademd, haalt u de inhalator uit uw mond en sluit u uw mond.
Stap 6. Houd je adem in zo lang als je kunt, tot 10 seconden, adem dan normaal.
Als uw arts u heeft gezegd meer sprays te gebruiken, wacht 1 minuut en schud de inhalator opnieuw. Herhaal stap 2 tot en met stap 6.
Stap 7. Plaats de dop terug op het mondstuk na elke keer dat u de inhalator gebruikt. Zorg ervoor dat de dop stevig op zijn plaats klikt.
Uw PROAIR HFA-apparaat reinigen:
Het is erg belangrijk om de plastic actuator schoon te houden, zodat het geneesmiddel zich niet ophoopt en de spray blokkeert. Zie afbeelding G en afbeelding H.
Figuur G en Figuur H 
- Probeer de metalen bus niet schoon te maken of nat te maken. De inhalator kan stoppen met spuiten als deze niet goed wordt schoongemaakt.
- Als u meer dan 1 PROAIR HFA-inhalator heeft, was dan elk apparaat op verschillende tijdstippen om te voorkomen dat u de verkeerde bus samen met de verkeerde plastic actuator plaatst. Zo weet u zeker dat u altijd het juiste aantal resterende doses PROAIR HFA weet.
- Was de actuator minimaal 1 keer per week als volgt:
- Haal de bus uit de actuator en verwijder de dop van het mondstuk.
- Houd de actuator onder de kraan en laat er ongeveer 30 seconden warm water doorheen lopen. Zie afbeelding I.
Figuur I 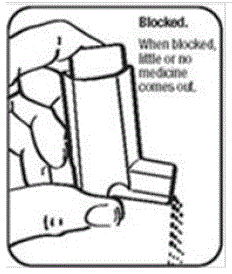
- Draai de actuator ondersteboven en laat ongeveer 30 seconden warm water door het mondstuk lopen. Zie figuur J.
figuur J 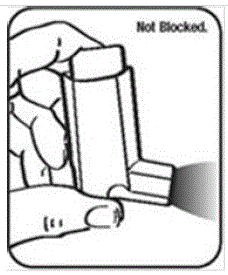
- Schud zoveel mogelijk water van de actuator af. Kijk in het mondstuk om er zeker van te zijn dat de ophoping van medicijnen volledig is weggespoeld. Als er aanslag is, herhaal dan de wasinstructies.
- Laat de actuator volledig aan de lucht drogen, bijvoorbeeld 's nachts. Zie figuur K.
figuur K 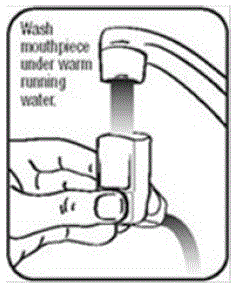
- Als de actuator droog is, plaatst u de bus in de actuator en zorgt u ervoor dat deze stevig vastzit. Schud de inhalator goed en spuit hem twee keer in de lucht, weg van je gezicht. Plaats de dop terug op het mondstuk.
Als u uw inhalator moet gebruiken voordat de actuator volledig droog is:
- Schud zoveel mogelijk water van de actuator.
- Plaats de bus in de actuator en zorg ervoor dat deze stevig vastzit.
- Schud de inhalator goed en spuit hem twee keer in de lucht, weg van je gezicht.
- Neem uw PROAIR HFA-dosis zoals voorgeschreven.
- Volg de reinigingsinstructies hierboven.
Uw PROAIR HFA-apparaat vervangen
- Als de dosisteller op de actuator het getal 20 aangeeft, de kleur van de cijfers verandert in rood. De rode cijfers zijn bedoeld om u eraan te herinneren dat u uw recept moet aanvullen of uw arts om een ander recept voor PROAIR HFA moet vragen. Wanneer de dosisteller 0 bereikt, verandert de achtergrondkleur in effen rood.
- Gooi de PROAIR HFA-inhalator weg zodra de dosisteller 0 aangeeft of na de vervaldatum op de PROAIR HFA-verpakking, afhankelijk van wat zich het eerst voordoet. U mag de inhalator na 200 verstuivingen niet blijven gebruiken, ook al is de bus misschien niet helemaal leeg. U kunt er niet zeker van zijn dat u een geneesmiddel krijgt na het gebruik van 200 verstuivingen.
- Gebruik de inhalator niet na de vervaldatum op de PROAIR HFA-verpakking.
Deze patiënteninformatie en gebruiksaanwijzing zijn goedgekeurd door de Amerikaanse Food and Drug Administration.
