Plavix 75mg Clopidogrel Gebruik, bijwerkingen en dosering. Prijs in online apotheek. Generieke medicijnen zonder recept.
Wat is Plavix 75 mg en hoe wordt het gebruikt?
Plavix 75 mg is een receptgeneesmiddel dat wordt gebruikt voor de behandeling van de symptomen van acuut coronair syndroom, zoals een beroerte, bloedstolsel of ernstige hartproblemen na een hartaanval, ernstige pijn op de borst of problemen met de bloedsomloop. Plavix 75 mg kan alleen of in combinatie met andere medicijnen worden gebruikt.
Plavix 75 mg behoort tot een klasse geneesmiddelen die bloedplaatjesaggregatieremmers, cardiovasculaire middelen, bloedplaatjesaggregatieremmers en hematologische middelen worden genoemd.
Het is niet bekend of Plavix veilig en effectief is bij kinderen.
Wat zijn de mogelijke bijwerkingen van Plavix 75 mg?
Plavix 75 mg kan ernstige bijwerkingen veroorzaken, waaronder:
- bleke huid,
- gemakkelijk blauwe plekken,
- paarse vlekken onder je huid of in je mond,
- geel worden van uw huid of ogen (geelzucht),
- snelle hartslagen,
- kortademigheid,
- hoofdpijn,
- koorts,
- zwakheid,
- zich moe voelen,
- weinig of geen plassen,
- toevallen (convulsies),
- plotselinge gevoelloosheid of zwakte,
- verwarring, en
- problemen met zicht of spraak
Roep meteen medische hulp in als u een van de bovenstaande symptomen heeft.
De meest voorkomende bijwerkingen van Plavix zijn:
- verhoogde bloeding,
- neusbloedingen,
- hoofdpijn,
- jeuk, en
- blauwe plekken
WAARSCHUWING
VERMINDERD ANTIPLETEN-EFFECT BIJ PATINTEN MET TWEE FUNCTIEVERLIES ALLELEN VAN HET CYP2C19-GEN
De werkzaamheid van Plavix 75 mg is het resultaat van zijn antibloedplaatjesactiviteit, die afhankelijk is van de omzetting in een actieve metaboliet door het cytochroom P450 (CYP) -systeem, voornamelijk CYP2C19 [zie WAARSCHUWINGEN EN VOORZORGSMAATREGELEN , KLINISCHE FARMACOLOGIE ]. Plavix vormt in de aanbevolen doseringen minder van de actieve metaboliet en heeft dus een verminderd effect op de bloedplaatjesactiviteit bij patiënten die homozygoot zijn voor niet-functionele allelen van het CYP2C19-gen (de zogenaamde "CYP2C19-slechte metaboliseerders"). Er zijn tests beschikbaar om patiënten te identificeren die CYP2C19-slechte metaboliseerders zijn [zie: KLINISCHE FARMACOLOGIE ]. Overweeg het gebruik van een andere P2Y12-remmer van bloedplaatjes bij patiënten die zijn geïdentificeerd als trage CYP2C19-metaboliseerders.
OMSCHRIJVING
Plavix (clopidogrelbisulfaat) is een thienopyridineklasse-remmer van P2Y12 ADP-bloedplaatjesreceptoren. Chemisch gezien is het methyl (+)-(S)-α-(2-chloorfenyl)-6,7-dihydrothieno[3,2-c]pyridine-5(4H)-acetaatsulfaat (1:1). De empirische formule van clopidogrelbisulfaat is C16H16ClNO2S•H2SO4 en het molecuulgewicht is 419,9. De structuurformule is als volgt:

Clopidogrelbisulfaat is een wit tot gebroken wit poeder. Het is praktisch onoplosbaar in water bij neutrale pH maar vrij oplosbaar bij pH 1. Het lost ook vrij op in methanol, lost spaarzaam op in methyleenchloride en is praktisch onoplosbaar in ethylether. Het heeft een specifieke optische rotatie van ongeveer +56°.
Plavix voor orale toediening wordt geleverd als roze, ronde, biconvexe filmomhulde tabletten met inscriptie die 97,875 mg clopidogrelbisulfaat bevatten, wat het molaire equivalent is van 75 mg clopidogrel-basis, of roze, langwerpige filmomhulde tabletten met inscriptie die 391,5 mg bevat. clopidogrelbisulfaat, wat het molaire equivalent is van 300 mg clopidogrelbase.
Elke tablet bevat gehydrogeneerde ricinusolie, hydroxypropylcellulose, mannitol, microkristallijne cellulose en polyethyleenglycol 6000 als inactieve ingrediënten. De roze filmomhulling bevat ijzeroxide, hypromellose 2910, lactosemonohydraat, titaniumdioxide en triacetine. De tabletten zijn gepolijst met Carnaubawas.
INDICATIES
Acuut coronair syndroom (ACS)
- Plavix 75 mg is geïndiceerd om de frequentie van myocardinfarct (MI) en beroerte te verlagen bij patiënten met niet-ST-segmentstijging ACS (instabiele angina [UA]/niet-ST-elevatie myocardinfarct [NSTEMI]), inclusief patiënten die medisch moeten worden behandeld en degenen die moeten worden behandeld met coronaire revascularisatie. Plavix 75 mg moet worden toegediend in combinatie met aspirine.
- Plavix is geïndiceerd om de frequentie van myocardinfarct en beroerte te verlagen bij patiënten met een acuut ST-elevatie myocardinfarct (STEMI) die medisch moeten worden behandeld. Plavix 75 mg moet worden toegediend in combinatie met aspirine.
Recent MI, recente beroerte of vastgestelde perifere arteriële ziekte
Bij patiënten met vastgestelde perifere arteriële ziekte of met een voorgeschiedenis van recent myocardinfarct (MI) of recente beroerte is Plavix 75 mg geïndiceerd om het aantal MI en beroerte te verminderen.
DOSERING EN ADMINISTRATIE
Acute kransslagader syndroom
Bij patiënten die binnen enkele uren een antibloedplaatjeseffect nodig hebben, start u Plavix met een eenmalige orale oplaaddosis van 300 mg en gaat u verder met 75 mg eenmaal daags. Het starten van Plavix 75 mg zonder oplaaddosis zal het optreden van een antibloedplaatjeseffect met enkele dagen vertragen [zie KLINISCHE FARMACOLOGIE en Klinische studies ].
Recent MI, recente beroerte of vastgestelde perifere arteriële ziekte
75 mg eenmaal daags oraal zonder oplaaddosis [zie KLINISCHE FARMACOLOGIE en Klinische studies ].
HOE GELEVERD
Doseringsvormen en sterke punten
- 75 mg tabletten: roze, ronde, biconvexe, filmomhulde tabletten met de inscriptie "75" aan de ene kant en "1171" aan de andere kant
- 300 mg tabletten: roze, langwerpige, filmomhulde tabletten met de inscriptie "300" aan de ene kant en "1332" aan de andere kant
Opslag en behandeling
Plavix (clopidogrelbisulfaat) 75 mg tabletten zijn verkrijgbaar als roze, ronde, biconvexe, filmomhulde tabletten met de inscriptie “75” aan de ene kant en “1171” aan de andere. Tabletten worden als volgt geleverd:
NDC 63653-1171-6 Flessen van 30 NDC 63653-1171-1 Flessen van 90 NDC 63653-1171-5 Flessen van 500 NDC 63653-1171-3 Blaren van 100
Plavix (clopidogrelbisulfaat) 300 mg tabletten zijn verkrijgbaar als roze, langwerpige, filmomhulde tabletten met de inscriptie “300” aan de ene kant en “1332” aan de andere. Tabletten worden als volgt geleverd:
NDC 63653-1332-2 Eenheidsdosisverpakkingen van 30
Bewaren bij 25°C (77°F); excursies toegestaan tot 15°C-30°C (59°F-86°F) [zie USP-gecontroleerde kamertemperatuur ].
Gedistribueerd door: Bristol-Myers Squibb/Sanofi Pharmaceuticals Partnership, Bridgewater, NJ 08807. Herzien: maart 2021
BIJWERKINGEN
De volgende ernstige bijwerkingen worden hieronder en elders in de etikettering besproken:
- Bloeden [zie WAARSCHUWINGEN EN VOORZORGSMAATREGELEN ]
- Trombotische trombocytopenische purpura [zie WAARSCHUWINGEN EN VOORZORGSMAATREGELEN ]
Ervaring met klinische proeven
Omdat klinische onderzoeken worden uitgevoerd onder sterk variërende omstandigheden en duur van de follow-up, kunnen de bijwerkingen die in de klinische onderzoeken van een geneesmiddel zijn waargenomen niet direct worden vergeleken met de percentages in de klinische onderzoeken van een ander geneesmiddel en komen deze mogelijk niet overeen met de percentages die in de praktijk worden waargenomen.
Plavix is beoordeeld op veiligheid bij meer dan 54.000 patiënten, waaronder meer dan 21.000 patiënten die een jaar of langer werden behandeld. De klinisch belangrijke bijwerkingen die zijn waargenomen in onderzoeken waarin Plavix 75 mg plus aspirine werd vergeleken met placebo plus aspirine en onderzoeken waarin Plavix alleen werd vergeleken met alleen aspirine, worden hieronder besproken.
Bloeden
GENEZING
In CURE was het gebruik van Plavix met aspirine geassocieerd met een toename van ernstige bloedingen (voornamelijk gastro-intestinaal en op de punctieplaatsen) in vergelijking met placebo met aspirine (zie tabel 1). De incidentie van intracraniële bloeding (0,1%) en fatale bloeding (0,2%) was in beide groepen hetzelfde. Andere bloedingen die vaker werden gemeld in de clopidogrelgroep waren epistaxis, hematurie en blauwe plekken.
De totale incidentie van bloedingen wordt beschreven in Tabel 1.
VERBINDEN
In COMMIT werden vergelijkbare percentages ernstige bloedingen waargenomen in de Plavix 75 mg- en placebogroep, die beide ook aspirine kregen (zie tabel 2).
CAPRIE (Plavix versus aspirine)
In CAPRIE trad gastro-intestinale bloeding op met een snelheid van 2,0% bij degenen die Plavix 75 mg gebruikten, versus 2,7% bij degenen die aspirine gebruikten; bloedingen waarvoor ziekenhuisopname nodig was, kwamen voor bij respectievelijk 0,7% en 1,1%. De incidentie van intracraniële bloeding was 0,4% voor Plavix vergeleken met 0,5% voor aspirine.
Andere bloedingen die vaker werden gemeld in de Plavix 75 mg-groep waren epistaxis en hematoom.
Andere bijwerkingen
In CURE en CHARISMA, die Plavix plus aspirine vergeleken met aspirine alleen, was er geen verschil in het aantal bijwerkingen (behalve bloedingen) tussen Plavix en placebo.
In CAPRIE, waarin Plavix 75 mg werd vergeleken met aspirine, werd pruritus vaker gemeld bij degenen die Plavix gebruikten. Er werd geen ander verschil in het aantal bijwerkingen (behalve bloedingen) gemeld.
Postmarketingervaring
De volgende bijwerkingen zijn vastgesteld tijdens het gebruik van Plavix na goedkeuring. Omdat deze reacties vrijwillig worden gemeld door een populatie van onbekende grootte, is het niet altijd mogelijk om een betrouwbare schatting van de frequentie ervan of een oorzakelijk verband met blootstelling aan geneesmiddelen vast te stellen.
Bloedingen, waaronder die met fatale afloop, zijn gemeld bij patiënten die met Plavix werden behandeld.
- Bloed- en lymfestelselaandoeningen: Agranulocytose, aplastische anemie/pancytopenie, trombotische trombocytopenische purpura (TTP), verworven hemofilie A
- Maagdarmstelselaandoeningen: Colitis (inclusief colitis ulcerosa of lymfatische colitis), pancreatitis, stomatitis, maag-/darmzweren, diarree
- Algemene aandoeningen en toestand van de toedieningsplaats: Koorts
- Lever- en galaandoeningen: Acuut leverfalen, hepatitis (niet-infectieus), abnormale leverfunctietest
- Immuunsysteemaandoeningen: Overgevoeligheidsreacties, anafylactoïde reacties, serumziekte, insuline-auto-immuunsyndroom, wat kan leiden tot ernstige hypoglykemie
- Skeletspierstelsel-, bindweefsel- en botaandoeningen: Myalgie, artralgie, artritis
- Zenuwstelselaandoeningen: Smaakstoornissen, hoofdpijn, ageusie
- Psychische stoornissen: Verwarring, hallucinaties
- Ademhalingsstelsel-, borstkas- en mediastinumaandoeningen: Bronchospasme, interstitiële pneumonitis, eosinofiele pneumonie
- Nier- en urinewegaandoeningen: Verhoogde creatininespiegels
- Huid- en onderhuidaandoeningen: Maculopapulaire, erythemateuze of exfoliatieve uitslag, urticaria, bulleuze dermatitis, eczeem, toxische epidermale necrolyse, Stevens-Johnson-syndroom, acute gegeneraliseerde exanthemateuze pustulosis (AGEP), angio-oedeem, geneesmiddelgeïnduceerd overgevoeligheidssyndroom, geneesmiddeluitslag met eosinofilie en systemische symptomen (DRESS), erythema multiforme, lichen planus, gegeneraliseerde pruritus
- Bloedvataandoeningen: Vasculitis, hypotensie
DRUG-INTERACTIES
CYP2C19-inductoren
Aangezien clopidogrel gedeeltelijk door CYP2C19 wordt gemetaboliseerd tot zijn actieve metaboliet, zou het gebruik van geneesmiddelen die de activiteit van dit enzym induceren naar verwachting leiden tot verhoogde geneesmiddelspiegels van de actieve metaboliet van clopidogrel.
Rifampicine induceert sterk CYP2C19, resulterend in zowel een verhoging van het niveau van de actieve metaboliet van clopidogrel als remming van bloedplaatjes, wat in het bijzonder het risico op bloedingen zou kunnen versterken. Vermijd uit voorzorg gelijktijdig gebruik van sterke CYP2C19-inductoren [zie: WAARSCHUWINGEN EN VOORZORGSMAATREGELEN en KLINISCHE FARMACOLOGIE ].
CYP2C19-remmers
Clopidogrel wordt gedeeltelijk door CYP2C19 gemetaboliseerd tot zijn actieve metaboliet. Gelijktijdig gebruik van geneesmiddelen die de activiteit van dit enzym remmen, resulteert in verlaagde plasmaconcentraties van de actieve metaboliet van clopidogrel en een afname van de bloedplaatjesremming [zie WAARSCHUWINGEN EN VOORZORGSMAATREGELEN ].
Omeprazol of esomeprazol
Vermijd gelijktijdig gebruik van Plavix 75 mg met omeprazol of esomeprazol. In klinische onderzoeken bleek omeprazol de plaatjesaggregatieremmende werking van Plavix 75 mg significant te verminderen bij gelijktijdige toediening of met een tussenpoos van 12 uur. Een vergelijkbare vermindering van de antibloedplaatjesactiviteit werd waargenomen met esomeprazol bij gelijktijdige toediening met Plavix. Dexlansoprazol, lansoprazol en pantoprazol hadden minder effect op de plaatjesaggregatieremming van Plavix dan omeprazol of esomeprazol [zie WAARSCHUWINGEN EN VOORZORGSMAATREGELEN en KLINISCHE FARMACOLOGIE ].
opioïden
Zoals met andere orale P2Y12-remmers, vertraagt en vermindert gelijktijdige toediening van opioïde-agonisten de absorptie van clopidogrel, vermoedelijk vanwege een vertraagde maaglediging, wat resulteert in verminderde blootstelling aan zijn metabolieten (zie KLINISCHE FARMACOLOGIE ]. Overweeg het gebruik van een parenteraal antibloedplaatjesaggregaat bij patiënten met acuut coronair syndroom die gelijktijdige toediening van morfine of andere opioïde-agonisten nodig hebben.
Niet-steroïde anti-inflammatoire geneesmiddelen (NSAID's)
Gelijktijdige toediening van Plavix 75 mg en NSAID's verhoogt het risico op gastro-intestinale bloedingen.
Warfarine (CYP2C9-substraten)
Hoewel de toediening van 75 mg clopidogrel per dag de farmacokinetiek van S-warfarine (een CYP2C9-substraat) of INR niet veranderde bij patiënten die langdurig met warfarine werden behandeld, verhoogt gelijktijdige toediening van Plavix 75 mg met warfarine het risico op bloedingen vanwege onafhankelijke effecten op hemostase.
Bij hoge concentraties in vitro remt clopidogrel echter CYP2C9.
SSRI's en SNRI's
Aangezien selectieve serotonineheropnameremmers (SSRI's) en serotonine-noradrenalineheropnameremmers (SNRI's) de bloedplaatjesactivatie beïnvloeden, kan de gelijktijdige toediening van SSRI's en SNRI's met clopidogrel het risico op bloedingen verhogen.
Repaglinide (CYP2C8-substraten)
De acyl-β-glucuronidemetaboliet van clopidogrel is een sterke remmer van CYP2C8. Plavix 75 mg kan de systemische blootstelling aan geneesmiddelen die voornamelijk worden geklaard door CYP2C8 verhogen, waardoor dosisaanpassing en passende monitoring nodig zijn.
Plavix verhoogde de blootstelling aan repaglinide met een factor 3,9 tot 5,1 [zie: KLINISCHE FARMACOLOGIE ]. Vermijd gelijktijdig gebruik van repaglinide met Plavix. Als gelijktijdig gebruik niet kan worden vermeden, start dan met 0,5 mg repaglinide vóór elke maaltijd en overschrijd een totale dagelijkse dosis van 4 mg niet. Bij gelijktijdig gebruik kan een verhoogde frequentie van glucosemonitoring nodig zijn.
WAARSCHUWINGEN
Inbegrepen als onderdeel van de PREVENTIEVE MAATREGELEN sectie.
PREVENTIEVE MAATREGELEN
Verminderde antibloedplaatjesactiviteit bij patiënten met een verminderde CYP2C19-functie
Clopidogrel is een prodrug. Remming van de bloedplaatjesaggregatie door clopidogrel wordt bereikt door een actieve metaboliet. Het metabolisme van clopidogrel tot zijn actieve metaboliet kan worden verstoord door genetische variaties in CYP2C19 [zie GEVAARLIJKE WAARSCHUWING: ].
Het metabolisme van clopidogrel kan ook verstoord worden door geneesmiddelen die CYP2C19 remmen, zoals omeprazol of esomeprazol. Vermijd gelijktijdig gebruik van Plavix met omeprazol of esomeprazol, omdat beide de antibloedplaatjesactiviteit van Plavix aanzienlijk verminderen (zie DRUG-INTERACTIES ].
Algemeen risico op bloedingen
P2Y12-remmers (Thienopyridines), waaronder Plavix, verhogen het risico op bloedingen.
P2Y12-remmers (Thienopyridines) remmen de bloedplaatjesaggregatie gedurende de levensduur van de bloedplaatjes (7-10 dagen). Omdat de halfwaardetijd van de actieve metaboliet van clopidogrel kort is, kan het mogelijk zijn de hemostase te herstellen door exogene bloedplaatjes toe te dienen; bloedplaatjestransfusies binnen 4 uur na de oplaaddosis of 2 uur na de onderhoudsdosis kunnen echter minder effectief zijn.
Het gebruik van geneesmiddelen die de activiteit van CYP2C19 induceren, zou naar verwachting leiden tot verhoogde geneesmiddelspiegels van de actieve metaboliet van clopidogrel en zou het bloedingsrisico kunnen versterken. Vermijd uit voorzorg gelijktijdig gebruik van sterke CYP2C19-inductoren [zie: DRUG-INTERACTIES en KLINISCHE FARMACOLOGIE ].
Stopzetting van Plavix
Stoppen met Plavix verhoogt het risico op cardiovasculaire voorvallen. Als Plavix tijdelijk moet worden gestaakt (bijv. om bloedingen te behandelen of voor een operatie met een groot risico op bloeding), start u het zo snel mogelijk opnieuw. Onderbreek indien mogelijk de therapie met Plavix gedurende vijf dagen voorafgaand aan een dergelijke operatie. Hervat Plavix 75 mg zodra hemostase is bereikt.
Trombotische trombocytopenische purpura (TTP)
TTP, soms fataal, is gemeld na gebruik van Plavix 75 mg, soms na een korte blootstelling ( ONGEWENSTE REACTIES ].
Kruisreactiviteit tussen thienopyridines
Overgevoeligheid waaronder huiduitslag, angio-oedeem of hematologische reactie is gemeld bij patiënten die Plavix 75 mg kregen, inclusief patiënten met een voorgeschiedenis van overgevoeligheid of hematologische reactie op andere thienopyridines [zie CONTRA-INDICATIES en ONGEWENSTE REACTIES ].
Informatie over patiëntbegeleiding
Adviseer patiënten om door de FDA goedgekeurde patiëntetikettering te lezen ( Medicatiegids ).
Stopzetting
Adviseer patiënten om niet te stoppen met Plavix zonder dit eerst te bespreken met de zorgverlener die het heeft voorgeschreven [zie WAARSCHUWINGEN EN VOORZORGSMAATREGELEN ].
Bloeden
Adviseer patiënten dat zij:
- zal gemakkelijker blauwe plekken krijgen en bloeden
- duurt het langer dan normaal om het bloeden te stoppen
- moeten onverwachte, langdurige of overmatige bloedingen of bloed in de ontlasting of urine melden [zie: WAARSCHUWINGEN EN VOORZORGSMAATREGELEN ]
Trombotische trombocytopenische purpura
Instrueer patiënten om onmiddellijk medische hulp in te roepen als ze symptomen van TTP ervaren die niet anders kunnen worden verklaard [zie WAARSCHUWINGEN EN VOORZORGSMAATREGELEN ].
Invasieve procedures
Adviseer patiënten om artsen en tandartsen te informeren dat ze Plavix gebruiken vóór een operatie of tandheelkundige ingreep [zie WAARSCHUWINGEN EN VOORZORGSMAATREGELEN ].
Protonpompremmers
Adviseer patiënten om geen omeprazol of esomeprazol te gebruiken tijdens het gebruik van Plavix. Dexlansoprazol, lansoprazol en pantoprazol hadden minder uitgesproken effecten op de antibloedplaatjesactiviteit van Plavix 75 mg dan omeprazol of esomeprazol [zie DRUG-INTERACTIES ].
Niet-klinische toxicologie
Carcinogenese, mutagenese, verminderde vruchtbaarheid
Er was geen bewijs van tumorigeniciteit bij toediening van clopidogrel gedurende 78 weken aan muizen en 104 weken aan ratten in doseringen tot 77 mg/kg per dag, wat leidde tot plasmablootstellingen >25 maal die bij mensen bij de aanbevolen dagelijkse dosis van 75 mg.
Clopidogrel was niet genotoxisch in vier in vitro tests (Ames-test, DNA-reparatietest in hepatocyten van ratten, genmutatietest in fibroblasten van Chinese hamsters en metafasechromosoomanalyse van menselijke lymfocyten) en in één in vivo test (micronucleustest via orale weg in muizen).
Clopidogrel bleek geen effect te hebben op de vruchtbaarheid van mannelijke en vrouwelijke ratten die werden behandeld vóór het koppelen en tijdens de dracht met orale doses tot 400 mg/kg per dag (52 maal de aanbevolen dosis voor de mens op basis van mg/m²).
Gebruik bij specifieke populaties
Zwangerschap
Risico Samenvatting
Beschikbare gegevens van gevallen die zijn gemeld in gepubliceerde literatuur en postmarketingsurveillance met het gebruik van clopidogrel bij zwangere vrouwen hebben geen geneesmiddelgerelateerde risico's voor ernstige geboorteafwijkingen of miskramen geïdentificeerd [zie Gegevens ]. Er zijn risico's voor de zwangere vrouw en de foetus verbonden aan een myocardinfarct en beroerte [zie Klinische overwegingen ]. Er werd geen bewijs van foetotoxiciteit waargenomen wanneer clopidogrel werd toegediend aan drachtige ratten en konijnen tijdens de organogenese in doses die overeenkomen met 65 en 78 maal de aanbevolen dagelijkse dosis voor de mens [zie Gegevens ].
Het geschatte achtergrondrisico van ernstige geboorteafwijkingen en miskraam voor de aangegeven populaties is niet bekend. Alle zwangerschappen hebben een achtergrondrisico op geboorteafwijkingen, verlies of andere nadelige gevolgen. In de algemene bevolking van de VS is het geschatte achtergrondrisico van ernstige geboorteafwijkingen en miskraam bij klinisch erkende zwangerschappen respectievelijk 2% tot 4% en 15% tot 20%.
Klinische overwegingen
Ziekte-geassocieerd maternale en/of embryo-/foetale risico
Myocardinfarct en beroerte zijn medische noodgevallen. Behandeling voor zwangere vrouwen mag niet worden onthouden vanwege mogelijke bezorgdheid over de effecten van clopidogrel op de foetus.
Arbeid of levering
Het gebruik van clopidogrel tijdens de bevalling of bevalling verhoogt het risico op maternale bloedingen en bloedingen. Vermijd neuraxiale blokkade tijdens het gebruik van clopidogrel vanwege het risico op spinale hematoom. Stop indien mogelijk 5 tot 7 dagen voor de bevalling, bevalling of neuraxiale blokkade met clopidogrel.
Gegevens
Menselijke gegevens
De beschikbare gegevens van gepubliceerde casusrapporten van meer dan twee decennia postmarketinggebruik hebben geen verband aangetoond met het gebruik van clopidogrel tijdens de zwangerschap en ernstige geboorteafwijkingen, miskraam of nadelige foetale uitkomsten.
Dierlijke gegevens
Er werden embryo-foetale ontwikkelingstoxicologische onderzoeken uitgevoerd bij zwangere ratten en konijnen met doses tot respectievelijk 500 en 300 mg/kg/dag, toegediend tijdens de organogenese. Deze doses, overeenkomend met respectievelijk 65 en 78 maal de aanbevolen dagelijkse dosis voor de mens, op basis van mg/m², lieten geen bewijs zien van verminderde vruchtbaarheid of foetotoxiciteit als gevolg van clopidogrel.
Borstvoeding
Risico Samenvatting
Er zijn geen gegevens over de aanwezigheid van clopidogrel in moedermelk of de effecten op de melkproductie. In een klein aantal postmarketinggevallen zijn bij gebruik van clopidogrel door de moeder tijdens de lactatie geen nadelige effecten waargenomen op zuigelingen die borstvoeding krijgen. Studies bij ratten hebben aangetoond dat clopidogrel en/of zijn metabolieten in de melk aanwezig zijn. Wanneer een geneesmiddel aanwezig is in dierlijke melk, is het waarschijnlijk dat het geneesmiddel ook in de moedermelk aanwezig zal zijn. De ontwikkelings- en gezondheidsvoordelen van borstvoeding moeten worden overwogen, samen met de klinische behoefte van de moeder aan PLAVIX en eventuele nadelige effecten op de zuigeling die borstvoeding krijgt van PLAVIX 75 mg of van een onderliggende maternale aandoening.
Pediatrisch gebruik
De veiligheid en werkzaamheid bij pediatrische populaties zijn niet vastgesteld.
Een gerandomiseerde, placebo-gecontroleerde studie (CLARINET) toonde geen klinisch voordeel aan van clopidogrel bij pasgeborenen en zuigelingen met cyanotische congenitale hartziekte verlicht met een systemische naar pulmonale arteriële shunt. Mogelijke factoren die bijdroegen aan dit resultaat waren de dosis clopidogrel, de gelijktijdige toediening van aspirine en de late start van de therapie na shuntpalliatie. Het kan niet worden uitgesloten dat een onderzoek met een andere opzet een klinisch voordeel zou aantonen bij deze patiëntenpopulatie.
Geriatrisch gebruik
Van het totale aantal proefpersonen in de CAPRIE- en CURE-gecontroleerde klinische onderzoeken was ongeveer 50% van de met Plavix behandelde patiënten 65 jaar en ouder en 15% 75 jaar en ouder. In COMMIT was ongeveer 58% van de met Plavix 75 mg behandelde patiënten 60 jaar en ouder, van wie 26% 70 jaar en ouder.
Het waargenomen risico op bloedingen met Plavix 75 mg plus aspirine versus placebo plus aspirine per leeftijdscategorie wordt gegeven in tabel 1 en tabel 2 voor respectievelijk de CURE- en COMMIT-onderzoeken [zie ONGEWENSTE REACTIES ]. Bij oudere patiënten is geen dosisaanpassing nodig.
Nierfunctiestoornis
De ervaring is beperkt bij patiënten met ernstige en matige nierinsufficiëntie [zie: KLINISCHE FARMACOLOGIE ].
Leverfunctiestoornis
Er is geen dosisaanpassing nodig bij patiënten met leverinsufficiëntie [zie: KLINISCHE FARMACOLOGIE ].
OVERDOSERING
Bloedplaatjesremming door Plavix is onomkeerbaar en duurt de levensduur van het bloedplaatje. Overdosering na toediening van clopidogrel kan leiden tot bloedingscomplicaties. Een enkele orale dosis clopidogrel van 1500 of 2000 mg/kg was dodelijk voor muizen en ratten en 3000 mg/kg voor bavianen. Symptomen van acute toxiciteit waren braken, uitputting, moeilijke ademhaling en gastro-intestinale bloeding bij dieren.
Op basis van biologische aannemelijkheid kan trombocytentransfusie het stollingsvermogen herstellen.
CONTRA-INDICATIES
Actieve bloeding
Plavix is gecontra-indiceerd bij patiënten met actieve pathologische bloedingen zoals maagzweer of intracraniële bloeding.
overgevoeligheid
Plavix 75 mg is gecontra-indiceerd bij patiënten met overgevoeligheid (bijv. anafylaxie) voor clopidogrel of een bestanddeel van het product [zie ONGEWENSTE REACTIES ].
KLINISCHE FARMACOLOGIE
Werkingsmechanisme
Clopidogrel is een remmer van de activering en aggregatie van bloedplaatjes door de onomkeerbare binding van zijn actieve metaboliet aan de P2Y12-klasse van ADP-receptoren op bloedplaatjes.
farmacodynamiek
Clopidogrel moet worden gemetaboliseerd door CYP450-enzymen om de actieve metaboliet te produceren die de bloedplaatjesaggregatie remt. De actieve metaboliet van clopidogrel remt selectief de binding van adenosinedifosfaat (ADP) aan zijn plaatjes P2Y12-receptor en de daaropvolgende ADP-gemedieerde activering van het glycoproteïne GPIIb/IIIa-complex, waardoor de plaatjesaggregatie wordt geremd. Deze actie is onomkeerbaar. Dientengevolge worden bloedplaatjes die worden blootgesteld aan de actieve metaboliet van clopidogrel gedurende de rest van hun levensduur (ongeveer 7 tot 10 dagen) aangetast. Bloedplaatjesaggregatie geïnduceerd door andere agonisten dan ADP wordt ook geremd door de amplificatie van bloedplaatjesactivatie door vrijgemaakt ADP te blokkeren.
Dosisafhankelijke remming van de bloedplaatjesaggregatie kan 2 uur na enkelvoudige orale doses Plavix worden waargenomen. Herhaalde doses van 75 mg Plavix per dag remmen de door ADP geïnduceerde trombocytenaggregatie op de eerste dag en de remming bereikt een steady state tussen dag 3 en dag 7. Bij steady state was het gemiddelde remmingsniveau dat werd waargenomen met een dosis van 75 mg Plavix per dag tussen 40% en 60%. Bloedplaatjesaggregatie en bloedingstijd keren geleidelijk terug naar de uitgangswaarden nadat de behandeling is stopgezet, in het algemeen na ongeveer 5 dagen.
Geriatrische patiënten
Ouderen (≥75 jaar) en jonge gezonde proefpersonen hadden vergelijkbare effecten op de bloedplaatjesaggregatie.
Patiënten met nierinsufficiëntie
Na herhaalde doses van 75 mg Plavix 75 mg per dag vertoonden patiënten met ernstige nierfunctiestoornis (creatinineklaring van 5 tot 15 ml/min) en matige nierfunctiestoornis (creatinineklaring van 30 tot 60 ml/min) een lage (25%) remming van ADP-geïnduceerde bloedplaatjesaggregatie.
Patiënten met een leverfunctiestoornis
Na herhaalde doses van 75 mg Plavix per dag gedurende 10 dagen bij patiënten met ernstige leverinsufficiëntie, was de remming van door ADP geïnduceerde bloedplaatjesaggregatie vergelijkbaar met die waargenomen bij gezonde proefpersonen.
Geslacht
In een kleine studie waarin mannen en vrouwen werden vergeleken, werd bij vrouwen minder remming van ADP-geïnduceerde bloedplaatjesaggregatie waargenomen.
Farmacokinetiek
Clopidogrel is een prodrug en wordt gemetaboliseerd tot een farmacologisch actieve metaboliet en inactieve metabolieten.
Absorptie
Na enkelvoudige en herhaalde orale doses van 75 mg per dag wordt clopidogrel snel geabsorbeerd. Absorptie is ten minste 50%, gebaseerd op uitscheiding via de urine van clopidogrelmetabolieten.
Effect van voedsel
Plavix kan met of zonder voedsel worden toegediend. In een onderzoek bij gezonde mannelijke proefpersonen waarin Plavix 75 mg per dag werd gegeven bij een standaardontbijt, was de gemiddelde remming van de door ADP geïnduceerde bloedplaatjesaggregatie met minder dan 9% verminderd. De actieve metaboliet AUC0-24 was onveranderd in aanwezigheid van voedsel, terwijl de actieve metaboliet Cmax met 57% daalde. Soortgelijke resultaten werden waargenomen wanneer een oplaaddosis Plavix 300 mg werd toegediend met een vetrijk ontbijt.
Metabolisme
Clopidogrel wordt uitgebreid gemetaboliseerd via twee belangrijke metabole routes: één gemedieerd door esterasen en leidt tot hydrolyse tot een inactief carbonzuurderivaat (85% van de circulerende metabolieten) en één gemedieerd door meerdere cytochroom P450-enzymen. Cytochromen oxideren eerst clopidogrel tot een 2-oxo-clopidogrel intermediaire metaboliet. Daaropvolgend metabolisme van de 2-oxoclopidogrel intermediaire metaboliet resulteert in de vorming van de actieve metaboliet, een thiolderivaat van clopidogrel. De actieve metaboliet wordt voornamelijk gevormd door CYP2C19 met bijdragen van verschillende andere CYP-enzymen, waaronder CYP1A2, CYP2B6 en CYP3A. De actieve thiolmetaboliet bindt snel en onomkeerbaar aan bloedplaatjesreceptoren, waardoor de bloedplaatjesaggregatie gedurende de levensduur van het bloedplaatje wordt geremd.
De Cmax van de actieve metaboliet is tweemaal zo hoog na een eenmalige oplaaddosis van 300 mg clopidogrel als na vier dagen onderhoudsdosis van 75 mg. Cmax treedt ongeveer 30 tot 60 minuten na toediening op. In het dosisbereik van 75 tot 300 mg wijkt de farmacokinetiek van de actieve metaboliet af van de dosisproportionaliteit: een 4-voudige dosis resulteert in respectievelijk een 2,0- en 2,7-voudige Cmax en AUC.
Eliminatie
Na een orale dosis 14C-gelabelde clopidogrel bij de mens werd ongeveer 50% van de totale radioactiviteit uitgescheiden in de urine en ongeveer 46% in de feces gedurende de 5 dagen na toediening. Na een enkelvoudige orale dosis van 75 mg heeft clopidogrel een halfwaardetijd van ongeveer 6 uur. De halfwaardetijd van de actieve metaboliet is ongeveer 30 minuten.
Geneesmiddelinteracties
Effect van andere geneesmiddelen op Plavix
Clopidogrel wordt gedeeltelijk door CYP2C19 gemetaboliseerd tot zijn actieve metaboliet.
CYP2C19-inductoren
Gelijktijdig gebruik van sterke inductoren van CYP2C19 resulteert in een verhoogde plasmaconcentratie van de actieve metaboliet van clopidogrel en een toename van de bloedplaatjesremming.
Rifampicine: Gelijktijdige toediening van rifampicine 300 mg tweemaal daags gedurende 7 dagen met een oplaaddosis van 600 mg clopidogrel bij gezonde volwassenen verhoogde de gemiddelde AUC en Cmax van de thiolmetabolieten van clopidogrel met een factor 3,8. De gemiddelde remming van de bloedplaatjesaggregatie 4 uur na toediening was 34% hoger in aanwezigheid van rifampicine in vergelijking met clopidogrel alleen toegediend.
CYP2C19-remmers
Gelijktijdig gebruik van bepaalde remmers van dit enzym resulteert in verlaagde plasmaconcentraties van de actieve metaboliet van clopidogrel en een afname van de bloedplaatjesremming.
Protonpompremmers (PPI)
Het effect van protonpompremmers (PPI) op de systemische blootstelling aan de actieve metaboliet van clopidogrel na meerdere doses Plavix 75 mg, geëvalueerd in specifieke onderzoeken naar geneesmiddelinteracties, wordt weergegeven in figuur 1.
Afbeelding 1: Blootstelling aan de actieve metaboliet van clopidogrel na meerdere doses Plavix 75 mg alleen of met protonpompremmers (PPI's)
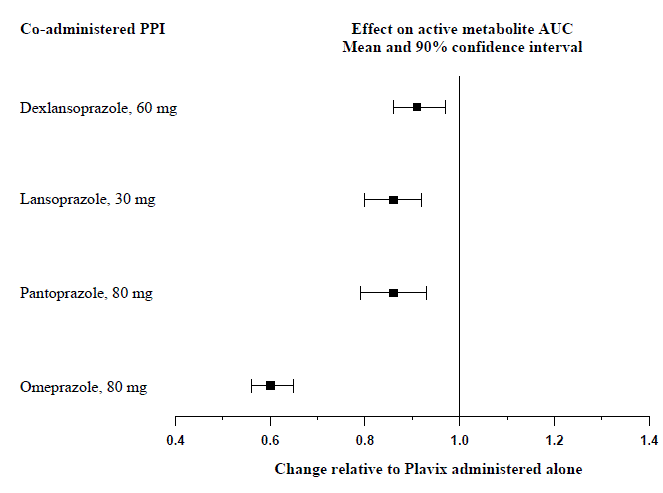
Farmacodynamische en farmacokinetische parameters gemeten in deze onderzoeken toonden aan dat de interactie het hoogst was met omeprazol en het minst met dexlansoprazol.
opioïden
Gelijktijdige toediening van 5 mg intraveneuze morfine met 600 mg oplaaddosis clopidogrel bij gezonde volwassenen verlaagde de AUC en Cmax van de thiolmetabolieten van clopidogrel met 34%. De gemiddelde bloedplaatjesaggregatie was hoger tot 2 tot 4 uur bij gelijktijdige toediening van morfine.
Effect van Plavix 75 mg op andere geneesmiddelen
In vitro-onderzoeken hebben aangetoond dat de glucuronidemetaboliet van clopidogrel een sterke remmer van CYP2C8 is. Gelijktijdige toediening van repaglinide met Plavix verhoogde de systemische blootstelling aan repaglinide (AUC0-∞) met een factor 5,1 na de oplaaddosis (300 mg) en met een factor 3,9 op dag 3 van de onderhoudsdosis (75 mg) van Plavix (zie DRUG-INTERACTIES ].
farmacogenomica
CYP2C19 is betrokken bij de vorming van zowel de actieve metaboliet als de intermediaire metaboliet 2-oxo-clopidogrel. De farmacokinetiek van de actieve metaboliet van clopidogrel en de effecten op de bloedplaatjesaggregatie, zoals gemeten met ex vivo bloedplaatjesaggregatietesten, verschillen afhankelijk van het CYP2C19-genotype. Patiënten die homozygoot zijn voor niet-functionele allelen van het CYP2C19-gen, worden "CYP2C19-slechte metaboliseerders" genoemd. Ongeveer 2% van de blanke en 4% van de zwarte patiënten zijn slechte metaboliseerders; de prevalentie van een slecht metabolisme is hoger bij Aziatische patiënten (bijv. 14% van de Chinezen). Er zijn tests beschikbaar om patiënten te identificeren die slechte CYP2C19-metaboliseerders zijn.
Een cross-overstudie bij 40 gezonde proefpersonen, elk 10 in de vier CYP2C19-metaboliseerdersgroepen, evalueerde farmacokinetische en antibloedplaatjesresponsen met 300 mg gevolgd door 75 mg per dag en 600 mg gevolgd door 150 mg per dag, elk gedurende een totaal van 5 dagen. Verlaagde blootstelling aan actieve metabolieten en verminderde remming van de bloedplaatjesaggregatie werden waargenomen bij de trage metaboliseerders in vergelijking met de andere groepen.
Klinische studies
Acute kransslagader syndroom
GENEZING
De CURE-studie omvatte 12.562 patiënten met ACS zonder ST-elevatie (UA of NSTEMI) en die zich binnen 24 uur na het begin van de meest recente episode van pijn op de borst of symptomen vertoonden die overeenkomen met ischemie. Patiënten moesten ofwel ECG-veranderingen hebben die compatibel zijn met nieuwe ischemie (zonder ST-elevatie) of verhoogde hartenzymen of troponine I of T tot ten minste tweemaal de bovengrens van normaal.
De patiënten werden gerandomiseerd om Plavix (300 mg oplaaddosis gevolgd door 75 mg eenmaal daags) of placebo te krijgen en werden tot een jaar behandeld. Patiënten kregen ook aspirine (75-325 mg eenmaal daags) en andere standaardtherapieën zoals heparine. Het gebruik van GPIIb/IIIa-remmers was drie dagen voorafgaand aan randomisatie niet toegestaan.
De patiëntenpopulatie was grotendeels blank (82%) en omvatte 38% vrouwen en 52% in de leeftijd ≥65 jaar. Slechts ongeveer 20% van de patiënten onderging een revascularisatie tijdens de eerste ziekenhuisopname en weinigen ondergingen een opkomende of dringende revascularisatie.
Het aantal patiënten met de primaire uitkomst (CV overlijden, MI of beroerte) was 582 (9,3%) in de met Plavix behandelde groep en 719 (11,4%) in de met placebo behandelde groep, een relatieve risicoreductie van 20% (95 % BI van 10%-28%; p
Het grootste deel van het voordeel van Plavix trad op in de eerste twee maanden, maar het verschil met placebo bleef in de loop van het onderzoek (tot 12 maanden) behouden (zie figuur 2).
Afbeelding 2: Cardiovasculaire dood, myocardinfarct en beroerte in het CURE-onderzoek
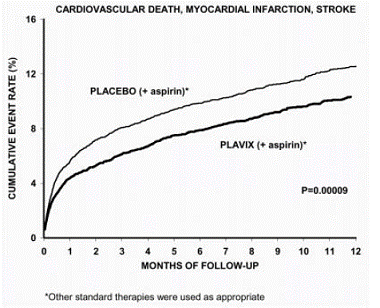
Het effect van Plavix 75 mg verschilde niet significant in verschillende subgroepen, zoals weergegeven in figuur 3. De voordelen van Plavix 75 mg waren onafhankelijk van het gebruik van andere acute en langdurige cardiovasculaire therapieën, waaronder heparine/LMWH, intraveneus glycoproteïne IIb/IIIa (GPIIb/IIIa)-remmers, lipidenverlagende medicijnen, bètablokkers en ACE-remmers. De werkzaamheid van Plavix werd onafhankelijk van de dosis aspirine (75-325 mg eenmaal daags) waargenomen. Het gebruik van orale anticoagulantia, niet-studie-antibloedplaatjesgeneesmiddelen en chronische NSAID's was niet toegestaan in CURE.
Afbeelding 3: Hazard Ratio voor patiëntkenmerken bij baseline en gelijktijdige medicatie/interventies tijdens het onderzoek voor het CURE-onderzoek
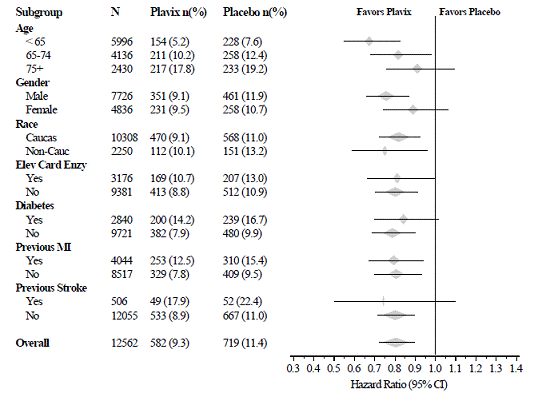
Afbeelding 3: Hazard Ratio voor patiëntkenmerken bij baseline en gelijktijdige medicatie/interventies tijdens het onderzoek voor het CURE-onderzoek (vervolg)
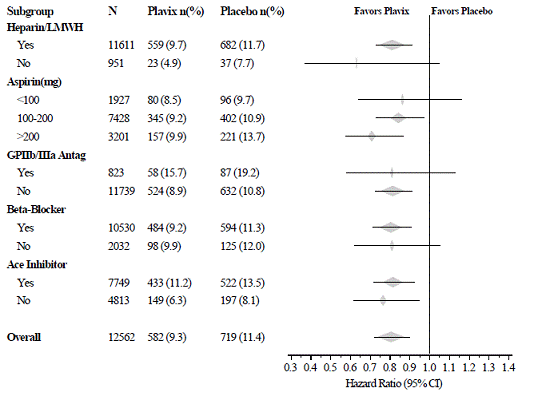
Het gebruik van Plavix in CURE ging gepaard met een afname van het gebruik van trombolytische therapie (71 patiënten [1,1%] in de Plavix 75 mg-groep, 126 patiënten [2,0%] in de placebogroep; relatieve risicoreductie van 43%) en GPIIb/IIIa-remmers (369 patiënten [5,9%] in de Plavix 75 mg-groep, 454 patiënten [7,2%] in de placebogroep, relatieve risicoreductie van 18%). Het gebruik van Plavix 75 mg in CURE had geen invloed op het aantal patiënten dat werd behandeld met CABG of PCI (met of zonder stent) (2253 patiënten [36,0%] in de Plavix 75 mg-groep, 2324 patiënten [36,9%] in de placebogroep; relatief risicoreductie van 4,0%).
VERBINDEN
Bij patiënten met STEMI werden de veiligheid en werkzaamheid van Plavix geëvalueerd in de gerandomiseerde, placebogecontroleerde, dubbelblinde studie COMMIT. COMMIT omvatte 45.852 patiënten die zich binnen 24 uur na het begin van de symptomen van een myocardinfarct presenteerden met ondersteunende ECG-afwijkingen (dwz ST-elevatie, ST-depressie of linker bundeltakblok). Patiënten werden gerandomiseerd naar Plavix (75 mg eenmaal daags) of placebo, in combinatie met aspirine (162 mg per dag), gedurende 28 dagen of tot ontslag uit het ziekenhuis, afhankelijk van wat zich het eerst voordeed.
De primaire eindpunten waren overlijden door welke oorzaak dan ook en het eerste optreden van een nieuw infarct, beroerte of overlijden.
De patiëntenpopulatie was 28% vrouwen en 58% leeftijd 60 jaar (26% leeftijd ≥70 jaar). Vijfenvijftig procent (55%) van de patiënten kreeg trombolytica en slechts 3% onderging een PCI.
Zoals weergegeven in Tabel 5 en Afbeelding 4 en Afbeelding 5 hieronder, verminderde Plavix het relatieve risico op overlijden door welke oorzaak dan ook significant met 7% (p=0,029) en het relatieve risico op de combinatie van her-infarct, beroerte of overlijden met 9% ( p=0,002).
Figuur 4: Cumulatieve voorvalpercentages voor overlijden in het COMMIT-onderzoek*
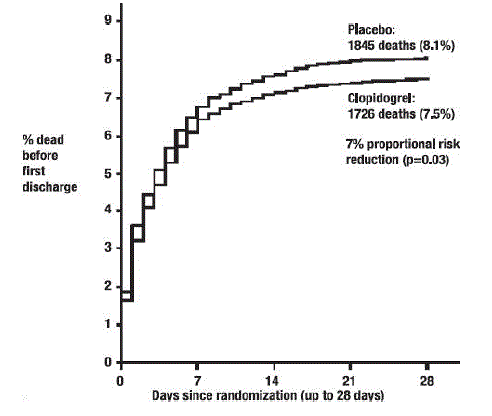
Afbeelding 5: Cumulatieve voorvalpercentages voor het gecombineerde eindpunt her-infarct, beroerte of overlijden in het COMMIT-onderzoek*
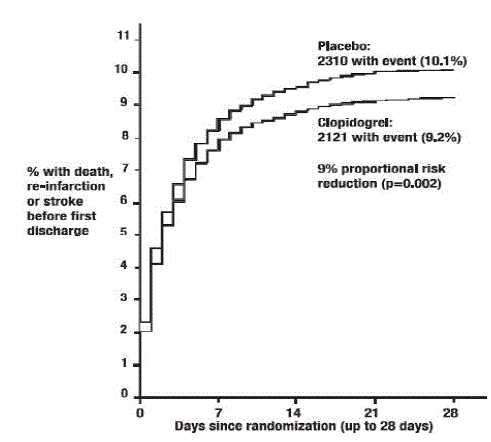
Het effect van Plavix 75 mg verschilde niet significant in verschillende vooraf gespecificeerde subgroepen, zoals weergegeven in Figuur 6. Het effect was ook vergelijkbaar in niet-vooraf gespecificeerde subgroepen, inclusief die op basis van infarctlocatie, Killip-klasse of eerdere MI-geschiedenis. Dergelijke subgroepanalyses moeten met voorzichtigheid worden geïnterpreteerd.
Afbeelding 6: Effecten van toevoeging van Plavix 75 mg aan aspirine op het gecombineerde primaire eindpunt over de baseline- en gelijktijdige medicatiesubgroepen voor de COMMIT-studie
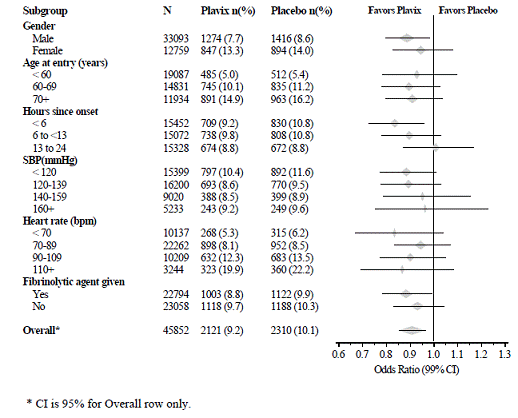
Recent myocardinfarct, recente beroerte of vastgestelde perifere arteriële ziekte
CAPRIE
De CAPRIE-studie was een internationale, gerandomiseerde, dubbelblinde studie met parallelle groepen van 19.185 patiënten, met 304 centra, waarin Plavix (75 mg per dag) werd vergeleken met aspirine (325 mg per dag). Om in aanmerking te komen voor inschrijving, moesten patiënten: 1) een recente geschiedenis van een myocardinfarct hebben (binnen 35 dagen); 2) recente geschiedenis van ischemische beroerte (binnen 6 maanden) met ten minste een week resterende neurologische symptomen; en/of 3) vastgestelde perifere arteriële ziekte (PAD). Patiënten kregen gerandomiseerde behandeling gedurende gemiddeld 1,6 jaar (maximaal 3 jaar).
De primaire uitkomstmaat van het onderzoek was de tijd tot het eerste optreden van een nieuwe ischemische beroerte (fataal of niet), een nieuw myocardinfarct (fataal of niet) of andere vasculaire dood. Sterfgevallen die niet gemakkelijk toe te schrijven waren aan niet-vasculaire oorzaken werden allemaal geclassificeerd als vasculair.
Zoals weergegeven in Tabel 6, was Plavix geassocieerd met een lagere incidentie van uitkomstgebeurtenissen, voornamelijk MI. De algehele relatieve risicoreductie (9,8% versus 10,6%) was 8,7%, p=0,045. Vergelijkbare resultaten werden verkregen wanneer sterfte door alle oorzaken en beroertes door alle oorzaken werden geteld in plaats van vasculaire mortaliteit en ischemische beroertes (risicoreductie 6,9%). Bij patiënten die een beroerte of een myocardinfarct tijdens het onderzoek overleefden, was de incidentie van daaropvolgende voorvallen lager in de Plavix 75 mg-groep.
De curven die het totale aantal voorvallen weergeven, worden weergegeven in figuur 7. De voorvalcurven gingen vroeg uit elkaar en bleven divergeren gedurende de follow-upperiode van 3 jaar.
Afbeelding 7: Fatale of niet-fatale vasculaire voorvallen in het CAPRIE-onderzoek
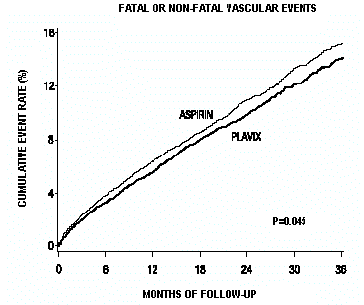
De statistische significantie die Plavix 75 mg bevoordeelde boven aspirine was marginaal (p=0,045). Omdat aspirine echter zelf effectief is in het verminderen van cardiovasculaire voorvallen bij patiënten met een recent myocardinfarct of beroerte, is het effect van Plavix 75 mg aanzienlijk.
In de CAPRIE-studie werd een populatie opgenomen met een recent MI, recente beroerte of PAD. De werkzaamheid van Plavix 75 mg ten opzichte van aspirine was heterogeen in deze subgroepen (p=0,043) (zie figuur 8). Desalniettemin kan dit verschil toeval zijn, omdat de CAPRIE-studie niet was opgezet om het relatieve voordeel van Plavix 75 mg ten opzichte van aspirine in de afzonderlijke patiëntensubgroepen te evalueren. Het voordeel was het duidelijkst bij patiënten die deelnamen vanwege perifere arteriële ziekte en minder duidelijk bij patiënten met een beroerte. Bij patiënten die deelnamen aan het onderzoek op basis van een recent myocardinfarct, was Plavix 75 mg numeriek niet superieur aan aspirine.
Afbeelding 8: Hazard Ratio en 95% BI per baseline-subgroep in het CAPRIE-onderzoek
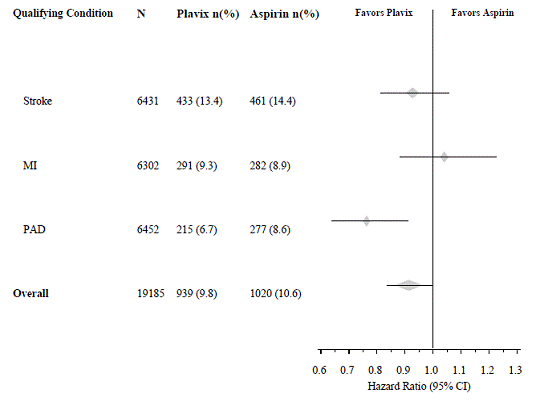
Geen aangetoond voordeel van Plavix 75 mg plus aspirine bij patiënten met meerdere risicofactoren of vastgestelde vaatziekte
CHARISMA
De CHARISMA-studie was een gerandomiseerde, dubbelblinde studie met parallelle groepen van 15.603 proefpersonen waarin Plavix (75 mg per dag) werd vergeleken met placebo voor de preventie van ischemische voorvallen bij patiënten met vaatziekte of meerdere risicofactoren voor atherosclerose. Alle proefpersonen werden behandeld met aspirine 75-162 mg per dag. De gemiddelde duur van de behandeling was 23 maanden. De studie kon geen vermindering aantonen van het optreden van het primaire eindpunt, een samenstelling van CV overlijden, MI of beroerte. In totaal hadden 534 (6,9%) patiënten in de Plavix-groep versus 573 (7,4%) patiënten in de placebogroep een primaire uitkomstmaat (p=0,22). Bloedingen van alle ernst kwamen vaker voor bij de proefpersonen die waren gerandomiseerd naar Plavix.
PATIËNT INFORMATIE
Plavix® (PLAV-iks) (clopidogrelbisulfaat) tabletten
Lees deze medicatiehandleiding voordat u begint met het innemen van Plavix en elke keer dat u een nieuwe vulling krijgt. Mogelijk is er nieuwe informatie. Deze medicatiehandleiding vervangt niet het praten met uw arts over uw medische toestand of uw behandeling.
Wat is de belangrijkste informatie die ik over Plavix 75 mg moet weten?
1. Plavix werkt mogelijk niet zo goed bij mensen die:
- bepaalde genetische factoren hebben die van invloed zijn op de manier waarop het lichaam Plavix afbreekt. Uw arts kan genetische tests doen om er zeker van te zijn dat Plavix geschikt voor u is.
- bepaalde medicijnen nemen, vooral omeprazol (Prilosec®) of esomeprazol (Nexium®). Uw arts kan het geneesmiddel dat u gebruikt voor maagzuurproblemen veranderen terwijl u Plavix gebruikt.
2. Plavix 75 mg kan bloedingen veroorzaken die ernstig kunnen zijn en soms tot de dood kunnen leiden. Plavix is een bloedverdunner die de kans op vorming van bloedstolsels in uw lichaam verkleint. Terwijl u Plavix inneemt:
- u kunt gemakkelijker blauwe plekken krijgen en bloeden
- je hebt meer kans op bloedneuzen
- het duurt langer voordat een bloeding stopt
Bel onmiddellijk uw arts als u een van deze tekenen of symptomen van bloeding heeft:
- onverwachte bloeding of bloeding die lang aanhoudt
- bloed in uw urine (roze, rode of bruine urine)
- rode of zwarte ontlasting (lijkt op teer)
- blauwe plekken die ontstaan zonder een bekende oorzaak of groter worden
- bloed of bloedstolsels ophoesten
- bloed overgeven of uw braaksel lijkt op koffiedik
Stop niet met het innemen van Plavix 75 mg zonder overleg met de arts die het u voorschrijft. Mensen die te snel stoppen met het innemen van Plavix 75 mg hebben een hoger risico op een hartaanval of overlijden. Als u moet stoppen met Plavix vanwege een bloeding, kan uw risico op een hartaanval groter zijn.
Wat is Plavix 75 mg?
Plavix is een receptgeneesmiddel dat wordt gebruikt voor de behandeling van mensen met een van de volgende aandoeningen:
- pijn op de borst als gevolg van hartproblemen
- slechte bloedsomloop in hun benen (perifere arteriële ziekte)
- een hartaanval
- een beroerte
Plavix wordt alleen of in combinatie met aspirine gebruikt om uw kans op een ander ernstig probleem met uw hart of bloedvaten, zoals een hartaanval, beroerte of bloedstolsel dat tot de dood kan leiden, te verkleinen.
Bloedplaatjes zijn bloedcellen die ervoor zorgen dat uw bloed normaal stolt. Plavix 75 mg helpt voorkomen dat bloedplaatjes aan elkaar gaan kleven en een stolsel vormen dat een slagader kan blokkeren.
Het is niet bekend of Plavix 75 mg veilig en effectief is bij kinderen.
Wie mag Plavix 75 mg niet gebruiken?
Gebruik Plavix niet als u:
- momenteel een aandoening heeft die bloedingen veroorzaakt, zoals een maagzweer
- zijn allergisch voor clopidogrel of andere bestanddelen van Plavix. Zie het einde van deze bijsluiter voor een volledige lijst van ingrediënten in Plavix.
Wat moet ik mijn arts vertellen voordat ik Plavix 75 mg inneem?
Vertel uw arts voordat u Plavix inneemt als u:
- een voorgeschiedenis heeft van darm- (gastro-intestinale) of maagzweren
- een voorgeschiedenis heeft van bloedingsproblemen
- van plan bent om een operatie of een tandheelkundige ingreep te ondergaan. Zien "Hoe moet ik Plavix innemen?"
- zwanger bent of van plan bent zwanger te worden. Het is niet bekend of Plavix 75 mg schadelijk is voor uw ongeboren baby
- borstvoeding geeft of van plan bent borstvoeding te geven. Het is niet bekend of Plavix 75 mg in uw moedermelk terechtkomt. Er moet een beslissing worden genomen met uw zorgverlener om borstvoeding te vermijden of stop te zetten wanneer het voortzetten van Plavix nodig is.
- een allergie of reactie heeft gehad op een geneesmiddel dat wordt gebruikt om uw ziekte te behandelen.
Vertel al uw artsen en uw tandarts dat u Plavix gebruikt. Voordat u een operatie of invasieve ingreep ondergaat, moeten zij overleggen met de arts die Plavix 75 mg aan u heeft voorgeschreven.
Vertel uw arts over alle medicijnen die u gebruikt, inclusief receptplichtige, niet-voorgeschreven medicijnen, vitamines en kruidensupplementen.
Plavix 75 mg kan de manier waarop andere geneesmiddelen werken beïnvloeden, en andere geneesmiddelen kunnen de werking van Plavix beïnvloeden. Zien "Wat is de belangrijkste informatie die ik moet weten over Plavix 75 mg?"
Plavix 75 mg kan de bloedspiegels van andere geneesmiddelen zoals repaglinide (Prandin®) verhogen.
Het gebruik van Plavix met bepaalde andere geneesmiddelen kan het risico op bloedingen verhogen.
Vertel het uw arts vooral als u:
- aspirine, vooral als u een beroerte heeft gehad. Overleg altijd met uw arts of u aspirine samen met Plavix 75 mg moet gebruiken om uw aandoening te behandelen.
- Niet-steroïde anti-inflammatoire geneesmiddelen (NSAID's). Vraag uw arts of apotheker om een lijst van NSAID-geneesmiddelen als u het niet zeker weet.
- warfarine (Coumadin®, Jantoven®).
- selectieve serotonineheropnameremmers (SSRI's) en serotonine-noradrenalineheropnameremmers (SNRI's). Vraag uw arts of apotheker om een lijst van SSRI- of SNRI-geneesmiddelen als u het niet zeker weet.
- rifampicine (gebruikt om ernstige infecties te behandelen)
Weet welke medicijnen u gebruikt. Houd er een lijst van bij om uw arts of apotheker te laten zien wanneer u een nieuw geneesmiddel krijgt.
Hoe moet ik Plavix innemen?
- Neem Plavix precies in zoals uw arts u dat heeft verteld.
- Verander uw dosis niet en stop niet met het innemen van Plavix 75 mg zonder eerst met uw arts te overleggen. Stoppen met Plavix kan uw risico op een hartaanval of beroerte verhogen.
- Neem Plavix 75 mg met aspirine in volgens de instructies van uw arts.
- Als u een dosis bent vergeten, neem dan Plavix in zodra u eraan denkt. Als het bijna tijd is voor uw volgende dosis, sla dan de gemiste dosis over. Neem de volgende dosis op uw normale tijd. Neem geen 2 doses Plavix 75 mg tegelijk in, tenzij uw arts u dat zegt.
- Als u te veel Plavix heeft ingenomen, neem dan onmiddellijk contact op met uw arts of ga naar de dichtstbijzijnde eerste hulpafdeling.
- Praat met uw arts over het stoppen van uw Plavix 75 mg voordat u een operatie ondergaat. Uw arts kan u vertellen dat u ten minste 5 dagen voor de operatie moet stoppen met het gebruik van Plavix 75 mg om overmatig bloeden tijdens de operatie te voorkomen.
Wat zijn de mogelijke bijwerkingen van Plavix?
Plavix 75 mg kan ernstige bijwerkingen veroorzaken, waaronder:
- Zie "Wat is de belangrijkste informatie die ik over Plavix moet weten?"
- Een bloedstollingsprobleem dat trombotische trombocytopenische purpura (TTP) wordt genoemd. TTP kan optreden met Plavix 75 mg, soms na korte tijd (minder dan 2 weken). TTP is een bloedstollingsprobleem waarbij zich bloedstolsels vormen in bloedvaten; en kan overal in het lichaam voorkomen. TTP moet meteen in een ziekenhuis worden behandeld, omdat het de dood kan veroorzaken. Roep meteen medische hulp in als u een van deze symptomen heeft en ze niet kunnen worden verklaard door een andere medische aandoening:
- paarsachtige vlekken (purpura genoemd) op de huid of in de mond (slijmvliezen) als gevolg van bloedingen onder de huid
- uw huid of het wit van uw ogen is geel (geelzucht)
- je voelt je moe of zwak
- je huid ziet er erg bleek uit
- koorts
- snelle hartslag of kortademigheid
- hoofdpijn
- spraakveranderingen
- verwardheid
- coma
- hartinfarct
- hartinfarct
- lage hoeveelheid urine, of urine die roze is of bloed bevat
- maagstreek (buik) pijn
- misselijkheid, braken of diarree
- visie verandert
- aanhoudende symptomen van een lage bloedsuikerspiegel
Vertel het uw arts als u een bijwerking heeft die u hindert of die niet weggaat. Vertel het uw arts als u een allergische reactie krijgt, waaronder huidreacties, terwijl u Plavix gebruikt.
Dit zijn niet alle mogelijke bijwerkingen van Plavix. Vraag uw arts of apotheker om meer informatie.
Bel uw arts voor medisch advies over bijwerkingen. U kunt bijwerkingen melden aan de FDA op 1-800-FDA-1088.
Hoe moet ik Plavix 75 mg bewaren?
- Bewaar Plavix 75 mg bij 59 ° F tot 86 ° F (15 ° C tot 30 ° C).
Houd Plavix en alle geneesmiddelen buiten het bereik van kinderen.
Algemene informatie over Plavix
Medicijnen worden soms voor andere doeleinden gebruikt dan in een Medicatiegids vermeld staan. Gebruik Plavix 75 mg niet voor een aandoening waarvoor het niet is voorgeschreven. Geef Plavix niet aan andere mensen, ook niet als zij dezelfde symptomen hebben als u. Het kan hen schaden.
Deze medicatiehandleiding vat de belangrijkste informatie over Plavix samen. Als u meer informatie wilt, neem dan contact op met uw arts. Vraag uw arts of apotheker om informatie over Plavix die is geschreven voor beroepsbeoefenaren in de gezondheidszorg.
Ga voor meer informatie naar www.sanofi-aventis.us of www.bms.com of bel 1-800-321-1335.
Wat zijn de ingrediënten in Plavix 75mg?
Actief ingrediënt: clopidogrel bisulfaat
Inactieve ingredienten:
Tablet: gehydrogeneerde ricinusolie, hydroxypropylcellulose, mannitol, microkristallijne cellulose, polyethyleenglycol 6000
Filmomhulling: ijzeroxide, hypromellose 2910, lactosemonohydraat, titaniumdioxide, triacetine, carnaubawas
Deze medicatiehandleiding is goedgekeurd door de Amerikaanse Food and Drug.
