Behandeling van hart- en vaatziekten: Coumadin 1mg, 2mg, 5mg Warfarin Gebruik, bijwerkingen en dosering. Prijs in online apotheek. Generieke medicijnen zonder recept.
Wat is Coumadin en hoe wordt het gebruikt?
Coumadin is een receptgeneesmiddel dat wordt gebruikt om bloedstolsels te behandelen en om de kans op vorming van bloedstolsels in uw lichaam te verkleinen. Bloedstolsels kunnen een beroerte, hartaanval of andere ernstige aandoeningen veroorzaken als ze zich in de benen of longen vormen.
Wat zijn bijwerkingen van Coumadin?
Coumadin kan ernstige bijwerkingen veroorzaken, waaronder:
- Afsterven van huidweefsel (huidnecro's is of gangreen). Dit kan kort na het starten van Coumadin gebeuren. Het gebeurt omdat zich bloedstolsels vormen en de bloedstroom naar een deel van uw lichaam blokkeren. Bel onmiddellijk uw zorgverlener als u pijn, kleur of temperatuurverandering heeft in een deel van uw lichaam. Mogelijk hebt u meteen medische zorg nodig om overlijden of verlies (amputatie) van uw aangedane lichaamsdeel te voorkomen.
- Nierproblemen. Nierletsel kan optreden bij mensen die Coumadin gebruiken. Vertel het uw zorgverlener meteen als u bloed in uw urine krijgt. Uw zorgverlener kan tijdens de behandeling met Coumadin vaker testen doen om te controleren op bloedingen als u al nierproblemen heeft.
- "Paarse tenen-syndroom." Bel onmiddellijk uw zorgverlener als u pijn in uw tenen heeft en ze paars van kleur of donker van kleur zijn.
Dit zijn niet alle bijwerkingen van Coumadin. Vraag uw zorgverlener of apotheker om meer informatie. Bel uw arts voor medisch advies over bijwerkingen. U kunt bijwerkingen melden aan de FDA op 1-800-FDA-1088.
WAARSCHUWING
BLOEDINGSRISICO
- COUMADIN kan ernstige of fatale bloedingen veroorzaken [zie WAARSCHUWINGEN EN VOORZORGSMAATREGELEN ].
- Voer regelmatige controle van de INR uit bij alle behandelde patiënten [zie DOSERING EN ADMINISTRATIE ].
- Geneesmiddelen, veranderingen in het dieet en andere factoren beïnvloeden de INR-waarden die worden bereikt met COUMADIN 5 mg-therapie [zie DRUG-INTERACTIES ].
- Instrueer patiënten over preventiemaatregelen om het risico op bloedingen te minimaliseren en om tekenen en symptomen van bloedingen te melden [zie: PATIËNT INFORMATIE ].
OMSCHRIJVING
COUMADIN (warfarine-natrium) tabletten en COUMADIN (warfarine-natrium) voor injectie bevatten warfarine-natrium, een anticoagulans dat werkt door remming van vitamine K-afhankelijke stollingsfactoren. De chemische naam van warfarine-natrium is 3-(α-acetonylbenzyl)-4-hydroxycoumarine-natriumzout, dat een racemisch mengsel is van de R- en S-enantiomeren. Kristallijn warfarine-natrium is een isopropanolclathraat. De empirische formule is C19H15NaO4 en de structuurformule wordt weergegeven door het volgende:
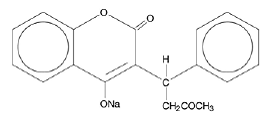
Kristallijn warfarine-natrium komt voor als een wit, geurloos, kristallijn poeder dat verkleurt door licht. Het is zeer oplosbaar in water, goed oplosbaar in alcohol en zeer slecht oplosbaar in chloroform en ether.
COUMADIN-tabletten voor oraal gebruik bevatten ook:
COUMADIN 1 mg voor injectie voor intraveneus gebruik wordt geleverd als een steriel, gevriesdroogd poeder dat, na reconstitutie met 2,7 ml steriel water voor injectie, het volgende bevat:
INDICATIES
COUMADIN® is geïndiceerd voor:
- Profylaxe en behandeling van veneuze trombose en de uitbreiding ervan, longembolie (PE).
- Profylaxe en behandeling van trombo-embolische complicaties geassocieerd met atriale fibrillatie (AF) en/of hartklepvervanging.
- Vermindering van het risico op overlijden, terugkerend myocardinfarct (MI) en trombo-embolische voorvallen zoals beroerte of systemische embolisatie na een myocardinfarct.
Beperkingen van gebruik
COUMADIN 2 mg heeft geen direct effect op een gevestigde trombus en herstelt ischemische weefselschade evenmin. Als er eenmaal een trombus is opgetreden, is het doel van behandeling met anticoagulantia echter het voorkomen van verdere uitbreiding van het gevormde stolsel en het voorkomen van secundaire trombo-embolische complicaties die kunnen leiden tot ernstige en mogelijk fatale gevolgen.
DOSERING EN ADMINISTRATIE
Geïndividualiseerde dosering
De dosering en toediening van COUMADIN 2 mg moet voor elke patiënt worden aangepast op basis van de INR-respons van de patiënt op het geneesmiddel. Pas de dosis aan op basis van de INR van de patiënt en de aandoening die wordt behandeld. Raadpleeg de nieuwste evidence-based klinische praktijkrichtlijnen met betrekking tot de duur en intensiteit van antistolling voor de aangegeven aandoeningen.
Aanbevolen INR-doelbereiken en -duur voor individuele indicaties
Een INR van meer dan 4,0 lijkt geen extra therapeutisch voordeel te bieden bij mos-patiënten en is geassocieerd met een hoger risico op bloedingen.
Veneuze trombo-embolie (inclusief diepe veneuze trombose [DVT] en PE)
Pas de warfarinedosis aan om een doel-INR van 2,5 (INR-bereik, 2,0-3,0) te behouden voor alle behandelingsduur.
De duur van de behandeling is als volgt gebaseerd op de indicatie:
- Voor patiënten met een DVT of PE secundair aan een voorbijgaande (reversibele) risicofactor, wordt een behandeling met warfarine gedurende 3 maanden aanbevolen.
- Voor patiënten met een niet-uitgelokte DVT of PE wordt behandeling met warfarine aanbevolen gedurende ten minste 3 maanden. Evalueer na 3 maanden therapie de risico-batenverhouding van langdurige behandeling voor de individuele patiënt.
- Voor patiënten met twee episodes van niet-uitgelokte DVT of PE wordt een langdurige behandeling met warfarine aanbevolen. Voor een patiënt die een langdurige antistollingsbehandeling krijgt, moet de risico-batenverhouding van het voortzetten van een dergelijke behandeling bij de individuele patiënt periodiek opnieuw worden beoordeeld.
Atriale fibrillatie
Bij patiënten met AF zonder klep, anticoaguleer met warfarine om een INR van 2,5 te bereiken (bereik 2,0-3,0).
- Bij patiënten met niet-valvulair AF dat persistent of paroxysmaal is en een hoog risico op een beroerte heeft (dwz met een van de volgende kenmerken: eerdere ischemische beroerte, voorbijgaande ischemische aanval of systemische embolie, of 2 van de volgende risicofactoren: leeftijd hoger ouder dan 75 jaar, matige of ernstige verminderde systolische functie van het linkerventrikel en/of hartfalen, voorgeschiedenis van hypertensie of diabetes mellitus), wordt langdurige antistolling met warfarine aanbevolen.
- Bij patiënten met niet-valvulair AF dat persistent of paroxysmaal is en met een intermediair risico op ischemische beroerte (dwz met 1 van de volgende risicofactoren: leeftijd ouder dan 75 jaar, matige of ernstige verminderde systolische linkerventrikelfunctie en/of hartfalen , voorgeschiedenis van hypertensie of diabetes mellitus), wordt langdurige antistolling met warfarine aanbevolen.
- Voor patiënten met AF en mitralisstenose wordt langdurige antistolling met warfarine aanbevolen.
- Voor patiënten met AF en prothetische hartkleppen wordt langdurige antistolling met warfarine aanbevolen; de beoogde INR kan worden verhoogd en aspirine kan worden toegevoegd, afhankelijk van het type en de positie van de klep en van patiëntfactoren.
Mechanische en bioprothetische hartkleppen
- Voor patiënten met een mechanische tweeklepsklep of een Medtronic Hall (Minneapolis, MN) kantelbare schijfklep in de aortapositie die in sinusritme zijn en zonder vergroting van het linker atrium, therapie met warfarine tot een beoogde INR van 2,5 (bereik, 2,0-3,0) is aanbevolen.
- Voor patiënten met kantelbare schijfkleppen en mechanische bileaflet-kleppen in de mitralispositie, wordt therapie met warfarine tot een beoogde INR van 3,0 (bereik 2,5-3,5) aanbevolen.
- Voor patiënten met gekooide kogelkleppen of gekooide schijfkleppen, wordt therapie met warfarine tot een beoogde INR van 3,0 (bereik, 2,5-3,5) aanbevolen.
- Voor patiënten met een bioprothetische klep in de mitralispositie wordt therapie met warfarine tot een beoogde INR van 2,5 (bereik, 2,0-3,0) aanbevolen gedurende de eerste 3 maanden na het inbrengen van de klep. Als er aanvullende risicofactoren voor trombo-embolie aanwezig zijn (AF, eerdere trombo-embolie, linkerventrikeldisfunctie), wordt een streef-INR van 2,5 (bereik 2,0-3,0) aanbevolen.
Post-myocardinfarct
- Voor hoogrisicopatiënten met MI (bijv. patiënten met een groot anterieur MI, patiënten met significant hartfalen, patiënten met intracardiale trombus zichtbaar op transthoracale echocardiografie, patiënten met AF en patiënten met een voorgeschiedenis van een trombo-embolisch voorval), therapie met gecombineerde matige intensiteit (INR, 2,0-3,0) warfarine plus een lage dosis aspirine (≤ 100 mg/dag) gedurende ten minste 3 maanden na het MI wordt aanbevolen.
Terugkerende systemische embolie en andere indicaties
Orale antistollingstherapie met warfarine is niet volledig geëvalueerd door klinische onderzoeken bij patiënten met klepziekte geassocieerd met AF, patiënten met mitralisstenose en patiënten met recidiverende systemische embolie met onbekende etiologie. Voor deze patiënten kan echter een matig doseringsschema (INR 2,0-3,0) worden gebruikt.
Initiële en onderhoudsdosering
De juiste aanvangsdosering van COUMADIN 2 mg varieert sterk voor verschillende patiënten. Niet alle factoren die verantwoordelijk zijn voor de variabiliteit van de warfarinedosis zijn bekend en de aanvangsdosis wordt beïnvloed door:
- Klinische factoren zoals leeftijd, ras, lichaamsgewicht, geslacht, gelijktijdige medicatie en comorbiditeiten
- Genetische factoren (CYP2C9- en VKORC1-genotypen) [zie KLINISCHE FARMACOLOGIE ].
Selecteer de startdosis op basis van de verwachte onderhoudsdosis, rekening houdend met bovenstaande factoren. Pas deze dosis aan op basis van patiëntspecifieke klinische factoren. Overweeg lagere aanvangs- en onderhoudsdoses voor oudere en/of verzwakte patiënten en bij Aziatische patiënten [zie: Gebruik bij specifieke populaties en KLINISCHE FARMACOLOGIE ]. Routinematig gebruik van oplaaddoses wordt niet aanbevolen omdat deze praktijk hemorragische en andere complicaties kan verhogen en geen snellere bescherming biedt tegen stolselvorming.
Individualiseer de duur van de therapie voor elke patiënt. In het algemeen dient de antistollingstherapie te worden voortgezet totdat het gevaar van trombose en embolie geweken is [zie Aanbevolen INR-doelbereiken en -duur voor individuele indicaties ].
Doseringsaanbevelingen zonder rekening te houden met genotype
Als de CYP2C9- en VKORC1-genotypen van de patiënt niet bekend zijn, is de aanvangsdosis van COUMADIN 1 mg gewoonlijk 2 tot 5 mg eenmaal daags. Bepaal de doseringsbehoeften van elke patiënt door nauwlettend toezicht te houden op de INR-respons en rekening te houden met de indicatie die wordt behandeld. Typische onderhoudsdoses zijn 2 tot 10 mg eenmaal daags.
Doseringsaanbevelingen met inachtneming van het genotype
Tabel 1 toont drie reeksen van verwachte onderhoudsdoses COUMADIN waargenomen in subgroepen van patiënten met verschillende combinaties van CYP2C9- en VKORC1-genvarianten [zie KLINISCHE FARMACOLOGIE ]. Als het CYP2C9- en/of VKORC1-genotype van de patiënt bekend is, moet u rekening houden met deze bereiken bij het kiezen van de startdosis. Patiënten met CYP2C9 *1/*3, *2/*2, *2/*3 en *3/*3 hebben mogelijk meer tijd nodig (>2 tot 4 weken) om een maximaal INR-effect te bereiken voor een bepaald doseringsschema dan patiënten zonder deze CYP-varianten.
Monitoring om optimale antistolling te bereiken
COUMADIN heeft een smal therapeutisch bereik (index) en de werking ervan kan worden beïnvloed door factoren zoals andere geneesmiddelen en vitamine K in de voeding. Daarom moet de antistolling zorgvuldig worden gecontroleerd tijdens de behandeling met COUMADIN. Bepaal dagelijks de INR na toediening van de aanvangsdosis totdat de INR-resultaten stabiliseren in het therapeutische bereik. Na stabilisatie de dosering binnen het therapeutische bereik houden door periodieke INR's uit te voeren. De frequentie van het uitvoeren van INR moet gebaseerd zijn op de klinische situatie, maar over het algemeen aanvaardbare intervallen voor INR-bepalingen zijn 1 tot 4 weken. Voer aanvullende INR-tests uit wanneer andere warfarineproducten worden uitgewisseld met COUMADIN, evenals wanneer andere medicijnen worden gestart, stopgezet of onregelmatig worden ingenomen. Heparine, een veelgebruikt gelijktijdig geneesmiddel, verhoogt de INR [zie Conversie van andere anticoagulantia en DRUG-INTERACTIES ].
Bepalingen van de stolling van volbloed en de bloedingstijd zijn geen effectieve maatregelen voor het controleren van de behandeling met COUMADIN 5 mg.
Nierfunctiestoornis
Bij patiënten met nierfalen is geen dosisaanpassing nodig. Controleer de INR vaker bij patiënten met een verminderde nierfunctie om de INR binnen het therapeutische bereik te houden [zie: WAARSCHUWINGEN EN VOORZORGSMAATREGELEN en Gebruik bij specifieke populaties ].
Gemiste dosis
Het anticoagulerende effect van COUMADIN houdt langer dan 24 uur aan. Als een patiënt een dosis COUMADIN op het beoogde tijdstip van de dag overslaat, moet de patiënt de dosis zo snel mogelijk op dezelfde dag innemen. De patiënt mag de dosis de volgende dag niet verdubbelen om een vergeten dosis in te halen.
Intraveneuze toedieningsweg
De intraveneuze dosis COUMADIN 1 mg is hetzelfde als de orale dosis. Dien na reconstitutie COUMADIN voor injectie toe als een langzame bolusinjectie in een perifere ader gedurende 1 tot 2 minuten.
COUMADIN 2 mg voor injectie wordt niet aanbevolen voor intramusculaire toediening.
Reconstitueer de injectieflacon met 2,7 ml steriel water voor injectie. De resulterende opbrengst is 2,5 ml van een oplossing van 2 mg per ml (5 mg in totaal). Parenterale geneesmiddelen moeten vóór toediening visueel worden geïnspecteerd op deeltjes en verkleuring, wanneer de oplossing en de container dit toelaten. Niet gebruiken als deeltjes of verkleuring worden opgemerkt.
Na reconstitutie is COUMADIN voor injectie 4 uur stabiel bij kamertemperatuur. Het bevat geen antimicrobieel conserveermiddel en daarom moet ervoor worden gezorgd dat de steriliteit van de bereide oplossing wordt gewaarborgd. De injectieflacon is uitsluitend voor eenmalig gebruik, gooi ongebruikte oplossing weg.
Behandeling tijdens tandheelkunde en chirurgie
Bij sommige tandheelkundige of chirurgische ingrepen kan het nodig zijn de behandeling met COUMADIN te onderbreken of te wijzigen. Overweeg de voordelen en risico's wanneer u stopt met COUMADIN 2 mg, zelfs voor een korte periode. Bepaal de INR onmiddellijk voorafgaand aan een tandheelkundige of chirurgische ingreep. Bij patiënten die minimaal invasieve procedures ondergaan en die vóór, tijdens of onmiddellijk na deze procedures moeten worden geanticoaguleerd, kan het aanpassen van de dosering van COUMADIN om de INR aan de lage kant van het therapeutische bereik te houden, veilig voortzetting van de anticoagulatie mogelijk maken.
Conversie van andere anticoagulantia
Heparine
Aangezien het volledige antistollingseffect van COUMADIN 2 mg pas enkele dagen wordt bereikt, heeft heparine de voorkeur voor een initiële snelle antistolling. Tijdens de initiële therapie met COUMADIN is de interferentie met heparine-anticoagulatie van minimaal klinisch belang. Conversie naar COUMADIN kan gelijktijdig met heparinetherapie beginnen of kan 3 tot 6 dagen worden uitgesteld. Om therapeutische antistolling te verzekeren, moet de heparine-therapie met volledige dosis worden voortgezet en de COUMADIN-therapie met heparine gedurende 4 tot 5 dagen worden overlapt en totdat COUMADIN 2 mg de gewenste therapeutische respons heeft opgeleverd, zoals bepaald door de INR, op welk punt de heparine kan worden stopgezet.
Aangezien heparine de INR kan beïnvloeden, moeten patiënten die zowel heparine als COUMADIN 1 mg krijgen, de INR-controle ten minste ondergaan:
- 5 uur na de laatste intraveneuze bolusdosis heparine, of
- 4 uur na stopzetting van een continue intraveneuze infusie van heparine, of
- 24 uur na de laatste subcutane injectie met heparine.
COUMADIN 1 mg kan de geactiveerde partiële tromboplastinetijd (aPTT)-test verhogen, zelfs in afwezigheid van heparine. Een ernstige verhoging (>50 seconden) in aPTT met een INR in het gewenste bereik is geïdentificeerd als een indicatie van een verhoogd risico op postoperatieve bloeding.
Andere anticoagulantia
Raadpleeg de etikettering van andere anticoagulantia voor instructies over conversie naar COUMADIN.
HOE GELEVERD
Doseringsvormen en sterke punten
Tabletten
COUMADIN tabletten met enkelvoudige score
Voor injectie
Voor injectie: 5 mg, gevriesdroogd poeder in een injectieflacon voor eenmalig gebruik.
Opslag en behandeling
Tabletten
COUMADIN-tabletten hebben een enkele breukgleuf met één kant numeriek bedrukt met 1, 2, 2-1, 2, 3, 4, 5, 6, 7-1 / 2 of 10 en gegraveerd met "COUMADIN" en met de andere kant vlak. COUMADIN is verkrijgbaar in flessen en blisterverpakkingen voor ziekenhuiseenheid met de volgende potenties en kleuren:
Beschermen tegen licht en vocht. Bewaren bij een gecontroleerde kamertemperatuur (59 ° -86 ° F, 15 ° - 30 ° C). Doseer in een strakke, lichtbestendige container zoals gedefinieerd in de USP.
Bewaar de blisterverpakkingen met ziekenhuiseenheidsdosis in de doos totdat de inhoud is gebruikt.
Injectie
COUMADIN voor injectieflacons leveren 5 mg warfarine op na reconstitutie met 2,7 ml steriel water voor injectie (maximale opbrengst is 2,5 ml van een oplossing van 2 mg/ml). De netto inhoud van de injectieflacon is 5,4 mg gevriesdroogd poeder.
5 mg injectieflacon (doos van 6) - NDC 0590-0324-35
Bescherm tegen licht. Bewaar de injectieflacon in de doos tot gebruik. Bewaren bij een gecontroleerde kamertemperatuur (59 ° -86 ° F, 15 ° - 30 ° C).
Na reconstitutie bewaren bij gecontroleerde kamertemperatuur (59°-86°F, 15°-30°C) en binnen 4 uur gebruiken.
Niet in de koelkast bewaren. Gooi ongebruikte oplossing weg.
Speciale behandeling
Procedures voor de juiste behandeling en verwijdering van potentieel gevaarlijke geneesmiddelen moeten worden overwogen.
Richtlijnen over dit onderwerp zijn gepubliceerd [ zie REFERENTIES ].
Apothekers en klinisch personeel dat zwanger is, moet blootstelling aan fijngemaakte of gebroken tabletten vermijden [zie: Gebruik bij specifieke populaties ].
REFERENTIES
OSHA Gevaarlijke Drugs. OSHA. http://www.osha.gov/SLTC/hazardousdrugs/index.html.
Gedistribueerd door: Bristol-Myers Squibb Company, Princeton, New Jersey 08543 VS. Herzien: juni 2017
BIJWERKINGEN
De volgende ernstige bijwerkingen van COUMADIN 2 mg worden in meer detail besproken in andere rubrieken van de etikettering:
- bloeding [zie DOOS WAARSCHUWING: , WAARSCHUWINGEN EN VOORZORGSMAATREGELEN en OVERDOSERING ]
- Weefselnecrose [zie WAARSCHUWINGEN EN VOORZORGSMAATREGELEN ]
- Calciphylaxis [zie WAARSCHUWINGEN EN VOORZORGSMAATREGELEN ]
- Acuut nierletsel [zie WAARSCHUWINGEN EN VOORZORGSMAATREGELEN ]
- Systemische atheroemboli en cholesterolmicro-emboli [zie WAARSCHUWINGEN EN VOORZORGSMAATREGELEN ]
- Ischemie, necrose en gangreen van de ledematen bij patiënten met HIT en HITTS [zie WAARSCHUWINGEN EN VOORZORGSMAATREGELEN ]
- Andere klinische instellingen met verhoogde risico's [zie WAARSCHUWINGEN EN VOORZORGSMAATREGELEN ]
Andere bijwerkingen van COUMADIN 1 mg zijn onder meer:
- Immuunsysteemaandoeningen: overgevoeligheid/allergische reacties (inclusief urticaria en anafylactische reacties)
- Bloedvataandoeningen: vasculitis
- Lever- en galaandoeningen: hepatitis, verhoogde leverenzymen. Cholestatische hepatitis is in verband gebracht met gelijktijdige toediening van COUMADIN en ticlopidine.
- Maagdarmstelselaandoeningen: misselijkheid, braken, diarree, smaakvervorming, buikpijn, winderigheid, opgeblazen gevoel
- Huidaandoeningen: huiduitslag, dermatitis (inclusief bulleuze erupties), pruritus, alopecia
- Ademhalingsstoornissen: tracheale of tracheobronchiale calcificatie
- Algemene aandoeningen: koude rillingen
DRUG-INTERACTIES
Geneesmiddelen kunnen interageren met COUMADIN 5 mg via farmacodynamische of farmacokinetische mechanismen. Farmacodynamische mechanismen voor geneesmiddelinteracties met COUMADIN 2 mg zijn synergisme (verminderde hemostase, verminderde synthese van stollingsfactoren), competitief antagonisme (vitamine K) en wijziging van de fysiologische regelkring voor vitamine K-metabolisme (erfelijke resistentie). Farmacokinetische mechanismen voor geneesmiddelinteracties met COUMADIN zijn voornamelijk enzyminductie, enzymremming en verminderde plasma-eiwitbinding. Het is belangrijk op te merken dat sommige geneesmiddelen kunnen interageren door meer dan één mechanisme. Frequentere INR-monitoring moet worden uitgevoerd bij het starten of stoppen van andere geneesmiddelen, waaronder plantaardige, of bij het wijzigen van doseringen van andere geneesmiddelen, inclusief geneesmiddelen die bedoeld zijn voor kortdurend gebruik (bijv. antibiotica, antischimmelmiddelen, corticosteroïden) [zie DOOS WAARSCHUWING: ].
Raadpleeg de etikettering van alle gelijktijdig gebruikte geneesmiddelen voor meer informatie over interacties met COUMADIN of bijwerkingen met betrekking tot bloedingen.
CYP450-interacties
CYP450-iso-zymen die betrokken zijn bij het metabolisme van warfarine zijn onder meer CYP2C9, 2C19, 2C8, 2C18, 1A2 en 3A4. Het krachtigere warfarine S-enantiomeer wordt gemetaboliseerd door CYP2C9, terwijl het R-enantiomeer wordt gemetaboliseerd door CYP1A2 en 3A4.
- Remmers van CYP2C9, 1A2 en/of 3A4 kunnen het effect (de INR verhogen) van warfarine versterken door de blootstelling aan warfarine te verhogen.
- Inductoren van CYP2C9, 1A2 en/of 3A4 kunnen het effect (verlaging van de INR) van warfarine verminderen door de blootstelling aan warfarine te verminderen.
Voorbeelden van remmers en inductoren van CYP2C9, 1A2 en 3A4 staan hieronder in tabel 2; deze lijst mag echter niet als allesomvattend worden beschouwd. Raadpleeg de etikettering van alle gelijktijdig gebruikte geneesmiddelen voor meer informatie over het CYP450-interactiepotentieel. Bij het starten, stoppen of wijzigen van de dosis van gelijktijdig toegediende medicatie moet rekening worden gehouden met het potentieel voor remming en inductie van CYP450. Houd de INR nauwlettend in de gaten als een gelijktijdig geneesmiddel een CYP2C9-, 1A2- en/of 3A4-remmer of -inductor is.
Geneesmiddelen die het bloedingsrisico vergroten
Voorbeelden van geneesmiddelen waarvan bekend is dat ze het risico op bloedingen verhogen, worden weergegeven in Tabel 3. Omdat het bloedingsrisico groter is wanneer deze geneesmiddelen gelijktijdig met warfarine worden gebruikt, moeten patiënten die een dergelijk geneesmiddel samen met warfarine krijgen nauwlettend worden gevolgd.
Antibiotica en antischimmelmiddelen
Er zijn meldingen geweest van veranderingen in INR bij patiënten die warfarine en antibiotica of antischimmelmiddelen gebruiken, maar klinische farmacokinetische onderzoeken hebben geen consistente effecten van deze middelen op de plasmaconcentraties van warfarine aangetoond.
Houd de INR nauwlettend in de gaten bij het starten of stoppen van een antibioticum of antischimmelmiddel bij patiënten die warfarine gebruiken.
Botanische (kruiden)producten en voedingsmiddelen
Frequentere INR-monitoring moet worden uitgevoerd bij het starten of stoppen van botanische middelen.
Er zijn maar weinig adequate, goed gecontroleerde onderzoeken die het potentieel voor metabole en/of farmacologische interacties tussen plantaardige en COUMADIN 2 mg evalueren. Door een gebrek aan productiestandaardisatie met botanische medicinale preparaten, kan de hoeveelheid actieve ingrediënten variëren. Dit zou het vermogen om mogelijke interacties en effecten op antistolling te beoordelen verder in de war kunnen brengen.
Sommige plantaardige middelen kunnen bloedingen veroorzaken wanneer ze alleen worden ingenomen (bijv. knoflook en Ginkgo biloba) en kunnen anticoagulantia, antibloedplaatjes en/of fibrinolytische eigenschappen hebben. Deze effecten zouden naar verwachting een aanvulling zijn op de anticoagulerende effecten van COUMADIN. Omgekeerd kunnen sommige plantaardige middelen de effecten van COUMADIN verminderen (bijv. co-enzym Q10, sint-janskruid, ginseng). Sommige plantaardige stoffen en voedingsmiddelen kunnen een wisselwerking hebben met COUMADIN 2 mg via CYP450-interacties (bijv. echinacea, grapefruitsap, ginkgo, goldenseal, sint-janskruid).
De hoeveelheid vitamine K in voedsel kan de behandeling met COUMADIN beïnvloeden. Adviseer patiënten die COUMADIN 1 mg gebruiken om een normaal, uitgebalanceerd dieet te volgen met behoud van een constante hoeveelheid vitamine K. Patiënten die COUMADIN 5 mg gebruiken, moeten drastische veranderingen in hun voedingsgewoonten vermijden, zoals het eten van grote hoeveelheden groene bladgroenten.
WAARSCHUWINGEN
Inbegrepen als onderdeel van de "PREVENTIEVE MAATREGELEN" Sectie
PREVENTIEVE MAATREGELEN
Bloeding
COUMADIN kan ernstige of fatale bloedingen veroorzaken. Bloedingen treden vaker op in de eerste maand. Risicofactoren voor bloedingen zijn onder meer hoge intensiteit van antistolling (INR >4,0), leeftijd hoger dan of gelijk aan 65, voorgeschiedenis van zeer variabele INR's, voorgeschiedenis van gastro-intestinale bloedingen, hypertensie, cerebrovasculaire ziekte, anemie, maligniteit, trauma, nierfunctiestoornis, bepaalde genetische factoren [zie KLINISCHE FARMACOLOGIE ], bepaalde gelijktijdig gebruikte geneesmiddelen [zie DRUG-INTERACTIES ], en langdurige behandeling met warfarine.
Voer regelmatige controle van de INR uit bij alle behandelde patiënten. Degenen met een hoog risico op bloedingen kunnen baat hebben bij frequentere INR-controle, zorgvuldige dosisaanpassing aan de gewenste INR en een kortste behandelingsduur die geschikt is voor de klinische toestand. Het handhaven van de INR binnen het therapeutische bereik elimineert het risico op bloedingen echter niet.
Geneesmiddelen, veranderingen in het dieet en andere factoren beïnvloeden de INR-waarden die worden bereikt met de behandeling met COUMADIN 1 mg. Voer vaker INR-controle uit bij het starten of stoppen van andere geneesmiddelen, inclusief plantaardige middelen, of bij het wijzigen van doseringen van andere geneesmiddelen [zie DRUG-INTERACTIES ].
Instrueer patiënten over preventiemaatregelen om het risico op bloedingen te minimaliseren en om tekenen en symptomen van bloedingen te melden [zie: PATIËNT INFORMATIE ].
Weefselnecrose
Necrose en/of gangreen van huid en andere weefsels is een ongewoon maar ernstig risico (
Zorgvuldige klinische evaluatie is vereist om te bepalen of necrose wordt veroorzaakt door een onderliggende ziekte. Hoewel verschillende behandelingen zijn geprobeerd, is geen enkele behandeling voor necrose als uniform effectief beschouwd. Stop de behandeling met COUMADIN 5 mg als necrose optreedt. Overweeg alternatieve geneesmiddelen als voortzetting van de antistollingstherapie noodzakelijk is.
calciphylaxis
Fatale en ernstige calciphylaxis of calcium-uremische arteriolopathie is gemeld bij patiënten met en zonder terminale nierziekte. Als bij deze patiënten calciphylaxis wordt vastgesteld, stop dan met COUMADIN 5 mg en behandel calciphylaxis waar nodig. Overweeg alternatieve antistollingstherapie.
Acuut nierletsel
Bij patiënten met veranderde glomerulaire integriteit of met een voorgeschiedenis van nierziekte, kan acuut nierletsel optreden met COUMADIN 2 mg, mogelijk in verband met episodes van overmatige antistolling en hematurie [zie Gebruik bij specifieke populaties ]. Bij patiënten met een verminderde nierfunctie wordt frequentere controle van de antistolling aanbevolen.
Systemische atheroemboli en cholesterolmicro-emboli
Antistollingstherapie met COUMADIN kan de afgifte van atheromateuze plaque-embolie bevorderen. Systemische atheroemboli en cholesterolmicro-embolieën kunnen verschillende tekenen en symptomen vertonen, afhankelijk van de plaats van embolisatie. De meest betrokken viscerale organen zijn de nieren, gevolgd door de pancreas, milt en lever. Sommige gevallen zijn geëvolueerd tot necrose of overlijden. Een duidelijk syndroom als gevolg van micro-emboli aan de voeten staat bekend als het "paarse tenen-syndroom". Stop de behandeling met COUMADIN als dergelijke verschijnselen worden waargenomen. Overweeg alternatieve geneesmiddelen als voortzetting van de antistollingstherapie noodzakelijk is.
Ischemie, necrose en gangreen van de ledematen bij patiënten met HIT en HITTS
Gebruik COUMADIN niet als initiële therapie bij patiënten met heparine-geïnduceerde trombocytopenie (HIT) en met heparine-geïnduceerde trombocytopenie met trombosesyndroom (HITTS). Gevallen van ischemie, necrose en gangreen van de ledematen zijn opgetreden bij patiënten met HIT en HITTS wanneer de behandeling met heparine werd stopgezet en de behandeling met warfarine werd gestart of voortgezet. Bij sommige patiënten waren de gevolgen amputatie van het betrokken gebied en/of overlijden. Behandeling met COUMADIN kan worden overwogen nadat het aantal bloedplaatjes is genormaliseerd.
Gebruik bij zwangere vrouwen met mechanische hartkleppen
COUMADIN kan schade aan de foetus veroorzaken wanneer het wordt toegediend aan een zwangere vrouw. Hoewel COUMADIN gecontra-indiceerd is tijdens de zwangerschap, kunnen de mogelijke voordelen van het gebruik van COUMADIN 1 mg opwegen tegen de risico's voor zwangere vrouwen met mechanische hartkleppen met een hoog risico op trombo-embolie. In die individuele situaties moet de beslissing om met COUMADIN 2 mg te starten of door te gaan met de patiënt worden besproken, waarbij rekening moet worden gehouden met de specifieke risico's en voordelen met betrekking tot de medische situatie van de individuele patiënt, evenals met de meest actuele medische richtlijnen. Blootstelling aan COUMADIN tijdens de zwangerschap veroorzaakt een erkend patroon van ernstige aangeboren misvormingen (warfarine-embryopathie en foetotoxiciteit), fatale foetale bloeding en een verhoogd risico op spontane abortus en foetale mortaliteit. Als dit geneesmiddel tijdens de zwangerschap wordt gebruikt, of als de patiënte zwanger wordt tijdens het gebruik van dit geneesmiddel, moet de patiënt op de hoogte worden gesteld van het mogelijke gevaar voor een foetus [zie Gebruik bij specifieke populaties ].
Andere klinische instellingen met verhoogde risico's
In de volgende klinische situaties kunnen de risico's van behandeling met COUMADIN verhoogd zijn:
- Matige tot ernstige leverfunctiestoornis
- Infectieziekten of verstoringen van de darmflora (bijv. spruw, antibioticatherapie)
- Gebruik van een verblijfskatheter
- Ernstige tot matige hypertensie
- Deficiëntie in proteïne C-gemedieerde antistollingsrespons: COUMADIN vermindert de synthese van de natuurlijk voorkomende anticoagulantia, proteïne C en proteïne S. Erfelijke of verworven deficiënties van proteïne C of zijn cofactor, proteïne S, zijn in verband gebracht met weefselnecrose na toediening van warfarine. Gelijktijdige antistollingstherapie met heparine gedurende 5 tot 7 dagen tijdens de start van de therapie met COUMADIN 2 mg kan de incidentie van weefselnecrose bij deze patiënten minimaliseren.
- Oogchirurgie: Bij cataractchirurgie ging het gebruik van COUMADIN gepaard met een significante toename van kleine complicaties van een scherpe naald en lokaal anesthesieblok, maar niet met potentieel gezichtsbedreigende operatieve hemorragische complicaties. Aangezien stopzetting of vermindering van COUMADIN 5 mg kan leiden tot ernstige trombo-embolische complicaties, moet de beslissing om met COUMADIN te stoppen vóór een relatief minder ingrijpende en complexe oogoperatie, zoals lenschirurgie, gebaseerd zijn op de risico's van anticoagulantia, afgewogen tegen de voordelen.
- Polycytemie Vera
- Vasculitis
- Suikerziekte
Endogene factoren die van invloed zijn op INR
De volgende factoren kunnen verantwoordelijk zijn voor een verhoogde INR-respons: diarree, leveraandoeningen, slechte voedingstoestand, steatorroe of vitamine K-tekort.
De volgende factoren kunnen verantwoordelijk zijn voor een verminderde INR-respons: verhoogde vitamine K-inname of erfelijke warfarineresistentie.
Informatie over patiëntbegeleiding
Adviseer de patiënt om de door de FDA goedgekeurde patiëntetikettering te lezen ( Medicatiegids ).
Instructies voor patiënten
Adviseer patiënten om:
- Houd u strikt aan het voorgeschreven doseringsschema [zie DOSERING EN ADMINISTRATIE ].
- Als de voorgeschreven dosis COUMADIN 1 mg is vergeten, neem de dosis dan zo snel mogelijk op dezelfde dag in, maar neem de volgende dag geen dubbele dosis COUMADIN 5 mg om een vergeten dosis in te halen [zie DOSERING EN ADMINISTRATIE ].
- Verkrijg protrombinetijdtests en breng regelmatig een bezoek aan hun arts of kliniek om de therapie te controleren [zie DOSERING EN ADMINISTRATIE ] .
- Houd er rekening mee dat als de behandeling met COUMADIN wordt stopgezet, de anticoagulerende effecten van COUMADIN 5 mg ongeveer 2 tot 5 dagen kunnen aanhouden (zie KLINISCHE FARMACOLOGIE ].
- Vermijd elke activiteit of sport die kan leiden tot traumatisch letsel [zie Gebruik bij specifieke populaties ]. En om hun arts te vertellen als ze vaak vallen, omdat dit hun risico op complicaties kan vergroten.
- Eet een normaal, uitgebalanceerd dieet om een constante inname van vitamine K te behouden. Vermijd drastische veranderingen in voedingsgewoonten, zoals het eten van grote hoeveelheden groene bladgroenten [zie DRUG-INTERACTIES ].
- Neem contact op met hun arts om een ernstige ziekte te melden, zoals ernstige diarree, infectie of koorts [zie WAARSCHUWINGEN EN VOORZORGSMAATREGELEN en ONGEWENSTE REACTIES ].
- Draag een identificatiebewijs waarin staat dat ze COUMADIN gebruiken.
Bloedingsrisico's
Adviseer patiënten om
- Breng hun arts onmiddellijk op de hoogte als er ongebruikelijke bloedingen of symptomen optreden. Tekenen en symptomen van bloeding zijn onder meer: pijn, zwelling of ongemak, langdurig bloeden door snijwonden, verhoogde menstruatie of vaginale bloedingen, neusbloedingen, tandvleesbloedingen door poetsen, ongewone bloedingen of blauwe plekken, rode of donkerbruine urine, rode of teerzwarte ontlasting, hoofdpijn, duizeligheid of zwakte [zie DOOS WAARSCHUWING: en WAARSCHUWINGEN EN VOORZORGSMAATREGELEN ].
Gelijktijdige medicatie en botanica (kruiden)
Adviseer patiënten om:
- Gebruik of stop geen andere geneesmiddelen, inclusief salicylaten (bijv. aspirine en actuele pijnstillers), andere vrij verkrijgbare medicijnen en botanische (kruiden) producten, behalve op advies van uw arts [zie DRUG-INTERACTIES ].
Zwangerschap en verpleging
Adviseer patiënten om:
- Neem contact op met hun arts
- onmiddellijk als ze denken dat ze zwanger zijn [zie Gebruik bij specifieke populaties ],
- zwangerschapsplanning bespreken [zie Gebruik bij specifieke populaties ],
- als ze overwegen borstvoeding te geven [zie Gebruik bij specifieke populaties ].
Niet-klinische toxicologie
Carcinogenese, mutagenese, verminderde vruchtbaarheid
Er zijn geen carcinogeniteits-, mutageniteits- of vruchtbaarheidsonderzoeken uitgevoerd met warfarine.
Gebruik bij specifieke populaties
Zwangerschap
Risico Samenvatting
COUMADIN 1 mg is gecontra-indiceerd bij vrouwen die zwanger zijn, behalve bij zwangere vrouwen met mechanische hartkleppen, die een hoog risico lopen op trombo-embolie en voor wie de voordelen van COUMADIN 5 mg opwegen tegen de risico's [zie WAARSCHUWINGEN EN VOORZORGSMAATREGELEN ]. COUMADIN 1 mg kan schade aan de foetus veroorzaken. Blootstelling aan warfarine tijdens het eerste trimester van de zwangerschap veroorzaakte een patroon van aangeboren afwijkingen bij ongeveer 5% van de blootgestelde nakomelingen. Omdat deze gegevens niet zijn verzameld in adequate en goed gecontroleerde onderzoeken, is deze incidentie van ernstige geboorteafwijkingen geen adequate basis voor vergelijking met de geschatte incidenties in de controlegroep of de Amerikaanse algemene bevolking en komt deze mogelijk niet overeen met de incidenties die in de praktijk zijn waargenomen. Overweeg de voordelen en risico's van COUMADIN en mogelijke risico's voor de foetus bij het voorschrijven van COUMADIN aan een zwangere vrouw.
Bijwerkingen tijdens de zwangerschap treden op ongeacht de gezondheid van de moeder of het gebruik van medicijnen. Het geschatte achtergrondrisico van ernstige geboorteafwijkingen en miskraam voor de aangegeven populatie is niet bekend. In de algemene bevolking van de VS is het geschatte achtergrondrisico van ernstige geboorteafwijkingen en miskraam bij klinisch erkende zwangerschappen respectievelijk 2% tot 4% en 15% tot 20%.
Klinische overwegingen
Foetale/neonatale bijwerkingen
Bij mensen passeert warfarine de placenta en de concentraties in foetaal plasma benaderen de maternale waarden. Blootstelling aan warfarine tijdens het eerste trimester van de zwangerschap veroorzaakte een patroon van aangeboren afwijkingen bij ongeveer 5% van de blootgestelde nakomelingen. Warfarine-embryopathie wordt gekenmerkt door nasale hypoplasie met of zonder gestippelde epifysen (chondrodysplasia punctata) en groeiachterstand (inclusief laag geboortegewicht). Afwijkingen van het centrale zenuwstelsel en het oog zijn ook gemeld, waaronder dysplasie van de dorsale middellijn, gekenmerkt door agenesie van het corpus callosum, Dandy-Walker-misvorming, cerebellaire atrofie van de middellijn en dysplasie van de ventrale middellijn gekenmerkt door optische atrofie. Mentale achterstand, blindheid, schizencefalie, microcefalie, hydrocephalus en andere nadelige zwangerschapsuitkomsten zijn gemeld na blootstelling aan warfarine tijdens het tweede en derde trimester van de zwangerschap [zie CONTRA-INDICATIES ].
Borstvoeding
Risico Samenvatting
Warfarine was niet aanwezig in moedermelk van moeders die werden behandeld met warfarine uit een beperkt gepubliceerd onderzoek. Vanwege de mogelijkheid van ernstige bijwerkingen, waaronder bloedingen bij een zuigeling die borstvoeding krijgt, dient u rekening te houden met de ontwikkelings- en gezondheidsvoordelen van borstvoeding, samen met de klinische behoefte van de moeder aan COUMADIN en eventuele nadelige effecten op de zuigeling die borstvoeding krijgt van COUMADIN 2 mg of van de onderliggende maternale aandoening voordat u COUMADIN 5 mg voorschrijft aan een vrouw die borstvoeding geeft.
Klinische overwegingen
Controleer zuigelingen die borstvoeding geven op blauwe plekken of bloedingen.
Gegevens
Menselijke gegevens
Op basis van gepubliceerde gegevens bij 15 moeders die borstvoeding geven, werd warfarine niet aangetroffen in moedermelk. Van de 15 voldragen pasgeborenen hadden 6 zuigelingen die borstvoeding gaven gedocumenteerde protrombinetijden binnen het verwachte bereik. Voor de andere 9 zuigelingen werden geen protrombinetijden verkregen. Effecten bij premature baby's zijn niet geëvalueerd.
Vrouwtjes en mannetjes met reproductief potentieel
Zwangerschapstesten
COUMADIN kan schade aan de foetus veroorzaken [zie Gebruik bij specifieke populaties ].
Controleer de zwangerschapsstatus van vruchtbare vrouwen voordat de behandeling met COUMADIN wordt gestart.
anticonceptie
vrouwen
Adviseer vrouwen in de vruchtbare leeftijd om effectieve anticonceptie te gebruiken tijdens de behandeling en gedurende ten minste 1 maand na de laatste dosis COUMADIN.
Pediatrisch gebruik
Adequate en goed gecontroleerde onderzoeken met COUMADIN zijn bij geen enkele pediatrische populatie uitgevoerd en de optimale dosering, veiligheid en werkzaamheid bij pediatrische patiënten is niet bekend. Pediatrisch gebruik van COUMADIN is gebaseerd op gegevens en aanbevelingen voor volwassenen en beschikbare beperkte pediatrische gegevens uit observationele onderzoeken en patiëntenregisters. Pediatrische patiënten die COUMADIN 1 mg krijgen toegediend, moeten elke activiteit of sport vermijden die kan leiden tot traumatisch letsel.
Het zich ontwikkelende hemostatische systeem bij zuigelingen en kinderen resulteert in een veranderende fysiologie van trombose en reactie op anticoagulantia. De dosering van warfarine bij de pediatrische populatie varieert per patiëntleeftijd, waarbij zuigelingen over het algemeen de hoogste dosis nodig hebben en adolescenten de laagste dosisvereisten in milligram per kilogram om de beoogde INR's te handhaven. Vanwege veranderende vereisten voor warfarine als gevolg van leeftijd, gelijktijdige medicatie, dieet en bestaande medische aandoening, kan het bij pediatrische patiënten moeilijk zijn om het doel-INR-bereik te bereiken en te handhaven, en frequentere INR-bepalingen worden aanbevolen.
Bloedingspercentages varieerden per patiëntenpopulatie en klinisch zorgcentrum in observatieonderzoeken bij kinderen en patiëntenregistraties.
Zuigelingen en kinderen die met vitamine K aangevulde voeding krijgen, inclusief zuigelingenvoeding, kunnen resistent zijn tegen behandeling met warfarine, terwijl zuigelingen die moedermelk krijgen gevoelig kunnen zijn voor behandeling met warfarine.
Geriatrisch gebruik
Van het totale aantal patiënten dat warfarine-natrium kreeg in gecontroleerde klinische onderzoeken waarvoor gegevens beschikbaar waren voor analyse, waren 1885 patiënten (24,4%) 65 jaar en ouder, terwijl 185 patiënten (2,4%) 75 jaar en ouder waren. Er werden geen algemene verschillen in werkzaamheid of veiligheid waargenomen tussen deze patiënten en jongere patiënten, maar een grotere gevoeligheid van sommige oudere personen kan niet worden uitgesloten.
Patiënten van 60 jaar of ouder lijken een groter dan verwachte INR-respons te vertonen op de anticoagulerende effecten van warfarine [zie: KLINISCHE FARMACOLOGIE ]. COUMADIN is gecontra-indiceerd bij patiënten zonder toezicht met seniliteit. Wees voorzichtig bij het toedienen van COUMADIN aan oudere patiënten in elke situatie of met elke fysieke aandoening waarbij een verhoogd risico op bloedingen aanwezig is. Overweeg lagere aanvangs- en onderhoudsdoses van COUMADIN bij oudere patiënten [zie: DOSERING EN ADMINISTRATIE ].
Nierfunctiestoornis
Nierklaring wordt beschouwd als een minder belangrijke determinant van de antistollingsrespons op warfarine. Er is geen dosisaanpassing nodig voor patiënten met nierinsufficiëntie. Instrueer patiënten met een nierfunctiestoornis die warfarine gebruiken om hun INR vaker te controleren [zie: WAARSCHUWINGEN EN VOORZORGSMAATREGELEN ].
Leverfunctiestoornis
Leverinsufficiëntie kan de respons op warfarine versterken door een gestoorde synthese van stollingsfactoren en een verminderd metabolisme van warfarine. Wees voorzichtig bij het gebruik van COUMADIN bij deze patiënten.
OVERDOSERING
Tekenen en symptomen
Bloedingen (bijv. verschijnen van bloed in ontlasting of urine, hematurie, overmatige menstruatiebloeding, melena, petechiën, overmatige blauwe plekken of aanhoudend sijpelen van oppervlakkige verwondingen, onverklaarbare daling van hemoglobine) is een manifestatie van overmatige antistolling.
Behandeling
De behandeling van overmatige antistolling is gebaseerd op het niveau van de INR, de aan- of afwezigheid van bloedingen en klinische omstandigheden. Omkering van COUMADIN 2 mg antistolling kan worden verkregen door stopzetting van de behandeling met COUMADIN 1 mg en, indien nodig, door toediening van orale of parenterale vitamine K1.
Het gebruik van vitamine K1 vermindert de respons op daaropvolgende behandeling met COUMADIN en patiënten kunnen terugkeren naar een trombotische status van voor de behandeling na de snelle omkering van een verlengde INR. Hervatting van de toediening van COUMADIN 2 mg keert het effect van vitamine K om en een therapeutische INR kan opnieuw worden verkregen door zorgvuldige dosisaanpassing. Als snelle hernieuwde antistolling geïndiceerd is, kan heparine de voorkeur hebben als initiële therapie.
Behandeling met protrombinecomplexconcentraat (PCC), vers ingevroren plasma of geactiveerde factor VII-behandeling kan worden overwogen als de noodzaak om de effecten van COUMADIN 2 mg om te keren dringend is. Een risico op hepatitis en andere virale ziekten is geassocieerd met het gebruik van bloedproducten; PCC en geactiveerde factor VII zijn ook geassocieerd met een verhoogd risico op trombose. Daarom mogen deze preparaten alleen worden gebruikt bij uitzonderlijke of levensbedreigende bloedingen die secundair zijn aan een overdosering met COUMADIN 2 mg.
CONTRA-INDICATIES
COUMADIN 1 mg is gecontra-indiceerd bij:
- Zwangerschap
COUMADIN 2 mg is gecontra-indiceerd bij vrouwen die zwanger zijn, behalve bij zwangere vrouwen met mechanische hartkleppen, die een hoog risico lopen op trombo-embolie [zie WAARSCHUWINGEN EN VOORZORGSMAATREGELEN en Gebruik bij specifieke populaties ]. COUMADIN 2 mg kan schade aan de foetus veroorzaken wanneer het wordt toegediend aan een zwangere vrouw. Blootstelling aan COUMADIN tijdens de zwangerschap veroorzaakt een erkend patroon van ernstige aangeboren misvormingen (warfarine-embryopathie en foetotoxiciteit), fatale foetale bloeding en een verhoogd risico op spontane abortus en foetale mortaliteit. Als COUMADIN tijdens de zwangerschap wordt gebruikt of als de patiënte zwanger wordt tijdens het gebruik van dit geneesmiddel, moet de patiënt op de hoogte zijn van het mogelijke gevaar voor een foetus (zie Gebruik bij specifieke populaties ].
COUMADIN is gecontra-indiceerd bij patiënten met:
- Hemorragische neigingen of bloeddyscrasieën
- Recente of overwogen operatie van het centrale zenuwstelsel of oog, of traumatische chirurgie die resulteert in grote open oppervlakken [zie WAARSCHUWINGEN EN VOORZORGSMAATREGELEN ]
- Bloedingsneigingen geassocieerd met:
- Actieve ulceratie of openlijke bloeding van het maagdarmkanaal, urogenitale of luchtwegen
- Bloeding in het centrale zenuwstelsel
- Cerebrale aneurysma's, aorta ontleden
- Pericarditis en pericardiale effusies
- Bacteriële endocarditis
- Dreigende abortus, eclampsie en pre-eclampsie
- Patiënten zonder toezicht met aandoeningen die verband houden met een mogelijk hoog niveau van niet-naleving
- Spinale punctie en andere diagnostische of therapeutische procedures met kans op oncontroleerbare bloedingen
- Overgevoeligheid voor warfarine of voor andere componenten van dit product (bijv. anafylaxie) [zie: ONGEWENSTE REACTIES ]
- Grote regionale of lumbale blokanesthesie
- Maligne hypertensie
KLINISCHE FARMACOLOGIE
Werkingsmechanisme
Warfarine remt de synthese van vitamine K-afhankelijke stollingsfactoren, waaronder de factoren II, VII, IX en X, en de anticoagulantia C en S. Vitamine K is een essentiële cofactor voor de post-ribosomale synthese van de vitamine K- afhankelijke stollingsfactoren. Vitamine K bevordert de biosynthese van γ-carboxyglutaminezuurresiduen in de eiwitten die essentieel zijn voor biologische activiteit. Men denkt dat warfarine de synthese van stollingsfactoren verstoort door remming van de C1-subeenheid van het vitamine K-epoxidereductase (VKORC1)-enzymcomplex, waardoor de regeneratie van vitamine K1-epoxide wordt verminderd [zie farmacogenomica ].
farmacodynamiek
Een antistollingseffect treedt over het algemeen op binnen 24 uur na toediening van warfarine. Het maximale antistollingseffect kan echter 72 tot 96 uur worden uitgesteld. De werkingsduur van een enkele dosis racemisch warfarine is 2 tot 5 dagen. De effecten van COUMADIN 1 mg kunnen sterker worden naarmate de effecten van dagelijkse onderhoudsdoses elkaar overlappen. Dit komt overeen met de halfwaardetijden van de aangetaste vitamine K-afhankelijke stollingsfactoren en anticoagulatie-eiwitten: Factor II - 60 uur, VII - 4 tot 6 uur, IX - 24 uur, X - 48 tot 72 uur, en eiwitten C en S zijn ongeveer 8 uur en 30 uur, respectievelijk.
Farmacokinetiek
COUMADIN is een racemisch mengsel van de R- en S-enantiomeren van warfarine. Het S-enantiomeer vertoont 2 tot 5 keer meer antistollingsactiviteit dan het R-enantiomeer bij mensen, maar heeft over het algemeen een snellere klaring.
Absorptie
Warfarine wordt in wezen volledig geabsorbeerd na orale toediening, waarbij de piekconcentratie over het algemeen binnen de eerste 4 uur wordt bereikt.
Verdeling
Warfarine wordt gedistribueerd in een relatief klein schijnbaar distributievolume van ongeveer 0,14 l/kg. Een distributiefase van 6 tot 12 uur is te onderscheiden na snelle intraveneuze of orale toediening van een waterige oplossing. Ongeveer 99% van het geneesmiddel is gebonden aan plasma-eiwitten.
Metabolisme
De eliminatie van warfarine is bijna volledig door metabolisme. Warfarine wordt stereoselectief gemetaboliseerd door hepatische cytochroom P-450 (CYP450) microsomale enzymen tot inactieve gehydroxyleerde metabolieten (overheersende route) en door reductasen tot gereduceerde metabolieten (warfarinealcoholen) met minimale antistollingsactiviteit. Geïdentificeerde metabolieten van warfarine omvatten dehydrowarfarine, twee diastereo-isomeeralcoholen en 4'-, 6-, 7-, 8- en 10-hydroxywarfarine. De CYP450-iso-enzymen die betrokken zijn bij het metabolisme van warfarine, zijn onder meer CYP2C9, 2C19, 2C8, 2C18, 1A2 en 3A4. CYP2C9, een polymorf enzym, is waarschijnlijk de belangrijkste vorm van CYP450 in de menselijke lever die de in vivo anticoagulerende activiteit van warfarine moduleert. Patiënten met een of meer variant CYP2C9-allelen hebben een verminderde klaring van S-warfarine [zie: farmacogenomica ].
uitscheiding
De terminale halfwaardetijd van warfarine na een enkele dosis is ongeveer 1 week; de effectieve halfwaardetijd varieert echter van 20 tot 60 uur, met een gemiddelde van ongeveer 40 uur. De klaring van R-warfarine is over het algemeen de helft van die van S-warfarine, dus aangezien de distributievolumes vergelijkbaar zijn, is de halfwaardetijd van Rwarfarine langer dan die van S-warfarine. De halfwaardetijd van R-warfarine varieert van 37 tot 89 uur, terwijl die van S-warfarine varieert van 21 tot 43 uur. Studies met radioactief gelabelde geneesmiddelen hebben aangetoond dat tot 92% van de oraal toegediende dosis in de urine wordt teruggevonden. Zeer weinig warfarine wordt onveranderd in de urine uitgescheiden. Uitscheiding via de urine vindt plaats in de vorm van metabolieten.
Geriatrische patiënten
Patiënten van 60 jaar of ouder lijken een sterker dan verwachte INR-respons op de anticoagulerende effecten van warfarine te vertonen. De oorzaak van de verhoogde gevoeligheid voor de anticoagulerende effecten van warfarine in deze leeftijdsgroep is niet bekend, maar kan te wijten zijn aan een combinatie van farmacokinetische en farmacodynamische factoren. Beperkte informatie suggereert dat er geen verschil is in de klaring van S-warfarine; er kan echter een lichte afname zijn in de klaring van R-warfarine bij ouderen in vergelijking met jongeren. Daarom is, naarmate de leeftijd van de patiënt toeneemt, gewoonlijk een lagere dosis warfarine nodig om een therapeutisch niveau van antistolling te produceren [zie DOSERING EN ADMINISTRATIE ].
Aziatische patiënten
Aziatische patiënten hebben mogelijk lagere aanvangs- en onderhoudsdoses warfarine nodig. Een niet-gecontroleerde studie van 151 Chinese poliklinische patiënten die gestabiliseerd waren op warfarine voor verschillende indicaties, rapporteerde een gemiddelde dagelijkse behoefte aan warfarine van 3,3 ± 1,4 mg om een INR van 2 tot 2,5 te bereiken. De leeftijd van de patiënt was de belangrijkste bepalende factor voor de behoefte aan warfarine bij deze patiënten, met een progressief lagere behoefte aan warfarine met toenemende leeftijd.
farmacogenomica
CYP2C9- en VKORC1-polymorfismen
Het S-enantiomeer van warfarine wordt voornamelijk gemetaboliseerd tot 7-hydroxywarfarine door CYP2C9, een polymorf enzym. De variante allelen, CYP2C9*2 en CYP2C9*3, resulteren in verminderde in vitro CYP2C9 enzymatische 7-hydroxylering van S-warfarine. De frequenties van deze allelen bij blanken zijn respectievelijk ongeveer 11% en 7% voor CYP2C9*2 en CYP2C9*3.
Andere CYP2C9-allelen die geassocieerd zijn met verminderde enzymatische activiteit komen bij lagere frequenties voor, waaronder *5, *6 en *11 allelen in populaties van Afrikaanse afkomst en *5, *9 en *11 allelen bij blanken.
Warfarine vermindert de regeneratie van vitamine K uit vitamine K-epoxide in de vitamine K-cyclus door remming van VKOR, een multiproteïne-enzymcomplex. Bepaalde polymorfismen van één nucleotide in het VKORC1-gen (bijv. .1639G>A) zijn in verband gebracht met variabele warfarine-dosisvereisten.
VKORC1- en CYP2C9-genvarianten verklaren over het algemeen het grootste deel van de bekende variabiliteit in de dosisvereisten voor warfarine.
CYP2C9- en VKORC1-genotype-informatie, indien beschikbaar, kan helpen bij de selectie van de initiële dosis warfarine [zie DOSERING EN ADMINISTRATIE ].
Klinische studies
Atriale fibrillatie
In vijf prospectieve, gerandomiseerde, gecontroleerde klinische onderzoeken met 3711 patiënten met niet-reumatisch AF, verminderde warfarine significant het risico op systemische trombo-embolie inclusief beroerte (zie tabel 4). De risicovermindering varieerde van 60% tot 86% in alle gevallen, behalve één studie (CAFA: 45%), die vroegtijdig werd stopgezet vanwege de gepubliceerde positieve resultaten van twee van deze onderzoeken. De incidentie van ernstige bloedingen in deze onderzoeken varieerde van 0,6% tot 2,7% (zie tabel 4).
Onderzoeken bij patiënten met zowel AF als mitralisstenose suggereren een voordeel van antistolling met COUMADIN [zie DOSERING EN ADMINISTRATIE ].
Mechanische en bioprothetische hartkleppen
In een prospectieve, gerandomiseerde, open-label, positief-gecontroleerde studie bij 254 patiënten met mechanische prothetische hartkleppen, bleek het trombo-embolische vrije interval significant groter te zijn bij patiënten behandeld met alleen warfarine in vergelijking met met dipyridamol/aspirine behandelde patiënten (p
In een prospectieve, open-label, klinische studie waarin matige (INR 2,65) versus hoge intensiteit (INR 9,0) warfarinetherapieën werden vergeleken bij 258 patiënten met mechanische prothetische hartkleppen, trad trombo-embolie met vergelijkbare frequentie op in de twee groepen (4,0 en 3,7 voorvallen per 100 respectievelijk patiëntjaren). Ernstige bloedingen kwamen vaker voor in de groep met hoge intensiteit. De resultaten van dit onderzoek zijn weergegeven in tabel 6.
In een gerandomiseerde studie bij 210 patiënten waarin twee intensiteiten van warfarinetherapie werden vergeleken (INR 2,0-2,25 vs. INR 2,5-4,0) gedurende een periode van drie maanden na vervanging van de weefselhartklep, trad trombo-embolie op met vergelijkbare frequentie in de twee groepen (ernstige embolische voorvallen respectievelijk 2,0% vs. 1,9% en kleine embolische voorvallen respectievelijk 10,8% vs. 10,2%). Ernstige bloedingen traden op bij 4,6% van de patiënten in de INR-groep met hogere intensiteit in vergelijking met nul in de INR-groep met lagere intensiteit.
Myocardinfarct
WARIS (The Warfarine Re-Infarction Study) was een dubbelblinde, gerandomiseerde studie bij 1214 patiënten die 2 tot 4 weken na het infarct werden behandeld met warfarine tot een beoogde INR van 2,8 tot 4,8. Het primaire eindpunt was een samenstelling van totale mortaliteit en recidiverend infarct. Een secundair eindpunt van cerebrovasculaire gebeurtenissen werd beoordeeld. De gemiddelde follow-up van de patiënten was 37 maanden. De resultaten voor elk eindpunt afzonderlijk, inclusief een analyse van vasculaire sterfte, worden gegeven in Tabel 7.
WARIS II (The Warfarine, Aspirin, Re-Infarction Study) was een open-label, gerandomiseerde studie bij 3630 patiënten die in het ziekenhuis waren opgenomen voor een acuut myocardinfarct en die werden behandeld met warfarine tot een streefwaarde van INR 2,8 tot 4,2, aspirine 160 mg per dag, of warfarine tot een streef INR 2,0 tot 2,5 plus aspirine 75 mg per dag voorafgaand aan ontslag uit het ziekenhuis. Het primaire eindpunt was een samenstelling van overlijden, niet-fataal herinfarct of trombo-embolische beroerte. De gemiddelde observatieduur was ongeveer 4 jaar. De resultaten voor WARIS II staan in tabel 8.
Er waren ongeveer vier keer zoveel ernstige bloedingen in de twee groepen die warfarine kregen dan in de groep die alleen aspirine kreeg. Ernstige bloedingen kwamen niet vaker voor bij patiënten die aspirine plus warfarine kregen dan bij degenen die alleen warfarine kregen, maar de incidentie van kleine bloedingen was hoger in de gecombineerde therapiegroep.
PATIËNT INFORMATIE
COUMADIN® (COU-ma-din) (warfarine-natrium)
Wat is de belangrijkste informatie die ik moet weten over COUMADIN 5 mg?
COUMADIN kan bloedingen veroorzaken die ernstig kunnen zijn en soms tot de dood kunnen leiden. Dit komt omdat COUMADIN een bloedverdunner is die de kans op vorming van bloedstolsels in uw lichaam vermindert.
- U kunt een hoger risico op bloedingen hebben als u COUMADIN gebruikt en:
- 65 jaar of ouder zijn
- een voorgeschiedenis heeft van maag- of darmbloedingen
- hoge bloeddruk hebben (hypertensie)
- een voorgeschiedenis heeft van een beroerte of een "mini-beroerte" (transient ischemic attack of TIA)
- een ernstige hartziekte hebben
- een laag bloedbeeld of kanker hebben
- een trauma hebben gehad, zoals een ongeval of een operatie
- nierproblemen hebben
- neem andere geneesmiddelen die het risico op bloedingen verhogen, waaronder:
- een geneesmiddel dat heparine bevat
- andere geneesmiddelen om bloedstolsels te voorkomen of te behandelen
- niet-steroïde anti-inflammatoire geneesmiddelen (NSAID's)
- lange tijd warfarine-natrium gebruiken. Warfarine-natrium is het actieve ingrediënt in COUMADIN.
Vertel het uw zorgverlener als u een van deze geneesmiddelen gebruikt. Vraag uw zorgverlener als u niet zeker weet of uw geneesmiddel hierboven vermeld staat.
Veel andere geneesmiddelen kunnen een wisselwerking hebben met COUMADIN 1 mg en de dosis die u nodig heeft beïnvloeden of de bijwerkingen van COUMADIN 1 mg verhogen. Verander of stop geen van uw geneesmiddelen en begin niet met nieuwe geneesmiddelen voordat u met uw zorgverlener heeft gesproken.
Gebruik geen andere geneesmiddelen die warfarine-natrium bevatten terwijl u COUMADIN gebruikt.
- Laat uw bloed regelmatig testen om te controleren of u op COUMADIN reageert. Deze bloedtest wordt een INR-test genoemd. De INR-test controleert hoe snel uw bloed stolt. Uw zorgverlener zal beslissen welke INR-nummers het beste voor u zijn. Uw dosis COUMADIN 2 mg zal worden aangepast om uw INR binnen een streefbereik voor u te houden.
- Bel onmiddellijk uw zorgverlener als u een van de volgende tekenen of symptomen van bloedingsproblemen krijgt:
- pijn, zwelling of ongemak
- hoofdpijn, duizeligheid of zwakte
- ongebruikelijke blauwe plekken (blauwe plekken die ontstaan zonder bekende oorzaak of groter worden)
- neusbloedingen
- bloedend tandvlees
- bloeden door snijwonden duurt lang om te stoppen
- menstruatiebloeding of vaginale bloeding die zwaarder is dan normaal
- roze of bruine urine
- rode of zwarte ontlasting
- bloed ophoesten
- bloed overgeven of materiaal dat op koffiedik lijkt
- Sommige voedingsmiddelen en dranken kunnen een wisselwerking hebben met COUMADIN en uw behandeling en dosis beïnvloeden.
- Eet een normaal, uitgebalanceerd dieet. Praat met uw zorgverlener voordat u wijzigingen in uw dieet aanbrengt. Eet geen grote hoeveelheden bladgroene groenten. Blad-, groene groenten bevatten vitamine K. Bepaalde plantaardige oliën bevatten ook grote hoeveelheden vitamine K. Te veel vitamine K kan de werking van COUMADIN verminderen.
- Vertel altijd al uw zorgverleners dat u COUMADIN gebruikt.
- Draag of draag informatie die u COUMADIN gebruikt.
Zie "Wat zijn de mogelijke bijwerkingen van COUMADIN 1 mg?" voor meer informatie over bijwerkingen.
Wat is COUMADIN?
COUMADIN is een receptgeneesmiddel dat wordt gebruikt om bloedstolsels te behandelen en om de kans op vorming van bloedstolsels in uw lichaam te verkleinen. Bloedstolsels kunnen een beroerte, hartaanval of andere ernstige aandoeningen veroorzaken als ze zich in de benen of longen vormen.
Wie mag COUMADIN niet gebruiken?
Gebruik COUMADIN 5 mg niet als:
- uw risico op bloedingsproblemen is groter dan het mogelijke voordeel van de behandeling. Uw zorgverlener zal beslissen of COUMADIN geschikt voor u is.
- u bent zwanger, tenzij u een mechanische hartklep heeft. COUMADIN kan geboorteafwijkingen, een miskraam of de dood van uw ongeboren baby veroorzaken.
- u allergisch bent voor warfarine of voor één van de andere bestanddelen van COUMADIN. Zie het einde van deze bijsluiter voor een volledige lijst van ingrediënten in COUMADIN.
Voordat u COUMADIN® inneemt
Vertel uw zorgverlener over al uw medische aandoeningen, ook als u:
- bloedingsproblemen hebben
- val vaak
- leverproblemen hebben
- nierproblemen heeft of dialyse ondergaat
- hoge bloeddruk hebben
- een hartprobleem heeft dat congestief hartfalen wordt genoemd
- diabetes hebben
- van plan bent om een operatie of een tandheelkundige ingreep te ondergaan
- andere medische aandoeningen heeft
- zwanger bent of van plan bent zwanger te worden. Zie "Wie mag COUMADIN 2 mg niet gebruiken?" Uw zorgverlener zal een zwangerschapstest doen voordat u begint met de behandeling met COUMADIN. Vrouwen die zwanger kunnen worden, moeten effectieve anticonceptie gebruiken tijdens de behandeling en gedurende ten minste 1 maand na de laatste dosis COUMADIN.
- zijn borstvoeding. U en uw zorgverlener moeten beslissen of u COUMADIN en borstvoeding gaat gebruiken. Controleer uw baby op blauwe plekken of bloedingen als u COUMADIN gebruikt en borstvoeding geeft.
Vertel al uw zorgverleners en tandartsen dat u COUMADIN gebruikt. Ze moeten overleggen met de zorgverlener die COUMADIN 1 mg voor u heeft voorgeschreven voordat u elk operatie of tandheelkundige ingreep. Uw COUMADIN moet mogelijk voor een korte tijd worden stopgezet of het kan zijn dat uw dosis moet worden aangepast.
Vertel uw zorgverlener over alle medicijnen die u gebruikt, inclusief recept- en vrij verkrijgbare medicijnen, vitamines en kruidensupplementen. Sommige van uw andere geneesmiddelen kunnen de manier waarop COUMADIN werkt beïnvloeden. Bepaalde geneesmiddelen kunnen het risico op bloedingen verhogen. Zien "Wat is de belangrijkste informatie die ik over COUMADIN moet weten?"
Hoe moet ik COUMADIN 1 mg innemen?
- Neem COUMADIN 1 mg precies zoals voorgeschreven. Uw zorgverlener zal uw dosis van tijd tot tijd aanpassen, afhankelijk van uw reactie op COUMADIN.
- U moet regelmatig bloedtesten ondergaan en uw arts raadplegen om uw toestand te controleren.
- Als u een dosis COUMADIN heeft overgeslagen, neem dan contact op met uw zorgverlener. Neem de dosis zo snel mogelijk op dezelfde dag in. Niet doen neem de volgende dag een dubbele dosis COUMADIN 5 mg om een vergeten dosis in te halen.
- Bel onmiddellijk uw zorgverlener als u:
- neem te veel COUMADIN
- ziek bent met diarree, een infectie of koorts heeft
- vallen of uzelf verwonden, vooral als u uw hoofd stoot. Uw zorgverlener moet u mogelijk controleren.
Wat moet ik vermijden tijdens het gebruik van COUMADIN 5 mg?
- Doe geen activiteiten of sport die ernstig letsel kunnen veroorzaken.
Wat zijn de mogelijke bijwerkingen van COUMADIN?
COUMADIN kan ernstige bijwerkingen veroorzaken, waaronder:
- Zien "Wat is de belangrijkste informatie die ik over COUMADIN moet weten?"
- Afsterven van huidweefsel (huidnecro's is of gangreen). Dit kan kort na het starten van COUMADIN gebeuren. Het gebeurt omdat zich bloedstolsels vormen en de bloedstroom naar een deel van uw lichaam blokkeren. Bel onmiddellijk uw zorgverlener als u pijn, kleur of temperatuurverandering heeft in een deel van uw lichaam. Mogelijk hebt u meteen medische zorg nodig om overlijden of verlies (amputatie) van uw aangedane lichaamsdeel te voorkomen.
- Nierproblemen. Nierletsel kan optreden bij mensen die COUMADIN gebruiken. Vertel het uw zorgverlener meteen als u bloed in uw urine krijgt. Uw zorgverlener kan tijdens de behandeling met COUMADIN 2 mg vaker testen doen om te controleren op bloedingen als u al nierproblemen heeft.
- "Paarse tenen-syndroom." Bel onmiddellijk uw zorgverlener als u pijn in uw tenen heeft en ze paars van kleur of donker van kleur zijn.
Dit zijn niet alle bijwerkingen van COUMADIN. Vraag uw zorgverlener of apotheker om meer informatie. Bel uw arts voor medisch advies over bijwerkingen. U kunt bijwerkingen melden aan de FDA op 1..800-FDA-1088.
Hoe moet ik COUMADIN 5 mg bewaren?
- Bewaar COUMADIN bij 59 ° F tot 86 ° F (15 ° C tot 30 ° C).
- Bewaar COUMADIN 2 mg in een goed gesloten container
- Houd COUMADIN uit het licht en vocht.
- Volg de instructies van uw zorgverlener of apotheker over de juiste manier om verouderde of ongebruikte COUMADIN weg te gooien.
- Vrouwen die zwanger zijn, mogen geen gemalen of gebroken COUMADIN-tabletten hanteren.
Houd COUMADIN 1 mg en alle geneesmiddelen buiten het bereik van kinderen.
Algemene informatie over het veilige en effectieve gebruik van COUMADIN.
Medicijnen worden soms voorgeschreven voor andere doeleinden dan die in een Medicatiewijzer vermeld staan. Gebruik COUMADIN 5 mg niet voor een aandoening waarvoor het niet is voorgeschreven. Geef COUMADIN 2 mg niet aan andere mensen, ook niet als zij dezelfde symptomen hebben als u. Het kan hen schaden.
U kunt uw zorgverlener of apotheker om informatie vragen over COUMADIN die is geschreven voor gezondheidswerkers.
Wat zijn de ingrediënten in COUMADIN 1 mg tabletten?
Actief ingrediënt: warfarine natrium
Inactieve ingredienten : lactose, zetmeel en magnesiumstearaat, daarnaast:
1 mg: D&C Red No. 6 Barium Lake
2 mg: FD&C Blue No. 2 Aluminium Lake en FD&C Red No. 40 Aluminium Lake
2,5 mg: D&C Yellow No. 10 Aluminium Lake en FD&C Blue No. 1 Aluminium Lake
3 mg: FD&C geel nr. 6 aluminium lak, FD&C blauw nr. 2 aluminium lak en FD&C rood nr. 40 aluminium lak
4 mg: FD&C blauw nr. 1 aluminiumlak
5 mg: FD&C geel nr. 6 aluminiumlak
mg: FD&C geel nr. 6 aluminium lak en FD&C blauw nr. 1 aluminium lak
7,5 mg: D&C Yellow No. 10 Aluminium Lake en FD&C Yellow No. 6 Aluminium Lake
Deze medicatiehandleiding is goedgekeurd door de Amerikaanse Food and Drug Administration.
