Precose 25mg, 50mg Acarbose Gebruik, bijwerkingen en dosering. Prijs in online apotheek. Generieke medicijnen zonder recept.
Wat is Precose 50 mg en hoe wordt het gebruikt?
Precose (acarbose-tabletten) is een orale alfa-glucosidaseremmer die wordt gebruikt voor de behandeling van type 2-diabetes. Precose 50 mg wordt soms gebruikt in combinatie met insuline of andere diabetesmedicatie die u via de mond inneemt. Precose 25 mg is beschikbaar in generieke vorm.
Wat zijn bijwerkingen van Precose 25 mg?
Vaak voorkomende bijwerkingen van Precose zijn onder meer:
- diarree,
- gas,
- opgeblazen gevoel,
- maagklachten, of
- maagpijn in de eerste paar weken van de behandeling omdat uw lichaam zich aanpast aan dit medicijn, maar gewoonlijk verbetert met de tijd.
Andere bijwerkingen van Precose 50 mg zijn huiduitslag of jeuk. Vertel het uw arts als u zeldzame maar zeer ernstige bijwerkingen van Precose 25 mg heeft, waaronder:
- ongebruikelijke vermoeidheid,
- aanhoudende misselijkheid of braken,
- ernstige maag- of buikpijn,
- anale bloeding,
- gele ogen of huid, of
- donkere urine.
OMSCHRIJVING
PRECOSE® (acarbose-tabletten) is een orale alfa-glucosidaseremmer voor gebruik bij de behandeling van type 2 diabetes mellitus. Acarbose is een oligosacharide die wordt verkregen uit fermentatieprocessen van een micro-organisme, Actinoplanes utahensis, en is chemisch bekend als O-4,6-dideoxy4-[[(1S,4R,5S,6S)-4,5,6-trihydroxy- 3-(hydroxymethyl)-2-cyclohexen-1-yl]amino]-a-D-glucopyranosyl-(1 -> 4)-O-a-D-glucopyranosyl-(1 ->4)-D-glucose. Het is een wit tot gebroken wit poeder met een molecuulgewicht van 645,6. Acarbose is oplosbaar in water en heeft een pKa van 5,1. De empirische formule is C25H43NO18 en de chemische structuur is als volgt:
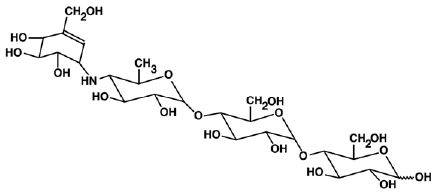
PRECOSE 50 mg is verkrijgbaar als tabletten van 25 mg, 50 mg en 100 mg voor oraal gebruik. De inactieve ingrediënten zijn zetmeel, microkristallijne cellulose, magnesiumstearaat en colloïdaal siliciumdioxide.
INDICATIES
PRECOSE is geïndiceerd als aanvulling op dieet en lichaamsbeweging om de glykemische controle te verbeteren bij volwassenen met type 2 diabetes mellitus.
DOSERING EN ADMINISTRATIE
Er is geen vast doseringsschema voor de behandeling van diabetes mellitus met PRECOSE of een ander farmacologisch middel. De dosering van PRECOSE 25 mg moet individueel worden bepaald op basis van zowel effectiviteit als tolerantie, terwijl de maximale aanbevolen dosis van 100 mg driemaal daags niet wordt overschreden. PRECOSE moet driemaal daags worden ingenomen aan het begin (bij de eerste hap) van elke hoofdmaaltijd.
PRECOSE moet worden gestart met een lage dosis, met geleidelijke dosisverhoging zoals hieronder beschreven, zowel om gastro-intestinale bijwerkingen te verminderen als om de identificatie mogelijk te maken van de minimale dosis die nodig is voor een adequate glykemische controle van de patiënt. Als het voorgeschreven dieet niet wordt gevolgd, kunnen de darmbijwerkingen worden versterkt. Als er ondanks het volgen van het voorgeschreven diabetesdieet toch ernstige symptomen ontstaan, moet de arts worden geraadpleegd en moet de dosis tijdelijk of permanent worden verlaagd.
Tijdens de start van de behandeling en dosistitratie (zie hieronder) kan één uur postprandiale plasmaglucose worden gebruikt om de therapeutische respons op PRECOSE te bepalen en de minimale effectieve dosis voor de patiënt te bepalen. Daarna moet het geglycosyleerde hemoglobine worden gemeten met tussenpozen van ongeveer drie maanden. Het therapeutische doel moet zijn om zowel postprandiale plasmaglucose als geglycosyleerde hemoglobinespiegels te verlagen tot normaal of bijna normaal door de laagste effectieve dosis PRECOSE te gebruiken, hetzij als monotherapie of in combinatie met sulfonylureumderivaten, insuline of metformine.
Initiële dosering:
De aanbevolen startdosering van PRECOSE 25 mg is driemaal daags 25 mg oraal aan het begin (bij de eerste hap) van elke hoofdmaaltijd. Sommige patiënten kunnen echter baat hebben bij een meer geleidelijke dosistitratie om gastro-intestinale bijwerkingen te minimaliseren. Dit kan worden bereikt door de behandeling te starten met eenmaal daags 25 mg en vervolgens de toedieningsfrequentie te verhogen om driemaal daags 25 mg te bereiken.
Onderhoudsdosering:
Zodra een driemaal daags doseringsschema van 25 mg is bereikt, moet de dosering van PRECOSE 50 mg met tussenpozen van 4-8 weken worden aangepast op basis van een uur postprandiale glucose- of geglycosyleerde hemoglobinespiegels en op tolerantie. De dosering kan worden verhoogd van 25 mg driemaal daags tot 50 mg driemaal daags Sommige patiënten kunnen baat hebben bij een verdere verhoging van de dosering tot 100 mg driemaal daags. De onderhoudsdosis varieert van 50 mg driemaal daags tot 100 mg driemaal daags. risico op verhoogde serumtransaminasen, alleen patiënten met een lichaamsgewicht > 60 kg dienen overwogen te worden voor dosistitratie boven 50 mg driemaal daags (zie PREVENTIEVE MAATREGELEN ). Als er geen verdere verlaging van de postprandiale glucose- of geglycosyleerde hemoglobinespiegels wordt waargenomen bij titratie tot 100 mg driemaal daags, moet worden overwogen de dosis te verlagen. Zodra een effectieve en getolereerde dosering is vastgesteld, moet deze worden gehandhaafd.
Maximale dosering
De maximale aanbevolen dosis voor patiënten ≤ 60 kg is 50 mg driemaal daags De maximale aanbevolen dosis voor patiënten > 60 kg is 100 mg driemaal daags
Patiënten die sulfonylureumderivaten of insuline krijgen
Sulfonylureumderivaten of insuline kunnen hypoglykemie veroorzaken. PRECOSE gegeven in combinatie met een sulfonylureumderivaat of insuline zal een verdere verlaging van de bloedglucose veroorzaken en kan de kans op hypoglykemie vergroten. Als hypoglykemie optreedt, moeten passende aanpassingen in de dosering van deze middelen worden gemaakt.
HOE GELEVERD
PRECOSE is verkrijgbaar als ronde, niet-gescoorde tabletten van 25 mg, 50 mg of 100 mg. Elke tabletsterkte is wit tot geel getint van kleur. De tablet van 25 mg is gecodeerd met het woord "PRECOSE" aan de ene kant en "25" aan de andere kant. De tablet van 50 mg is gecodeerd met het woord "PRECOSE" en "50" aan dezelfde kant. De tablet van 100 mg is gecodeerd met het woord "PRECOSE" en "100" aan dezelfde kant. PRECOSE is verkrijgbaar in flessen met een sterkte van 100 en 50 mg in eenheidsdosisverpakkingen van 100.
Niet bewaren boven 25°C (77°F). Beschermen tegen vocht. Voor flessen, houd de container goed gesloten.
Bayer HealthCare Pharmaceuticals Inc. Wayne, NJ 07470. Gemaakt in Duitsland. 11/11
BIJWERKINGEN
Spijsverteringskanaal
Gastro-intestinale symptomen zijn de meest voorkomende reacties op PRECOSE. In placebogecontroleerde onderzoeken in de VS waren de incidenties van buikpijn, diarree en winderigheid respectievelijk 19%, 31% en 74% bij 1255 patiënten die werden behandeld met PRECOSE 50-300 mg driemaal daags, terwijl de overeenkomstige incidenties 9%, 12% waren en 29% bij 999 met placebo behandelde patiënten.
In een eenjarig veiligheidsonderzoek, waarin patiënten dagboeken bijhielden van gastro-intestinale symptomen, hadden buikpijn en diarree de neiging om na verloop van tijd terug te keren naar het niveau van voor de behandeling, en de frequentie en intensiteit van winderigheid namen na verloop van tijd af. De toegenomen symptomen van het maagdarmkanaal bij patiënten die worden behandeld met PRECOSE 50 mg zijn een manifestatie van het werkingsmechanisme van PRECOSE en houden verband met de aanwezigheid van onverteerde koolhydraten in het lagere maagdarmkanaal.
Als het voorgeschreven dieet niet wordt gevolgd, kunnen de darmbijwerkingen worden versterkt. Als er ondanks het volgen van het voorgeschreven diabetesdieet toch ernstige symptomen ontstaan, moet de arts worden geraadpleegd en moet de dosis tijdelijk of permanent worden verlaagd.
Verhoogde serumtransaminasespiegels
Zien PREVENTIEVE MAATREGELEN .
Andere abnormale laboratoriumbevindingen
Kleine verlagingen van hematocriet kwamen vaker voor bij met PRECOSE behandelde patiënten dan bij met placebo behandelde patiënten, maar gingen niet gepaard met verlagingen van hemoglobine. Lage serumcalciumspiegels en lage plasma-vitamine B6-spiegels werden geassocieerd met PRECOSE 50 mg-therapie, maar er wordt aangenomen dat ze onecht zijn of geen klinische betekenis hebben.
Rapporten over ongewenste voorvallen na marketing
Bijkomende bijwerkingen die zijn gemeld uit wereldwijde postmarketingervaring zijn onder meer fulminante hepatitis met fatale afloop, overgevoelige huidreacties (bijvoorbeeld uitslag, erytheem, exantheem en uticaria), oedeem, ileus/subileus, geelzucht en/of hepatitis en geassocieerde leverbeschadiging, trombocytopenie en pneumatose cystoides intestinalis (zie PREVENTIEVE MAATREGELEN ).
Pneumatose Cystoides Intestinalis
Er zijn zeldzame postmarketingmeldingen geweest van pneumatosis cystoides intestinalis in verband met het gebruik van alfa-glucosidaseremmers, waaronder Precose. Pneumatosis cystoides intestinalis kan zich presenteren met symptomen van diarree, slijmafscheiding, rectale bloeding en constipatie. Complicaties kunnen zijn: pneumoperitoneum, volvulus, darmobstructie, intussusceptie, darmbloeding en darmperforatie. Als pneumatosis cystoides intestinalis wordt vermoed, stop dan met Precose 25 mg en voer de juiste diagnostische beeldvorming uit.
DRUG-INTERACTIES
Bepaalde geneesmiddelen hebben de neiging om hyperglykemie te veroorzaken en kunnen leiden tot verlies van bloedglucoseregulatie. Deze geneesmiddelen omvatten de thiaziden en andere diuretica, corticosteroïden, fenothiazinen, schildklierproducten, oestrogenen, orale anticonceptiva, fenytoïne, nicotinezuur, sympathicomimetica, calciumkanaalblokkerende geneesmiddelen en isoniazide. Wanneer dergelijke geneesmiddelen worden toegediend aan een patiënt die PRECOSE 25 mg krijgt, moet de patiënt nauwlettend worden gecontroleerd op verlies van bloedglucoseregulatie. Wanneer dergelijke geneesmiddelen worden stopgezet bij patiënten die PRECOSE 50 mg krijgen in combinatie met sulfonylureumderivaten of insuline, moeten patiënten nauwlettend worden geobserveerd op tekenen van hypoglykemie.
Patiënten die sulfonylureumderivaten of insuline krijgen: Sulfonylureumderivaten of insuline kunnen hypoglykemie veroorzaken. PRECOSE 25 mg gegeven in combinatie met een sulfonylureumderivaat of insuline kan een verdere verlaging van de bloedglucose veroorzaken en kan de kans op hypoglykemie vergroten. Als hypoglykemie optreedt, moeten passende aanpassingen in de dosering van deze middelen worden gemaakt. Zeer zelden zijn individuele gevallen van hypoglykemische shock gemeld bij patiënten die PRECOSE-therapie kregen in combinatie met sulfonylureumderivaten en/of insuline.
Intestinale adsorbentia (bijvoorbeeld houtskool) en spijsverteringsenzympreparaten die koolhydraatsplitsende enzymen bevatten (bijvoorbeeld amylase, pancreatine) kunnen het effect van PRECOSE verminderen en mogen niet gelijktijdig worden ingenomen.
Van PRECOSE 25 mg is aangetoond dat het de biologische beschikbaarheid van digoxine verandert wanneer het gelijktijdig wordt toegediend, wat een aanpassing van de digoxinedosis kan vereisen. (Zien KLINISCHE FARMACOLOGIE , Geneesmiddel-geneesmiddelinteracties .)
WAARSCHUWINGEN
Geen informatie verstrekt
PREVENTIEVE MAATREGELEN
Algemeen
Macrovasculaire resultaten
Er zijn geen klinische onderzoeken geweest die overtuigend bewijs hebben geleverd van macrovasculaire risicovermindering met PRECOSE 25 mg of een ander antidiabetisch geneesmiddel.
Hypoglykemie
Vanwege het werkingsmechanisme zou PRECOSE, wanneer het alleen wordt toegediend, geen hypoglykemie moeten veroorzaken in nuchtere of postprandiale toestand. Sulfonylureumderivaten of insuline kunnen hypoglykemie veroorzaken. Omdat PRECOSE 50 mg gegeven in combinatie met een sulfonylureumderivaat of insuline een verdere verlaging van de bloedglucose zal veroorzaken, kan dit de kans op hypoglykemie vergroten. Hypoglykemie treedt niet op bij patiënten die alleen metformine krijgen onder de gebruikelijke gebruiksomstandigheden, en er werd geen verhoogde incidentie van hypoglykemie waargenomen bij patiënten wanneer PRECOSE 50 mg werd toegevoegd aan metforminetherapie.
Orale glucose (dextrose), waarvan de absorptie niet wordt geremd door PRECOSE, moet worden gebruikt in plaats van sucrose (rietsuiker) bij de behandeling van milde tot matige hypoglykemie. Sucrose, waarvan de hydrolyse tot glucose en fructose wordt geremd door PRECOSE, is niet geschikt voor de snelle correctie van hypoglykemie. Ernstige hypoglykemie kan het gebruik van intraveneuze glucose-infusie of glucagon-injectie vereisen.
Verhoogde serumtransaminasespiegels
In langetermijnstudies (tot 12 maanden, en met PRECOSE 25 mg doses tot 300 mg driemaal daags) uitgevoerd in de Verenigde Staten, kwamen tijdens de behandeling optredende verhogingen van serumtransaminasen (AST en/of ALT) boven de bovengrens van normaal (ULN) ), meer dan 1,8 keer de ULN en meer dan 3 keer de ULN kwam voor bij respectievelijk 14%, 6% en 3% van de met PRECOSE behandelde patiënten in vergelijking met respectievelijk 7%, 2% en 1%, van met placebo behandelde patiënten. Hoewel deze verschillen tussen behandelingen statistisch significant waren, waren deze verhogingen asymptomatisch, reversibel, kwamen vaker voor bij vrouwen en waren ze in het algemeen niet geassocieerd met ander bewijs van leverdisfunctie. Bovendien bleken deze serumtransaminaseverhogingen dosisgerelateerd te zijn. In Amerikaanse onderzoeken met PRECOSE-doses van 50 mg tot de maximaal goedgekeurde dosis van 100 mg driemaal daags, waren tijdens de behandeling optredende verhogingen van ASAT en/of ALAT op elk niveau van ernst vergelijkbaar tussen met PRECOSE behandelde patiënten en met placebo behandelde patiënten (p ≥ 0,496) .
In internationale postmarketingervaring van ongeveer 3 miljoen patiëntjaren met PRECOSE 50 mg zijn 62 gevallen gemeld van verhogingen van serumtransaminase > 500 IE/l (waarvan 29 geassocieerd met geelzucht). Eenenveertig van deze 62 patiënten werden behandeld met 100 mg driemaal daags of meer en 33 van de 45 patiënten van wie het gewicht werd gemeld, wogen
Verlies van controle over bloedglucose
Wanneer diabetespatiënten worden blootgesteld aan stress, zoals koorts, trauma, infectie of operatie, kan een tijdelijk verlies van controle over de bloedglucose optreden. Op zulke momenten kan tijdelijke insulinetherapie nodig zijn.
Laboratorium testen
De therapeutische respons op PRECOSE moet worden gecontroleerd door middel van periodieke bloedglucosetests. Meting van geglycosyleerde hemoglobinespiegels wordt aanbevolen voor het bewaken van de glykemische controle op lange termijn.
PRECOSE 25 mg, vooral bij doses van meer dan 50 mg driemaal daags, kan aanleiding geven tot verhogingen van serumtransaminasen en, in zeldzame gevallen, tot hyperbilirubinemie. Het wordt aanbevolen om de serumtransaminasespiegels elke 3 maanden te controleren tijdens het eerste jaar van de behandeling met PRECOSE en daarna periodiek. Als verhoogde transaminasen worden waargenomen, kan een verlaging van de dosering of stopzetting van de therapie aangewezen zijn, vooral als de verhogingen aanhouden.
Nierfunctiestoornis
Plasmaconcentraties van PRECOSE bij vrijwilligers met een nierfunctiestoornis waren proportioneel verhoogd in verhouding tot de mate van nierdisfunctie. Klinische langetermijnonderzoeken bij diabetespatiënten met een significante nierfunctiestoornis (serumcreatinine > 2,0 mg/dl) zijn niet uitgevoerd. Daarom wordt de behandeling van deze patiënten met PRECOSE 50 mg niet aanbevolen.
Carcinogenese, mutagenese en verminderde vruchtbaarheid
Er zijn acht carcinogeniteitsonderzoeken uitgevoerd met acarbose. Zes studies werden uitgevoerd bij ratten (twee stammen, Sprague-Dawley en Wistar) en twee studies werden uitgevoerd bij hamsters.
In het eerste onderzoek bij ratten kregen Sprague-Dawley-ratten gedurende 104 weken acarbose in het voer in hoge doses (tot ongeveer 500 mg/kg lichaamsgewicht). Behandeling met acarbose resulteerde in een significante toename van de incidentie van niertumoren (adenomen en adenocarcinomen) en goedaardige Leydig-celtumoren. Dit onderzoek werd herhaald met een vergelijkbaar resultaat. Verdere studies werden uitgevoerd om de directe carcinogene effecten van acarbose te scheiden van de indirecte effecten die het gevolg zijn van de ondervoeding van koolhydraten die wordt veroorzaakt door de hoge doses acarbose die in de studies werden gebruikt. In één onderzoek met Sprague-Dawley-ratten werd acarbose gemengd met voer, maar koolhydraattekort werd voorkomen door de toevoeging van glucose aan het dieet.

In een 26 maanden durende studie van Sprague-Dawley-ratten werd acarbose toegediend via dagelijkse postprandiale sondevoeding om de farmacologische effecten van het geneesmiddel te vermijden. In beide onderzoeken kwam de verhoogde incidentie van niertumoren die in de oorspronkelijke onderzoeken werd gevonden niet voor. Acarbose werd ook in voedsel en via postprandiale sondevoeding gegeven in twee afzonderlijke onderzoeken bij Wistar-ratten. In geen van deze Wistar-onderzoeken bij ratten werd een verhoogde incidentie van niertumoren gevonden. In twee voedingsonderzoeken met hamsters, met en zonder glucosesuppletie, was er ook geen bewijs van carcinogeniteit.
Acarbose veroorzaakte in vitro geen DNA-schade in de CHO-test op chromosomale aberratie, bacteriële mutagenese (Ames) of een DNA-bindingstest. In vivo werd geen DNA-schade gedetecteerd in de dominante letale test bij mannelijke muizen of de micronucleustest bij muizen.
Vruchtbaarheidsonderzoeken uitgevoerd bij ratten na orale toediening hadden geen nadelig effect op de vruchtbaarheid of op het algehele vermogen om zich voort te planten.
Zwangerschap
Teratogene effecten: Zwangerschap categorie B.
De veiligheid van PRECOSE bij zwangere vrouwen is niet vastgesteld. Er zijn reproductieonderzoeken uitgevoerd bij ratten met doses tot 480 mg/kg (overeenkomend met 9 keer de blootstelling bij mensen, gebaseerd op de bloedspiegels van geneesmiddelen) en er zijn geen aanwijzingen gevonden voor verminderde vruchtbaarheid of schade aan de foetus als gevolg van acarbose. Bij konijnen kan een verminderde gewichtstoename van de moeder, waarschijnlijk het gevolg van de farmacodynamische activiteit van hoge doses acarbose in de darmen, verantwoordelijk zijn geweest voor een lichte toename van het aantal embryonale verliezen. Echter, konijnen die 160 mg/kg acarbose kregen (overeenkomend met 10 maal de dosis bij de mens, gebaseerd op lichaamsoppervlak) vertoonden geen bewijs van embryotoxiciteit en er was geen bewijs van teratogeniteit bij een dosis van 32 maal de dosis bij de mens (gebaseerd op oppervlakte). Er zijn echter geen adequate en goed gecontroleerde onderzoeken met PRECOSE 25 mg bij zwangere vrouwen. Omdat reproductiestudies bij dieren niet altijd voorspellend zijn voor de respons bij de mens, mag dit medicijn alleen tijdens de zwangerschap worden gebruikt als dit duidelijk nodig is. Omdat de huidige informatie er sterk op wijst dat abnormale bloedglucosespiegels tijdens de zwangerschap geassocieerd zijn met een hogere incidentie van aangeboren afwijkingen en een verhoogde neonatale morbiditeit en mortaliteit, bevelen de meeste deskundigen aan om tijdens de zwangerschap insuline te gebruiken om de bloedglucosespiegels zo normaal mogelijk te houden. .
Moeders die borstvoeding geven
Er is een kleine hoeveelheid radioactiviteit gevonden in de melk van zogende ratten na toediening van radioactief gelabeld acarbose. Het is niet bekend of dit geneesmiddel wordt uitgescheiden in de moedermelk. Omdat veel geneesmiddelen worden uitgescheiden in de moedermelk, mag PRECOSE 25 mg niet worden toegediend aan een vrouw die borstvoeding geeft.
Pediatrisch gebruik
De veiligheid en werkzaamheid van PRECOSE 25 mg bij pediatrische patiënten zijn niet vastgesteld.
Geriatrisch gebruik
Van het totale aantal proefpersonen in klinische onderzoeken met PRECOSE 25 mg in de Verenigde Staten was 27% 65 jaar en ouder, terwijl 4% 75 jaar en ouder was. Er werden geen algemene verschillen in veiligheid en werkzaamheid waargenomen tussen deze proefpersonen en jongere proefpersonen. De gemiddelde steady-state oppervlakte onder de curve (AUC) en maximale concentraties van acarbose waren ongeveer 1,5 keer hoger bij ouderen dan bij jonge vrijwilligers; deze verschillen waren echter niet statistisch significant.
OVERDOSERING
In tegenstelling tot sulfonylureumderivaten of insuline leidt een overdosis PRECOSE niet tot hypoglykemie. Een overdosis kan resulteren in een voorbijgaande toename van winderigheid, diarree en buikpijn die snel weer verdwijnen. In geval van overdosering mag de patiënt gedurende de volgende 4-6 uur geen dranken of maaltijden met koolhydraten (polysachariden, oligosachariden en disachariden) krijgen.
CONTRA-INDICATIES
PRECOSE 25 mg is gecontra-indiceerd bij patiënten met een bekende overgevoeligheid voor het geneesmiddel. Precose 25 mg is gecontra-indiceerd bij patiënten met diabetische ketoacidose of cirrose. PRECOSE 25 mg is ook gecontra-indiceerd bij patiënten met inflammatoire darmaandoeningen, colonulcera, gedeeltelijke darmobstructie of bij patiënten met aanleg voor darmobstructie. Bovendien is PRECOSE gecontra-indiceerd bij patiënten met chronische darmaandoeningen die gepaard gaan met duidelijke stoornissen in de spijsvertering of absorptie en bij patiënten met aandoeningen die kunnen verslechteren als gevolg van verhoogde gasvorming in de darm.
KLINISCHE FARMACOLOGIE
Acarbose is een complexe oligosacharide die de vertering van ingenomen koolhydraten vertraagt, wat resulteert in een kleinere stijging van de bloedglucoseconcentratie na maaltijden. Als gevolg van de verlaging van de plasmaglucose verlaagt PRECOSE de spiegels van geglycosyleerd hemoglobine bij patiënten met type 2 diabetes mellitus. Systemische niet-enzymatische eiwitglycosylering, zoals weerspiegeld door de niveaus van geglycosyleerd hemoglobine, is een functie van de gemiddelde bloedglucoseconcentratie in de loop van de tijd.
Werkingsmechanisme
In tegenstelling tot sulfonylureumderivaten verhoogt PRECOSE 50 mg de insulinesecretie niet. De antihyperglykemische werking van acarbose is het gevolg van een competitieve, omkeerbare remming van pancreas-alfa-amylase en membraangebonden intestinale alfa-glucosidehydrolase-enzymen. Pancreatische alfa-amylase hydrolyseert complexe zetmelen tot oligosachariden in het lumen van de dunne darm, terwijl de membraangebonden intestinale alfa-glucosidasen oligosachariden, trisachariden en disachariden hydrolyseren tot glucose en andere monosachariden in de borstelrand van de dunne darm. Bij diabetespatiënten resulteert deze enzymremming in een vertraagde glucoseabsorptie en een verlaging van postprandiale hyperglykemie.
Omdat het werkingsmechanisme anders is, is het effect van PRECOSE om de glykemische controle te verbeteren, additief aan dat van sulfonylureumderivaten, insuline of metformine wanneer ze in combinatie worden gebruikt. Bovendien vermindert PRECOSE 50 mg de insulinotrope en gewichtsverhogende effecten van sulfonylureumderivaten.
Acarbose heeft geen remmende activiteit tegen lactase en daarom wordt niet verwacht dat het lactose-intolerantie veroorzaakt.
Farmacokinetiek
Absorptie
In een onderzoek bij 6 gezonde mannen werd minder dan 2% van een orale dosis acarbose als actief geneesmiddel geabsorbeerd, terwijl ongeveer 35% van de totale radioactiviteit van een 14C-gelabelde orale dosis werd geabsorbeerd. Gemiddeld 51% van een orale dosis werd binnen 96 uur na inname uitgescheiden in de feces als niet-geabsorbeerde geneesmiddelgerelateerde radioactiviteit. Omdat acarbose lokaal in het maagdarmkanaal werkt, is deze lage systemische biologische beschikbaarheid van de moederverbinding therapeutisch gewenst. Na orale toediening van 14C-gelabelde acarbose aan gezonde vrijwilligers werden 14-24 uur na toediening piekplasmaconcentraties van radioactiviteit bereikt, terwijl piekplasmaconcentraties van het actieve geneesmiddel na ongeveer 1 uur werden bereikt. De vertraagde absorptie van acarbose-gerelateerde radioactiviteit weerspiegelt de absorptie van metabolieten die kunnen worden gevormd door darmbacteriën of intestinale enzymatische hydrolyse.
Metabolisme
Acarbose wordt uitsluitend in het maagdarmkanaal gemetaboliseerd, voornamelijk door darmbacteriën, maar ook door spijsverteringsenzymen. Een fractie van deze metabolieten (ongeveer 34% van de dosis) werd geabsorbeerd en vervolgens uitgescheiden in de urine. Ten minste 13 metabolieten zijn chromatografisch gescheiden van urinemonsters. De belangrijkste metabolieten zijn geïdentificeerd als 4-methylpyrogallolderivaten (dat wil zeggen sulfaat-, methyl- en glucuronideconjugaten). Eén metaboliet (gevormd door splitsing van een glucosemolecuul van acarbose) heeft ook een alfa-glucosidaseremmende activiteit. Deze metaboliet, samen met de moederverbinding, teruggevonden in de urine, vertegenwoordigt minder dan 2% van de totale toegediende dosis.
uitscheiding
De fractie acarbose die als intact geneesmiddel wordt geabsorbeerd, wordt bijna volledig door de nieren uitgescheiden. Wanneer acarbose intraveneus werd toegediend, werd binnen 48 uur 89% van de dosis als actief geneesmiddel in de urine teruggevonden. Daarentegen werd minder dan 2% van een orale dosis in de urine teruggevonden als actief (dat wil zeggen moederverbinding en actieve metaboliet) geneesmiddel. Dit komt overeen met de lage biologische beschikbaarheid van het oorspronkelijke geneesmiddel. De plasma-eliminatiehalfwaardetijd van acarbose-activiteit is ongeveer 2 uur bij gezonde vrijwilligers. Dientengevolge treedt geen accumulatie van het geneesmiddel op bij driemaal daagse (tid) orale dosering.
Speciale populaties
De gemiddelde steady-state oppervlakte onder de curve (AUC) en maximale concentraties van acarbose waren ongeveer 1,5 keer hoger bij ouderen dan bij jonge vrijwilligers; deze verschillen waren echter niet statistisch significant. Patiënten met een ernstige nierfunctiestoornis (Clcr
Geneesmiddel-geneesmiddelinteracties
Studies bij gezonde vrijwilligers hebben aangetoond dat PRECOSE geen effect heeft op de farmacokinetiek of farmacodynamiek van nifedipine, propranolol of ranitidine. PRECOSE interfereerde niet met de absorptie of dispositie van het sulfonylureumglyburide bij diabetespatiënten. PRECOSE kan de biologische beschikbaarheid van digoxine beïnvloeden en kan een dosisaanpassing van digoxine met 16% (90% betrouwbaarheidsinterval: 8-23%), verlaging van de gemiddelde Cmax van digoxine met 26% (90% betrouwbaarheidsinterval: 16-34%) en verlaging van de gemiddelde dalwaarde vereisen digoxineconcentraties met 9% (90% betrouwbaarheidslimiet: 19% afname tot 2% toename). (Zien PREVENTIEVE MAATREGELEN: DRUG-INTERACTIES .)
De hoeveelheid metformine die werd geabsorbeerd tijdens het gebruik van PRECOSE was bio-equivalent aan de hoeveelheid die werd geabsorbeerd bij het nemen van placebo, zoals aangegeven door de plasma-AUC-waarden. De piekplasmaspiegel van metformine werd echter met ongeveer 20% verlaagd bij gebruik van PRECOSE vanwege een lichte vertraging in de absorptie van metformine. Er is weinig of geen klinisch significante interactie tussen PRECOSE en metformine.
Klinische proeven
Klinische ervaring van dosisbepalingsonderzoeken bij patiënten met diabetes mellitus type 2, alleen met dieetbehandeling
Resultaten van zes gecontroleerde, monotherapieonderzoeken met vaste dosis van PRECOSE bij de behandeling van diabetes mellitus type 2, waarbij 769 met PRECOSE behandelde patiënten waren betrokken, werden gecombineerd en een gewogen gemiddelde van het verschil met placebo in de gemiddelde verandering ten opzichte van baseline in geglycosyleerd hemoglobine ( HbA1c) werd berekend voor elk dosisniveau zoals hieronder weergegeven:
Hoewel studies een maximale dosis van 200 of 300 mg driemaal daags gebruikten, is de maximale aanbevolen dosis voor patiënten 60 kg is 100 mg driemaal daags
De resultaten van deze zes monotherapieonderzoeken met vaste dosis werden ook gecombineerd om een gewogen gemiddelde te verkrijgen van het verschil met placebo in de gemiddelde verandering ten opzichte van de uitgangswaarde voor één uur postprandiale plasmaglucosespiegels, zoals weergegeven in de volgende afbeelding:
Figuur 1 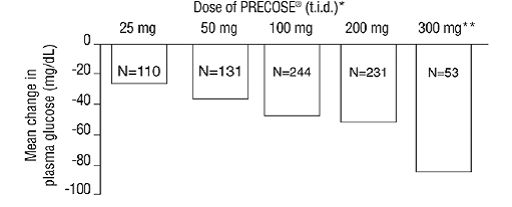
* PRECOSE 50 mg was bij alle doses statistisch significant verschillend van placebo wat betreft het effect op één uur postprandiale plasmaglucose. **Het 300 mg driemaal daags PRECOSE 50 mg-regime was superieur aan lagere doses, maar er waren geen statistisch significante verschillen van 50 tot 200 mg driemaal daags
Klinische ervaring bij patiënten met diabetes mellitus type 2 die monotherapie of in combinatie met sulfonylureumderivaten, metformine of insuline krijgen
PRECOSE werd onderzocht als monotherapie en als combinatietherapie voor behandeling met sulfonylureumderivaten, metformine of insuline. De effecten van de behandeling op HbA1c-spiegels en één uur postprandiale glucosespiegels zijn samengevat voor vier placebogecontroleerde, dubbelblinde, gerandomiseerde onderzoeken die in de Verenigde Staten zijn uitgevoerd in respectievelijk Tabellen 2 en 3. De behandelingsverschillen waarbij placebo werd afgetrokken, die hieronder worden samengevat, waren in al deze onderzoeken statistisch significant voor beide variabelen.
Bij onderzoek 1 (n=109) waren patiënten betrokken die alleen een achtergrondbehandeling kregen met een dieet. Het gemiddelde effect van de toevoeging van PRECOSE aan dieettherapie was een verandering in HbA1c van -0,78% en een verbetering van één uur postprandiale glucose van -74,4 mg/dL.
In onderzoek 2 (n=137) was het gemiddelde effect van de toevoeging van PRECOSE 25 mg aan maximale sulfonylureumtherapie een verandering in HbA1c van -0,54% en een verbetering van één uur postprandiale glucose van -33,5 mg/dL.
In onderzoek 3 (n=147) was het gemiddelde effect van de toevoeging van PRECOSE 50 mg aan maximale metforminetherapie een verandering in HbA1c van -0,65% en een verbetering van één uur postprandiale glucose van -34,3 mg/dL.
Onderzoek 4 (n=145) toonde aan dat PRECOSE toegevoegd aan patiënten die een achtergrondbehandeling met insuline kregen, resulteerde in een gemiddelde verandering in HbA1c van -0,69% en een verbetering van één uur postprandiale glucose van -36,0 mg/dL.
Een eenjarig onderzoek naar PRECOSE als monotherapie of in combinatie met behandeling met sulfonylureumderivaten, metformine of insuline werd uitgevoerd in Canada, waarbij 316 patiënten werden opgenomen in de primaire werkzaamheidsanalyse (Figuur 2). In de dieet-, sulfonylureum- en metforminegroepen was de gemiddelde afname van HbA1c geproduceerd door toevoeging van PRECOSE 50 mg statistisch significant na zes maanden, en dit effect hield aan na één jaar. Bij de met PRECOSE behandelde patiënten die insuline gebruikten, was er een statistisch significante afname van HbA1c na zes maanden en een trend naar een afname na één jaar.
Figuur 2 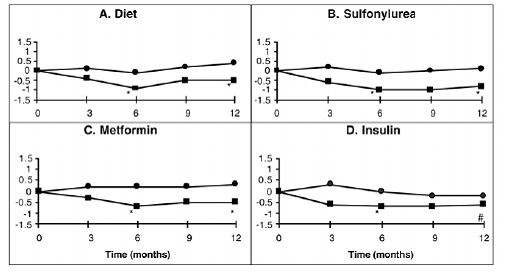
Figuur 2: Effecten van PRECOSE (III) en Placebo (III) op de gemiddelde verandering in HbA1c-spiegels vanaf baseline gedurende een eenjarig onderzoek bij patiënten met diabetes mellitus type 2 bij gebruik in combinatie met: (A) alleen dieet; (B) sulfonylureum; (C) metformine; of (D) insuline. Behandelingsverschillen na 6 en 12 maanden werden getest: * p
PATIËNT INFORMATIE
Patiënten moeten worden verteld om driemaal daags PRECOSE 50 mg oraal in te nemen aan het begin (bij de eerste hap) van elke hoofdmaaltijd. Het is belangrijk dat patiënten zich blijven houden aan de voedingsinstructies, een regelmatig trainingsprogramma en het regelmatig testen van urine en/of bloedglucose.
PRECOSE zelf veroorzaakt geen hypoglykemie, zelfs niet wanneer het wordt toegediend aan patiënten in nuchtere toestand. Sulfonylureumderivaten en insuline kunnen echter de bloedsuikerspiegel voldoende verlagen om symptomen of soms levensbedreigende hypoglykemie te veroorzaken. Omdat PRECOSE in combinatie met een sulfonylureumderivaat of insuline een verdere verlaging van de bloedsuikerspiegel zal veroorzaken, kan dit het hypoglykemische potentieel van deze middelen verhogen. Hypoglykemie treedt niet op bij patiënten die alleen metformine krijgen onder de gebruikelijke gebruiksomstandigheden, en er werd geen verhoogde incidentie van hypoglykemie waargenomen bij patiënten wanneer PRECOSE werd toegevoegd aan metforminetherapie. Het risico op hypoglykemie, de symptomen en behandeling ervan, en aandoeningen die vatbaar zijn voor de ontwikkeling ervan, moeten goed worden begrepen door patiënten en verantwoordelijke familieleden. Omdat PRECOSE 50 mg de afbraak van tafelsuiker voorkomt, moeten patiënten een direct beschikbare glucosebron (dextrose, D-glucose) hebben om symptomen van een lage bloedsuikerspiegel te behandelen wanneer PRECOSE in combinatie met een sulfonylureumderivaat of insuline wordt gebruikt.
Als er bijwerkingen optreden met PRECOSE, ontstaan deze gewoonlijk tijdens de eerste paar weken van de behandeling. Het zijn meestal milde tot matige gastro-intestinale effecten, zoals winderigheid, diarree of buikpijn, en nemen in de loop van de tijd in frequentie en intensiteit af.
