Flonase Nasal Spray 50mcg Fluticasone Gebruik, bijwerkingen en dosering. Prijs in online apotheek. Generieke medicijnen zonder recept.
Wat is Flonase en hoe wordt het gebruikt?
Flonase is een receptgeneesmiddel dat wordt gebruikt voor de behandeling van de symptomen van allergische rhinitis (niezen, loopneus en jeukende of tranende ogen) en neuspoliepen. Flonase kan alleen of in combinatie met andere medicijnen worden gebruikt.
Flonase behoort tot een klasse geneesmiddelen die corticosteroïden, intranasale, immunosuppressiva, PHD worden genoemd.
Het is niet bekend of Flonase veilig en effectief is bij kinderen jonger dan 4 jaar.
Wat zijn de mogelijke bijwerkingen van Flonase?
Flonase kan ernstige bijwerkingen veroorzaken, waaronder:
- ernstige of aanhoudende bloedneuzen,
- luidruchtige ademhaling,
- loopneus,
- korstvorming rond je neusgaten,
- roodheid, zweren of witte vlekken in uw mond of keel,
- koorts,
- rillingen,
- pijn in het lichaam,
- wazig zien,
- oogpijn,
- halo's rond lichten zien,
- wonden die niet genezen,
- verergering van vermoeidheid,
- spier zwakte,
- duizeligheid,
- misselijkheid, en
- braken
Roep meteen medische hulp in als u een van de bovenstaande symptomen heeft.
De meest voorkomende bijwerkingen van Flonase zijn:
- kleine bloedneus,
- branderig gevoel of jeuk in je neus,
- zweren of witte vlekken in of rond uw neus,
- hoesten,
- moeite met ademhalen,
- hoofdpijn,
- rugpijn,
- sinuspijn,
- keelpijn,
- koorts,
- misselijkheid, en
- braken
OMSCHRIJVING
Het actieve bestanddeel van FLONASE Neusspray 50mcg is fluticasonpropionaat, een corticosteroïde met de chemische naam S-(fluormethyl) 6α,9-difluor-11β,17-dihydroxy-16α-methyl-3oxoandrosta-1,4-dieen-17β-carbothioaat , 17-propionaat en de volgende chemische structuur:
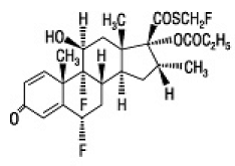
Fluticasonpropionaat is een wit poeder met een molecuulgewicht van 500,6 en de empirische formule is C25H31F3O5S. Het is praktisch onoplosbaar in water, vrij oplosbaar in dimethylsulfoxide en dimethylformamide, en enigszins oplosbaar in methanol en 95% ethanol.
FLONASE Neusspray, 50 mcg is een waterige suspensie van microfijn fluticasonpropionaat voor plaatselijke toediening aan het neusslijmvlies door middel van een doseer-, vernevelingsspraypomp. FLONASE Neusspray 50mcg bevat ook microkristallijne cellulose en carboxymethylcellulose-natrium, dextrose, 0,02% w/w benzalkoniumchloride, polysorbaat 80 en 0,25% w/w fenylethylalcohol, en heeft een pH tussen 5 en 7.
Na de eerste priming levert elke verstuiving 50 mcg fluticasonpropionaat in 100 mg formulering via de neusadapter.
INDICATIES
FLONASE®-neusspray is geïndiceerd voor de behandeling van de neussymptomen van niet-seizoensgebonden niet-allergische rhinitis bij volwassen en pediatrische patiënten van 4 jaar en ouder.
DOSERING EN ADMINISTRATIE
Dien FLONASE-neusspray alleen intranasaal toe. Prime FLONASE Neusspray voor het eerste gebruik of na een periode van niet-gebruik (1 week of langer) door de inhoud goed te schudden en 6 verstuivingen in de lucht weg van het gezicht. Schud FLONASE Neusspray voorzichtig voor elk gebruik.
Patiënten moeten FLONASE-neusspray met regelmatige tussenpozen gebruiken, aangezien de effectiviteit ervan afhangt van regelmatig gebruik. Het maximale effect kan enkele dagen duren en individuele patiënten zullen een variabele tijd tot het begin en een verschillende mate van symptoomverlichting ervaren.
volwassenen
De aanbevolen startdosering bij volwassenen is eenmaal daags 2 verstuivingen (elk 50 mcg fluticasonpropionaat) in elk neusgat (totale dagelijkse dosis 200 mcg). Dezelfde totale dagelijkse dosis, tweemaal daags 1 verstuiving in elk neusgat (bijv. 8 uur en 20 uur) is ook effectief. Na de eerste paar dagen kunnen patiënten hun dosis mogelijk verlagen tot eenmaal daags 1 verstuiving in elk neusgat voor onderhoudstherapie.
De maximale totale dagelijkse dosis mag niet hoger zijn dan 2 verstuivingen in elk neusgat (totale dosis, 200 mcg/dag). Er is geen bewijs dat overschrijding van de aanbevolen dosis effectiever is.
Adolescenten en kinderen (4 jaar en ouder)
De aanbevolen startdosering bij adolescenten en kinderen van 4 jaar en ouder is eenmaal daags 1 verstuiving in elk neusgat (totale dagelijkse dosis, 100 mcg). Patiënten die niet adequaat reageren op 1 verstuiving in elk neusgat, mogen eenmaal daags 2 verstuivingen in elk neusgat gebruiken (totale dagelijkse dosis, 200 mcg). Zodra adequate controle is bereikt, moet de dosering worden verlaagd tot eenmaal daags 1 verstuiving in elk neusgat.
De maximale totale dagelijkse dosering mag niet hoger zijn dan 2 verstuivingen in elk neusgat (200 mcg/dag). Er is geen bewijs dat overschrijding van de aanbevolen dosis effectiever is.
HOE GELEVERD
Doseringsvormen en sterke punten
FLONASE Neusspray is een suspensie voor neusspray. Elke spray van 100 mg levert 50 mcg fluticasonpropionaat.
Opslag en behandeling
FLONASE Neusspray, 50 mcg wordt geleverd in een amberkleurige glazen fles voorzien van een witte verstuiverpomp, witte neusadapter en groene stofkap in een doos van 1 ( NDC 0173-0453-01) met FDA-goedgekeurd Patiëntlabeling (zien Gebruiksinstructies voor de patiënt voor een juiste bediening van het apparaat ). Elke fles bevat een netto vulgewicht van 16 g en is goed voor 120 verstuivingen. Elke verstuiving levert 50 mcg fluticasonpropionaat in 100 mg formulering via de neusadapter. De juiste hoeveelheid medicatie in elke verstuiving kan niet worden gegarandeerd na 120 verstuivingen, ook al is de fles niet helemaal leeg. De fles moet worden weggegooid wanneer het aangegeven aantal verstuivingen is gebruikt.
Bewaren tussen 4° en 30°C (39° en 86°F).
GlaxoSmithKline Research Triangle Park, NC 27709. Herzien: januari 2015
BIJWERKINGEN
Systemisch en lokaal gebruik van corticosteroïden kan het volgende tot gevolg hebben:
- Epistaxis, neusulcera, Candida albicans-infectie, neusseptumperforatie en verminderde wondgenezing [zie WAARSCHUWINGEN EN VOORZORGSMAATREGELEN ]
- Staar en glaucoom [zie WAARSCHUWINGEN EN VOORZORGSMAATREGELEN ]
- Immunosuppressie [zie WAARSCHUWINGEN EN VOORZORGSMAATREGELEN ]
- Hypercorticisme en bijniersuppressie [zie WAARSCHUWINGEN EN VOORZORGSMAATREGELEN ]
- Effect op groei [zie WAARSCHUWINGEN EN VOORZORGSMAATREGELEN ]
Ervaring met klinische proeven
Omdat klinische onderzoeken onder sterk uiteenlopende omstandigheden worden uitgevoerd, kunnen de bijwerkingen die in de klinische onderzoeken van een geneesmiddel zijn waargenomen niet direct worden vergeleken met de percentages in de klinische onderzoeken van een ander geneesmiddel en komen mogelijk niet overeen met de percentages die in de praktijk worden waargenomen.
In gecontroleerde klinische onderzoeken in de VS werden meer dan 3.300 proefpersonen met allergische en niet-allergische rhinitis behandeld met intranasaal fluticasonpropionaat. Over het algemeen zijn bijwerkingen in klinische onderzoeken voornamelijk in verband gebracht met irritatie van de neusslijmvliezen, en de bijwerkingen werden met ongeveer dezelfde frequentie gemeld door proefpersonen die met placebo werden behandeld. Minder dan 2% van de proefpersonen in klinische onderzoeken stopte vanwege bijwerkingen; dit percentage was vergelijkbaar voor vehikel-placebo en actieve comparatoren.
De hieronder beschreven veiligheidsgegevens zijn gebaseerd op 7 placebogecontroleerde klinische onderzoeken bij proefpersonen met allergische rhinitis. De 7 onderzoeken omvatten 536 proefpersonen (57 meisjes en 108 jongens in de leeftijd van 4 tot 11 jaar, 137 vrouwen en 234 mannelijke adolescenten en volwassenen) behandeld met FLONASE 200 mcg eenmaal daags gedurende 2 tot 4 weken en 2 placebogecontroleerde klinische onderzoeken met 246 proefpersonen (119 vrouwelijke en 127 mannelijke adolescenten en volwassenen) behandeld met FLONASE 200 mcg eenmaal daags gedurende 6 maanden (tabel 1). Ook opgenomen in tabel 1 zijn bijwerkingen van 2 onderzoeken waarin 167 kinderen (45 meisjes en 122 jongens van 4 tot 11 jaar) eenmaal daags gedurende 2 tot 4 weken werden behandeld met FLONASE 100 mcg.
Andere bijwerkingen met FLONASE-neusspray 50 mcg waargenomen met een incidentie van minder dan of gelijk aan 3% maar groter dan of gelijk aan 1% en vaker voor dan bij placebo waren: bloed in neusslijm, loopneus, buikpijn, diarree, koorts, griepachtige symptomen, pijntjes, duizeligheid en bronchitis.
Postmarketingervaring
Naast de bijwerkingen die zijn gemeld in klinische onderzoeken, zijn de volgende bijwerkingen vastgesteld tijdens het gebruik van intranasaal fluticasonpropionaat na goedkeuring. Omdat deze reacties vrijwillig worden gemeld door een populatie van onbekende grootte, is het niet altijd mogelijk om op betrouwbare wijze hun frequentie te schatten of een oorzakelijk verband met blootstelling aan geneesmiddelen vast te stellen. Deze voorvallen zijn gekozen voor opname vanwege hun ernst, frequentie van rapportage of oorzakelijk verband met fluticasonpropionaat of een combinatie van deze factoren.
Algemene aandoeningen en toedieningsplaatsvoorwaarden
Overgevoeligheidsreacties, waaronder angio-oedeem, huiduitslag, oedeem van het gezicht en de tong, pruritus, urticaria, bronchospasme, piepende ademhaling, dyspneu en anafylaxie/anafylactoïde reacties, die in zeldzame gevallen ernstig waren.
Oor- en labyrintaandoeningen
Verandering of verlies van smaak- en/of reukzin en, in zeldzame gevallen, neusseptumperforatie, neuszweer, keelpijn, irritatie en droogheid van de keel, hoesten, heesheid en stemveranderingen.
Oogaandoeningen
Droogte en irritatie, conjunctivitis, wazig zien, glaucoom, verhoogde intraoculaire druk en cataracten.
Er zijn gevallen van groeionderdrukking gemeld voor intranasale corticosteroïden, waaronder FLONASE [zie: WAARSCHUWINGEN EN VOORZORGSMAATREGELEN ].
DRUG-INTERACTIES
Remmers van cytochroom P450 3A4
Fluticasonpropionaat is een substraat van CYP3A4. Het gebruik van sterke CYP3A4-remmers (bijv. ritonavir, atazanavir, claritromycine, indinavir, itraconazol, nefazodon, nelfinavir, saquinavir, ketoconazol, telitromycine, conivaptan, lopinavir, nefazodon, voriconazole corticosteroïden) met FLONA-corticosteroïden worden niet aanbevolen omdat de bijwerkingen van Nasal-spray worden verhoogd. kan gebeuren.
Ritonavir
Een geneesmiddelinteractieonderzoek met fluticasonpropionaat waterige neusspray bij gezonde proefpersonen heeft aangetoond dat ritonavir (een sterke CYP3A4-remmer) de plasmablootstelling aan fluticasonpropionaat significant kan verhogen, wat resulteert in significant verlaagde serumcortisolconcentraties [zie KLINISCHE FARMACOLOGIE ]. Tijdens postmarketinggebruik zijn er meldingen geweest van klinisch significante geneesmiddelinteracties bij patiënten die fluticasonpropionaatproducten, waaronder FLONASE, met ritonavir kregen, resulterend in systemische corticosteroïd-effecten, waaronder het syndroom van Cushing en bijniersuppressie.
Ketoconazol
Gelijktijdige toediening van oraal geïnhaleerd fluticasonpropionaat (1.000 mcg) en ketoconazol (200 mg eenmaal daags) resulteerde in een 1,9-voudige toename van de plasmablootstelling aan fluticasonpropionaat en een afname van 45% van de plasmacortisol-area under the curve (AUC), maar had geen effect op de uitscheiding van cortisol via de urine.
WAARSCHUWINGEN
Inbegrepen als onderdeel van de PREVENTIEVE MAATREGELEN sectie.
PREVENTIEVE MAATREGELEN
Lokale nasale effecten
Epistaxis
In klinische onderzoeken met een duur van 2 tot 26 weken werd epistaxis vaker waargenomen bij proefpersonen die werden behandeld met FLONASE-neusspray dan bij degenen die placebo kregen [zie ONGEWENSTE REACTIES ].
Neuszweer
Postmarketinggevallen van neusulcera zijn gemeld bij patiënten die werden behandeld met FLONASE-neusspray (zie: ONGEWENSTE REACTIES ].
Candida-infectie
In klinische onderzoeken met intranasale toediening van fluticasonpropionaat is de ontwikkeling van gelokaliseerde infecties van neus en keelholte met Candida albicans opgetreden. Wanneer een dergelijke infectie zich ontwikkelt, kan behandeling met geschikte lokale therapie en stopzetting van FLONASE-neusspray nodig zijn. Patiënten die gedurende meerdere maanden of langer FLONASE-neusspray gebruiken, moeten periodiek worden onderzocht op tekenen van een Candida-infectie of andere tekenen van nadelige effecten op het neusslijmvlies.
Neusseptumperforatie
Postmarketinggevallen van neusseptumperforatie zijn gemeld bij patiënten die werden behandeld met FLONASE-neusspray (zie: ONGEWENSTE REACTIES ].
Verminderde wondgenezing
Vanwege het remmende effect van corticosteroïden op de wondgenezing, moeten patiënten die recente neuszweren, neusoperaties of neustrauma hebben gehad, het gebruik van FLONASE-neusspray vermijden totdat genezing is opgetreden.
Glaucoom en staar
Het gebruik van intranasale en inhalatiecorticosteroïden kan leiden tot de ontwikkeling van glaucoom en/of cataracten. Daarom is nauwlettende controle geboden bij patiënten met een veranderd gezichtsvermogen of met een voorgeschiedenis van verhoogde intraoculaire druk, glaucoom en/of cataracten.
Overgevoeligheidsreacties waaronder anafylaxie
Overgevoeligheidsreacties (bijv. anafylaxie, angio-oedeem, urticaria, contactdermatitis en huiduitslag) zijn gemeld na toediening van FLONASE-neusspray. FLONASE stopzetten
Neusspray als dergelijke reacties optreden [zie CONTRA-INDICATIES ]. In zeldzame gevallen kunnen onmiddellijke overgevoeligheidsreacties optreden na toediening van FLONASE-neusspray.
Immunosuppressie
Personen die geneesmiddelen gebruiken die het immuunsysteem onderdrukken, zijn vatbaarder voor infecties dan gezonde personen. Waterpokken en mazelen kunnen bijvoorbeeld een ernstiger of zelfs fataal verloop hebben bij gevoelige kinderen of volwassenen die corticosteroïden gebruiken. Bij dergelijke kinderen of volwassenen die deze ziekten niet hebben gehad of niet goed zijn geïmmuniseerd, moet bijzondere aandacht worden besteed aan het vermijden van blootstelling. Hoe de dosis, de route en de duur van de toediening van corticosteroïden het risico op het ontwikkelen van een gedissemineerde infectie beïnvloeden, is niet bekend. De bijdrage van de onderliggende ziekte en/of eerdere behandeling met corticosteroïden aan het risico is ook niet bekend. Als een patiënt wordt blootgesteld aan waterpokken, kan profylaxe met varicella zoster-immunoglobuline (VZIG) geïndiceerd zijn. Als een patiënt wordt blootgesteld aan mazelen, kan profylaxe met gepoold intramusculair immunoglobuline (IG) geïndiceerd zijn. (Zien de volledige voorschrijfinformatie voor VZIG en IG. Als zich waterpokken ontwikkelen, kan behandeling met antivirale middelen worden overwogen.
Intranasale corticosteroïden moeten met voorzichtigheid of helemaal niet worden gebruikt bij patiënten met actieve of latente tuberculeuze infecties van de luchtwegen; systemische schimmel-, bacteriële, virale of parasitaire infecties; of oculaire herpes simplex.
Hypercorticisme en bijniersuppressie
Wanneer intranasale corticosteroïden worden gebruikt in hogere dan de aanbevolen doseringen of bij gevoelige personen in de aanbevolen doseringen, kunnen systemische corticosteroïd-effecten zoals hypercorticisme en bijniersuppressie optreden. Als dergelijke veranderingen optreden, moet de dosering van FLONASE-neusspray langzaam worden stopgezet in overeenstemming met de geaccepteerde procedures voor het stopzetten van de behandeling met orale corticosteroïden.
De vervanging van een systemische corticosteroïde door een lokale corticosteroïde kan gepaard gaan met tekenen van bijnierinsufficiëntie. Bovendien kunnen sommige patiënten symptomen van ontwenning van corticosteroïden ervaren (bijv. gewrichts- en/of spierpijn, vermoeidheid, depressie). Patiënten die eerder gedurende langere perioden zijn behandeld met systemische corticosteroïden en zijn overgeschakeld op lokale corticosteroïden, moeten zorgvuldig worden gecontroleerd op acute bijnierinsufficiëntie als reactie op stress. Bij patiënten met astma of andere klinische aandoeningen die een langdurige behandeling met systemische corticosteroïden vereisen, kunnen snelle verlagingen van de dosering van systemische corticosteroïden een ernstige verergering van hun symptomen veroorzaken.
Geneesmiddelinteracties met sterke cytochroom P450 3A4-remmers
Het gebruik van sterke cytochroom P450 3A4-remmers (CYP3A4) (bijv. ritonavir, atazanavir, claritromycine, indinavir, itraconazol, nefazodon, nelfinavir, saquinavir, ketoconazol, telitromycine, conivaptan, lopinavir, nefazodon) omdat SE niet wordt aanbevolen met FLONAvoriconazol Na verhoogde systemische bijwerkingen van corticosteroïden kunnen optreden [zie: DRUG-INTERACTIES , KLINISCHE FARMACOLOGIE ].
Effect op groei
Intranasale corticosteroïden kunnen een vermindering van de groeisnelheid veroorzaken bij toediening aan pediatrische patiënten [zie: Gebruik in specifieke populaties ]. Controleer regelmatig de groei van pediatrische patiënten die FLONASE-neusspray krijgen. Om de systemische effecten van intranasale corticosteroïden, waaronder FLONASE-neusspray, te minimaliseren, moet de dosis van elke patiënt worden getitreerd tot de laagste dosering die zijn/haar symptomen effectief onder controle houdt [zie DOSERING EN ADMINISTRATIE , Gebruik bij specifieke populaties ].
Informatie over patiëntbegeleiding
Adviseer de patiënt om de door de FDA goedgekeurde patiëntetikettering te lezen ( PATINTINFORMATIE en gebruiksaanwijzing ).
Lokale nasale effecten
Informeer patiënten dat behandeling met FLONASE-neusspray 50 mcg kan leiden tot bijwerkingen, waaronder epistaxis en neusulcera. Candida-infectie kan ook optreden bij behandeling met FLONASE-neusspray. Bovendien is FLONASE Neusspray 50mcg in verband gebracht met neusseptumperforatie en verminderde wondgenezing. Patiënten die recent neuszweren, neusoperaties of neustrauma hebben gehad, mogen FLONASE Neusspray 50mcg niet gebruiken totdat genezing is opgetreden [zie WAARSCHUWINGEN EN VOORZORGSMAATREGELEN ].
Glaucoom en staar
Informeer patiënten dat glaucoom en cataracten verband houden met het gebruik van neus- en inhalatiecorticosteroïden. Adviseer patiënten om hun zorgverleners op de hoogte te stellen als een verandering in het gezichtsvermogen wordt opgemerkt tijdens het gebruik van FLONASE-neusspray [zie: WAARSCHUWINGEN EN VOORZORGSMAATREGELEN ].
Overgevoeligheidsreacties, waaronder anafylaxie
Informeer patiënten dat overgevoeligheidsreacties, waaronder anafylaxie, angio-oedeem, urticaria, contactdermatitis en huiduitslag, kunnen optreden na toediening van FLONASE-neusspray. Als dergelijke reacties optreden, moeten patiënten stoppen met het gebruik van FLONASE-neusspray (zie: WAARSCHUWINGEN EN VOORZORGSMAATREGELEN ].
Immunosuppressie
Waarschuw patiënten die immunosuppressieve doses corticosteroïden gebruiken om blootstelling aan waterpokken of mazelen te voorkomen en als ze worden blootgesteld om hun zorgverlener onmiddellijk te raadplegen. Patiënten informeren over mogelijke verergering van bestaande tuberculose; schimmel-, bacteriële, virale of parasitaire infecties; of oculaire herpes simplex [zie WAARSCHUWINGEN EN VOORZORGSMAATREGELEN ].
Verminderde groeisnelheid
Adviseer ouders dat FLONASE Neusspray 50mcg een vermindering van de groeisnelheid kan veroorzaken bij toediening aan pediatrische patiënten. Artsen moeten de groei nauwlettend volgen van kinderen en adolescenten die corticosteroïden gebruiken via welke route dan ook [zie WAARSCHUWINGEN EN VOORZORGSMAATREGELEN , Pediatrisch gebruik ].
Gebruik dagelijks voor het beste effect
Informeer patiënten dat ze regelmatig FLONASE-neusspray 50mcg moeten gebruiken. FLONASE Neusspray 50mcg heeft, net als andere corticosteroïden, geen onmiddellijk effect op de symptomen van rhinitis. De maximale uitkering kan enkele dagen niet worden bereikt. Patiënten dienen de voorgeschreven dosering niet te verhogen, maar dienen contact op te nemen met hun zorgverlener als de symptomen niet verbeteren of als de aandoening verergert.
Houd de spray uit de ogen en mond
Informeer patiënten om te voorkomen dat ze FLONASE-neusspray in hun ogen en mond spuiten.
Niet-klinische toxicologie
Carcinogenese, mutagenese, verminderde vruchtbaarheid
Fluticasonpropionaat vertoonde geen tumorverwekkend vermogen bij muizen bij orale doses tot 1.000 mcg/kg (ongeveer 20 maal de MRHDID bij volwassenen en ongeveer 10 maal de MRHDID bij kinderen op basis van mcg/m²) gedurende 78 weken of bij ratten bij inhalatiedoses hoger tot 57 mcg/kg (ongeveer 2 keer de MRHDID bij volwassenen en ongeveer gelijk aan de MRHDID bij kinderen op basis van mcg/m²) gedurende 104 weken.
Fluticasonpropionaat induceerde in vitro geen genmutatie in prokaryote of eukaryote cellen. Er werd geen significant clastogeen effect waargenomen in gekweekte menselijke perifere lymfocyten in vitro of in de micronucleustest bij muizen.
Er werden geen aanwijzingen voor verminderde vruchtbaarheid waargenomen bij mannelijke en vrouwelijke ratten bij subcutane doses tot 50 mcg/kg (ongeveer 2 maal de MRHDID bij volwassenen op basis van mcg/m²). Het prostaatgewicht was significant verminderd bij een subcutane dosis van 50 mcg/kg.
Klinische studies
Meerjarige niet-allergische rhinitis
Drie gerandomiseerde, dubbelblinde placebogecontroleerde onderzoeken met parallelle groepen werden uitgevoerd bij 1.191 proefpersonen om regelmatig gebruik van FLONASE-neusspray 50 mcg te onderzoeken bij proefpersonen met niet-allergische rhinitis. Deze onderzoeken evalueerden door de patiënt beoordeelde totale nasale symptoomscores (TNSS), waaronder neusobstructie, postnasale infusie, rinorroe bij proefpersonen die 28 dagen dubbelblind werden behandeld en in 1 van de 3 onderzoeken gedurende 6 maanden open-label behandeling. Twee van deze onderzoeken toonden aan dat proefpersonen die werden behandeld met FLONASE-neusspray (100 mcg tweemaal daags) statistisch significante afnamen in TNSS vertoonden in vergelijking met proefpersonen die met vehiculum werden behandeld.
Gebruik bij specifieke populaties
Zwangerschap
Teratogene effecten
Zwangerschap Categorie C. Er zijn geen adequate en goed gecontroleerde onderzoeken met FLONASE-neusspray bij zwangere vrouwen. Van corticosteroïden is aangetoond dat ze teratogeen zijn bij laboratoriumdieren wanneer ze systemisch worden toegediend in relatief lage doseringen. Omdat reproductiestudies bij dieren niet altijd voorspellend zijn voor de respons bij de mens, mag FLONASE-neusspray alleen tijdens de zwangerschap worden gebruikt als het potentiële voordeel het potentiële risico voor de foetus rechtvaardigt. Vrouwen moeten worden geadviseerd om contact op te nemen met hun arts als ze zwanger worden terwijl ze FLONASE-neusspray gebruiken.
Muizen en ratten bij doses fluticasonpropionaat van respectievelijk ongeveer 1 en 4 maal de maximaal aanbevolen dagelijkse intranasale dosis voor de mens (MRHDID) voor volwassenen (op basis van mg/m² bij maternale subcutane doses van respectievelijk 45 en 100 mcg/kg/dag) vertoonde foetale toxiciteit die kenmerkend is voor krachtige corticosteroïden, waaronder embryonale groeivertraging, omphalocele, gespleten gehemelte en vertraagde craniale ossificatie. Er werd geen teratogeniteit waargenomen bij ratten bij doses tot 3 maal de MRHDID (op basis van mg/m² bij maternale inhalatiedoses tot 68,7 mcg/kg/dag).
Bij konijnen werden foetale gewichtsafname en gespleten gehemelte waargenomen bij een dosis fluticasonpropionaat van ongeveer 0,3 maal de MRHDID voor volwassenen (op basis van mg/m² bij een maternale subcutane dosis van 4 mcg/kg/dag). Er werden echter geen teratogene effecten gemeld bij doses fluticasonpropionaat tot ongeveer 20 keer de MRHDID voor volwassenen (op basis van mg/m² bij een orale dosis voor de moeder tot 300 mcg/kg/dag). In dit onderzoek werd geen fluticasonpropionaat in het plasma gedetecteerd, wat consistent is met de vastgestelde lage biologische beschikbaarheid na orale toediening [zie KLINISCHE FARMACOLOGIE ].
Fluticasonpropionaat passeerde de placenta na subcutane toediening aan muizen en ratten en orale toediening aan konijnen.
Ervaring met orale corticosteroïden sinds hun introductie in farmacologische, in tegenstelling tot fysiologische doses, suggereert dat knaagdieren vatbaarder zijn voor teratogene effecten van corticosteroïden dan mensen. Omdat er tijdens de zwangerschap een natuurlijke toename van de productie van corticosteroïden is, zullen de meeste vrouwen bovendien een lagere dosis exogene corticosteroïden nodig hebben en zullen velen tijdens de zwangerschap geen behandeling met corticosteroïden nodig hebben.
Nietteratogene effecten
Hypoadrenalisme kan optreden bij baby's die zijn geboren uit moeders die tijdens de zwangerschap corticosteroïden krijgen. Dergelijke zuigelingen moeten zorgvuldig worden gecontroleerd.
Moeders die borstvoeding geven
Het is niet bekend of fluticasonpropionaat wordt uitgescheiden in de moedermelk. Er zijn echter andere corticosteroïden aangetroffen in moedermelk. Subcutane toediening aan zogende ratten van getritieerd fluticasonpropionaat in een dosis van ongeveer 0,4 maal de MRHDID voor volwassenen op basis van mg/m² resulteerde in meetbare radioactiviteit in melk.
Aangezien er geen gegevens zijn uit gecontroleerde onderzoeken over het gebruik van intranasale FLONASE-neusspray 50 mcg door moeders die borstvoeding geven, is voorzichtigheid geboden wanneer FLONASE-neusspray 50 mcg wordt toegediend aan een vrouw die borstvoeding geeft.
Pediatrisch gebruik
De veiligheid en werkzaamheid van FLONASE-neusspray bij kinderen van 4 jaar en ouder zijn vastgesteld [zie: ONGEWENSTE REACTIES , KLINISCHE FARMACOLOGIE ]. Zeshonderdvijftig (650) proefpersonen in de leeftijd van 4 tot 11 jaar en 440 proefpersonen van 12 tot 17 jaar werden bestudeerd in klinische onderzoeken in de VS met fluticasonpropionaat-neusspray. De veiligheid en werkzaamheid van FLONASE Neusspray 50mcg bij kinderen jonger dan 4 jaar zijn niet vastgesteld.
Effecten op groei
Gecontroleerde klinische onderzoeken hebben aangetoond dat intranasale corticosteroïden een vermindering van de groeisnelheid kunnen veroorzaken bij toediening aan pediatrische patiënten. Dit effect werd waargenomen bij afwezigheid van laboratoriumgegevens van onderdrukking van de hypothalamus-hypofyse-bijnieras (HPA), wat suggereert dat groeisnelheid een gevoeligere indicator is voor systemische blootstelling aan corticosteroïden bij pediatrische patiënten dan sommige veelgebruikte tests van de HPA-asfunctie. De langetermijneffecten van deze verlaging van de groeisnelheid geassocieerd met intranasale corticosteroïden, inclusief de impact op de uiteindelijke volwassen lengte, zijn onbekend. Het potentieel voor "inhaalgroei" na stopzetting van de behandeling met intranasale corticosteroïden is niet voldoende onderzocht. De groei van pediatrische patiënten die intranasale corticosteroïden krijgen, waaronder FLONASE-neusspray, moet routinematig worden gecontroleerd (bijv. via stadiometrie). De mogelijke groei-effecten van langdurige behandeling moeten worden afgewogen tegen de klinische voordelen die worden verkregen en de risico's die gepaard gaan met alternatieve therapieën. Om de systemische effecten van intranasale corticosteroïden, waaronder FLONASE-neusspray, te minimaliseren, moet de dosering van elke patiënt worden getitreerd tot de laagste dosering die zijn/haar symptomen effectief onder controle houdt.
Een 1-jarige placebogecontroleerde studie werd uitgevoerd bij 150 pediatrische proefpersonen (in de leeftijd van 3 tot 9 jaar) om het effect van FLONASE-neusspray (eenmalige dagelijkse dosis van 200 mcg) op de groeisnelheid te beoordelen. Van de primaire populatie die FLONASE-neusspray (n = 56) en placebo (n = 52) kreeg, was de puntschatting voor groeisnelheid met FLONASE-neusspray 50 mcg 0,14 cm/jaar lager dan placebo (95% BI: -0,54, 0,27 cm /jaar). Er werd dus geen statistisch significant effect op de groei waargenomen in vergelijking met placebo. Er werd geen bewijs van klinisch relevante veranderingen in de HPA-asfunctie of botmineraaldichtheid waargenomen, zoals beoordeeld door respectievelijk 12-uurs urinecortisolexcretie en dual-energy röntgenabsorptiometrie.
Het kan niet worden uitgesloten dat FLONASE-neusspray 50 mcg groeionderdrukking veroorzaakt bij gevoelige patiënten of wanneer het wordt gegeven in hogere dan aanbevolen doseringen.
Geriatrisch gebruik
Een beperkt aantal proefpersonen van 65 jaar en ouder (n = 129) of 75 jaar en ouder (n = 11) is in klinische onderzoeken behandeld met FLONASE-neusspray. Hoewel het aantal proefpersonen te klein is om een afzonderlijke analyse van de werkzaamheid en veiligheid mogelijk te maken, waren de bijwerkingen die in deze populatie werden gemeld vergelijkbaar met de bijwerkingen die door jongere patiënten werden gemeld. Over het algemeen moet de dosiskeuze voor een oudere patiënt voorzichtig zijn, meestal beginnend aan het lage uiteinde van het doseringsbereik, als gevolg van de grotere frequentie van verminderde lever-, nier- of hartfunctie en van gelijktijdige ziekte of andere medicamenteuze behandeling.
Leverfunctiestoornis
Er zijn geen formele farmacokinetische onderzoeken uitgevoerd met FLONASE-neusspray 50 mcg bij proefpersonen met een leverfunctiestoornis. Aangezien fluticasonpropionaat voornamelijk wordt geklaard door levermetabolisme, kan een leverfunctiestoornis leiden tot accumulatie van fluticasonpropionaat in plasma. Daarom moeten patiënten met een leveraandoening nauwlettend worden gecontroleerd.

Nierfunctiestoornis
Er zijn geen formele farmacokinetische onderzoeken uitgevoerd met FLONASE-neusspray bij proefpersonen met een nierfunctiestoornis.
OVERDOSERING
Chronische overdosering kan leiden tot tekenen/symptomen van hypercorticisme (zie: PREVENTIEVE MAATREGELEN ). Intranasale toediening van 2 mg (10 maal de aanbevolen dosis) fluticasonpropionaat tweemaal daags gedurende 7 dagen aan gezonde menselijke vrijwilligers werd goed verdragen. Enkelvoudige orale doses tot 16 mg zijn onderzocht bij menselijke vrijwilligers zonder dat er acute toxische effecten zijn gemeld. Herhaalde orale doses tot 80 mg per dag gedurende 10 dagen bij vrijwilligers en herhaalde orale doses tot 10 mg per dag gedurende 14 dagen bij patiënten werden goed verdragen. Bijwerkingen waren van lichte of matige ernst en de incidenties waren vergelijkbaar in actieve en placebobehandelingsgroepen. Acute overdosering met deze doseringsvorm is onwaarschijnlijk, aangezien 1 fles FLONASE (fluticasonpropionaat) neusspray ongeveer 8 mg fluticasonpropionaat bevat.
De orale en subcutane mediane dodelijke doses bij muizen en ratten waren >1.000 mg/kg (respectievelijk >20.000 en >41.000 maal de maximaal aanbevolen dagelijkse intranasale dosis bij volwassenen en respectievelijk >10.000 en >20.000 maal de maximaal aanbevolen dagelijkse intranasale dosis). dosis bij kinderen op basis van mg/m²).
CONTRA-INDICATIES
FLONASE (fluticasonpropionaat) Neusspray is gecontra-indiceerd bij patiënten met een overgevoeligheid voor een van de ingrediënten.
KLINISCHE FARMACOLOGIE
Werkingsmechanisme
Fluticasonpropionaat is een synthetisch getrifluoreerd corticosteroïde met ontstekingsremmende werking. Van fluticasonpropionaat is in vitro aangetoond dat het een bindingsaffiniteit voor de humane glucocorticoïdreceptor vertoont die 18 keer zo hoog is als die van dexamethason, bijna twee keer die van beclomethason-17-monopropionaat (BMP), de actieve metaboliet van beclomethasondipropionaat, en meer dan 3 keer die van budesonide. Gegevens van de McKenzie vasoconstrictor-assay bij de mens zijn consistent met deze resultaten. De klinische betekenis van deze bevindingen is niet bekend.
Het precieze mechanisme waardoor fluticasonpropionaat de symptomen van rhinitis beïnvloedt, is niet bekend. Van corticosteroïden is aangetoond dat ze een breed scala aan effecten hebben op meerdere celtypen (bijv. mestcellen, eosinofielen, neutrofielen, macrofagen, lymfocyten) en mediatoren (bijv. histamine, eicosanoïden, leukotriënen, cytokinen) die betrokken zijn bij ontstekingen. In 7 onderzoeken bij volwassenen heeft FLONASE-neusspray het aantal eosinofielen in het neusslijmvlies verminderd bij 66% van de patiënten (35% voor placebo) en basofielen bij 39% van de patiënten (28% voor placebo). De directe relatie van deze bevindingen met langdurige symptoomverlichting is niet bekend.
farmacodynamiek
HPA-aseffect
De mogelijke systemische effecten van FLONASE-neusspray 50 mcg op de HPA-as werden geëvalueerd. FLONASE Neusspray 50 mcg gegeven als 200 mcg eenmaal daags of 400 mcg tweemaal daags werd vergeleken met placebo of orale prednison 7,5 of 15 mg 's ochtends. FLONASE-neusspray had bij beide doseringen gedurende 4 weken geen invloed op de bijnierrespons op 6 uur durende cosyntropinestimulatie, terwijl beide doseringen van oraal prednison de respons op cosyntropine significant verminderden.
Cardiale elektrofysiologie
Er is geen onderzoek uitgevoerd dat specifiek is opgezet om het effect van FLONASE op het QT-interval te evalueren.
Farmacokinetiek
De activiteit van FLONASE-neusspray 50 mcg is te wijten aan het moedergeneesmiddel, fluticasonpropionaat. Vanwege de lage biologische beschikbaarheid via de intranasale route, werden de meeste farmacokinetische gegevens verkregen via andere toedieningsroutes.
Absorptie
Indirecte berekeningen geven aan dat fluticasonpropionaat, toegediend via de intranasale route, een absolute biologische beschikbaarheid heeft van gemiddeld minder dan 2%. Proeven met orale dosering van gelabeld en ongelabeld geneesmiddel hebben aangetoond dat de orale systemische biologische beschikbaarheid van fluticasonpropionaat verwaarloosbaar is (
Verdeling
Na intraveneuze toediening was de initiële dispositiefase voor fluticasonpropionaat snel en consistent met de hoge oplosbaarheid van lipiden en weefselbinding. Het distributievolume was gemiddeld 4,2 l/kg.
Het percentage fluticasonpropionaat gebonden aan humane plasma-eiwitten was gemiddeld 99%. Fluticasonpropionaat is zwak en reversibel gebonden aan erytrocyten en is niet significant gebonden aan humaan transcortine.
Eliminatie
Na intraveneuze toediening vertoonde fluticasonpropionaat een polyexponentiële kinetiek en had het een terminale eliminatiehalfwaardetijd van ongeveer 7,8 uur. De totale bloedklaring van fluticasonpropionaat is hoog (gemiddeld: 1.093 ml/min), waarbij de nierklaring minder dan 0,02% van het totaal uitmaakt.
Metabolisme: De enige circulerende metaboliet die bij de mens is gedetecteerd, is het 17β-carbonzuurderivaat van fluticasonpropionaat, dat wordt gevormd via de CYP3A4-route. Deze metaboliet had in vitro minder affiniteit (ongeveer 1/2.000) dan het oorspronkelijke geneesmiddel voor de glucocorticoïdreceptor van humaan longcytosol en verwaarloosbare farmacologische activiteit in dierstudies. Andere metabolieten die in vitro zijn gedetecteerd met behulp van gekweekte humane hepatoomcellen zijn niet gedetecteerd bij de mens.
Uitscheiding: Minder dan 5% van een radioactief gelabelde orale dosis werd als metabolieten in de urine uitgescheiden, terwijl de rest als moedergeneesmiddel en metabolieten in de feces werd uitgescheiden.
Speciale populaties
Fluticasonpropionaat neusspray is niet onderzocht bij speciale populaties en er zijn geen geslachtsspecifieke farmacokinetische gegevens verkregen.
Geneesmiddelinteracties
Remmers van Cytochroom P450 3A4: Ritonavir: Fluticasonpropionaat is een substraat van CYP3A4. Gelijktijdige toediening van fluticasonpropionaat en de sterke CYP3A4-remmer, ritonavir, wordt niet aanbevolen op basis van een cross-over onderzoek naar geneesmiddelinteracties met meerdere doses bij 18 gezonde proefpersonen. Fluticasonpropionaat waterige neusspray (200 mcg eenmaal daags) werd gedurende 7 dagen gelijktijdig toegediend met ritonavir (100 mg tweemaal daags). De plasmaconcentraties van fluticasonpropionaat na waterige neusspray met fluticasonpropionaat alleen waren bij de meeste proefpersonen niet detecteerbaar (
Ketoconazol: Gelijktijdige toediening van oraal geïnhaleerd fluticasonpropionaat (1.000 mcg) en ketoconazol (200 mg eenmaal daags) resulteerde in een 1,9-voudige toename van de plasmablootstelling aan fluticasonpropionaat en een afname van 45% van de plasmacortisol AUC, maar had geen effect op de urinaire excretie van cortisol.
Erytromycine: In een geneesmiddelinteractiestudie met meerdere doses had gelijktijdige toediening van oraal geïnhaleerd fluticasonpropionaat (500 mcg tweemaal daags) en erytromycine (333 mg driemaal daags) geen invloed op de farmacokinetiek van fluticasonpropionaat.
PATIËNT INFORMATIE
FLANASE® [flow'naz] (fluticasonpropionaat) Neusspray, 50 mcg
Lees de patiënteninformatie die bij FLONASE-neusspray wordt geleverd voordat u deze gaat gebruiken en elke keer dat u een nieuwe vulling krijgt. Mogelijk is er nieuwe informatie. Deze patiëntinformatie vervangt niet het praten met uw zorgverlener over uw medische toestand of behandeling.
Wat is FLONASE-neusspray?
FLONASE Neusspray 50mcg is een receptgeneesmiddel dat wordt gebruikt voor de behandeling van niet-allergische neussymptomen zoals loopneus, verstopte neus, niezen en jeukende neus bij volwassenen en kinderen van 4 jaar en ouder.
Het is niet bekend of FLONASE Neusspray 50mcg veilig en effectief is bij kinderen jonger dan 4 jaar.
Wie mag FLONASE Neusspray 50mcg niet gebruiken?
Gebruik FLONASE Neusspray 50mcg niet als u allergisch bent voor fluticasonpropionaat of voor één van de ingrediënten in FLONASE Neusspray. Zie "Wat zijn de ingrediënten in FLONASE Neusspray 50mcg?" hieronder voor een volledige lijst van ingrediënten.
Wat moet ik mijn zorgverlener vertellen voordat ik FLONASE-neusspray 50mcg gebruik?
Vertel uw zorgverlener over al uw gezondheidsproblemen, ook als u:
- neuszweren, neusoperaties of neusletsel heeft of heeft gehad.
- oogproblemen heeft, zoals staar of glaucoom.
- een probleem met het immuunsysteem hebben.
- zijn allergisch voor een van de ingrediënten in FLONASE-neusspray, andere medicijnen of voedingsproducten. Zien "Wat zijn de ingrediënten in FLONASE-neusspray?" hieronder voor een volledige lijst van ingrediënten.
- elk type virale, bacteriële of schimmelinfectie heeft.
- worden blootgesteld aan waterpokken of mazelen.
- andere medische aandoeningen heeft.
- zwanger bent of van plan bent zwanger te worden. Het is niet bekend of FLONASE-neusspray schadelijk kan zijn voor uw ongeboren baby.
- borstvoeding geeft of van plan bent borstvoeding te geven. Het is niet bekend of FLONASE Neusspray 50mcg in uw moedermelk terechtkomt en of het schadelijk kan zijn voor uw baby.
Vertel uw zorgverlener over alle medicijnen die u gebruikt, inclusief recept- en vrij verkrijgbare medicijnen, vitamines en kruidensupplementen. FLONASE Neusspray en bepaalde andere geneesmiddelen kunnen met elkaar interageren. Dit kan ernstige bijwerkingen veroorzaken. Vertel uw zorgverlener vooral als u antischimmel- of hiv-geneesmiddelen gebruikt.
Weet welke medicijnen u gebruikt. Houd er een lijst van bij om uw zorgverlener en apotheker te laten zien wanneer u een nieuw geneesmiddel krijgt.
Hoe moet ik FLONASE-neusspray gebruiken?
Lees de stapsgewijze instructies voor het gebruik van FLONASE-neusspray aan het einde van deze patiënteninformatie.
- FLONASE Neusspray is alleen voor gebruik in uw neus. Spuit het niet in uw ogen of mond.
- Kinderen moeten FLONASE-neusspray gebruiken met de hulp van een volwassene, volgens de instructies van de zorgverlener van het kind.
- Gebruik FLONASE Neusspray 50mcg precies zoals uw zorgverlener u dat vertelt. Gebruik FLONASE Neusspray niet vaker dan is voorgeschreven.
- FLONASE-neusspray kan bij regelmatig gebruik enkele dagen duren voordat uw rinitissymptomen beter worden. Als uw symptomen niet verbeteren of verergeren, neem dan contact op met uw zorgverlener.
- krijgt de beste resultaten als u FLONASE-neusspray elke dag regelmatig blijft gebruiken zonder een dosis te missen. Nadat u zich beter begint te voelen, kan uw zorgverlener uw dosis verlagen. Niet doen stop met het gebruik van FLONASE Neusspray 50mcg tenzij uw zorgverlener u dat zegt.
Wat zijn de mogelijke bijwerkingen van FLONASE Neusspray 50mcg?
FLONASE Neusspray 50mcg kan ernstige bijwerkingen veroorzaken, waaronder:
- neus problemen. Neusproblemen kunnen zijn:
- neus bloedt.
- zweren (zweren) in uw neus.
- een bepaalde schimmelinfectie in uw neus, mond en/of keel (spruw).
- gat in het kraakbeen van uw neus (neusseptumperforatie). Symptomen van neusseptumperforatie kunnen zijn:
- korstvorming in de neus
- neusbloedingen
- loopneus
- fluitend geluid als je ademt
- langzame wondgenezing. mag FLONASE-neusspray pas gebruiken als uw neus is genezen als u een zweertje in uw neus heeft, een operatie aan uw neus heeft ondergaan of als uw neus gewond is geraakt.
- oogproblemen, waaronder glaucoom en staar. U moet regelmatig oogonderzoeken ondergaan terwijl u FLONASE-neusspray gebruikt.
- ernstige allergische reacties. Bel uw zorgverlener of zoek medische noodhulp als u een van de volgende tekenen van een ernstige allergische reactie krijgt:
- uitslag
- netelroos
- zwelling van uw gezicht, mond en tong
- ademhalingsproblemen
- verzwakt immuunsysteem en verhoogde kans op het krijgen van infecties (immunosuppressie). Als u medicijnen gebruikt die uw immuunsysteem verzwakken, heeft u meer kans op infecties en kunnen bepaalde infecties verergeren. Deze infecties kunnen omvatten tuberculose (TB), oculaire herpes simplex-infecties en infecties veroorzaakt door schimmels, bacteriën, virussen en parasieten. Vermijd contact met mensen die een besmettelijke ziekte hebben zoals waterpokken of mazelen tijdens het gebruik van FLONASE Neusspray. Als u in contact komt met iemand die waterpokken of mazelen heeft, bel dan onmiddellijk uw zorgverlener. Symptomen van een infectie kunnen zijn:
- koorts
- zich moe voelen
- pijn
- misselijkheid
- pijnen
- braken
- rillingen
- verlaagde steroïdhormoonspiegels (bijnierinsufficiëntie). Bijnierinsufficiëntie treedt op wanneer uw bijnieren niet genoeg steroïde hormonen aanmaken. Dit kan gebeuren als u stopt met het innemen van orale corticosteroïden (zoals prednison) en begint met het innemen van een geneesmiddel dat een geïnhaleerde steroïde bevat (zoals FLONASE-neusspray). Symptomen van bijnierinsufficiëntie kunnen zijn:
- zich moe voelen
- gebrek aan energie
- zwakheid
- misselijkheid en overgeven
- lage bloeddruk
- vertraagde groei bij kinderen. De groei van een kind moet vaak worden gecontroleerd.
De meest voorkomende bijwerkingen van FLONASE Neusspray 50mcg zijn:
- hoofdpijn
- misselijkheid en overgeven
- keelpijn
- moeite met ademhalen
- neusbloedingen
- hoesten
- neus branden of jeuk
Vertel uw zorgverlener over elke bijwerking die u hindert of niet weggaat.
Dit zijn niet alle bijwerkingen van FLONASE Neusspray. Vraag uw zorgverlener of apotheker om meer informatie.
Bel uw arts voor medisch advies over bijwerkingen. U kunt bijwerkingen melden aan de FDA op 1-800-FDA-1088.
Hoe bewaar ik FLONASE Neusspray 50mcg?
- Bewaar FLONASE tussen 39 ° F en 86 ° F (4 ° C en 30 ° C).
Houd FLONASE Neusspray 50mcg en alle geneesmiddelen buiten het bereik van kinderen.
Algemene informatie over het veilige en effectieve gebruik van FLONASE Neusspray.
Geneesmiddelen worden soms voorgeschreven voor doeleinden die niet in een patiëntenbijsluiter worden vermeld. Gebruik FLONASE Neusspray niet voor een aandoening waarvoor het niet is voorgeschreven. Geef uw FLONASE-neusspray niet aan andere mensen, ook niet als zij dezelfde aandoening hebben als u. Het kan hen schaden.
Deze bijsluiter voor patiënten geeft een samenvatting van de belangrijkste informatie over FLONASE-neusspray. Als u meer informatie wilt, neem dan contact op met uw zorgverlener. U kunt uw apotheker of zorgverlener om informatie vragen over FLONASE-neusspray die is geschreven voor beroepsbeoefenaren in de gezondheidszorg.
Bel 1-888-825-5249 voor meer informatie over FLONASE-neusspray.
Wat zijn de ingrediënten in FLONASE Neusspray 50mcg?
Actief bestanddeel: fluticasonpropionaat.
Inactieve ingrediënten: microkristallijne cellulose, carboxymethylcellulose-natrium, dextrose, 0,02% w/w benzalkoniumchloride, polysorbaat 80 en 0,25% w/w fenylethylalcohol.
Gebruiksaanwijzing
FLANASE® [flow'naz] (fluticasonpropionaat) Neusspray, 50 mcg
FLONASE Neusspray 50mcg is alleen voor gebruik in uw neus.
Lees deze informatie voordat u uw FLONASE-neusspray gaat gebruiken.
Onderdelen van uw FLONASE-neusspray (Zie afbeelding A)
Afbeelding A 
Uw FLONASE Neusspray 50mcg moet worden geprimed voordat u het voor de eerste keer gebruikt en wanneer u het een week of langer niet hebt gebruikt.
Hoe u uw FLONASE-neusspray moet primen?
- Schud de fles voorzichtig en verwijder vervolgens de stofkap (zie afbeelding B).
Figuur B 
- Houd de fles vast zoals weergegeven (zie afbeelding C) met de neusapplicator van u af gericht en met uw wijsvinger en middelvinger aan weerszijden van de neusapplicator en uw duim onder de fles.
- Druk 6 keer in en laat los totdat er een fijne straal verschijnt (zie afbeelding C). De pomp is nu klaar voor gebruik.
Figuur C 
Uw FLONASE-neusspray gebruiken:
Stap 1 . Snuit je neus om je neusgaten schoon te maken.
Stap 2 . Sluit 1 neusgat. Kantel uw hoofd iets naar voren en, terwijl u de fles rechtop houdt, breng de neusapplicator voorzichtig in het andere neusgat (zie afbeelding D).
Figuur D 
Stap 3 Begin door je neus in te ademen en druk terwijl je inademt stevig en snel 1 keer op de applicator om de spray vrij te geven. Om een volledige dosis te krijgen, gebruikt u uw wijsvinger en middelvinger om te sprayen terwijl u de basis van de fles met uw duim ondersteunt. Vermijd sprayen in uw ogen. Adem rustig in door het neusgat (zie afbeelding E).
Figuur E 
Stap 4 . Adem uit door je mond.
Stap 5 . Als een tweede verstuiving in dat neusgat nodig is, herhaal dan stap 2 tot en met 4.
Stap 6 . Herhaal stap 2 tot en met 5 in het andere neusgat.
Stap 7 . Veeg de neusapplicator af met een schone tissue en plaats de stofkap terug (zie afbeelding F).
Figuur F 
Gebruik deze fles niet voor meer dan het aangegeven aantal verstuivingen, ook al is de fles niet helemaal leeg. Voordat u de fles weggooit, moet u met uw zorgverlener overleggen of een nieuwe vulling nodig is. Neem geen extra doses en stop niet met het gebruik van FLONASE Neusspray 50mcg zonder met uw zorgverlener te overleggen.
Uw FLONASE-neusspray reinigen:
Uw neusspray moet minstens 1 keer per week worden schoongemaakt.
1. Verwijder het stofkapje en trek het voorzichtig omhoog om de neusapplicator los te maken.
2. Was de applicator en stofkap onder warm kraanwater. Laat drogen bij kamertemperatuur.
3. Plaats de applicator en de stofkap terug op de fles.
4. Als de neusapplicator verstopt raakt, kan deze worden verwijderd en in warm water worden geweekt. Spoel de neusapplicator af met koud kraanwater. Droog de neusapplicator en plaats deze terug op de fles. Probeer de neusapplicator niet te deblokkeren door er een speld of ander scherp voorwerp in te steken.
Uw FLONASE-neusspray bewaren:
- Bewaar FLONASE-neusspray 50 mcg tussen 39 ° F en 86 ° F (4 ° C en 30 ° C).
- Gebruik uw FLONASE-neusspray niet na de datum die op het etiket of de doos wordt vermeld als "EXP".
