Clarinex 5mg Desloratadine Gebruik, bijwerkingen en dosering. Prijs in online apotheek. Generieke medicijnen zonder recept.
CLARINEX® (desloratadine) Tabletten
OMSCHRIJVING
CLARINEX (desloratadine) Tabletten zijn lichtblauwe, ronde, filmomhulde tabletten die 5 mg desloratadine, een antihistaminicum, oraal moeten worden toegediend. CLARINEX 5 mg tabletten bevatten ook de volgende hulpstoffen: dibasisch calciumfosfaatdihydraat USP, microkristallijne cellulose NF, maïszetmeel NF, talk USP, carnaubawas NF, witte was NF, coatingmateriaal bestaande uit lactosemonohydraat, hypromellose, titaniumdioxide, polyethyleenglycol en FD&C blauw #2 aluminiumlak.
CLARINEX drank is een heldere oranjekleurige vloeistof die 0,5 mg/1 ml desloratadine bevat. De orale oplossing bevat de volgende inactieve ingrediënten: propyleenglycol USP, sorbitoloplossing USP, citroenzuur (watervrij) USP, natriumcitraatdihydraat USP, natriumbenzoaat NF, dinatriumedetaat USP, gezuiverd water USP. Het bevat ook kristalsuiker, natuurlijke en kunstmatige smaakstoffen voor kauwgom en FDC Yellow #6-kleurstof.
Desloratadine is een wit tot gebroken wit poeder dat enigszins oplosbaar is in water, maar zeer goed oplosbaar is in ethanol en propyleenglycol. Het heeft een empirische formule: C19H19ClN2 en een molecuulgewicht van 310,8. De chemische naam is 8-chloor-6,11-dihydro-11-(4-piperdinylideen)-5H-benzo[5,6]cyclohepta[1,2-b]pyridine en heeft de volgende structuur:
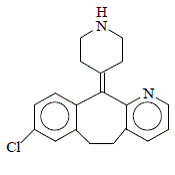
INDICATIES
Seizoensgebonden allergische rhinitis
CLARINEX® is geïndiceerd voor de verlichting van de nasale en niet-nasale symptomen van seizoensgebonden allergische rhinitis bij patiënten van 2 jaar en ouder.
Meerjarige allergische rhinitis
CLARINEX is geïndiceerd voor de verlichting van de nasale en niet-nasale symptomen van niet-seizoensgebonden allergische rhinitis bij patiënten van 6 maanden en ouder.
Chronische idiopathische urticaria
CLARINEX 5 mg is geïndiceerd voor de symptomatische verlichting van jeuk, vermindering van het aantal netelroos en de grootte van netelroos bij patiënten met chronische idiopathische urticaria van 6 maanden en ouder.
DOSERING EN ADMINISTRATIE
Hoewel er mogelijk een oraal uiteenvallende tabletformulering van desloratadine op de markt verkrijgbaar is, worden CLARINEX® RediTabs®-tabletten niet langer op de markt gebracht.
CLARINEX 5 mg tabletten, drank of RediTabs tabletten kunnen zonder rekening worden gehouden met maaltijden. Plaats CLARINEX (desloratadine) RediTabs-tabletten op de tong en laat het uiteenvallen voordat u het doorslikt. Desintegratie van tabletten vindt snel plaats. Met of zonder water toedienen. Neem de tablet onmiddellijk na het openen van de blisterverpakking in.
De bij de leeftijd passende dosis CLARINEX drank moet worden toegediend met een in de handel verkrijgbare maatdruppelaar of spuit die is gekalibreerd om 2 ml en 2,5 ml (½ theelepel) af te geven.
Volwassenen en adolescenten van 12 jaar en ouder
De aanbevolen dosering van CLARINEX-tabletten of CLARINEX RediTabs-tabletten is eenmaal daags één tablet van 5 mg. De aanbevolen dosis CLARINEX drank is eenmaal daags 2 theelepels (5 mg in 10 ml).
Kinderen van 6 tot 11 jaar
De aanbevolen dosis CLARINEX drank is eenmaal daags 1 theelepel (2,5 mg in 5 ml). De aanbevolen dosis CLARINEX RediTabs-tabletten is eenmaal daags één tablet van 2,5 mg.
Kinderen van 12 maanden tot 5 jaar oud
De aanbevolen dosis CLARINEX 5 mg drank is eenmaal daags ½ theelepel (1,25 mg in 2,5 ml).
Kinderen van 6 tot 11 maanden oud
De aanbevolen dosis CLARINEX drank is eenmaal daags 2 ml (1 mg).
Volwassenen met lever- of nierfunctiestoornissen
Bij volwassen patiënten met een lever- of nierfunctiestoornis wordt op basis van farmacokinetische gegevens een startdosering van één tablet van 5 mg om de dag aanbevolen. Doseringsaanbeveling voor kinderen met een lever- of nierfunctiestoornis kan niet worden gedaan vanwege een gebrek aan gegevens [zie: KLINISCHE FARMACOLOGIE ].
HOE GELEVERD
Doseringsvormen en sterke punten
CLARINEX-tabletten zijn lichtblauwe, filmomhulde tabletten met de inscriptie "C5" die 5 mg desloratadine bevatten. CLARINEX drank is een heldere oranjekleurige vloeistof die 0,5 mg desloratadine/1 ml bevat.
Opslag en behandeling
CLARINEX 5 mg tabletten: In reliëf gemaakte "C5", lichtblauwe, filmomhulde tabletten die zijn verpakt in plastic flessen van hoge dichtheid polyethyleen van 100 ( NDC 0085-1264-01).
CLARINEX 5 mg orale oplossing: Heldere oranjekleurige vloeistof met 0,5 mg/1 ml desloratadine in een 16-ounce Amber glazen fles ( NDC 0085-1334-01) en een 4-ounce Amber glazen fles ( NDC 0085-1334-02).
Opslag
CLARINEX-tabletten: Bescherm de eenheidsverpakking en de eenheidsdosis ziekenhuisverpakking tegen overmatig vocht. Bewaren bij 25°C (77°F); excursies toegestaan tot 15-30°C (59-86°F) [zie USP-gecontroleerde kamertemperatuur ]. Hitte gevoelig. Vermijd blootstelling bij of boven 30°C (86°F).
CLARINEX orale oplossing: Bewaren bij 25°C (77°F); excursies toegestaan tot 15-30°C (59-86°F) [zie USP-gecontroleerde kamertemperatuur ]. Bescherm tegen licht.
Gefabriceerd voor: Merck Sharp & Dohme Corp., een dochteronderneming van MERCK & CO., INC., Whitehouse Station, NJ 08889, VS. Herzien: maart 2019
BIJWERKINGEN
De volgende bijwerkingen worden in andere secties van het etiket in meer detail besproken:
- Overgevoeligheidsreacties. [Zien WAARSCHUWINGEN EN VOORZORGSMAATREGELEN ]
Ervaring met klinische proeven
Omdat klinische onderzoeken onder sterk uiteenlopende omstandigheden worden uitgevoerd, kunnen de bijwerkingen die in de klinische onderzoeken van een geneesmiddel zijn waargenomen niet direct worden vergeleken met de percentages in de klinische onderzoeken van een ander geneesmiddel en komen mogelijk niet overeen met de percentages die in de klinische praktijk worden waargenomen.
Volwassenen en adolescenten
Allergische rhinitis
In placebogecontroleerde onderzoeken met meerdere doses kregen 2834 patiënten van 12 jaar of ouder CLARINEX-tabletten in doses van 2, 5 mg tot 20 mg per dag, van wie 1655 patiënten de aanbevolen dagelijkse dosis van 5 mg. Bij patiënten die dagelijks 5 mg kregen, was het aantal bijwerkingen vergelijkbaar tussen CLARINEX 5 mg en de met placebo behandelde patiënten. Het percentage patiënten dat voortijdig stopte vanwege bijwerkingen was 2,4% in de CLARINEX 5 mg-groep en 2,6% in de placebogroep. Er waren geen ernstige bijwerkingen in deze onderzoeken bij patiënten die desloratadine kregen. Alle bijwerkingen die werden gemeld door meer dan of gelijk aan 2% van de patiënten die de aanbevolen dagelijkse dosis CLARINEX 5 mg tabletten (5 mg eenmaal daags) kregen en die vaker voorkwamen bij CLARINEX-tabletten dan bij placebo, staan vermeld in Tabel 1.
De frequentie en omvang van laboratorium- en elektrocardiografische afwijkingen waren vergelijkbaar bij met CLARINEX en met placebo behandelde patiënten.
Er waren geen verschillen in bijwerkingen voor subgroepen van patiënten zoals gedefinieerd door geslacht, leeftijd of ras.
Chronische idiopathische urticaria
In placebogecontroleerde onderzoeken met meerdere doses naar chronische idiopathische urticaria kregen 211 patiënten van 12 jaar of ouder CLARINEX 5 mg tabletten en 205 kregen een placebo. Bijwerkingen die werden gemeld door meer dan of gelijk aan 2% van de patiënten die CLARINEX 5 mg kregen en die vaker voorkwamen bij CLARINEX 5 mg dan bij placebo waren (percentages voor respectievelijk CLARINEX 5 mg en placebo): hoofdpijn (14%, 13%) misselijkheid (5%, 2%), vermoeidheid (5%, 1%), duizeligheid (4%, 3%), faryngitis (3%, 2%), dyspepsie (3%, 1%) en spierpijn (3 %, 1%).
Kindergeneeskunde
Tweehonderdzesenveertig pediatrische proefpersonen van 6 maanden tot 11 jaar kregen gedurende 15 dagen CLARINEX orale oplossing in drie placebogecontroleerde klinische onderzoeken. Pediatrische proefpersonen van 6 tot 11 jaar kregen 2,5 mg eenmaal per dag, proefpersonen van 1 tot 5 jaar kregen 1,25 mg eenmaal per dag en proefpersonen van 6 tot 11 maanden oud kregen 1,0 mg eenmaal per dag.
Bij proefpersonen van 6 tot 11 jaar werd door 2 procent of meer van de proefpersonen geen individuele bijwerking gemeld.
Bij proefpersonen van 2 tot 5 jaar waren de bijwerkingen die werden gemeld voor CLARINEX en placebo bij ten minste 2 procent van de proefpersonen die CLARINEX 5 mg drank kregen en met een frequentie die hoger was dan bij placebo koorts (5,5%, 5,4%), urineweginfectie (3,6). %, 0%) en varicella (3,6%, 0%).
Bij proefpersonen van 12 maanden tot 23 maanden oud waren de bijwerkingen die werden gemeld voor het CLARINEX 5 mg-product en placebo bij ten minste 2 procent van de proefpersonen die CLARINEX drank kregen en met een frequentie die hoger was dan bij placebo koorts (16,9%, 12,9%), diarree ( 15,4%, 11,3%), bovenste luchtweginfecties (10,8%, 9,7%), hoesten (10,8%, 6,5%), toegenomen eetlust (3,1%, 1,6%), emotionele labiliteit (3,1%, 0%), epistaxis ( 3,1%, 0%), parasitaire infectie (3,1%, 0%), faryngitis (3,1%, 0%), maculopapulaire uitslag (3,1%, 0%).
Bij proefpersonen van 6 maanden tot 11 maanden oud waren de bijwerkingen die werden gemeld voor CLARINEX 5 mg en placebo bij ten minste 2 procent van de proefpersonen die CLARINEX 5 mg drank kregen en met een frequentie die hoger was dan bij placebo infecties van de bovenste luchtwegen (21,2%, 12,9%), diarree (19,7%, 8,1%), koorts (12,1%, 1,6%), prikkelbaarheid (12,1%, 11,3%), hoesten (10,6%, 9,7%), slaperigheid (9,1%, 8,1%), bronchitis (6,1%, 0%), middenoorontsteking (6,1%, 1,6%), braken (6,1%, 3,2%), anorexia (4,5%, 1,6%), faryngitis (4,5%, 1,6%), slapeloosheid (4,5%, 0%), rinorroe (4,5%, 3,2%), erytheem (3,0%, 1,6%) en misselijkheid (3,0%, 0%).
Er waren geen klinisch betekenisvolle veranderingen in enige elektrocardiografische parameter, inclusief het QTc-interval. Slechts één van de 246 pediatrische proefpersonen die CLARINEX 5 mg drank kregen in de klinische onderzoeken stopte met de behandeling vanwege een bijwerking.
Postmarketingervaring
Omdat bijwerkingen vrijwillig worden gemeld door een populatie van onbekende grootte, is het niet altijd mogelijk om een betrouwbare schatting van hun frequentie te maken of een oorzakelijk verband met blootstelling aan geneesmiddelen vast te stellen. De volgende spontane bijwerkingen zijn gemeld tijdens het op de markt brengen van desloratadine:
Hartaandoeningen: tachycardie, hartkloppingen
Ademhalingsstelsel-, borstkas- en mediastinumaandoeningen: kortademigheid
Huid- en onderhuidaandoeningen: uitslag, jeuk
Zenuwstelselaandoeningen: psychomotorische hyperactiviteit, bewegingsstoornissen (waaronder dystonie, tics en extrapiramidale symptomen), toevallen (gemeld bij patiënten met en zonder bekende epileptische aandoening)
Immuunsysteemaandoeningen: overgevoeligheidsreacties (zoals urticaria, oedeem en anafylaxie)
onderzoeken: verhoogde leverenzymen waaronder bilirubine
Lever- en galaandoeningen: hepatitis
Metabolisme en voedingsstoornissen: verhoogde eetlust
DRUG-INTERACTIES
Remmers van cytochroom P450 3A4
In gecontroleerde klinische onderzoeken resulteerde gelijktijdige toediening van desloratadine met ketoconazol, erytromycine of azitromycine in verhoogde plasmaconcentraties van desloratadine en 3-hydroxydesloratadine, maar er waren geen klinisch relevante veranderingen in het veiligheidsprofiel van desloratadine. [Zien KLINISCHE FARMACOLOGIE ]
Fluoxetine
In gecontroleerde klinische onderzoeken resulteerde gelijktijdige toediening van desloratadine met fluoxetine, een selectieve serotonineheropnameremmer (SSRI), in verhoogde plasmaconcentraties van desloratadine en 3-hydroxydesloratadine, maar er waren geen klinisch relevante veranderingen in het veiligheidsprofiel van desloratadine. [Zien KLINISCHE FARMACOLOGIE ]
cimetidine
In gecontroleerde klinische onderzoeken resulteerde gelijktijdige toediening van desloratadine met cimetidine, een histamine-H2-receptorantagonist, in verhoogde plasmaconcentraties van desloratadine en 3-hydroxydesloratadine, maar er waren geen klinisch relevante veranderingen in het veiligheidsprofiel van desloratadine. [Zien KLINISCHE FARMACOLOGIE ]
Drugsmisbruik en afhankelijkheid
Er is geen informatie die erop wijst dat misbruik of afhankelijkheid optreedt met CLARINEX-tabletten.
WAARSCHUWINGEN
Inbegrepen als onderdeel van de PREVENTIEVE MAATREGELEN sectie.
PREVENTIEVE MAATREGELEN
Overgevoeligheidsreacties
Overgevoeligheidsreacties, waaronder huiduitslag, pruritus, urticaria, oedeem, dyspneu en anafylaxie zijn gemeld na toediening van desloratadine. Als een dergelijke reactie optreedt, moet de behandeling met CLARINEX 5 mg worden stopgezet en moet een alternatieve behandeling worden overwogen. [Zien ONGEWENSTE REACTIES ]
Informatie over patiëntbegeleiding
Adviseer de patiënt om de door de FDA goedgekeurde patiëntetikettering te lezen ( PATIËNT INFORMATIE ).
Informatie voor patiënten
- Patiënten moeten worden geïnstrueerd om CLARINEX 5 mg te gebruiken zoals aangegeven.
- Aangezien er geen voedseleffecten zijn op de biologische beschikbaarheid, kunnen patiënten worden geïnstrueerd dat CLARINEX 5 mg tabletten, drank of RediTabs tabletten zonder maaltijden mogen worden ingenomen.
- Patiënten dienen te worden geadviseerd de dosis of de doseringsfrequentie niet te verhogen, aangezien onderzoeken geen verhoogde werkzaamheid bij hogere doses hebben aangetoond en slaperigheid kan optreden.
- Fenylketonurie: CLARINEX RediTabs-tabletten bevatten fenylalanine.
Niet-klinische toxicologie
Carcinogenese, mutagenese, verminderde vruchtbaarheid
Carcinogeniteitsonderzoeken
Het carcinogene potentieel van desloratadine werd beoordeeld met behulp van een loratadine-onderzoek bij ratten en een desloratadine-onderzoek bij muizen. In een 2 jaar durende studie bij ratten werd loratadine via de voeding toegediend in doses tot 25 mg/kg/dag (geschatte blootstelling aan desloratadine en desloratadinemetaboliet was ongeveer 30 keer de AUC bij mensen bij de aanbevolen dagelijkse orale dosis). Een significant hogere incidentie van hepatocellulaire tumoren (gecombineerde adenomen en carcinomen) werd waargenomen bij mannen die 10 mg/kg/dag loratadine kregen en bij mannen en vrouwen die 25 mg/kg/dag loratadine kregen. De geschatte blootstelling aan desloratadine en desloratadinemetabolieten bij ratten die 10 mg/kg loratadine kregen, was ongeveer 7 keer de AUC bij mensen bij de aanbevolen dagelijkse orale dosis. De klinische betekenis van deze bevindingen bij langdurig gebruik van desloratadine is niet bekend.
In een 2 jaar durend voedingsonderzoek bij muizen, mannetjes en vrouwtjes die respectievelijk tot 16 mg/kg/dag en 32 mg/kg/dag kregen, liet desloratadine geen significante toename van de incidentie van tumoren zien. De geschatte blootstelling aan desloratadine en desloratadinemetabolieten bij muizen bij deze doses was respectievelijk 12 en 27 keer de AUC bij mensen bij de aanbevolen dagelijkse orale dosis.
Genotoxiciteitsstudies
In genotoxiciteitsonderzoeken met desloratadine was er geen bewijs van genotoxisch potentieel in een reverse-mutatietest (Salmonella/E. coli-test op bacteriële mutageniteit van zoogdiermicrosoom) of in 2 testen op chromosomale afwijkingen (test op clastogeniciteit van menselijke perifere bloedlymfocyten en test op micronucleus van beenmerg bij muizen ).
Aantasting van de vruchtbaarheid
Er was geen effect op de vrouwelijke vruchtbaarheid bij ratten bij doses desloratadine tot 24 mg/kg/dag (geschatte blootstellingen aan desloratadine en desloratadinemetabolieten waren ongeveer 130 keer de AUC bij mensen bij de aanbevolen dagelijkse orale dosis). Een mannelijke specifieke afname van de vruchtbaarheid, aangetoond door verminderde vrouwelijke conceptiecijfers, verminderde spermaaantallen en -motiliteit, en histopathologische veranderingen in de testikels, trad op bij een orale dosis desloratadine van 12 mg/kg bij ratten (geschatte blootstelling aan desloratadine en desloratadinemetaboliet was ongeveer 45 keer de AUC bij mensen bij de aanbevolen dagelijkse orale dosis). Desloratadine had geen effect op de vruchtbaarheid bij ratten bij een orale dosis van 3 mg/kg/dag (geschatte blootstelling aan desloratadine en desloratadinemetaboliet was ongeveer 8 keer de AUC bij mensen bij de aanbevolen dagelijkse orale dosis).
Gebruik bij specifieke populaties
Zwangerschap
Zwangerschap Categorie C
Er zijn geen adequate en goed gecontroleerde onderzoeken bij zwangere vrouwen. Omdat reproductiestudies bij dieren niet altijd voorspellend zijn voor de respons bij de mens, mag desloratadine alleen tijdens de zwangerschap worden gebruikt als dit duidelijk nodig is.
Desloratadine was niet teratogeen bij ratten of konijnen bij respectievelijk ongeveer 210 en 230 maal de oppervlakte onder de concentratie-tijdcurve (AUC) bij mensen bij de aanbevolen dagelijkse orale dosis. Een toename van pre-implantatieverlies en een verminderd aantal implantaties en foetussen werd echter opgemerkt in een afzonderlijk onderzoek bij vrouwelijke ratten bij ongeveer 120 keer de AUC bij mensen bij de aanbevolen dagelijkse orale dosis. Een verminderd lichaamsgewicht en een trage oprichtreflex werden gemeld bij pups bij ongeveer 50 keer of meer dan de AUC bij mensen bij de aanbevolen dagelijkse orale dosis. Desloratadine had geen effect op de ontwikkeling van de jongen bij ongeveer 7 keer de AUC bij mensen bij de aanbevolen dagelijkse orale dosis. De AUC's in vergelijking hadden betrekking op respectievelijk de blootstelling aan desloratadine bij konijnen en de som van de blootstellingen aan desloratadine en zijn metabolieten bij ratten. [Zien Niet-klinische toxicologie ]
Moeders die borstvoeding geven
Desloratadine gaat over in de moedermelk; daarom moet worden besloten of de borstvoeding moet worden gestaakt of dat desloratadine moet worden gestaakt, waarbij het voordeel van het geneesmiddel voor de zogende moeder en het mogelijke risico voor het kind in overweging moeten worden genomen.
Pediatrisch gebruik
De aanbevolen dosis CLARINEX 5 mg drank bij pediatrische patiënten is gebaseerd op een kruisstudie van de plasmaconcentratie van CLARINEX 5 mg bij volwassenen en pediatrische proefpersonen. De veiligheid van CLARINEX drank is vastgesteld bij 246 pediatrische proefpersonen in de leeftijd van 6 maanden tot 11 jaar in drie placebogecontroleerde klinische onderzoeken. Aangezien het verloop van seizoensgebonden en niet-seizoensgebonden allergische rhinitis en chronische idiopathische urticaria en de effecten van CLARINEX voldoende vergelijkbaar zijn bij pediatrische en volwassen populaties, is extrapolatie van de werkzaamheidsgegevens bij volwassenen naar pediatrische patiënten mogelijk. De werkzaamheid van CLARINEX 5 mg drank bij deze leeftijdsgroepen wordt ondersteund door bewijs uit adequate en goed gecontroleerde onderzoeken met CLARINEX 5 mg tabletten bij volwassenen. De veiligheid en werkzaamheid van CLARINEX 5 mg tabletten of CLARINEX 5 mg drank zijn niet aangetoond bij pediatrische patiënten jonger dan 6 maanden. [Zien KLINISCHE FARMACOLOGIE ]
De CLARINEX RediTabs 2,5 mg tablet is niet onderzocht bij pediatrische patiënten. De bio-equivalentie van de CLARINEX 5 mg RediTabs-tablet en de eerder op de markt gebrachte RediTabs-tablet is vastgesteld bij volwassenen. In combinatie met de beschreven dosisbepalingsonderzoeken in de kindergeneeskunde, ondersteunen de farmacokinetische gegevens voor CLARINEX 5 mg RediTabs het gebruik van de dosissterkte van 2,5 mg bij pediatrische patiënten van 6 tot 11 jaar.
Geriatrisch gebruik
Klinische onderzoeken met desloratadine omvatten niet voldoende aantallen proefpersonen van 65 jaar en ouder om te bepalen of zij anders reageren dan jongere proefpersonen. Andere gerapporteerde klinische ervaringen hebben geen verschillen aangetoond tussen oudere en jongere patiënten. Over het algemeen moet de dosiskeuze voor een oudere patiënt voorzichtig zijn, gezien de grotere frequentie van verminderde lever-, nier- of hartfunctie en van gelijktijdige ziekte of andere medicamenteuze behandeling. [Zien KLINISCHE FARMACOLOGIE ]
Nierfunctiestoornis
Aanpassing van de dosering voor patiënten met nierinsufficiëntie wordt aanbevolen [zie DOSERING EN ADMINISTRATIE en KLINISCHE FARMACOLOGIE ].
Leverfunctiestoornis
Aanpassing van de dosering voor patiënten met leverinsufficiëntie wordt aanbevolen [zie DOSERING EN ADMINISTRATIE en KLINISCHE FARMACOLOGIE ].
OVERDOSERING
Overweeg in geval van overdosering standaardmaatregelen om niet-geabsorbeerd geneesmiddel te verwijderen. Symptomatische en ondersteunende behandeling wordt aanbevolen. Desloratadine en 3-hydroxydesloratadine worden niet geëlimineerd door hemodialyse.
Informatie over acute overdosering is beperkt tot ervaringen uit postmarketingmeldingen van bijwerkingen en uit klinische onderzoeken die zijn uitgevoerd tijdens de ontwikkeling van het product CLARINEX 5 mg. In een dosisbereikonderzoek werd bij doses van 10 mg en 20 mg/dag slaperigheid gemeld.
In een ander onderzoek werden geen klinisch relevante bijwerkingen gemeld bij normale mannelijke en vrouwelijke vrijwilligers die gedurende 10 dagen een enkele dagelijkse dosis CLARINEX 45 mg kregen [zie KLINISCHE FARMACOLOGIE ].

Letaliteit trad op bij ratten bij orale doses van 250 mg/kg of meer (geschatte blootstellingen aan desloratadine en desloratadinemetabolieten waren ongeveer 120 keer de AUC bij mensen bij de aanbevolen dagelijkse orale dosis). De orale mediane dodelijke dosis bij muizen was 353 mg/kg (geschatte blootstelling aan desloratadine was ongeveer 290 maal de dagelijkse orale dosis voor mensen op basis van mg/m²). Er waren geen sterfgevallen bij orale doses tot 250 mg/kg bij apen (geschatte blootstelling aan desloratadine was ongeveer 810 maal de dagelijkse orale dosis voor mensen op basis van mg/m²).
CONTRA-INDICATIES
CLARINEX 5 mg tabletten, RediTabs en drank zijn gecontra-indiceerd bij patiënten die overgevoelig zijn voor dit medicijn of voor een van de bestanddelen of voor loratadine [zie WAARSCHUWINGEN EN VOORZORGSMAATREGELEN en ONGEWENSTE REACTIES ].
KLINISCHE FARMACOLOGIE
Werkingsmechanisme
Desloratadine is een langwerkende tricyclische histamine-antagonist met selectieve H1-receptor histamine-antagonistische activiteit. Gegevens over receptorbinding geven aan dat desloratadine bij een concentratie van 2-3 ng/ml (7 nanomolair) een significante interactie vertoont met de menselijke histamine H1-receptor. Desloratadine remde in vitro de afgifte van histamine uit menselijke mestcellen. Resultaten van een radioactief gelabeld weefseldistributieonderzoek bij ratten en een radioligand H1-receptorbindingsonderzoek bij cavia's toonden aan dat desloratadine de bloed-hersenbarrière niet gemakkelijk passeert. De klinische betekenis van deze bevinding is niet bekend.
farmacodynamiek
Wheal En Flare
Onderzoek naar histamine-huidaandoeningen bij mensen na enkelvoudige en herhaalde doses desloratadine van 5 mg heeft aangetoond dat het geneesmiddel een antihistaminisch effect vertoont na 1 uur; deze activiteit kan tot 24 uur aanhouden. Er was geen bewijs van histamine-geïnduceerde tachyfylaxie van de huid in de desloratadine 5-mg-groep gedurende de behandelingsperiode van 28 dagen. De klinische relevantie van histamine-huidtesten is niet bekend.
Effecten op QTc
Enkele dagelijkse doses van 45 mg werden gedurende 10 dagen aan normale mannelijke en vrouwelijke vrijwilligers gegeven. Alle ECG's die in dit onderzoek werden verkregen, werden handmatig geblindeerd gelezen door een cardioloog. Bij met CLARINEX behandelde proefpersonen was er een toename van de gemiddelde hartslag van 9,2 slagen per minuut in vergelijking met placebo. Het QT-interval werd gecorrigeerd voor de hartslag (QTc) door zowel de Bazett- als de Fridericia-methode. Bij gebruik van de QTc (Bazett) was er een gemiddelde toename van 8,1 msec bij met CLARINEX behandelde proefpersonen in vergelijking met placebo. Bij gebruik van QTc (Fridericia) was er een gemiddelde toename van 0,4 msec bij met CLARINEX behandelde proefpersonen in vergelijking met placebo. Er werden geen klinisch relevante bijwerkingen gemeld.
Farmacokinetiek
Absorptie
Na orale toediening van een tablet van 5 mg desloratadine eenmaal daags gedurende 10 dagen aan normale gezonde vrijwilligers, trad de gemiddelde tijd tot maximale plasmaconcentraties (Tmax) ongeveer 3 uur na de dosis op en de gemiddelde steady-state piekplasmaconcentraties (Cmax) en AUC van Er werden respectievelijk 4 ng/ml en 56,9 ng.hr/ml waargenomen. Noch voedsel, noch grapefruitsap had een effect op de biologische beschikbaarheid (Cmax en AUC) van desloratadine.
Het farmacokinetische profiel van CLARINEX drank werd geëvalueerd in een drievoudig cross-overonderzoek bij 30 volwassen vrijwilligers. Een enkele dosis van 10 ml CLARINEX drank met 5 mg desloratadine was bio-equivalent aan een enkele dosis CLARINEX-tablet van 5 mg. Voedsel had geen effect op de biologische beschikbaarheid (AUC en Cmax) van CLARINEX 5 mg drank.
Het farmacokinetische profiel van CLARINEX 5 mg RediTabs-tabletten werd geëvalueerd in een drievoudig cross-overonderzoek bij 24 volwassen vrijwilligers. Een enkele CLARINEX RediTabs-tablet met 5 mg desloratadine was bio-equivalent aan een enkele CLARINEX RediTabs-tablet van 5 mg (oorspronkelijke formulering) voor zowel desloratadine als 3-hydroxydesloratadine. Voedsel en water hadden geen effect op de biologische beschikbaarheid (AUC en Cmax) van CLARINEX RediTabs-tabletten.
Verdeling
Desloratadine en 3-hydroxydesloratadine zijn respectievelijk ongeveer 82% tot 87% en 85% tot 89% gebonden aan plasma-eiwitten. De eiwitbinding van desloratadine en 3-hydroxydesloratadine was onveranderd bij proefpersonen met een verminderde nierfunctie.
Metabolisme
Desloratadine (een belangrijke metaboliet van loratadine) wordt uitgebreid gemetaboliseerd tot 3-hydroxydesloratadine, een actieve metaboliet, die vervolgens wordt geglucuronideerd. De enzymen die verantwoordelijk zijn voor de vorming van 3-hydroxydesloratadine zijn niet geïdentificeerd. Gegevens uit klinische onderzoeken geven aan dat een subgroep van de algemene bevolking een verminderd vermogen heeft om 3hydroxydesloratadine te vormen en slechte metaboliseerders van desloratadine zijn. In farmacokinetische onderzoeken (n=3748) was ongeveer 6% van de proefpersonen slechte metaboliseerders van desloratadine (gedefinieerd als een proefpersoon met een AUC-verhouding van 3-hydroxydesloratadine tot desloratadine van minder dan 0,1, of een proefpersoon met een desloratadinehalfwaardetijd van meer dan 50 uur ). Deze farmacokinetische onderzoeken omvatten proefpersonen in de leeftijd van 2 tot 70 jaar, waaronder 977 proefpersonen van 2 tot 5 jaar, 1575 proefpersonen van 6 tot 11 jaar en 1196 proefpersonen van 12 tot 70 jaar. Er was geen verschil in de prevalentie van slechte metaboliseerders tussen leeftijdsgroepen. De frequentie van trage metaboliseerders was hoger bij negroïde personen (17%, n=988) in vergelijking met blanken (2%, n=1.462) en Hispanics (2%, n=1.063). De mediane blootstelling (AUC) aan desloratadine bij de trage metaboliseerders was ongeveer 6 keer groter dan bij de proefpersonen die geen trage metaboliseerders zijn. Proefpersonen die slechte metaboliseerders van desloratadine zijn, kunnen niet prospectief worden geïdentificeerd en zullen worden blootgesteld aan hogere niveaus van desloratadine na toediening van de aanbevolen dosis desloratadine. In klinische veiligheidsstudies met meerdere doses, waarbij de status van metaboliseerder werd vastgesteld, werden in totaal 94 trage metaboliseerders en 123 normale metaboliseerders geïncludeerd en behandeld met CLARINEX drank gedurende 15-35 dagen. In deze onderzoeken werden geen algemene verschillen in veiligheid waargenomen tussen trage metaboliseerders en normale metaboliseerders. Hoewel niet waargenomen in deze onderzoeken, kan een verhoogd risico op blootstellinggerelateerde bijwerkingen bij patiënten die trage metaboliseerders zijn, niet worden uitgesloten.
Eliminatie
De gemiddelde plasma-eliminatiehalfwaardetijd van desloratadine was ongeveer 27 uur. De Cmax- en AUC-waarden namen dosisproportioneel toe na enkelvoudige orale doses tussen 5 en 20 mg. De mate van accumulatie na 14 dagen dosering was consistent met de halfwaardetijd en doseringsfrequentie. Een humane massabalansstudie documenteerde een terugwinning van ongeveer 87% van de 14C-desloratadine-dosis, die gelijkelijk werd verdeeld in urine en feces als stofwisselingsproducten. Analyse van plasma-3-hydroxydesloratadine toonde vergelijkbare Tmax- en halfwaardetijden in vergelijking met desloratadine.
Speciale populaties
Geriatrische onderwerpen
Bij oudere proefpersonen (≥65 jaar oud; n=17) waren de gemiddelde Cmax- en AUC-waarden voor desloratadine na toediening van meerdere doses CLARINEX 5 mg 20% hoger dan bij jongere proefpersonen (
Pediatrische onderwerpen
Bij proefpersonen van 6 tot 11 jaar resulteerde een enkele dosis van 5 ml CLARINEX drank met 2,5 mg desloratadine in plasmaconcentraties van desloratadine die vergelijkbaar waren met de plasmaconcentraties die werden bereikt bij volwassenen die een enkele CLARINEX-tablet van 5 mg kregen toegediend. Bij proefpersonen van 2 tot 5 jaar oud resulteerde een enkele dosis van 2,5 ml CLARINEX drank met 1,25 mg desloratadine in plasmaconcentraties van desloratadine die vergelijkbaar waren met de plasmaconcentraties die werden bereikt bij volwassenen die een enkele CLARINEX-tablet van 5 mg kregen toegediend. De Cmax en AUC van de metaboliet (3-hydroxydesloratadine) waren echter 1,27 en 1,61 keer hoger voor de dosis van 5 mg drank die aan volwassenen werd toegediend in vergelijking met de Cmax en AUC die werden verkregen bij kinderen van 2 tot 11 jaar die 1,25- 2,5 mg CLARINEX drank.
Een enkele dosis van 2,5 ml of 1,25 ml CLARINEX 5 mg drank met respectievelijk 1,25 mg of 0,625 mg desloratadine werd toegediend aan proefpersonen van 6 tot 11 maanden en 12 tot 23 maanden oud. De resultaten van een populatiefarmacokinetische analyse gaven aan dat een dosis van 1 mg voor proefpersonen van 6 tot 11 maanden en 1,25 mg voor proefpersonen van 12 tot 23 maanden nodig is om desloratadineplasmaconcentraties te verkrijgen die vergelijkbaar zijn met die bereikt bij volwassenen die een enkele 5- mg dosis CLARINEX drank.
De CLARINEX 5 mg RediTabs 2,5 mg tablet is niet onderzocht bij pediatrische patiënten. Bio-equivalentie van de CLARINEX 5 mg RediTabs-tablet en de originele CLARINEX 5 mg RediTabs-tabletten is vastgesteld bij volwassenen. In combinatie met de beschreven dosisbepalingsonderzoeken in de kindergeneeskunde, ondersteunen de farmacokinetische gegevens voor CLARINEX 5 mg RediTabs-tabletten het gebruik van de dosissterkte van 2,5 mg bij pediatrische patiënten van 6 tot 11 jaar.
Nierfunctiestoornis
De farmacokinetiek van desloratadine na een enkelvoudige dosis van 7,5 mg werd gekarakteriseerd bij patiënten met milde (n=7; creatinineklaring 51-69 ml/min/1,73 m²), matige (n=6; creatinineklaring 34-43 ml/min/1,73 m²) ) en ernstige (n=6; creatinineklaring 5-29 ml/min/1,73 m²) nierfunctiestoornis of hemodialyse-afhankelijke (n=6) patiënten. Bij patiënten met lichte en matige nierinsufficiëntie namen de mediane Cmax- en AUC-waarden respectievelijk ongeveer 1,2 en 1,9-voudig toe in vergelijking met proefpersonen met een normale nierfunctie. Bij patiënten met een ernstige nierfunctiestoornis of die afhankelijk waren van hemodialyse, namen de Cmax- en AUC-waarden respectievelijk ongeveer 1,7- en 2,5-voudig toe. Er werden minimale veranderingen in de 3-hydroxydesloratadineconcentraties waargenomen. Desloratadine en 3-hydroxydesloratadine werden slecht verwijderd door hemodialyse. De plasma-eiwitbinding van desloratadine en 3-hydroxydesloratadine was onveranderd door nierinsufficiëntie. Aanpassing van de dosering voor patiënten met nierinsufficiëntie wordt aanbevolen [zie DOSERING EN ADMINISTRATIE ].
Leverfunctiestoornis
De farmacokinetiek van desloratadine werd gekarakteriseerd na een enkelvoudige orale dosis bij patiënten met lichte (n=4), matige (n=4) en ernstige (n=4) leverinsufficiëntie zoals gedefinieerd door de Child-Pugh-classificatie van leverfunctie en 8 proefpersonen met normale leverfunctie. Patiënten met leverinsufficiëntie hadden, ongeacht de ernst, een ongeveer 2,4-voudige toename van de AUC in vergelijking met normale proefpersonen. De schijnbare orale klaring van desloratadine bij patiënten met lichte, matige en ernstige leverinsufficiëntie was respectievelijk 37%, 36% en 28% van die bij normale proefpersonen. Een verhoging van de gemiddelde eliminatiehalfwaardetijd van desloratadine werd waargenomen bij patiënten met leverinsufficiëntie. Voor 3-hydroxydesloratadine waren de gemiddelde Cmax- en AUC-waarden voor patiënten met een leverfunctiestoornis niet statistisch significant verschillend van die van proefpersonen met een normale leverfunctie. Aanpassing van de dosering voor patiënten met leverinsufficiëntie wordt aanbevolen [zie DOSERING EN ADMINISTRATIE ].
Geslacht
Vrouwelijke proefpersonen die 14 dagen met CLARINEX 5 mg tabletten werden behandeld, hadden respectievelijk 10% en 3% hogere desloratadine Cmax- en AUC-waarden in vergelijking met mannelijke proefpersonen. De Cmax- en AUC-waarden van 3-hydroxydesloratadine waren ook verhoogd met respectievelijk 45% en 48% bij vrouwen in vergelijking met mannen. Het is echter niet waarschijnlijk dat deze schijnbare verschillen klinisch relevant zijn en daarom wordt geen dosisaanpassing aanbevolen.
Ras
Na 14 dagen behandeling met CLARINEX-tabletten waren de Cmax- en AUC-waarden voor desloratadine respectievelijk 18% en 32% hoger bij negroïde personen dan bij blanken. Voor 3-hydroxydesloratadine was er een overeenkomstige verlaging van 10% in Cmax- en AUC-waarden bij negroïde mensen in vergelijking met blanken. Deze verschillen zijn waarschijnlijk niet klinisch relevant en daarom wordt geen dosisaanpassing aanbevolen.
Geneesmiddelinteracties
In twee gecontroleerde cross-over klinische farmacologische onderzoeken bij gezonde mannelijke (n=12 in elke studie) en vrouwelijke (n=12 in elke studie) vrijwilligers, werd desloratadine 7,5 mg (1,5 maal de dagelijkse dosis) eenmaal daags gelijktijdig toegediend met 500 mg erytromycine om de 8 uur of ketoconazol 200 mg elke 12 uur gedurende 10 dagen. In drie afzonderlijke gecontroleerde klinische farmacologische onderzoeken met parallelle groepen werd desloratadine in een klinische dosis van 5 mg gelijktijdig toegediend met azitromycine 500 mg gevolgd door 250 mg eenmaal daags gedurende 4 dagen (n=18) of met fluoxetine 20 mg eenmaal daags gedurende 7 dagen na een voorbehandelingsperiode van 23 dagen met fluoxetine (n=18) of met cimetidine 600 mg elke 12 uur gedurende 14 dagen (n=18) onder steady-state omstandigheden aan normale gezonde mannelijke en vrouwelijke vrijwilligers. Hoewel verhoogde plasmaconcentraties (Cmax en AUC0-24 uur) van desloratadine en 3hydroxydesloratadine werden waargenomen (zie tabel 2), waren er geen klinisch relevante veranderingen in het veiligheidsprofiel van desloratadine, zoals beoordeeld aan de hand van elektrocardiografische parameters (inclusief het gecorrigeerde QT-interval), klinische laboratoriumtests, vitale functies en bijwerkingen.
Diertoxicologie en/of farmacologie Reproductietoxiciteitsonderzoeken
Desloratadine was niet teratogeen bij ratten bij doses tot 48 mg/kg/dag (geschatte blootstellingen aan desloratadine en desloratadinemetabolieten waren ongeveer 210 maal de AUC bij mensen bij de aanbevolen dagelijkse orale dosis) of bij konijnen bij doses tot 60 mg/kg/ dag (geschatte blootstelling aan desloratadine was ongeveer 230 maal de AUC bij mensen bij de aanbevolen dagelijkse orale dosis). In een afzonderlijke studie werd een toename van pre-implantatieverlies en een verminderd aantal implantaties en foetussen waargenomen bij vrouwelijke ratten bij een dosering van 24 mg/kg (geschatte blootstelling aan desloratadine en desloratadinemetaboliet was ongeveer 120 keer de AUC bij mensen bij de aanbevolen dagelijkse orale dosering). dosis). Een verminderd lichaamsgewicht en een langzame oprichtreflex werden gemeld bij pups bij doses van 9 mg/kg/dag of hoger (geschatte blootstelling aan desloratadine en desloratadinemetaboliet was ongeveer 50 keer of hoger dan de AUC bij mensen bij de aanbevolen dagelijkse orale dosis). Desloratadine had geen effect op de ontwikkeling van de jongen bij een orale dosis van 3 mg/kg/dag (de geschatte blootstelling aan desloratadine en de metaboliet van desloratadine was ongeveer 7 keer de AUC bij mensen bij de aanbevolen dagelijkse orale dosis).
Klinische studies
Seizoensgebonden allergische rhinitis
De klinische werkzaamheid en veiligheid van CLARINEX-tabletten werden geëvalueerd bij meer dan 2300 patiënten van 12 tot 75 jaar met seizoensgebonden allergische rhinitis. In totaal kregen 1838 patiënten 2,5 tot 20 mg/dag CLARINEX in 4 dubbelblinde, gerandomiseerde, placebogecontroleerde klinische onderzoeken met een duur van 2 tot 4 weken, uitgevoerd in de Verenigde Staten. De resultaten van deze onderzoeken hebben de werkzaamheid en veiligheid van CLARINEX 5 mg aangetoond bij de behandeling van volwassen en adolescente patiënten met seizoensgebonden allergische rhinitis. In een dosisbereikonderzoek werd CLARINEX 2,5 tot 20 mg/dag bestudeerd. Doses van 5, 7,5, 10 en 20 mg/dag waren superieur aan placebo; en er werd geen bijkomend voordeel gezien bij doses hoger dan 5,0 mg. In hetzelfde onderzoek werd een toename van de incidentie van slaperigheid waargenomen bij doses van 10 mg/dag en 20 mg/dag (respectievelijk 5,2% en 7,6%), vergeleken met placebo (2,3%).
In twee onderzoeken van 4 weken onder 924 patiënten (in de leeftijd van 15 tot 75 jaar) met seizoensgebonden allergische rhinitis en gelijktijdig astma, verbeterde CLARINEX 5 mg tabletten 5 mg eenmaal daags de symptomen van rhinitis, zonder afname van de longfunctie. Dit ondersteunt de veiligheid van het toedienen van CLARINEX 5 mg tabletten aan volwassen patiënten met seizoensgebonden allergische rinitis met lichte tot matige astma.
CLARINEX-tabletten van 5 mg eenmaal daags verlaagden de totale symptoomscore (de som van individuele scores van nasale en niet-nasale symptomen) significant bij patiënten met seizoensgebonden allergische rhinitis. Zie Tabel 3.
Er waren geen significante verschillen in de werkzaamheid van CLARINEX 5 mg tabletten 5 mg tussen subgroepen van patiënten gedefinieerd naar geslacht, leeftijd of ras.
Meerjarige allergische rhinitis
De klinische werkzaamheid en veiligheid van CLARINEX-tabletten 5 mg werden geëvalueerd bij meer dan 1300 patiënten van 12 tot 80 jaar met niet-seizoensgebonden allergische rhinitis. In totaal kregen 685 patiënten 5 mg/dag CLARINEX 5 mg in twee dubbelblinde, gerandomiseerde, placebogecontroleerde klinische onderzoeken met een duur van 4 weken, uitgevoerd in de Verenigde Staten en internationaal. In een van deze onderzoeken bleek CLARINEX 5 mg tabletten 5 mg eenmaal daags de totale symptoomscore significant te verlagen bij patiënten met niet-seizoensgebonden allergische rhinitis (tabel 4).
Chronische idiopathische urticaria
De werkzaamheid en veiligheid van CLARINEX 5 mg tabletten 5 mg eenmaal daags werd onderzocht bij 416 patiënten met chronische idiopathische urticaria van 12 tot 84 jaar oud, van wie er 211 CLARINEX kregen. In twee dubbelblinde, placebogecontroleerde, gerandomiseerde klinische onderzoeken met een duur van zes weken, verminderden CLARINEX-tabletten op de vooraf gespecificeerde evaluatie van het primaire tijdstip van één week de ernst van jeuk significant in vergelijking met placebo (tabel 5). Secundaire eindpunten werden ook geëvalueerd en tijdens de eerste week van de behandeling verminderde CLARINEX 5 mg tabletten 5 mg de secundaire eindpunten, "Aantal netelroos" en "Grootte van de grootste netelroos", in vergelijking met placebo.
De klinische veiligheid van CLARINEX drank werd gedocumenteerd in drie, 15-daagse, dubbelblinde, placebogecontroleerde veiligheidsonderzoeken bij pediatrische proefpersonen met een gedocumenteerde voorgeschiedenis van allergische rhinitis, chronische idiopathische urticaria of proefpersonen die in aanmerking kwamen voor antihistaminica. In de eerste studie werd 2,5 mg CLARINEX drank toegediend aan 60 pediatrische proefpersonen van 6 tot 11 jaar. De tweede studie evalueerde 1,25 mg CLARINEX drank toegediend aan 55 pediatrische proefpersonen van 2 tot 5 jaar. In het derde onderzoek werd 1,25 mg CLARINEX 5 mg drank toegediend aan 65 pediatrische proefpersonen van 12 tot 23 maanden en 1,0 mg CLARINEX drank werd toegediend aan 66 pediatrische proefpersonen van 6 tot 11 maanden oud. De resultaten van deze onderzoeken hebben de veiligheid van CLARINEX 5 mg drank aangetoond bij pediatrische proefpersonen van 6 maanden tot 11 jaar oud.
PATIËNT INFORMATIE
CLARINEX® (CLA-RI-NEX) (desloratadine) Tabletten, RediTabs® en orale oplossing
Lees de patiënteninformatie die bij CLARINEX® wordt geleverd voordat u begint met het innemen ervan en elke keer dat u een nieuwe vulling krijgt. Mogelijk is er nieuwe informatie. Deze bijsluiter is een samenvatting van de informatie voor patiënten. Uw arts of apotheker kan u aanvullende informatie geven. Deze bijsluiter vervangt niet het praten met uw arts over uw medische toestand of behandeling.
Wat is CLARINEX 5 mg?
CLARINEX is een receptgeneesmiddel dat het geneesmiddel desloratadine (een antihistaminicum) bevat.
CLARINEX wordt gebruikt om de symptomen onder controle te houden van:
- seizoensgebonden allergische rhinitis (niezen, verstopte neus, loopneus en jeukende neus) bij mensen van 2 jaar en ouder.
- niet-seizoensgebonden allergische rhinitis (niezen, verstopte neus, loopneus en jeukende neus) bij mensen van 6 maanden en ouder.
- chronische idiopathische urticaria (langdurige jeuk) en om het aantal en de grootte van netelroos te verminderen bij mensen van 6 maanden en ouder.
CLARINEX is niet bedoeld voor kinderen jonger dan 6 maanden.
Wie mag CLARINEX niet gebruiken?
Gebruik CLARINEX 5 mg niet als u:
- zijn allergisch voor desloratadine of voor één van de bestanddelen van CLARINEX-tabletten, CLARINEX RediTabs® of CLARINEX-drank. Zie het einde van deze bijsluiter voor een volledige lijst van ingrediënten.
- zijn allergisch voor loratadine (Alavert, Claritin).
Neem contact op met uw arts voordat u dit geneesmiddel inneemt als u vragen heeft over het al dan niet gebruiken van dit geneesmiddel.
Wat moet ik mijn arts vertellen voordat ik CLARINEX 5 mg inneem?
Vertel uw arts voordat u CLARINEX 5 mg inneemt als u:
- lever- of nierproblemen heeft.
- andere medische aandoeningen heeft.
- zwanger bent of van plan bent zwanger te worden. Het is niet bekend of CLARINEX 5 mg schadelijk is voor uw ongeboren baby. Neem contact op met uw arts als u zwanger bent of van plan bent zwanger te worden.
- borstvoeding geeft of van plan bent borstvoeding te geven. CLARINEX 5 mg kan in uw moedermelk terechtkomen. Praat met uw arts over de beste manier om uw baby te voeden als u CLARINEX gebruikt.
Vertel uw arts over alle medicijnen die u gebruikt, waaronder geneesmiddelen op recept en zonder recept, vitamines en kruidensupplementen. CLARINEX 5 mg kan de werking van andere geneesmiddelen beïnvloeden, en andere geneesmiddelen kunnen de werking van CLARINEX 5 mg beïnvloeden. Vertel het uw arts vooral als u:
- ketoconazol (Nizoral)
- erytromycine (Ery-tab, Eryc, PCE)
- azithromycine (Zithromax, Zmax)
- antihistaminica
- fluoxetine (Prozac)
- cimetidine (Tagamet)
Weet welke medicijnen u gebruikt. Houd een lijst bij van uw geneesmiddelen en toon deze aan uw arts en apotheker als u een nieuw geneesmiddel krijgt.
Hoe moet ik CLARINEX gebruiken?
- Neem CLARINEX 5 mg precies in zoals uw arts u zegt.
- Verander uw dosis CLARINEX 5 mg niet en neem niet vaker dan voorgeschreven.
- CLARINEX 5 mg kan met of zonder voedsel worden ingenomen.
- Plaats CLARINEX RediTabs Tablet op uw tong en laat het oplossen voordat u het doorslikt. CLARINEX 5 mg RediTabs kan met of zonder water worden ingenomen. Neem uw CLARINEX 5 mg RediTabs-tablet meteen in nadat u de blisterverpakking hebt geopend.
- Neem CLARINEX drank in met een maatdruppelaar of orale spuit die 2 ml of 2,5 ml kan afmeten. Vraag uw apotheker om een druppelaar of spuit als u die niet heeft.
- Als u te veel CLARINEX heeft ingenomen, neem dan onmiddellijk contact op met uw arts of roep medische hulp in.
Wat zijn de mogelijke bijwerkingen van CLARINEX-tabletten?
CLARINEX 5 mg kan ernstige bijwerkingen veroorzaken, waaronder:
- Allergische reacties. Stop met het innemen van CLARINEX 5 mg en bel onmiddellijk uw arts of zoek noodhulp als u een van deze symptomen heeft:
- uitslag
- jeuk
- netelroos
- zwelling van uw lippen, tong, gezicht en keel
- kortademigheid of moeite met ademhalen
De meest voorkomende bijwerkingen van CLARINEX bij volwassenen en kinderen van 12 jaar en ouder met allergische rhinitis zijn:
- keelpijn
- droge mond
- spierpijn
- vermoeidheid
- slaperigheid
- menstruatie pijn
Verhoogde slaperigheid of vermoeidheid kan optreden als u meer CLARINEX heeft ingenomen dan uw arts u heeft voorgeschreven.
Vertel het uw arts als u een bijwerking heeft die u hindert of die niet weggaat.
Dit zijn niet alle mogelijke bijwerkingen van CLARINEX. Vraag uw arts of apotheker om meer informatie.
Bel uw arts voor medisch advies over bijwerkingen. U kunt bijwerkingen melden aan de FDA op 1-800-FDA-1088.
Hoe moet ik CLARINEX 5 mg bewaren?
- Op te slaan CLARINEX-tabletten tussen 59°F tot 86°F (15°C tot 30°C).
- CLARINEX-tabletten zijn gevoelig voor warmte. Niet bewaren boven 30 °C (86 °F).
- Beschermen CLARINEX 5 mg tabletten van vocht.
- Op te slaan CLARINEX 5 mg orale oplossing tussen 59°F tot 86°F (15°C tot 30°C). Bescherm CLARINEX 5 mg drank tegen licht.
Houden CLARINEX-tabletten, RediTabs-tabletten , en Orale oplossing en alle medicijnen buiten het bereik van kinderen.
Algemene informatie over CLARINEX
Geneesmiddelen worden soms voorgeschreven voor andere doeleinden dan vermeld in de bijsluiter. Gebruik CLARINEX 5 mg niet voor een aandoening waarvoor het niet is voorgeschreven. Geef CLARINEX 5 mg niet aan andere mensen, ook niet als zij dezelfde aandoening hebben als u. Het kan hen schaden.
Deze bijsluiter voor patiënten vat de belangrijkste informatie over CLARINEX samen. Als u meer informatie wilt, neem dan contact op met uw arts. U kunt uw apotheker of arts om informatie vragen over CLARINEX die is geschreven voor gezondheidswerkers.
Ga voor meer informatie naar www.CLARINEX.com
Wat zijn de ingrediënten in CLARINEX 5 mg?
Actief ingrediënt: desloratadine
Patiënten met fenylketonurie: CLARINEX RediTabs-tabletten bevatten fenylalanine.
Inactieve ingrediënten in CLARINEX 5 mg tabletten: dibasisch calciumfosfaatdihydraat USP, microkristallijne cellulose NF, maïszetmeel NF, talk USP, carnaubawas NF, witte was NF, coatingmateriaal bestaande uit lactosemonohydraat, hypromellose, titaniumdioxide, polyethyleenglycol en FD&C Blue #2 Aluminium Lake.
Inactieve ingrediënten in CLARINEX 5 mg orale oplossing: propyleenglycol USP, sorbitoloplossing USP, citroenzuur (watervrij) USP, natriumcitraatdihydraat USP, natriumbenzoaat NF, dinatriumedetaat USP, gezuiverd water USP. Het bevat ook kristalsuiker, natuurlijke en kunstmatige smaakstoffen voor kauwgom en FDC Yellow #6-kleurstof.
