Behandeling van kanker: Nolvadex 10mg, 20mg Tamoxifen Gebruik, bijwerkingen en dosering. Prijs in online apotheek. Generieke medicijnen zonder recept.
Wat is Nolvadex en hoe wordt het gebruikt?
Nolvadex 10 mg is een receptgeneesmiddel dat wordt gebruikt om de symptomen van borstkanker te behandelen. Nolvadex kan alleen of in combinatie met andere medicijnen worden gebruikt.
Nolvadex 20 mg behoort tot een klasse geneesmiddelen die antineoplastische middelen, oestrogeenreceptorantagonisten, worden genoemd.
Het is niet bekend of Nolvadex 20 mg veilig en effectief is bij kinderen.
Wat zijn de mogelijke bijwerkingen van Nolvadex 20 mg?
Nolvadex kan ernstige bijwerkingen veroorzaken, waaronder:
- visie verandert,
- oogpijn,
- gemakkelijk blauwe plekken of bloedingen,
- stemmingswisselingen,
- zwelling van de enkels of voeten, en
- ongewone vermoeidheid
Roep meteen medische hulp in als u een van de bovenstaande symptomen heeft.
De meest voorkomende bijwerkingen van Nolvadex zijn:
- opvliegers,
- blozen,
- veranderingen in menstruatie,
- misselijkheid,
- beenkrampen,
- buikkrampen,
- bot pijn,
- spierpijn,
- hoesten,
- zwelling,
- vermoeidheid,
- dunner wordend haar,
- hoofdpijn,
- depressie, en
- verlies van seksuele bekwaamheid/interesse (bij mannen)
Vertel het uw arts als u een bijwerking heeft die u hindert of die niet weggaat.
Dit zijn niet alle mogelijke bijwerkingen van Nolvadex. Vraag uw arts of apotheker om meer informatie.
WAARSCHUWING
Voor vrouwen met ductaal carcinoom in situ (DCIS) en vrouwen met een hoog risico op borstkanker: Ernstige en levensbedreigende voorvallen geassocieerd met NOLVADEX (tamoxifencitraat) in de risicoverlagende setting (vrouwen met een hoog risico op kanker en vrouwen met DCIS) omvatten baarmoedermaligniteiten, beroerte en longembolie. De incidentiecijfers voor deze voorvallen werden geschat op basis van de NSABP P-1-studie (zie: KLINISCHE FARMACOLOGIE - Klinische studies - Vermindering van de incidentie van borstkanker bij vrouwen met een hoog risico ). Baarmoedermaligniteiten bestaan uit zowel endometrium adenocarcinoom (incidentie per 1.000 vrouwjaren van 2,20 voor NOLVADEX (tamoxifencitraat) versus 0,71 voor placebo) en baarmoedersarcoom (incidentie per 1.000 vrouwjaren van 0,17 voor NOLVADEX (tamoxifencitraat) versus 0,4 voor placebo)*. Voor een beroerte was de incidentie per 1.000 vrouwjaren 1,43 voor NOLVADEX (tamoxifencitraat) versus 1,00 voor placebo**. Voor longembolie was de incidentie per 1.000 vrouwjaren 0,75 voor NOLVADEX (tamoxifencitraat) versus 0,25 voor placebo**.
Sommige beroertes, longembolie en baarmoedermaligniteiten waren fataal.
Zorgverleners moeten de mogelijke voordelen versus de mogelijke risico's van deze ernstige gebeurtenissen bespreken met vrouwen met een hoog risico op borstkanker en vrouwen met DCIS die NOLVADEX (tamoxifencitraat) overwegen om hun risico op het ontwikkelen van borstkanker te verminderen.
De voordelen van NOLVADEX (tamoxifencitraat) wegen op tegen de risico's bij vrouwen die al met borstkanker zijn gediagnosticeerd.
REFERENTIES
* Bijgewerkte langetermijnfollow-upgegevens (mediane duur van follow-up is 6,9 jaar) uit NSABP P-1-onderzoek. Zien WAARSCHUWINGEN: Effecten op baarmoeder-endometriumkanker en baarmoedersarcoom .
**Zie Tabel 3 onder KLINISCHE FARMACOLOGIE-Klinische studies .
OMSCHRIJVING
NOLVADEX® (tamoxifencitraat) Tabletten, een niet-steroïde anti-oestrogeen, zijn voor orale toediening. NOLVADEX (tamoxifencitraat) Tabletten zijn verkrijgbaar als:
10 mg-tabletten
Elke tablet bevat 15,2 mg tamoxifencitraat, wat overeenkomt met 10 mg tamoxifen.
20 mg tabletten
Elke tablet bevat 30,4 mg tamoxifencitraat, wat overeenkomt met 20 mg tamoxifen.
Inactieve ingrediënten: carboxymethylcellulose calcium, magnesiumstearaat, mannitol en zetmeel.
Chemisch gezien is NOLVADEX (tamoxifencitraat) het trans-isomeer van een trifenylethyleenderivaat. De chemische naam is (Z)2-[4-(1,2-difenyl-1-butenyl)fenoxy]-N,N-dimethylethanamine-2-hydroxy-1,2,3-propaantricarboxylaat (1:1). De structurele en empirische formules zijn:
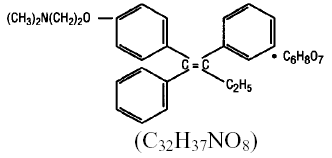
Tamoxifencitraat heeft een molecuulgewicht van 563,62, de pKa' is 8,85, de evenwichtsoplosbaarheid in water bij 37°C is 0,5 mg/ml en in 0,02 N HCl bij 37°C is deze 0,2 mg/ml.
INDICATIES
Gemetastaseerde borstkanker
NOLVADEX (tamoxifencitraat) is effectief bij de behandeling van uitgezaaide borstkanker bij vrouwen en mannen. Bij premenopauzale vrouwen met uitgezaaide borstkanker is NOLVADEX (tamoxifencitraat) een alternatief voor ovariëctomie of bestraling van de eierstokken. Beschikbare gegevens wijzen erop dat patiënten bij wie de tumoren oestrogeenreceptorpositief zijn, meer kans hebben om baat te hebben bij behandeling met NOLVADEX (tamoxifencitraat).
Adjuvante behandeling van borstkanker
NOLVADEX (tamoxifencitraat) is geïndiceerd voor de behandeling van klierpositieve borstkanker bij vrouwen na totale borstamputatie of segmentale borstamputatie, okseldissectie en borstbestraling. In sommige adjuvante onderzoeken met NOLVADEX (tamoxifencitraat) was het grootste voordeel tot nu toe in de subgroep met vier of meer positieve okselklieren.
NOLVADEX (tamoxifencitraat) is geïndiceerd voor de behandeling van okselklier-negatieve borstkanker bij vrouwen na totale borstamputatie of segmentale borstamputatie, okseldissectie en borstbestraling.
De oestrogeen- en progesteronreceptorwaarden kunnen helpen voorspellen of adjuvante behandeling met NOLVADEX (tamoxifencitraat) waarschijnlijk gunstig is.
NOLVADEX (tamoxifencitraat) vermindert het optreden van contralaterale borstkanker bij patiënten die adjuvante NOLVADEX (tamoxifencitraat) -therapie voor borstkanker krijgen.
Ductaal carcinoom in situ (DCIS)
Bij vrouwen met DCIS is NOLVADEX (tamoxifencitraat) na een borstoperatie en bestraling geïndiceerd om het risico op invasieve borstkanker te verminderen (zie GEVAARLIJKE WAARSCHUWING: aan het begin van het etiket). De beslissing met betrekking tot therapie met NOLVADEX (tamoxifencitraat) voor de vermindering van de incidentie van borstkanker moet gebaseerd zijn op een individuele beoordeling van de voordelen en risico's van behandeling met NOLVADEX (tamoxifencitraat).
Huidige gegevens uit klinische onderzoeken ondersteunen vijf jaar adjuvante NOLVADEX (tamoxifencitraat) -therapie voor patiënten met borstkanker.
Vermindering van de incidentie van borstkanker bij vrouwen met een hoog risico
NOLVADEX (tamoxifencitraat) is geïndiceerd om de incidentie van borstkanker te verminderen bij vrouwen met een hoog risico op borstkanker. Dit effect werd aangetoond in een studie met een geplande duur van 5 jaar met een mediane follow-up van 4,2 jaar. Vijfentwintig procent van de deelnemers kreeg 5 jaar lang medicatie. De effecten op langere termijn zijn niet bekend. In deze studie was er geen invloed van tamoxifen op de algehele of borstkankergerelateerde mortaliteit (zie: GEVAARLIJKE WAARSCHUWING: aan het begin van het etiket).
NOLVADEX (tamoxifencitraat) is alleen geïndiceerd voor vrouwen met een hoog risico. "Hoog risico" wordt gedefinieerd als vrouwen van ten minste 35 jaar oud met een voorspeld risico van 5 jaar op borstkanker ≥ 1,67%, zoals berekend door het Gail-model.
Voorbeelden van combinaties van factoren die een 5-jaarsrisico ≥ 1,67% voorspellen zijn:
Leeftijd 35 jaar of ouder en een van de volgende combinaties van factoren:
- Een eerstegraads familielid met een voorgeschiedenis van borstkanker, 2 of meer goedaardige biopsieën en een voorgeschiedenis van een borstbiopsie die atypische hyperplasie vertoont; of
- Ten minste 2 eerstegraads familieleden met een voorgeschiedenis van borstkanker en een persoonlijke voorgeschiedenis van ten minste één borstbiopsie; of
- LCIS
Leeftijd 40 jaar of ouder en een van de volgende combinaties van factoren:
- Een eerstegraads familielid met een voorgeschiedenis van borstkanker, 2 of meer goedaardige biopsieën, leeftijd bij eerste levendgeborene 25 of ouder, en leeftijd bij menarche 11 of jonger; of
- Ten minste 2 eerstegraads familieleden met een voorgeschiedenis van borstkanker en leeftijd bij eerste levendgeborene 19 jaar of jonger; of
- Een eerstegraads familielid met een voorgeschiedenis van borstkanker en een persoonlijke voorgeschiedenis van een borstbiopsie die atypische hyperplasie laat zien.
Leeftijd 45 jaar of ouder en een van de volgende combinaties van factoren:
- Ten minste 2 eerstegraads familieleden met een voorgeschiedenis van borstkanker en leeftijd bij eerste levendgeborene 24 of jonger; of
- Een eerstegraads familielid met een voorgeschiedenis van borstkanker met een persoonlijke voorgeschiedenis van een goedaardige borstbiopsie, leeftijd bij menarche 11 of minder en leeftijd bij eerste levendgeborene 20 of meer.
Leeftijd 50 of ouder en een van de volgende combinaties van factoren:
- Minimaal 2 eerstegraads familieleden met een voorgeschiedenis van borstkanker; of
- Geschiedenis van één borstbiopsie met atypische hyperplasie, en leeftijd bij eerste levende geboorte 30 of ouder en leeftijd bij menarche 11 of minder; of
- Geschiedenis van ten minste twee borstbiopten met een voorgeschiedenis van atypische hyperplasie en leeftijd bij eerste levendgeborene 30 of meer.
55 jaar of ouder en een van de volgende combinaties van factoren:
- Een eerstegraads familielid met een voorgeschiedenis van borstkanker met een persoonlijke voorgeschiedenis van een goedaardige borstbiopsie en een menarcheleeftijd van 11 of minder; of
- Geschiedenis van ten minste 2 borstbiopten met een voorgeschiedenis van atypische hyperplasie en leeftijd bij eerste levendgeborene 20 jaar of ouder.
60 jaar of ouder en:
- 5-jaars voorspeld risico op borstkanker ≥ 1,67%, berekend door het Gail-model.
Voor vrouwen van wie de risicofactoren niet in de bovenstaande voorbeelden zijn beschreven, is het Gail-model nodig om het absolute risico op borstkanker in te schatten. Beroepsbeoefenaren in de gezondheidszorg kunnen een Gail Model Risk Assessment Tool verkrijgen door 1-800-544-2007 te bellen.
Er zijn onvoldoende gegevens beschikbaar over het effect van NOLVADEX (tamoxifencitraat) op de incidentie van borstkanker bij vrouwen met erfelijke mutaties (BRCA1, BRCA2) om specifieke aanbevelingen te kunnen doen over de werkzaamheid van NOLVADEX (tamoxifencitraat) bij deze patiënten.
Na een beoordeling van het risico op het ontwikkelen van borstkanker, moet de beslissing over therapie met NOLVADEX (tamoxifencitraat) voor de vermindering van de incidentie van borstkanker worden gebaseerd op een individuele beoordeling van de voordelen en risico's van behandeling met NOLVADEX (tamoxifencitraat). In het NSABP P-1-onderzoek verlaagde behandeling met NOLVADEX (tamoxifencitraat) het risico op het ontwikkelen van borstkanker tijdens de follow-upperiode van het onderzoek, maar elimineerde het risico op borstkanker niet (zie tabel 3 in KLINISCHE FARMACOLOGIE ).
DOSERING EN ADMINISTRATIE
Voor patiënten met borstkanker is de aanbevolen dagelijkse dosis 20-40 mg. Doseringen hoger dan 20 mg per dag moeten in verdeelde doses worden gegeven ('s ochtends en' s avonds).
In drie onderzoeken met enkelvoudig adjuvans bij vrouwen werd één 10 mg NOLVADEX (tamoxifencitraat) tablet twee (ECOG en NATO) of drie (Toronto) keer per dag toegediend gedurende twee jaar. In de NSABP B-14 adjuvante studie bij vrouwen met kliernegatieve borstkanker werd één 10 mg NOLVADEX (tamoxifencitraat) tablet tweemaal daags gegeven gedurende tenminste 5 jaar. De resultaten van het B-14-onderzoek suggereren dat voortzetting van de therapie na vijf jaar geen bijkomend voordeel oplevert (zie: KLINISCHE FARMACOLOGIE ). In het EBCTCG-overzicht van 1995 was de vermindering van recidief en mortaliteit groter in de onderzoeken die ongeveer 5 jaar tamoxifen gebruikten dan in de onderzoeken die tamoxifen voor een kortere therapieperiode gebruikten. Er waren geen aanwijzingen dat doses hoger dan 20 mg per dag effectiever waren. Huidige gegevens uit klinische onderzoeken ondersteunen 5 jaar adjuvante NOLVADEX (tamoxifencitraat) -therapie voor patiënten met borstkanker.
Ductaal carcinoom in situ (DCIS)
De aanbevolen dosis is NOLVADEX (tamoxifencitraat) 20 mg per dag gedurende 5 jaar.
Vermindering van de incidentie van borstkanker bij vrouwen met een hoog risico
De aanbevolen dosis is NOLVADEX (tamoxifencitraat) 20 mg per dag gedurende 5 jaar. Er zijn geen gegevens die het gebruik van NOLVADEX (tamoxifencitraat) ondersteunen behalve gedurende 5 jaar (zie KLINISCHE FARMACOLOGIE - Klinische studies - Vermindering van de incidentie van borstkanker bij vrouwen met een hoog risico ).
HOE GELEVERD
10 mg-tabletten met tamoxifen als het citraat in een hoeveelheid die overeenkomt met 10 mg tamoxifen (ronde, biconvexe, niet-omhulde, witte tablet geïdentificeerd met NOLVADEX (tamoxifencitraat) 600 ingeslagen aan de ene kant en een camee ingeslagen aan de andere kant) worden geleverd in flessen van 60 tabletten. NDC 0310-0600-60.
20 mg tabletten met tamoxifen als het citraat in een hoeveelheid die overeenkomt met 20 mg tamoxifen (ronde, biconvexe, niet-omhulde, witte tablet geïdentificeerd met NOLVADEX (tamoxifencitraat) 604 ingeslagen aan de ene kant en een camee ingeslagen aan de andere kant) worden geleverd in flessen van 30 tabletten. NDC 0310-0604-30.
Bewaren bij een gecontroleerde kamertemperatuur, 20-25 ° C (68-77 ° F) (zie USP). Doseer in een goed gesloten, lichtbestendige container.
*Coumadin® is een geregistreerd handelsmerk van Bristol-Myers Squibb Pharmaceuticals. Alle andere handelsmerken zijn eigendom van de AstraZeneca-groep, AstraZeneca Pharmaceuticals LP Wilmington, Delaware 19850-5437. Herz 27-09-05. FDA-revisiedatum: 9-3-2006
BIJWERKINGEN
Bijwerkingen van NOLVADEX (tamoxifencitraat) zijn relatief mild en zelden ernstig genoeg om stopzetting van de behandeling bij borstkankerpatiënten te vereisen.
Voortgezette klinische onderzoeken hebben geleid tot verdere informatie die de incidentie van bijwerkingen met NOLVADEX (tamoxifencitraat) beter aangeeft in vergelijking met placebo.
Gemetastaseerde borstkanker
Verhoogde bot- en tumorpijn en ook lokale opflakkering van de ziekte zijn opgetreden, die soms gepaard gaan met een goede tumorrespons. Patiënten met verhoogde botpijn kunnen aanvullende pijnstillers nodig hebben. Patiënten met een aandoening van de weke delen kunnen plotselinge toename van de omvang van reeds bestaande laesies hebben, soms geassocieerd met uitgesproken erytheem binnen en rond de laesies en/of de ontwikkeling van nieuwe laesies. Wanneer ze zich voordoen, worden de botpijn of de opflakkering van de ziekte gezien kort na het starten met NOLVADEX (tamoxifencitraat) en nemen ze over het algemeen snel af.
Bij patiënten die worden behandeld met NOLVADEX (tamoxifencitraat) voor gemetastaseerde borstkanker, is de meest voorkomende bijwerking van NOLVADEX (tamoxifencitraat) opvliegers.
Andere bijwerkingen die niet vaak worden gezien, zijn hypercalciëmie, perifeer oedeem, afkeer van voedsel, pruritus vulvae, depressie, duizeligheid, licht gevoel in het hoofd, hoofdpijn, dunner wordend haar en/of gedeeltelijk haarverlies en vaginale droogheid.
Premenopauzale vrouwen
De volgende tabel geeft een samenvatting van de incidentie van bijwerkingen die zijn gemeld met een frequentie van 2% of meer uit klinische onderzoeken (Ingle, Pritchard, Buchanan) waarin de behandeling met NOLVADEX (tamoxifencitraat) werd vergeleken met ovariumablatie bij premenopauzale patiënten met gemetastaseerde borstkanker.
Borstkanker bij mannen
NOLVADEX (tamoxifencitraat) wordt goed verdragen door mannen met borstkanker. Rapporten uit de literatuur en casusrapporten suggereren dat het veiligheidsprofiel van NOLVADEX (tamoxifencitraat) bij mannen vergelijkbaar is met dat bij vrouwen. Verlies van libido en impotentie hebben geleid tot stopzetting van de behandeling met tamoxifen bij mannelijke patiënten. Ook bij oligospermische mannen die met tamoxifen werden behandeld, waren de LH-, FSH-, testosteron- en oestrogeenspiegels verhoogd. Er werden geen significante klinische veranderingen gemeld.
Adjuvante borstkanker
In de NSABP B-14-studie werden vrouwen met okselklier-negatieve borstkanker gerandomiseerd naar 5 jaar NOLVADEX (tamoxifencitraat) 20 mg / dag of placebo na primaire chirurgie. De gemelde bijwerkingen zijn hieronder weergegeven (gemiddelde follow-up van ongeveer 6,8 jaar) en laten bijwerkingen zien die vaker voorkomen bij NOLVADEX (tamoxifencitraat) dan bij placebo. De incidentie van opvliegers (64% versus 48%), vaginale afscheiding (30% versus 15%) en onregelmatige menstruatie (25% versus 19%) was hoger met NOLVADEX (tamoxifencitraat) in vergelijking met placebo. Alle andere bijwerkingen traden met vergelijkbare frequentie op in de 2 behandelingsgroepen, met uitzondering van trombotische voorvallen; een hogere incidentie werd gezien bij met NOLVADEX (tamoxifencitraat) behandelde patiënten (tot en met 5 jaar, 1,7% vs. 0,4%). Twee van de patiënten die met NOLVADEX (tamoxifencitraat) werden behandeld en trombotische voorvallen hadden, stierven.
In de Eastern Cooperative Oncology Group (ECOG) adjuvante borstkankerstudie werd NOLVADEX (tamoxifencitraat) of placebo gedurende 2 jaar toegediend aan vrouwen na borstamputatie. In vergelijking met placebo vertoonde NOLVADEX (tamoxifencitraat) een significant hogere incidentie van opvliegers (19% versus 8% voor placebo). De incidentie van alle andere bijwerkingen was vergelijkbaar in de 2 behandelingsgroepen, met uitzondering van trombocytopenie, waar de incidentie voor NOLVADEX (tamoxifencitraat) 10% was versus 3% voor placebo, een observatie van statistische significantie op de grens.
In andere adjuvante onderzoeken, Toronto en NOLVADEX (tamoxifencitraat) Adjuvant Trial Organization (NAVO), kregen vrouwen NOLVADEX (tamoxifencitraat) of geen therapie. In de Toronto-studie werden opvliegers waargenomen bij 29% van de patiënten voor NOLVADEX (tamoxifencitraat) versus 1% in de onbehandelde groep. In het NAVO-onderzoek werden opvliegers en vaginale bloedingen gemeld bij respectievelijk 2,8% en 2,0% van de vrouwen voor NOLVADEX (tamoxifencitraat) versus 0,2% voor elk in de onbehandelde groep.
Anastrozol Adjuvant Trial - Studie van anastrozol vergeleken met NOLVADEX (tamoxifencitraat) voor adjuvante behandeling van vroege borstkanker (zien KLINISCHE FARMACOLOGIE - Klinische studies).
Bij een mediane follow-up van 33 maanden vertoonde de combinatie van anastrozol en NOLVADEX (tamoxifencitraat) geen enkel werkzaamheidsvoordeel in vergelijking met de behandeling met NOLVADEX (tamoxifencitraat) alleen gegeven bij alle patiënten en bij de hormoonreceptorpositieve subpopulatie. Deze behandelarm werd uit de studie gehaald. De mediane duur van adjuvante behandeling voor veiligheidsevaluatie was 59,8 maanden en 59,6 maanden voor patiënten die respectievelijk anastrozol 1 mg en NOLVADEX (tamoxifencitraat) 20 mg kregen.
Bijwerkingen die optreden met een incidentie van ten minste 5% in beide behandelingsgroepen tijdens de behandeling of binnen 14 dagen na het einde van de behandeling worden weergegeven in de volgende tabel.
Bijwerkingen die optreden met een incidentie van ten minste 5% in beide behandelingsgroepen tijdens de behandeling of binnen 14 dagen na het einde van de behandeling
Bepaalde bijwerkingen en combinaties van bijwerkingen werden prospectief gespecificeerd voor analyse, op basis van de bekende farmacologische eigenschappen en bijwerkingenprofielen van de twee geneesmiddelen (zie de volgende tabel).
Aantal (%) patiënten met een vooraf gespecificeerde bijwerking in de anastrozol-adjuvante studie1
Patiënten die anastrozol kregen, hadden een toename van gewrichtsaandoeningen (waaronder artritis, artrose en artralgie) in vergelijking met patiënten die NOLVADEX (tamoxifencitraat) kregen. Patiënten die anastrozol kregen, hadden een toename in de incidentie van alle fracturen (met name fracturen van wervelkolom, heup en pols) [315 (10%)] in vergelijking met patiënten die NOLVADEX (tamoxifencitraat) [209 (7%)] kregen. Patiënten die anastrozol kregen, hadden een afname van opvliegers, vaginale bloedingen, vaginale afscheiding, endometriumkanker, veneuze trombo-embolische voorvallen en ischemische cerebrovasculaire voorvallen in vergelijking met patiënten die NOLVADEX (tamoxifencitraat) kregen.
Patiënten die NOLVADEX (tamoxifencitraat) kregen, hadden een afname van hypercholesterolemie (108 [3,5%]) vergeleken met patiënten die anastrozol kregen (278 [9%]). Angina pectoris werd gemeld bij 71 [2,3%] patiënten in de anastrozol-arm en 51 [1,6%] patiënten in de NOLVADEX (tamoxifencitraat)-arm; myocardinfarct werd gemeld bij 37 [1,2%] patiënten in de anastrozol-arm en bij 34 [1,1%] patiënten in de NOLVADEX (tamoxifencitraat)-arm.
Resultaten van de adjuvante botsubstudie, na 12 en 24 maanden, toonden aan dat patiënten die anastrozol kregen, een gemiddelde afname hadden in zowel de lumbale wervelkolom als de totale botmineraaldichtheid (BMD) van de heup in vergelijking met baseline. Patiënten die NOLVADEX (tamoxifencitraat) kregen, hadden een gemiddelde toename van zowel de lumbale wervelkolom als de totale heup-BMD in vergelijking met baseline.
Ductaal carcinoom in situ (DCIS)
Het type en de frequentie van bijwerkingen in de NSABP B-24-studie waren consistent met die waargenomen in de andere adjuvante onderzoeken die werden uitgevoerd met NOLVADEX (tamoxifencitraat).
Vermindering van de incidentie van borstkanker bij vrouwen met een hoog risico
In het NSABP P-1-onderzoek was er een toename van vijf ernstige bijwerkingen in de NOLVADEX-groep (tamoxifencitraat): endometriumkanker (33 gevallen in de NOLVADEX-groep (tamoxifencitraat) versus 14 in de placebogroep); longembolie (18 gevallen in de groep NOLVADEX (tamoxifencitraat) versus 6 in de placebogroep); diepe veneuze trombose (30 gevallen in de NOLVADEX-groep (tamoxifencitraat) versus 19 in de placebogroep); beroerte (34 gevallen in de groep NOLVADEX (tamoxifencitraat) versus 24 in de placebogroep); cataractvorming (540 gevallen in de NOLVADEX (tamoxifencitraat) groep vs. 483 in de placebogroep) en cataractchirurgie (101 gevallen in de NOLVADEX (tamoxifen citraat) groep vs. 63 in de placebogroep) (zie WAARSCHUWINGEN en Tabel 3 in KLINISCHE FARMACOLOGIE ).
De volgende tabel geeft de bijwerkingen weer die zijn waargenomen bij NSABP P-1 per behandelarm. Alleen bijwerkingen die vaker voorkomen bij NOLVADEX (tamoxifencitraat) dan bij placebo worden getoond.
In de NSABP P-1-studie trok 15,0% en 9,7% van de deelnemers die respectievelijk NOLVADEX (tamoxifencitraat) en placebo kregen, zich om medische redenen terug uit de studie. Hieronder volgen de medische redenen om te stoppen met respectievelijk NOLVADEX (tamoxifencitraat) en placebotherapie: opvliegers (3,1% vs. 1,5%) en vaginale afscheiding (0,5% vs. 0,1%).
In de NSABP P-1-studie trok 8,7% en 9,6% van de deelnemers die respectievelijk NOLVADEX (tamoxifencitraat) en placebo kregen, zich terug om niet-medische redenen.
In de NSABP P-1-studie kwamen opvliegers van elke ernst voor bij 68% van de vrouwen op placebo en bij 80% van de vrouwen op NOLVADEX (tamoxifencitraat). Ernstige opvliegers traden op bij 28% van de vrouwen op placebo en 45% van de vrouwen op NOLVADEX (tamoxifencitraat). Vaginale afscheiding trad op bij respectievelijk 35% en 55% van de vrouwen die placebo en NOLVADEX (tamoxifencitraat) kregen; en was ernstig in respectievelijk 4,5% en 12,3%. Er was geen verschil in de incidentie van vaginale bloedingen tussen de behandelarmen.
Pediatrische patiënten - McCune-Albright-syndroom
Het gemiddelde baarmoedervolume nam toe na 6 maanden behandeling en verdubbelde aan het einde van de eenjarige studie. Er is geen causaal verband vastgesteld; er is echter een toename van de incidentie van endometriumadenocarcinoom en baarmoedersarcoom waargenomen bij volwassenen die met NOLVADEX werden behandeld (zie GEVAARLIJKE WAARSCHUWING: ), wordt aanbevolen om McCune-Albright-patiënten die met NOLVADEX (tamoxifencitraat) worden behandeld te blijven controleren op langetermijneffecten. De veiligheid en werkzaamheid van NOLVADEX (tamoxifencitraat) voor meisjes van twee tot tien jaar met het McCune-Albright-syndroom en vroegtijdige puberteit zijn niet onderzocht na een behandeling van meer dan één jaar. De langetermijneffecten van behandeling met NOLVADEX (tamoxifencitraat) bij meisjes zijn niet vastgesteld.
Postmarketing ervaring
Minder vaak gemelde bijwerkingen zijn vaginale bloedingen, vaginale afscheiding, onregelmatige menstruatie, huiduitslag en hoofdpijn. Gewoonlijk waren deze niet van voldoende ernst om dosisverlaging of stopzetting van de behandeling te vereisen. Zeer zeldzame meldingen van erythema multiforme, Stevens-Johnson-syndroom, bulleus pemfigoïd, interstitiële pneumonitis en zeldzame meldingen van overgevoeligheidsreacties, waaronder angio-oedeem, zijn gemeld bij behandeling met NOLVADEX (tamoxifencitraat). In sommige van deze gevallen was de aanvangstijd meer dan een jaar. Zelden kan een verhoging van de serumtriglyceridenspiegels, in sommige gevallen met pancreatitis, in verband worden gebracht met het gebruik van NOLVADEX (tamoxifencitraat) (zie VOORZORGSMAATREGELEN- Geneesmiddel-/laboratoriumtestinteracties sectie).
DRUG-INTERACTIES
Wanneer NOLVADEX (tamoxifencitraat) wordt gebruikt in combinatie met anticoagulantia van het cumarine-type, kan een significante toename van het anticoagulerende effect optreden. Wanneer een dergelijke gelijktijdige toediening bestaat, wordt zorgvuldige controle van de protrombinetijd van de patiënt aanbevolen.
In het NSABP P-1-onderzoek kwamen vrouwen die om welke reden dan ook anticoagulantia van het cumarine-type nodig hadden niet in aanmerking voor deelname aan het onderzoek (zie CONTRA-INDICATIES ).
Er is een verhoogd risico op trombo-embolische voorvallen wanneer cytotoxische middelen worden gebruikt in combinatie met NOLVADEX (tamoxifencitraat).
Tamoxifen verlaagde de plasmaconcentraties van letrozol met 37%. Het effect van tamoxifen op het metabolisme en de uitscheiding van andere antineoplastische geneesmiddelen, zoals cyclofosfamide en andere geneesmiddelen die oxidasen met gemengde functie nodig hebben voor activering, is niet bekend. Het is aangetoond dat de plasmaconcentraties van tamoxifen en N-desmethyltamoxifen worden verlaagd bij gelijktijdige toediening met rifampicine of aminoglutethimide. Inductie van CYP3A4-gemedieerd metabolisme wordt beschouwd als het mechanisme waardoor deze verlagingen plaatsvinden; andere CYP3A4-inducerende middelen zijn niet onderzocht om dit effect te bevestigen.
Eén patiënt die NOLVADEX (tamoxifencitraat) met gelijktijdig fenobarbital kreeg, vertoonde een steady-state serumspiegel van tamoxifen die lager was dan die waargenomen bij andere patiënten (dwz 26 ng/ml versus gemiddelde waarde van 122 ng/ml). De klinische betekenis van deze bevinding is echter niet bekend. Rifampicine induceerde het metabolisme van tamoxifen en verminderde significant de plasmaconcentraties van tamoxifen bij 10 patiënten. Aminoglutethimide verlaagt de plasmaconcentraties van tamoxifen en N-desmethyltamoxifen. Medroxyprogesteron verlaagt de plasmaconcentraties van N-desmethyl, maar niet van tamoxifen.
Het is aangetoond dat gelijktijdige behandeling met bromocriptine het serumtamoxifen en N-desmethyltamoxifen verhoogt.
Op basis van klinische en farmacokinetische resultaten van het onderzoek met anastrozol-adjuvans, mag NOLVADEX (tamoxifencitraat) niet worden toegediend met anastrozol (zie KLINISCHE FARMACOLOGIE - Geneesmiddel-geneesmiddelinteracties sectie).
Geneesmiddel-/laboratoriumtestinteracties
Tijdens postmarketingsurveillance werden bij enkele postmenopauzale patiënten T4-verhogingen gemeld, wat kan worden verklaard door verhogingen van schildklierbindend globuline. Deze verhogingen gingen niet gepaard met klinische hyperthyreoïdie.
Variaties in de karyopyknotische index op vaginale uitstrijkjes en verschillende graden van oestrogeeneffect op uitstrijkjes zijn zelden gezien bij postmenopauzale patiënten die NOLVADEX (tamoxifencitraat) kregen.
In de postmarketingervaring met NOLVADEX (tamoxifencitraat) zijn zeldzame gevallen van hyperlipidemieën gemeld. Periodieke controle van plasmatriglyceriden en cholesterol kan geïndiceerd zijn bij patiënten met reeds bestaande hyperlipidemieën (zie BIJWERKINGEN - Postmarketingervaring sectie).
WAARSCHUWINGEN
Effecten bij patiënten met gemetastaseerde borstkanker
Net als bij andere aanvullende hormonale therapie (oestrogenen en androgenen), is hypercalciëmie gemeld bij sommige borstkankerpatiënten met botmetastasen binnen enkele weken na aanvang van de behandeling met NOLVADEX (tamoxifencitraat). Als hypercalciëmie optreedt, moeten passende maatregelen worden genomen en, indien ernstig, moet NOLVADEX (tamoxifencitraat) worden stopgezet.
Effecten op baarmoeder-endometriumkanker en baarmoedersarcoom
Een verhoogde incidentie van baarmoedermaligniteiten is gemeld in verband met behandeling met NOLVADEX (tamoxifencitraat). Het onderliggende mechanisme is onbekend, maar kan verband houden met het oestrogeenachtige effect van NOLVADEX (tamoxifencitraat). De meeste baarmoedermaligniteiten die worden gezien in verband met NOLVADEX (tamoxifencitraat) worden geclassificeerd als adenocarcinoom van het endometrium. Er zijn echter ook zeldzame baarmoedersarcomen gemeld, waaronder maligne gemengde mulleriaanse tumoren (MMMT). Baarmoedersarcoom wordt over het algemeen geassocieerd met een hoger FIGO-stadium (III/IV) bij diagnose, een slechtere prognose en een kortere overleving. Van baarmoedersarcoom is gemeld dat het vaker voorkomt bij langdurige gebruikers (≥ 2 jaar) van NOLVADEX (tamoxifencitraat) dan bij niet-gebruikers. Sommige baarmoedermaligniteiten (endometriumcarcinoom of baarmoedersarcoom) waren fataal.
In de NSABP P-1-studie was er onder deelnemers die waren gerandomiseerd naar NOLVADEX (tamoxifencitraat) een statistisch significante toename van de incidentie van endometriumkanker (33 gevallen van invasieve endometriumkanker, vergeleken met 14 gevallen onder deelnemers die waren gerandomiseerd naar placebo (RR=2,48). , 95% BI: 1,27-4,92. De 33 gevallen bij deelnemers die NOLVADEX (tamoxifencitraat) kregen waren FIGO Stadium I, inclusief 20 IA, 12 IB en 1 IC endometriumadenocarcinomen. Bij deelnemers gerandomiseerd naar placebo, waren 13 FIGO Stadium I (8 IA en 5 IB) en 1 was FIGO stadium IV. Vijf vrouwen op NOLVADEX (tamoxifencitraat) en 1 op placebo kregen naast chirurgie ook postoperatieve radiotherapie. Deze toename werd voornamelijk waargenomen bij vrouwen van ten minste 50 jaar tijdstip van randomisatie (26 gevallen van invasieve endometriumkanker, vergeleken met 6 gevallen onder deelnemers gerandomiseerd naar placebo (RR=4,50, 95% BI: 1,78-13,16). Onder vrouwen ≤ 49 jaar oud op het moment van randomisatie waren er 7 gevallen van i vasieve endometriumkanker, vergeleken met 8 gevallen onder deelnemers gerandomiseerd naar placebo (RR=0.94, 95% CI: 0.28-2.89). Als rekening wordt gehouden met de leeftijd op het moment van diagnose, waren er 4 gevallen van endometriumkanker onder deelnemers ≤ 49 gerandomiseerd naar NOLVADEX (tamoxifencitraat) vergeleken met 2 onder deelnemers die waren gerandomiseerd naar placebo (RR=2,21, 95% BI: 0,4-12,0). Voor vrouwen ≥ 50 op het moment van diagnose waren er 29 gevallen onder deelnemers die waren gerandomiseerd naar NOLVADEX (tamoxifencitraat) vergeleken met 12 onder vrouwen op placebo (RR=2,5, 95% BI: 1,3-4,9). De risicoverhoudingen waren vergelijkbaar in de twee groepen, hoewel er minder voorvallen optraden bij jongere vrouwen. De meeste (29 van de 33 gevallen in de NOLVADEX-groep (tamoxifencitraat)) endometriumkankers werden gediagnosticeerd bij symptomatische vrouwen, hoewel 5 van de 33 gevallen in de NOLVADEX-groep (tamoxifencitraat) optraden bij asymptomatische vrouwen. Bij vrouwen die NOLVADEX (tamoxifencitraat) kregen, verschenen de voorvallen tussen 1 en 61 maanden (gemiddeld = 32 maanden) vanaf het begin van de behandeling.
In een bijgewerkt overzicht van langetermijngegevens (mediane duur van de totale follow-up is 6,9 jaar, inclusief geblindeerde follow-up) van 8.306 vrouwen met een intacte baarmoeder bij randomisatie in het NSABP P-1-onderzoek naar risicovermindering, bleek de incidentie van beide adenocarcinomen en zeldzame baarmoedersarcomen waren verhoogd bij vrouwen die NOLVADEX (tamoxifencitraat) gebruikten. Tijdens geblindeerde follow-up waren er 36 gevallen van FIGO Stadium I endometrium adenocarcinoom (22 waren FIGO Stadium IA, 13 IB en 1 IC) bij vrouwen die NOLVADEX (tamoxifencitraat) kregen en 15 gevallen bij vrouwen die placebo kregen [14 waren FIGO Stadium I (9 IA en 5 IB), en 1 geval was FIGO Stadium IV]. Van de patiënten die NOLVADEX (tamoxifencitraat) kregen en endometriumkanker ontwikkelden, kregen één met stadium IA en 4 met stadium IB-kankers bestralingstherapie. In de placebogroep kreeg één patiënt met FIGO Stadium 1B-kanker radiotherapie en de patiënt met FIGO Stadium IVB-kanker chemotherapie en hormonale therapie. Tijdens de totale follow-up werd endometrium adenocarcinoom gemeld bij 53 vrouwen gerandomiseerd naar NOLVADEX (tamoxifencitraat) (30 gevallen van FIGO stadium IA, 20 waren stadium IB, 1 was stadium IC en 2 waren stadium IIIC), en 17 vrouwen waren gerandomiseerd naar placebo (9 gevallen waren FIGO stadium IA, 6 waren stadium IB, 1 was stadium IIIC en 1 was stadium IVB) (incidentie per 1.000 vrouwjaren van respectievelijk 2,20 en 0,71). Sommige patiënten kregen naast een operatie ook postoperatieve radiotherapie. Baarmoedersarcomen werden gemeld bij 4 vrouwen gerandomiseerd naar NOLVADEX (tamoxifencitraat) (1 was FIGO IA, 1 was FIGO IB, 1 was FIGO IIA en 1 was FIGO IIIC) en één patiënt was gerandomiseerd naar placebo (FIGO 1A); incidentie per 1.000 vrouwjaren van respectievelijk 0,17 en 0,04. Van de patiënten gerandomiseerd naar NOLVADEX (tamoxifencitraat), waren de FIGO IA- en IB-gevallen respectievelijk een MMMT en sarcoom; de FIGO II was een MMMT; en de FIGO III was een sarcoom; en de ene patiënt gerandomiseerd naar placebo had een MMMT. Een vergelijkbare verhoogde incidentie van endometrium adenocarcinoom en baarmoedersarcoom werd waargenomen bij vrouwen die NOLVADEX (tamoxifencitraat) kregen in vijf andere NSABP-klinische onderzoeken.
Elke patiënt die NOLVADEX (tamoxifencitraat) krijgt of eerder heeft gekregen en die abnormale vaginale bloedingen meldt, moet onmiddellijk worden geëvalueerd. Patiënten die NOLVADEX (tamoxifencitraat) krijgen of eerder hebben gekregen, moeten jaarlijks gynaecologisch onderzoek ondergaan en moeten hun arts onmiddellijk informeren als ze abnormale gynaecologische symptomen ervaren, bijv. onregelmatige menstruatie, abnormale vaginale bloedingen, veranderingen in vaginale afscheiding of bekkenpijn of druk.
In de P-1-studie veranderde endometriumbemonstering het detectiepercentage van endometriumkanker niet in vergelijking met vrouwen die geen endometriumbemonstering hadden ondergaan (0,6% met bemonstering, 0,5% zonder bemonstering) voor vrouwen met een intacte baarmoeder. Er zijn geen gegevens die erop wijzen dat routinematige endometriumbemonstering bij asymptomatische vrouwen die NOLVADEX (tamoxifencitraat) gebruiken om de incidentie van borstkanker te verminderen gunstig zou zijn.
Niet-kwaadaardige effecten op de baarmoeder
Een verhoogde incidentie van endometriale veranderingen, waaronder hyperplasie en poliepen, is gemeld in verband met behandeling met NOLVADEX (tamoxifencitraat). De incidentie en het patroon van deze toename suggereren dat het onderliggende mechanisme gerelateerd is aan de oestrogene eigenschappen van NOLVADEX (tamoxifencitraat).
Er zijn enkele meldingen geweest van endometriose en baarmoederfibromen bij vrouwen die NOLVADEX (tamoxifencitraat) kregen. Het onderliggende mechanisme kan te wijten zijn aan het gedeeltelijke oestrogene effect van NOLVADEX (tamoxifencitraat). Eierstokcysten zijn ook waargenomen bij een klein aantal premenopauzale patiënten met gevorderde borstkanker die werden behandeld met NOLVADEX (tamoxifencitraat).
Van NOLVADEX (tamoxifencitraat) is gemeld dat het onregelmatige menstruatie of amenorroe veroorzaakt.
Trombo-embolische effecten van NOLVADEX (tamoxifencitraat)
Er zijn aanwijzingen voor een verhoogde incidentie van trombo-embolische voorvallen, waaronder diepe veneuze trombose en longembolie, tijdens behandeling met NOLVADEX (tamoxifencitraat). Wanneer NOLVADEX (tamoxifencitraat) samen met chemotherapie wordt toegediend, kan de incidentie van trombo-embolische effecten verder toenemen. Voor de behandeling van borstkanker moeten de risico's en voordelen van NOLVADEX (tamoxifencitraat) zorgvuldig worden afgewogen bij vrouwen met een voorgeschiedenis van trombo-embolische voorvallen. In een kleine substudie (N=81) van de NSABP P-1-studie leek het geen voordeel te hebben om vrouwen te screenen op Factor V Leiden- en Protrombine-mutaties G20210A als middel om diegenen te identificeren die mogelijk geen geschikte kandidaten zijn voor NOLVADEX (tamoxifen citraat) therapie.
Gegevens uit de NSABP P-1-studie laten zien dat deelnemers die NOLVADEX (tamoxifencitraat) kregen zonder een voorgeschiedenis van longembolie (PE) een statistisch significante toename van longembolie hadden (18-NOLVADEX (tamoxifencitraat), 6-placebo, RR = 3,01 , 95%-BI: 1,15-9,27). Drie van de longembolie, alle in de NOLVADEX (tamoxifencitraat) arm, waren fataal. Zevenentachtig procent van de gevallen van longembolie deed zich bij randomisatie voor bij vrouwen van ten minste 50 jaar oud. Bij vrouwen die NOLVADEX (tamoxifencitraat) kregen, verschenen de voorvallen tussen 2 en 60 maanden (gemiddeld = 27 maanden) vanaf het begin van de behandeling.
In dezelfde populatie werd een niet-statistisch significante toename van diepe veneuze trombose (DVT) gezien in de NOLVADEX (tamoxifencitraat)-groep (30-NOLVADEX (tamoxifencitraat), 19-placebo; RR=1,59, 95% BI: 0,86 -2,98). Dezelfde toename van het relatieve risico werd gezien bij vrouwen 49 en bij vrouwen ≥ 50, hoewel er minder voorvallen optraden bij jongere vrouwen. Vrouwen met trombo-embolische voorvallen liepen risico op een tweede gerelateerd voorval (7 van de 25 vrouwen op placebo, 5 van de 48 vrouwen op NOLVADEX (tamoxifencitraat)) en liepen risico op complicaties van het voorval en de behandeling ervan (0/25 op placebo, 4/48 op NOLVADEX (tamoxifencitraat)). Bij vrouwen die NOLVADEX (tamoxifencitraat) kregen, traden diepe veneuze trombose-gebeurtenissen op tussen 2 en 57 maanden (gemiddeld = 19 maanden) vanaf het begin van de behandeling.
Er was een niet-statistisch significante toename van beroerte bij patiënten die waren gerandomiseerd naar NOLVADEX (tamoxifencitraat) (24-Placebo; 34-NOLVADEX (tamoxifencitraat); RR=1,42; 95% BI 0,82-2,51). Zes van de 24 beroertes in de placebogroep werden als hemorragisch beschouwd en 10 van de 34 beroertes in de NOLVADEX (tamoxifencitraat) groep werden gecategoriseerd als hemorragisch. Zeventien van de 34 beroertes in de groep NOLVADEX (tamoxifencitraat) werden als occlusief beschouwd en 7 werden als van onbekende etiologie beschouwd. Van 14 van de 24 beroertes in de placebo-arm werd gemeld dat ze occlusief waren en 4 van onbekende etiologie. Van deze beroertes waren 3 beroertes in de placebogroep en 4 beroertes in de NOLVADEX (tamoxifencitraat) groep fataal. Achtentachtig procent van de beroertes deed zich voor bij vrouwen die ten minste 50 jaar oud waren op het moment van randomisatie. Bij vrouwen die NOLVADEX (tamoxifencitraat) kregen, traden de voorvallen op tussen 1 en 63 maanden (gemiddeld = 30 maanden) vanaf het begin van de behandeling.
Effecten op de lever: Leverkanker
In het Zweedse onderzoek met adjuvans NOLVADEX (tamoxifencitraat) 40 mg/dag gedurende 2-5 jaar, zijn 3 gevallen van leverkanker gemeld in de met NOLVADEX (tamoxifencitraat) behandelde groep versus 1 geval in de observatiegroep (zie VOORZORGSMAATREGELEN- Carcinogenese ). In andere klinische onderzoeken naar NOLVADEX (tamoxifencitraat) zijn tot op heden geen gevallen van leverkanker gemeld.
Eén geval van leverkanker werd gemeld in NSABP P-1 bij een deelnemer die was gerandomiseerd naar NOLVADEX (tamoxifencitraat).
Effecten op de lever: niet-kwaadaardige effecten
NOLVADEX (tamoxifencitraat) is in verband gebracht met veranderingen in leverenzymspiegels en in zeldzame gevallen met een spectrum van ernstigere leverafwijkingen, waaronder leververvetting, cholestase, hepatitis en levernecrose. Enkele van deze ernstige gevallen waren dodelijke slachtoffers. In de meeste gemelde gevallen is de relatie met NOLVADEX (tamoxifencitraat) onzeker. Er zijn echter enkele positieve heruitdagingen en dechallenges gemeld.
In de NSABP P-1-studie werden enkele graad 3-4 veranderingen in de leverfunctie (SGOT, SGPT, bilirubine, alkalische fosfatase) waargenomen (10 op placebo en 6 op NOLVADEX (tamoxifencitraat)). Serumlipiden werden niet systematisch verzameld.
andere kankers
Een aantal tweede primaire tumoren, die voorkomen op andere plaatsen dan het endometrium, zijn gemeld na de behandeling van borstkanker met NOLVADEX (tamoxifencitraat) in klinische onderzoeken. Gegevens uit de NSABP B-14- en P-1-onderzoeken laten geen toename zien van andere (niet-baarmoederlijke) kankers bij patiënten die NOLVADEX (tamoxifencitraat) kregen. Of een verhoogd risico op andere (niet-baarmoederlijke) kankers geassocieerd is met NOLVADEX (tamoxifencitraat) is nog steeds onzeker en wordt nog steeds geëvalueerd.
Effecten op het oog
Bij patiënten die NOLVADEX (tamoxifencitraat) kregen, zijn oogstoornissen gemeld, waaronder veranderingen in het hoornvlies, afname van de perceptie van kleuren, trombose van de retinale ader en retinopathie. Een verhoogde incidentie van cataract en de noodzaak van cataractchirurgie is gemeld bij patiënten die NOLVADEX (tamoxifencitraat) kregen.
In de NSABP P-1-studie was een verhoogd risico op borderline significantie van het ontwikkelen van cataract bij die vrouwen zonder cataract bij baseline (540-NOLVADEX (tamoxifencitraat); 483-placebo; RR=1,13, 95% BI: 1,00-1,28). opgemerkt. Bij deze zelfde vrouwen werd NOLVADEX (tamoxifencitraat) geassocieerd met een verhoogd risico op cataractchirurgie (101-NOLVADEX (tamoxifencitraat); 63-placebo; RR=1,62, 95% BI 1,18-2,22) (zie tabel 3 in KLINISCHE FARMACOLOGIE ). Van alle vrouwen in de studie (met of zonder cataract bij aanvang), werd NOLVADEX (tamoxifencitraat) geassocieerd met een verhoogd risico op een cataractoperatie (201-NOLVADEX (tamoxifencitraat); 129-placebo; RR=1,58, 95% BI 1,26-1,97). Oogonderzoek was tijdens het onderzoek niet nodig. Er kunnen geen andere conclusies worden getrokken met betrekking tot niet-cataracte oftalmische voorvallen.
Zwangerschap Categorie D
NOLVADEX (tamoxifencitraat) kan schade aan de foetus veroorzaken bij toediening aan een zwangere vrouw. Vrouwen moeten worden geadviseerd niet zwanger te worden tijdens het gebruik van NOLVADEX (tamoxifencitraat) of binnen 2 maanden na het stoppen met NOLVADEX (tamoxifencitraat) en moeten barrière- of niet-hormonale anticonceptiemaatregelen nemen als ze seksueel actief zijn. Tamoxifen veroorzaakt geen onvruchtbaarheid, zelfs niet bij een onregelmatige menstruatie. Effecten op de voortplantingsfuncties worden verwacht van de anti-oestrogene eigenschappen van het geneesmiddel. In reproductieonderzoeken bij ratten bij dosisniveaus gelijk aan of lager dan de dosis voor de mens, werden niet-teratogene skeletveranderingen in de ontwikkeling gezien en deze werden reversibel gevonden. Bovendien werd in vruchtbaarheidsonderzoeken bij ratten en in teratologieonderzoeken bij konijnen met doses die gelijk of lager waren dan die gebruikt bij mensen, een lagere incidentie van embryo-implantatie en een hogere incidentie van foetale sterfte of vertraagde utero-groei waargenomen, met langzamer leergedrag bij sommige rattenpups in vergelijking met historische controles. Verschillende zwangere zijdeaapjes kregen tijdens de organogenese of in de laatste helft van de zwangerschap een dosis van 10 mg/kg/dag (ongeveer het dubbele van de maximaal aanbevolen dagelijkse dosis voor de mens op basis van mg/m²). Er werden geen vervormingen gezien en hoewel de dosis hoog genoeg was om de zwangerschap bij sommige dieren te beëindigen, vertoonden degenen die de zwangerschap in stand hielden geen bewijs van teratogene misvormingen.
In knaagdiermodellen voor de ontwikkeling van het voortplantingsstelsel van de foetus veroorzaakte tamoxifen (in doses van 0,002 tot 2,4 maal de dagelijkse maximale aanbevolen dosis voor de mens op basis van mg/m²) veranderingen bij beide geslachten die vergelijkbaar zijn met die veroorzaakt door estradiol, ethynylestradiol en diethylstilbestrol. Hoewel de klinische relevantie van deze veranderingen niet bekend is, zijn sommige van deze veranderingen, met name vaginale adenose, vergelijkbaar met de veranderingen die werden gezien bij jonge vrouwen die in utero werden blootgesteld aan diethylstilbestrol en die een risico van 1 op 1000 hebben op het ontwikkelen van clear-cell adenocarcinoom van de vagina of baarmoederhals. Tot op heden is bij jonge vrouwen niet aangetoond dat blootstelling aan tamoxifen in utero vaginale adenose of clear-cell adenocarcinoom van de vagina of de baarmoederhals veroorzaakt. Slechts een klein aantal jonge vrouwen is echter in utero blootgesteld aan tamoxifen en een kleiner aantal is lang genoeg gevolgd (tot 15-20 jaar) om te bepalen of vaginale of cervicale neoplasie zou kunnen optreden als gevolg van deze blootstelling.
Er zijn geen adequate en goed gecontroleerde onderzoeken naar tamoxifen bij zwangere vrouwen. Er is een klein aantal meldingen geweest van vaginale bloedingen, spontane abortussen, geboorteafwijkingen en foetale sterfte bij zwangere vrouwen. Als dit geneesmiddel tijdens de zwangerschap wordt gebruikt, of als de patiënte zwanger wordt tijdens het gebruik van dit geneesmiddel, of binnen ongeveer twee maanden na het staken van de behandeling, moet de patiënt op de hoogte worden gesteld van de mogelijke risico's voor de foetus, waaronder het mogelijke langetermijnrisico van een DES- zoals syndroom.
Vermindering van de incidentie van borstkanker bij vrouwen met een hoog risico - Zwangerschapscategorie D
Voor seksueel actieve vrouwen in de vruchtbare leeftijd moet de behandeling met NOLVADEX (tamoxifencitraat) worden gestart tijdens de menstruatie. Bij vrouwen met een onregelmatige menstruatie is een negatieve B-HCG direct voor aanvang van de therapie voldoende (zie VOORZORGSMAATREGELEN-INFORMATIE VOOR PATINTEN - Vermindering van de incidentie van borstkanker bij vrouwen met een hoog risico ).
PREVENTIEVE MAATREGELEN
Algemeen
Verlaging van het aantal bloedplaatjes, meestal tot 50.000-100.000 / mm³, soms lager, is af en toe gemeld bij patiënten die NOLVADEX (tamoxifencitraat) gebruikten voor borstkanker. Bij patiënten met significante trombocytopenie zijn zeldzame hemorragische episodes opgetreden, maar het is niet zeker of deze episodes te wijten zijn aan behandeling met NOLVADEX (tamoxifencitraat). Leukopenie is waargenomen, soms in combinatie met anemie en/of trombocytopenie. Er zijn zeldzame meldingen geweest van neutropenie en pancytopenie bij patiënten die NOLVADEX (tamoxifencitraat) kregen; dit kan soms ernstig zijn.
In de NSABP P-1-studie ondervonden 6 vrouwen op NOLVADEX (tamoxifencitraat) en 2 op placebo een graad 3-4 daling van het aantal bloedplaatjes (≤ 50.000/mm³).
Informatie voor patiënten
Patiënten moeten worden geïnstrueerd om de Medicatiegids geleverd zoals wettelijk vereist wanneer NOLVADEX 10 mg wordt verstrekt. De volledige tekst van de Medicatiegids wordt herdrukt aan het einde van dit document.
Vermindering van invasieve borstkanker en DCIS bij vrouwen met DCIS
Vrouwen met DCIS die worden behandeld met lumpectomie en bestralingstherapie die NOLVADEX (tamoxifencitraat) overwegen om de incidentie van een tweede borstkankergebeurtenis te verminderen, moeten de risico's en voordelen van de therapie beoordelen, aangezien behandeling met NOLVADEX (tamoxifencitraat) de incidentie van invasieve borstkanker verminderde. kanker, maar het is niet aangetoond dat het de overleving beïnvloedt (zie tabel 1 in: KLINISCHE FARMACOLOGIE ).
Vermindering van de incidentie van borstkanker bij vrouwen met een hoog risico
Vrouwen met een hoog risico op borstkanker kunnen overwegen om NOLVADEX (tamoxifencitraat) te gebruiken om de incidentie van borstkanker te verminderen. Of de voordelen van de behandeling opwegen tegen de risico's, hangt af van de persoonlijke gezondheidsgeschiedenis van een vrouw en van hoe zij de voordelen en risico's afweegt. Behandeling met NOLVADEX (tamoxifencitraat) om de incidentie van borstkanker te verminderen, is daarom mogelijk niet geschikt voor alle vrouwen met een hoog risico op borstkanker. Vrouwen die een behandeling met NOLVADEX (tamoxifencitraat) overwegen, moeten hun beroepsbeoefenaar in de gezondheidszorg raadplegen voor een beoordeling van de mogelijke voordelen en risico's voordat ze beginnen met de behandeling voor vermindering van de incidentie van borstkanker (zie tabel 3 in KLINISCHE FARMACOLOGIE ). Vrouwen moeten begrijpen dat NOLVADEX (tamoxifencitraat) de incidentie van borstkanker vermindert, maar het risico mogelijk niet wegneemt. NOLVADEX (tamoxifencitraat) verminderde de incidentie van kleine oestrogeenreceptor-positieve tumoren, maar veranderde de incidentie van oestrogeenreceptor-negatieve tumoren of grotere tumoren niet. Bij vrouwen met borstkanker die een hoog risico lopen op het ontwikkelen van een tweede borstkanker, verminderde behandeling met ongeveer 5 jaar NOLVADEX (tamoxifencitraat) de jaarlijkse incidentie van een tweede borstkanker met ongeveer 50%.
Vrouwen die zwanger zijn of van plan zijn zwanger te worden, mogen NOLVADEX (tamoxifencitraat) niet gebruiken om haar risico op borstkanker te verminderen. Effectieve niet-hormonale anticonceptie moet worden gebruikt door alle premenopauzale vrouwen die NOLVADEX (tamoxifencitraat) gebruiken en gedurende ongeveer twee maanden na het staken van de behandeling als ze seksueel actief zijn. Tamoxifen veroorzaakt geen onvruchtbaarheid, zelfs niet bij een onregelmatige menstruatie. Voor seksueel actieve vrouwen in de vruchtbare leeftijd moet de behandeling met NOLVADEX (tamoxifencitraat) worden gestart tijdens de menstruatie. Bij vrouwen met een onregelmatige menstruatie is een negatieve B-HCG direct voor aanvang van de therapie voldoende (zie WAARSCHUWINGEN-Zwangerschap Categorie D ).
Twee Europese onderzoeken met tamoxifen om het risico op borstkanker te verminderen werden uitgevoerd en lieten geen verschil zien in het aantal gevallen van borstkanker tussen de tamoxifen- en placebo-arm. Deze onderzoeken hadden een proefopzet die verschilde van die van NSABP P-1, die kleiner waren dan die van NSABP P-1 en waarin vrouwen werden opgenomen met een lager risico op borstkanker dan die van P-1.
Monitoring tijdens NOLVADEX (tamoxifencitraat) therapie
Vrouwen die NOLVADEX (tamoxifencitraat) gebruiken of eerder hebben gebruikt, moeten de instructie krijgen om onmiddellijk medische hulp in te roepen voor nieuwe borstknobbels, vaginale bloedingen, gynaecologische symptomen (onregelmatige menstruatie, veranderingen in vaginale afscheiding of bekkenpijn of -druk), symptomen van zwelling van de benen of gevoeligheid, onverklaarbare kortademigheid of veranderingen in het gezichtsvermogen. Vrouwen moeten alle zorgverleners informeren, ongeacht de reden voor evaluatie, dat ze NOLVADEX (tamoxifencitraat) gebruiken.
Vrouwen die NOLVADEX (tamoxifencitraat) gebruiken om de incidentie van borstkanker te verminderen, moeten een borstonderzoek, een mammogram en een gynaecologisch onderzoek ondergaan voordat de behandeling wordt gestart. Deze onderzoeken moeten met regelmatige tussenpozen worden herhaald tijdens de behandeling, in overeenstemming met de goede medische praktijk. Vrouwen die NOLVADEX (tamoxifencitraat) gebruiken als adjuvante behandeling van borstkanker, moeten dezelfde controleprocedures volgen als voor vrouwen die NOLVADEX (tamoxifencitraat) gebruiken om de incidentie van borstkanker te verminderen. Vrouwen die NOLVADEX (tamoxifencitraat) gebruiken als behandeling voor gemetastaseerde borstkanker, moeten dit monitoringplan met hun zorgverlener doornemen en de juiste modaliteiten en het evaluatieschema selecteren.
Laboratorium testen
Periodieke volledige bloedtellingen, inclusief bloedplaatjestellingen, en periodieke leverfunctietesten moeten worden verkregen.
Tijdens de ATAC-studie werd gemeld dat meer patiënten die anastrozol kregen een verhoogd serumcholesterol hadden in vergelijking met patiënten die NOLVADEX (tamoxifencitraat) kregen (respectievelijk 9% versus 3,5%).
Carcinogenese
Een conventioneel onderzoek naar carcinogenese bij ratten in doses van 5, 20 en 35 mg/kg/dag (ongeveer één, drie en zeven keer de dagelijkse maximale aanbevolen dosis voor de mens op basis van mg/m²) toegediend via orale sondevoeding gedurende maximaal 2 jaar ) onthulde een significante toename van hepatocellulair carcinoom bij alle doses. De incidentie van deze tumoren was significant groter bij ratten die 20 of 35 mg/kg/dag (69%) kregen toegediend dan bij ratten die 5 mg/kg/dag kregen (14%). In een afzonderlijk onderzoek kregen ratten 45 mg/kg/dag tamoxifen toegediend (ongeveer negenmaal de maximaal aanbevolen dagelijkse dosis voor de mens op basis van mg/m²); hepatocellulaire neoplasie werd vertoond na 3 tot 6 maanden.
Eierstoktumoren van granulosacellen en testiculaire tumoren van interstitiële cellen werden waargenomen in twee afzonderlijke muisstudies. De muizen kregen gedurende 13 tot 15 maanden de trans- en racemische vormen van tamoxifen toegediend in doses van 5, 20 en 50 mg/kg/dag (ongeveer de helft, twee en vijf keer de dagelijks aanbevolen dosis voor de mens op een mg/m² basis).
Mutagenese
Er werd geen genotoxisch potentieel gevonden in een conventionele reeks in vivo en in vitro tests met pro- en eukaryote testsystemen met geneesmiddelmetaboliserende systemen. Er werden echter verhoogde niveaus van DNA-adducten waargenomen door post-labeling met 32P in DNA van rattenlever en gekweekte menselijke lymfocyten. Van tamoxifen is ook gevonden dat het de niveaus van micronucleusvorming in vitro verhoogt in menselijke lymfoblastoïde cellijn (MCL-5). Op basis van deze bevindingen is tamoxifen genotoxisch in MCL-5-cellen van knaagdieren en mensen.
Aantasting van de vruchtbaarheid
Tamoxifen veroorzaakte een verslechtering van de vruchtbaarheid en conceptie bij vrouwelijke ratten bij doses van 0,04 mg/kg/dag (ongeveer 0,01 maal de maximaal aanbevolen dagelijkse dosis voor de mens op basis van mg/m²) bij toediening gedurende twee weken voorafgaand aan de paring tot en met dag 7 van de dracht . Bij deze dosis waren de vruchtbaarheids- en reproductie-indexen aanzienlijk verminderd met totale foetale mortaliteit. De foetale mortaliteit nam ook toe bij doses van 0,16 mg/kg/dag (ongeveer 0,03-maal de maximaal aanbevolen dagelijkse dosis voor de mens op basis van mg/m²) wanneer vrouwelijke ratten werden gedoseerd vanaf dag 7-17 van de zwangerschap. Tamoxifen veroorzaakte abortus, vroeggeboorte en foetale sterfte bij konijnen die doses kregen die gelijk waren aan of hoger dan 0,125 mg/kg/dag (ongeveer 0,05 maal de maximaal aanbevolen dagelijkse dosis voor de mens op basis van mg/m²). Er waren geen teratogene veranderingen bij ratten of konijnen.
Zwangerschap Categorie D
Zien WAARSCHUWINGEN .
Moeders die borstvoeding geven
Van tamoxifen is gemeld dat het de lactatie remt. Twee placebogecontroleerde onderzoeken bij meer dan 150 vrouwen hebben aangetoond dat tamoxifen de melkproductie vroeg na de bevalling significant remt. In beide onderzoeken werd tamoxifen toegediend binnen 24 uur na de bevalling gedurende 5 tot 18 dagen. Het effect van tamoxifen op de bestaande melkproductie is niet bekend.
Er zijn geen gegevens die aangeven of tamoxifen wordt uitgescheiden in de moedermelk. Indien uitgescheiden, zijn er geen gegevens over de effecten van tamoxifen in moedermelk op zuigelingen die borstvoeding krijgen of dieren die borstvoeding krijgen. Directe neonatale blootstelling van tamoxifen aan muizen en ratten (niet via moedermelk) veroorzaakte echter 1) laesies van de voortplantingsorganen bij vrouwelijke knaagdieren (vergelijkbaar met die waargenomen bij mensen na intra-uteriene blootstelling aan diethylstilbestrol) en 2) functionele defecten van het voortplantingsstelsel bij mannelijke knaagdieren zoals testiculaire atrofie en arrestatie van spermatogenese.
Het is niet bekend of NOLVADEX (tamoxifencitraat) wordt uitgescheiden in de moedermelk. Vanwege het potentieel voor ernstige bijwerkingen bij zuigelingen die borstvoeding geven van NOLVADEX (tamoxifencitraat), mogen vrouwen die NOLVADEX (tamoxifencitraat) gebruiken geen borstvoeding geven.
Vermindering van de incidentie van borstkanker bij vrouwen met een hoog risico met DCIS
Het is niet bekend of NOLVADEX (tamoxifencitraat) wordt uitgescheiden in de moedermelk. Vanwege het potentieel voor ernstige bijwerkingen bij zuigelingen die borstvoeding geven van NOLVADEX (tamoxifencitraat), mogen vrouwen die NOLVADEX (tamoxifencitraat) gebruiken geen borstvoeding geven.
Pediatrisch gebruik
De veiligheid en werkzaamheid van NOLVADEX (tamoxifencitraat) voor meisjes van twee tot tien jaar met het McCune-Albright-syndroom en vroegtijdige puberteit zijn niet onderzocht na een behandeling van meer dan één jaar. De langetermijneffecten van behandeling met NOLVADEX (tamoxifencitraat) voor meisjes zijn niet vastgesteld. Bij volwassenen die werden behandeld met NOLVADEX (tamoxifencitraat) is een toename van de incidentie van baarmoederkanker, beroerte en longembolie waargenomen (zie GEVAARLIJKE WAARSCHUWING: , en KLINISCHE FARMACOLOGIE-Klinische studies-McCune-Albright-syndroom onderafdeling).
Geriatrisch gebruik
In de NSABP P-1-studie was het percentage vrouwen van ten minste 65 jaar 16%. Vrouwen van ten minste 70 jaar waren goed voor 6% van de deelnemers. Er werd een vermindering van de incidentie van borstkanker waargenomen bij deelnemers in elk van de subgroepen: in totaal werden 28 en 10 invasieve borstkankers waargenomen bij deelnemers van 65 jaar en ouder in respectievelijk de placebo- en NOLVADEX-groep (tamoxifencitraat). Bij alle andere uitkomsten weerspiegelen de resultaten in deze subset de resultaten die zijn waargenomen bij de subset van vrouwen van ten minste 50 jaar oud. Er werden geen algemene verschillen in verdraagbaarheid waargenomen tussen oudere en jongere patiënten (zie: KLINISCHE FARMACOLOGIE - Klinische studies - Vermindering van de incidentie van borstkanker bij vrouwen met een hoog risico sectie).
In de NSABP B-24-studie was het percentage vrouwen van ten minste 65 jaar 23%. Vrouwen van ten minste 70 jaar waren goed voor 10% van de deelnemers. Een totaal van 14 en 12 invasieve borstkankers werden gezien bij deelnemers van 65 jaar en ouder in respectievelijk de placebo- en NOLVADEX-groepen (tamoxifencitraat). Deze subset is te klein om conclusies te trekken over de werkzaamheid. Voor alle andere eindpunten waren de resultaten in deze subset vergelijkbaar met die van jongere vrouwen die deelnamen aan dit onderzoek. Er werden geen algemene verschillen in verdraagbaarheid waargenomen tussen oudere en jongere patiënten.
OVERDOSERING
Tekenen die werden waargenomen bij de hoogste doses na onderzoeken om de LD50 bij dieren te bepalen, waren ademhalingsmoeilijkheden en convulsies.
Acute overdosering bij mensen is niet gemeld. In een onderzoek bij patiënten met gevorderde gemetastaseerde kanker die specifiek de maximaal getolereerde dosis NOLVADEX (tamoxifencitraat) bepaalden bij de evaluatie van het gebruik van zeer hoge doses om resistentie tegen meerdere geneesmiddelen om te keren, werden acute neurotoxiciteit die zich manifesteerde door tremor, hyperreflexie, onvaste gang en duizeligheid opgemerkt. Deze symptomen traden op binnen 3-5 dagen na het begin van NOLVADEX (tamoxifencitraat) en verdwenen binnen 2-5 dagen na het stoppen van de therapie. Er werd geen permanente neurologische toxiciteit opgemerkt. Eén patiënt kreeg enkele dagen nadat NOLVADEX (tamoxifencitraat) was gestopt een aanval en de neurotoxische symptomen waren verdwenen. Het oorzakelijk verband tussen de aanval en de behandeling met NOLVADEX (tamoxifencitraat) is niet bekend. De doses die bij deze patiënten werden gegeven, waren allemaal hoger dan 400 mg/m² oplaaddosis, gevolgd door onderhoudsdoses van 150 mg/m² NOLVADEX (tamoxifencitraat) tweemaal daags.
In hetzelfde onderzoek werd een verlenging van het QT-interval op het elektrocardiogram opgemerkt wanneer patiënten doses kregen die hoger waren dan 250 mg/m² oplaaddosis, gevolgd door onderhoudsdoses van 80 mg/m² NOLVADEX (tamoxifencitraat) tweemaal daags. Voor een vrouw met een lichaamsoppervlak van 1,5 m² waren de minimale oplaaddosis en onderhoudsdoses die werden gegeven waarbij neurologische symptomen en QT-veranderingen optraden, ten minste 6 keer hoger dan de maximaal aanbevolen dosis.
Er is geen specifieke behandeling voor overdosering bekend; behandeling moet symptomatisch zijn.
CONTRA-INDICATIES
NOLVADEX (tamoxifencitraat) is gecontra-indiceerd bij patiënten met een bekende overgevoeligheid voor het geneesmiddel of voor een van de ingrediënten.
Vermindering van de incidentie van borstkanker bij vrouwen met een hoog risico en vrouwen met DCIS
NOLVADEX (tamoxifencitraat) is gecontra-indiceerd bij vrouwen die gelijktijdige anticoagulantia van het cumarine-type nodig hebben of bij vrouwen met een voorgeschiedenis van diepe veneuze trombose of longembolie.
KLINISCHE FARMACOLOGIE
NOLVADEX (tamoxifencitraat) is een niet-steroïde middel dat krachtige anti-oestrogene eigenschappen heeft aangetoond in dierproefsystemen. De anti-oestrogene effecten kunnen verband houden met het vermogen om te concurreren met oestrogeen voor bindingsplaatsen in doelweefsels zoals borst. Tamoxifen remt de inductie van mammacarcinoom bij ratten veroorzaakt door dimethylbenzanthraceen (DMBA) en veroorzaakt de regressie van reeds gevestigde DMBA-geïnduceerde tumoren. In dit rattenmodel lijkt tamoxifen zijn antitumoreffecten uit te oefenen door de oestrogeenreceptoren te binden.
In cytosolen die zijn afgeleid van menselijke borstadenocarcinomen, concurreert tamoxifen met oestradiol voor oestrogeenreceptoreiwit.
Absorptie en distributie
Na een enkelvoudige orale dosis van 20 mg tamoxifen werd ongeveer 5 uur na toediening een gemiddelde piekplasmaconcentratie van 40 ng/ml (bereik 35 tot 45 ng/ml) bereikt. De afname van de plasmaconcentraties van tamoxifen is bifasisch met een terminale eliminatiehalfwaardetijd van ongeveer 5 tot 7 dagen. De gemiddelde piekplasmaconcentratie van N-desmethyltamoxifen is 15 ng/ml (bereik 10 tot 20 ng/ml). Chronische toediening van 10 mg tamoxifen tweemaal daags gedurende 3 maanden aan patiënten resulteert in gemiddelde steady-state plasmaconcentraties van 120 ng/ml (bereik 67-183 ng/ml) voor tamoxifen en 336 ng/ml (bereik 148-654 ng/ ml) voor N-desmethyltamoxifen. De gemiddelde steady-state plasmaconcentraties van tamoxifen en N-desmethyltamoxifen na toediening van 20 mg tamoxifen eenmaal daags gedurende 3 maanden zijn 122 ng/ml (bereik 71-183 ng/ml) en 353 ng/ml (bereik 152-706 ng /ml), respectievelijk. Na het starten van de therapie worden steady-state-concentraties voor tamoxifen bereikt in ongeveer 4 weken en steady-state-concentraties voor N-desmethyltamoxifen worden bereikt in ongeveer 8 weken, wat wijst op een halfwaardetijd van ongeveer 14 dagen voor deze metaboliet. In een steady-state, cross-over-onderzoek van 10 mg NOLVADEX (tamoxifencitraat) tabletten tweemaal daags versus een 20 mg NOLVADEX (tamoxifencitraat) tablet eenmaal daags, was de 20 mg NOLVADEX (tamoxifencitraat) tablet bio-equivalent aan de 10 mg NOLVADEX (tamoxifencitraat) tabletten.
Metabolisme
Tamoxifen wordt uitgebreid gemetaboliseerd na orale toediening. N-desmethyltamoxifen is de belangrijkste metaboliet die in het plasma van patiënten wordt aangetroffen. De biologische activiteit van N-desmethyltamoxifen lijkt vergelijkbaar te zijn met die van tamoxifen. 4-Hydroxytamoxifen en een zijketen primair alcoholderivaat van tamoxifen zijn geïdentificeerd als minder belangrijke metabolieten in plasma. Tamoxifen is een substraat van cytochroom P-450 3A, 2C9 en 2D6 en een remmer van P-glycoproteïne.
uitscheiding
Studies bij vrouwen die 20 mg 14C-tamoxifen kregen, hebben aangetoond dat ongeveer 65% van de toegediende dosis gedurende een periode van 2 weken uit het lichaam werd uitgescheiden, met fecale excretie als primaire eliminatieroute. Het geneesmiddel wordt voornamelijk uitgescheiden als polaire conjugaten, waarbij onveranderd geneesmiddel en ongeconjugeerde metabolieten minder dan 30% van de totale fecale radioactiviteit uitmaken.
Speciale populaties
De effecten van leeftijd, geslacht en ras op de farmacokinetiek van tamoxifen zijn niet vastgesteld. De effecten van een verminderde leverfunctie op het metabolisme en de farmacokinetiek van tamoxifen zijn niet vastgesteld.
Pediatrische patiënten
De farmacokinetiek van tamoxifen en N-desmethyltamoxifen werd gekarakteriseerd met behulp van een populatiefarmacokinetische analyse met schaarse monsters per patiënt verkregen van 27 vrouwelijke pediatrische patiënten van 2 tot 10 jaar die deelnamen aan een onderzoek dat was opgezet om de veiligheid, werkzaamheid en farmacokinetiek van NOLVADEX (tamoxifen citraat) bij de behandeling van het McCune-Albright-syndroom. Rijke gegevens van twee farmacokinetische onderzoeken met tamoxifencitraat waarin 59 postmenopauzale vrouwen met borstkanker de onderzoeken voltooiden, werden opgenomen in de analyse om het structurele farmacokinetische model voor tamoxifen te bepalen. Een model met één compartiment paste het beste bij de gegevens.
Bij pediatrische patiënten waren een gemiddelde steady-state piekplasmaconcentratie (Css, max) en AUC van respectievelijk 187 ng/ml en 4110 ng uur/ml, en Css, max trad ongeveer 8 uur na toediening op. De klaring (CL/F) als lichaamsgewicht aangepast bij vrouwelijke pediatrische patiënten was ongeveer 2,3 maal hoger dan bij vrouwelijke borstkankerpatiënten. In het jongste cohort van vrouwelijke pediatrische patiënten (2-6 jaar oud) was de CL/F 2,6-voudig hoger; in het oudste cohort (7-10,9-jarigen) was de CL/F ongeveer 1,9-voudig hoger. Blootstelling aan N-desmethyltamoxifen was vergelijkbaar tussen pediatrische en volwassen patiënten. De veiligheid en werkzaamheid van NOLVADEX (tamoxifencitraat) voor meisjes van twee tot tien jaar met het McCune-Albright-syndroom en vroegtijdige puberteit zijn niet onderzocht na een behandeling van meer dan één jaar. De langetermijneffecten van behandeling met NOLVADEX (tamoxifencitraat) bij meisjes zijn niet vastgesteld. Bij volwassenen die werden behandeld met NOLVADEX (tamoxifencitraat) is een toename van de incidentie van baarmoedermaligniteiten, beroerte en longembolie waargenomen (zie GEVAARLIJKE WAARSCHUWING: ).
Geneesmiddel-geneesmiddelinteracties
In vitro-onderzoeken hebben aangetoond dat erytromycine, cyclosporine, nifedipine en diltiazem de vorming van N-desmethyltamoxifen competitief remden met een schijnbare K1 van respectievelijk 20, 1, 45 en 30 µM. De klinische betekenis van deze in vitro-onderzoeken is niet bekend.
Tamoxifen verlaagde de plasmaconcentratie van letrozol met 37% bij gelijktijdige toediening van deze geneesmiddelen. Rifampicine, een cytochroom P-450 3A4-inductor, verminderde de AUC en Cmax van tamoxifen met respectievelijk 86% en 55%. Aminoglutethimide verlaagt de plasmaconcentraties van tamoxifen en N-desmethyltamoxifen. Medroxyprogesteron verlaagt de plasmaconcentraties van N-desmethyl, maar niet van tamoxifen.
In de anastrozol-adjuvante studie verminderde gelijktijdige toediening van anastrozol en NOLVADEX (tamoxifencitraat) bij borstkankerpatiënten de plasmaconcentratie van anastrozol met 27% in vergelijking met de concentraties die werden bereikt met alleen anastrozol; de gelijktijdige toediening had echter geen invloed op de farmacokinetiek van tamoxifen of N-desmethyltamoxifen (zie VOORZORGSMAATREGELEN - DRUG-INTERACTIES ). NOLVADEX (tamoxifencitraat) mag niet gelijktijdig met anastrozol worden toegediend.
Klinische studies
Gemetastaseerde borstkanker
Premenopauzale vrouwen (NOLVADEX (tamoxifencitraat) versus ablatie)
Drie prospectieve, gerandomiseerde onderzoeken (Ingle, Pritchard, Buchanan) vergeleken NOLVADEX (tamoxifencitraat) met ovariële ablatie (ovariëctomie of eierstokbestraling) bij premenopauzale vrouwen met gevorderde borstkanker. Hoewel het objectieve responspercentage, de tijd tot het falen van de behandeling en de overleving vergelijkbaar waren bij beide behandelingen, verhinderde de beperkte opbouw van de patiënt een bewijs van gelijkwaardigheid. In een overzichtsanalyse van overlevingsgegevens uit de 3 onderzoeken was de hazard ratio voor overlijden (NOLVADEX (tamoxifencitraat)/ovariumablatie) 1,00 met tweezijdige 95%-betrouwbaarheidsintervallen van 0,73 tot 1,37. Verhoogde serum- en plasma-oestrogenen zijn waargenomen bij premenopauzale vrouwen die NOLVADEX (tamoxifencitraat) kregen, maar de gegevens van de gerandomiseerde onderzoeken wijzen niet op een nadelig effect van deze toename. Een beperkt aantal premenopauzale patiënten met ziekteprogressie tijdens behandeling met NOLVADEX (tamoxifencitraat) reageerde op daaropvolgende ovariële ablatie.
Borstkanker bij mannen
Gepubliceerde resultaten van 122 patiënten (119 evalueerbaar) en casusrapporten bij 16 patiënten (13 evalueerbaar) behandeld met NOLVADEX (tamoxifencitraat) hebben aangetoond dat NOLVADEX (tamoxifencitraat) effectief is voor de palliatieve behandeling van mannelijke borstkanker. Zesenzestig van deze 132 evalueerbare patiënten reageerden op NOLVADEX (tamoxifencitraat), wat neerkomt op een objectief responspercentage van 50%.
Adjuvante borstkanker
Overzicht
De Early Breast Cancer Trialists' Collaborative Group (EBCTCG) heeft in 1985, 1990 en opnieuw in 1995 wereldwijde overzichten van systemische adjuvante therapie voor vroege borstkanker uitgevoerd. adjuvans NOLVADEX (tamoxifencitraat) met doses van 20-40 mg / dag gedurende 1-5+ jaar. Vijfentwintig procent van de patiënten kreeg 1 jaar of minder proefbehandeling, 52% kreeg 2 jaar en 23% kreeg ongeveer 5 jaar. Achtenveertig procent van de tumoren was oestrogeenreceptor (ER) positief (> 10 fmol/mg), 21% was ER-arm (
Onder vrouwen met ER-positieve of onbekende borstkanker en positieve klieren die ongeveer 5 jaar behandeling kregen, was de totale overleving na 10 jaar 61,4% voor NOLVADEX (tamoxifencitraat) versus 50,5% voor controle (logrank 2p
Het effect van de geplande duur van tamoxifen kan als volgt worden beschreven. Bij vrouwen met ER-positieve of onbekende borstkanker die 1 jaar of minder, 2 jaar of ongeveer 5 jaar NOLVADEX (tamoxifencitraat) kregen, was de proportionele afname van de mortaliteit respectievelijk 12%, 17% en 26% (trend significant bij 2p
Voordeel is minder duidelijk voor vrouwen met ER-arme borstkanker bij wie de proportionele vermindering van recidief 10% (2p = 0,007) was voor alle duur samen, of 9% (2p = 0,02) als contralaterale borstkankers worden uitgesloten. De overeenkomstige vermindering van de mortaliteit was 6% (NS). De effecten van ongeveer 5 jaar NOLVADEX (tamoxifencitraat) op recidief en mortaliteit waren vergelijkbaar, ongeacht leeftijd en gelijktijdige chemotherapie. Er waren geen aanwijzingen dat doses hoger dan 20 mg per dag effectiever waren.
Anastrozol Adjuvant ATAC Trial - Studie van anastrozol vergeleken met NOLVADEX (tamoxifencitraat) voor adjuvante behandeling van vroege borstkanker - Er werd een adjuvante studie met anastrozol uitgevoerd bij 9366 postmenopauzale vrouwen met operabele borstkanker die gerandomiseerd waren om een adjuvante behandeling te krijgen met ofwel 1 mg anastrozol per dag, NOLVADEX (tamoxifencitraat) 20 mg per dag, of een combinatie van deze twee behandelingen gedurende vijf jaar of tot recidief van de ziekte. Bij een mediane follow-up van 33 maanden vertoonde de combinatie van anastrozol en NOLVADEX (tamoxifencitraat) geen enkel werkzaamheidsvoordeel in vergelijking met therapie met NOLVADEX (tamoxifencitraat) alleen bij alle patiënten en bij de hormoonreceptorpositieve subpopulatie. Deze behandelarm werd uit de studie gehaald. Raadpleeg a.u.b.: KLINISCHE FARMACOLOGIE - Speciale populaties - Geneesmiddel-geneesmiddelinteracties , VOORZORGSMAATREGELEN-Laboratoriumtests , VOORZORGSMAATREGELEN - Geneesmiddelinteracties en ONGEWENSTE REACTIES secties voor veiligheidsinformatie uit deze proef. Raadpleeg de volledige voorschrijfinformatie voor ARIMIDEX® (anastrozol) 1 mg tabletten voor aanvullende informatie over deze studie.
Patiënten in de twee monotherapie-armen van de ATAC-studie werden gedurende een mediane periode van 60 maanden (5 jaar) behandeld en gevolgd gedurende een mediane periode van 68 maanden. Ziektevrije overleving in de intent-to-treat-populatie was statistisch significant verbeterd [Hazard Ratio (HR) = 0,87, 95% BI: 0,78, 0,97, p=0,0127] in de anastrazool-arm vergeleken met de NOLVADEX (tamoxifencitraat)-arm .
Knooppunt Positief - Individuele studies
Twee studies (Hubay en NSABP B-09) toonden een verbeterde ziektevrije overleving aan na radicale of gewijzigde radicale mastectomie bij postmenopauzale vrouwen of vrouwen van 50 jaar of ouder met chirurgisch geneesbare borstkanker met positieve okselklieren wanneer NOLVADEX (tamoxifencitraat) werd toegevoegd aan adjuvante cytotoxische chemotherapie. In de Hubay-studie werd NOLVADEX (tamoxifencitraat) toegevoegd aan "lage dosis" CMF (cyclofosfamide, methotrexaat en fluorouracil). In de NSABP B-09-studie werd NOLVADEX (tamoxifencitraat) toegevoegd aan melfalan [L-fenylalaninemosterd (P)] en fluorouracil (F).
In de Hubay-studie hadden patiënten met een positieve (meer dan 3 fmol) oestrogeenreceptor meer kans om baat te hebben. In de NSABP B-09-studie bij vrouwen in de leeftijd van 50-59 jaar hadden alleen vrouwen met zowel oestrogeen- als progesteronreceptorniveaus van 10 fmol of hoger duidelijk voordeel, terwijl er een niet-statistisch significante trend was in de richting van bijwerkingen bij vrouwen met zowel oestrogeen- als progesteronreceptorniveaus minder dan 10 fmol. Bij vrouwen van 60-70 jaar was er een trend naar een gunstig effect van NOLVADEX (tamoxifencitraat) zonder enige duidelijke relatie met de oestrogeen- of progesteronreceptorstatus.
Drie prospectieve onderzoeken (ECOG-1178, Toronto, NATO) waarbij NOLVADEX (tamoxifencitraat) adjuvans als enkelvoudig middel werd gebruikt, toonden een verbeterde ziektevrije overleving aan na totale borstamputatie en okseldissectie voor postmenopauzale vrouwen met positieve okselklieren in vergelijking met placebo/geen behandelingscontroles . De NAVO-studie toonde ook een algemeen overlevingsvoordeel aan.
Knooppunt negatief - individuele onderzoeken
NSABP B-14, een prospectieve, dubbelblinde, gerandomiseerde studie, vergeleek NOLVADEX (tamoxifencitraat) met placebo bij vrouwen met okselklier-negatieve, oestrogeenreceptor-positieve (≥ 10 fmol/mg cytosol-eiwit) borstkanker (als adjuvante therapie , na totale borstamputatie en okseldissectie, of segmentale resectie
PATIËNT INFORMATIE
MEDICIJNGIDS
NOLVADEX (tamoxifencitraat) ® (NOLE-vah-dex) Tabletten Generieke naam: tamoxifen (ta-MOX-I-fen)
Geschreven voor vrouwen die NOLVADEX (tamoxifencitraat) gebruiken om hun hoge kans op het krijgen van borstkanker te verlagen of die ductaal carcinoom in situ (DCIS) hebben
Deze medicatiehandleiding bespreekt alleen het gebruik van NOLVADEX (tamoxifencitraat) om de kans op het krijgen van borstkanker te verlagen bij vrouwen met een hoog risico en bij vrouwen die worden behandeld voor DCIS.
Mensen die NOLVADEX (tamoxifencitraat) gebruiken behandelen borstkanker hebben andere voordelen en andere beslissingen die moeten worden genomen dan vrouwen met een hoog risico of vrouwen met ductaal carcinoom in situ (DCIS) die NOLVADEX (tamoxifencitraat) gebruiken om de kans op het krijgen van borstkanker te verkleinen. Als u al borstkanker heeft, bespreek dan met uw arts hoe de voordelen van de behandeling van borstkanker met NOLVADEX (tamoxifencitraat) zich verhouden tot de risico's die in dit document worden beschreven.
Waarom zou ik deze medicatiehandleiding lezen?
Deze gids bevat informatie om u te helpen beslissen of u NOLVADEX (tamoxifencitraat) moet gebruiken om uw kans op het krijgen van borstkanker te verkleinen.
U en uw arts moeten bespreken of het mogelijke voordeel van NOLVADEX (tamoxifencitraat) bij het verlagen van uw grote kans op het krijgen van borstkanker groter is dan de mogelijke risico's. Uw arts heeft een speciaal computerprogramma of een draagbare rekenmachine om te bepalen of u tot de risicogroep behoort. Als u DCIS heeft en bent behandeld met een operatie en bestralingstherapie, kan uw arts NOLVADEX (tamoxifencitraat) voorschrijven om uw kans op het krijgen van invasieve (verspreidende) borstkanker te verkleinen.
Lees deze gids aandachtig door voordat u start met NOLVADEX (tamoxifencitraat). Het is belangrijk om de informatie die u krijgt te lezen elke keer dat u meer geneesmiddel krijgt. Er kan iets nieuws zijn. Deze gids vertelt u niet alles over NOLVADEX (tamoxifencitraat) en wel niet vervangen door een gesprek met uw arts.
Alleen u en uw arts kunnen bepalen of NOLVADEX (tamoxifencitraat) geschikt voor u is.
Wat is de belangrijkste informatie die ik moet weten over het gebruik van NOLVADEX (tamoxifencitraat) om de kans op het krijgen van borstkanker te verkleinen?
NOLVADEX (tamoxifencitraat) is een receptgeneesmiddel dat in sommige opzichten op oestrogeen (vrouwelijk hormoon) lijkt en op andere manieren anders. In de borst kan NOLVADEX (tamoxifencitraat) de effecten van oestrogeen blokkeren. Omdat het dit doet, kan NOLVADEX (tamoxifencitraat) de groei blokkeren van borstkankers die oestrogeen nodig hebben om te groeien (kankers die oestrogeen- of progesteronreceptorpositief zijn).
NOLVADEX (tamoxifencitraat) kan de kans op het krijgen van borstkanker verlagen bij vrouwen met een hoger dan normale kans op het krijgen van borstkanker in de komende vijf jaar (hoogrisicovrouwen) en vrouwen met DCIS.
Omdat vrouwen met een hoog risico nog geen kanker hebben, is het belangrijk om goed na te denken of het mogelijke voordeel van NOLVADEX (tamoxifencitraat) bij het verlagen van de kans op het krijgen van borstkanker groter is dan de mogelijke risico's.
Deze medicatiehandleiding beoordeelt de risico's en voordelen van het gebruik van NOLVADEX (tamoxifencitraat) om de kans op het krijgen van borstkanker bij vrouwen met een hoog risico en vrouwen met DCIS te verminderen. Deze gids doet: niet bespreek de speciale voordelen en beslissingen voor mensen die al borstkanker hebben.
Waarom gebruiken vrouwen en mannen NOLVADEX (tamoxifencitraat)?
NOLVADEX (tamoxifencitraat) heeft meer dan één gebruik. NOLVADEX (tamoxifencitraat) wordt gebruikt:
om de kans te verkleinen om borstkanker te krijgen bij vrouwen met een grotere kans dan normaal om in de komende 5 jaar borstkanker te krijgen (vrouwen met een hoog risico)
om de kans te verkleinen van het krijgen van invasieve (verspreidende) borstkanker bij vrouwen die een operatie en bestraling hebben ondergaan voor ductaal carcinoom in situ (DCIS). DCIS betekent dat de kanker zich alleen in de melkkanalen bevindt.
behandelen borstkanker bij vrouwen nadat ze de vroege behandeling hebben beëindigd. Vroege behandeling kan chirurgie, bestraling en chemotherapie omvatten. NOLVADEX (tamoxifencitraat) kan voorkomen dat de kanker zich naar andere delen van het lichaam verspreidt. Het kan ook de kans van de vrouw op het krijgen van een nieuwe borstkanker verminderen. bij vrouwen en mannen,
behandelen borstkanker die is uitgezaaid naar andere delen van het lichaam (uitgezaaide borstkanker).
In deze gids wordt alleen gesproken over het gebruik van NOLVADEX (tamoxifencitraat) om de kans op het krijgen van borstkanker te verkleinen (#1 en #2 hierboven).
Wat zijn de voordelen van NOLVADEX (tamoxifencitraat) om de kans op het krijgen van borstkanker te verlagen bij vrouwen met een hoog risico en bij vrouwen die worden behandeld voor DCIS?
Een grote Amerikaanse studie keek naar risicovolle vrouwen en vergeleken degenen die NOLVADEX (tamoxifencitraat) gedurende 5 jaar gebruikten met anderen die een pil namen zonder NOLVADEX (tamoxifencitraat) (placebo). Vrouwen met een hoog risico werden gedefinieerd als vrouwen die op basis van een speciaal computerprogramma een kans van 1,7% of meer hebben om in de komende 5 jaar borstkanker te krijgen. In dit onderzoek:
- Op elke 1.000 vrouwen met een hoog risico wie nam een placebo? , kregen elk jaar ongeveer 7 borstkanker.
- Op elke 1.000 vrouwen met een hoog risico die NOLVADEX (tamoxifencitraat) heeft gebruikt , kregen elk jaar ongeveer 4 borstkanker.
De studie toonde aan dat vrouwen met een hoog risico die NOLVADEX (tamoxifencitraat) gebruikten, gemiddeld hun kans op het krijgen van borstkanker met 44% verlaagden, van 7 op 1.000 tot 4 op 1.000.
Een andere Amerikaanse studie keek naar vrouwen met DCIS en vergeleken degenen die NOLVADEX (tamoxifencitraat) gedurende 5 jaar gebruikten met anderen die een placebo namen. In dit onderzoek:
- Op elke 1.000 vrouwen met DCIS wie nam placebo? kregen elk jaar ongeveer 17 borstkanker.
- Op elke 1.000 vrouwen met DCIS die NOLVADEX (tamoxifencitraat) heeft gebruikt , kregen elk jaar ongeveer 10 borstkanker.
De studie toonde aan dat vrouwen met DCIS die NOLVADEX (tamoxifencitraat) gebruikten, gemiddeld hun kans op het krijgen van invasieve (verspreidende) borstkanker met 43% verlaagden, van 17 op 1.000 tot 10 op 1.000.
Deze onderzoeken betekenen niet dat het gebruik van NOLVADEX (tamoxifencitraat) uw persoonlijke kans op het krijgen van borstkanker zal verminderen. We weten niet wat de voordelen zullen zijn voor een vrouw die NOLVADEX (tamoxifencitraat) gebruikt om haar kans op het krijgen van borstkanker te verkleinen.
Wat zijn de risico's van NOLVADEX (tamoxifencitraat)?
In de onderzoeken die worden beschreven onder "Wat zijn de voordelen van NOLVADEX (tamoxifencitraat)?", kregen de risicovolle vrouwen die NOLVADEX (tamoxifencitraat) gebruikten bepaalde bijwerkingen in een hoger percentage dan degenen die een placebo namen.
Sommige van deze bijwerkingen kunnen de dood veroorzaken.
In één onderzoek bij vrouwen die hun baarmoeder nog hadden
- Van elke 1.000 vrouwen die een placebo namen, kreeg er elk jaar 1 endometriumkanker (kanker van het baarmoederslijmvlies) en geen enkele kreeg baarmoedersarcoom (kanker van het baarmoederlichaam).
- Van elke 1.000 vrouwen die NOLVADEX (tamoxifencitraat) gebruikten, kregen er elk jaar 2 endometriumkanker en minder dan 1 baarmoedersarcoom.
Deze resultaten laten zien dat, gemiddeld, bij vrouwen met een hoog risico die hun baarmoeder nog hadden? NOLVADEX (tamoxifencitraat) verdubbelde de kans op het krijgen van endometriumkanker van 1 op 1.000 tot 2 op 1.000, en het verhoogde de kans op het krijgen van baarmoedersarcoom. Dit betekent niet dat het gebruik van NOLVADEX (tamoxifencitraat) uw persoonlijke kans op het krijgen van endometriumkanker zal verdubbelen of uw kans op het krijgen van baarmoedersarcoom zal vergroten. We weten niet wat dit risico zal zijn voor welke vrouw dan ook. Het risico is anders voor vrouwen die hun baarmoeder niet meer hebben.
Voor alle vrouwen in deze studie verhoogde het gebruik van NOLVADEX (tamoxifencitraat) het risico op een bloedstolsel in hun longen of aderen, of op een beroerte. In sommige gevallen stierven vrouwen aan deze effecten.
NOLVADEX (tamoxifencitraat) verhoogde het risico op het krijgen van cataract (troebeling van de ooglens) of op het nodig hebben van een staaroperatie. (Zie "Wat zijn de mogelijke bijwerkingen van NOLVADEX (tamoxifencitraat)?" voor meer informatie over bijwerkingen.)
Wat weten we niet over het gebruik van NOLVADEX (tamoxifencitraat) om de kans op het krijgen van borstkanker te verkleinen?
We weten het niet
- als NOLVADEX (tamoxifencitraat) de kans op het krijgen van borstkanker verlaagt bij vrouwen met abnormale borstkankergenen (BRCA1 en BRCA2)
- als het gebruik van NOLVADEX (tamoxifencitraat) gedurende 5 jaar het aantal borstkankers vermindert dat een vrouw in haar leven zal krijgen of als het slechts enkele borstkankers vertraagt
- als NOLVADEX (tamoxifencitraat) een vrouw helpt langer te leven
- de effecten van het gebruik van NOLVADEX (tamoxifencitraat) met hormoonvervangende therapie (HST), anticonceptiepillen of androgenen (mannelijke hormonen)
- de voordelen van het gebruik van NOLVADEX (tamoxifencitraat) als u jonger bent dan 35 jaar
Er worden onderzoeken uitgevoerd om meer te weten te komen over de voordelen en risico's op de lange termijn van het gebruik van NOLVADEX (tamoxifencitraat) om de kans op het krijgen van borstkanker te verkleinen.
Wat zijn de mogelijke bijwerkingen van NOLVADEX (tamoxifencitraat)?
De meest voorkomende bijwerking van NOLVADEX (tamoxifencitraat) is opvliegers. Dit is geen teken van een ernstig probleem.
De volgende meest voorkomende bijwerking is vaginale afscheiding. Als de afscheiding bloederig is, kan dit een teken zijn van een ernstig probleem. [Zie "Veranderingen in het slijmvlies (endometrium) of het lichaam van uw baarmoeder" hieronder.]
Minder vaak voorkomende maar ernstige bijwerkingen van NOLVADEX (tamoxifencitraat) worden hieronder vermeld. Deze kunnen op elk moment optreden. Bel onmiddellijk uw arts als u tekenen van bijwerkingen heeft die hieronder worden vermeld:
- Veranderingen in het slijmvlies (endometrium) of het lichaam van uw baarmoeder. Deze veranderingen kunnen betekenen dat er ernstige problemen ontstaan, waaronder baarmoederkanker. De tekenen van veranderingen in de baarmoeder zijn:
- Vaginale bloeding of bloederige afscheiding die een roestige of bruine kleur kan hebben. U moet uw arts bellen, zelfs als er slechts een kleine hoeveelheid bloeding optreedt.
- Verandering in uw maandelijkse bloeding, zoals de hoeveelheid of het tijdstip van bloeding of verhoogde stolling.
- Pijn of druk in uw bekken (onder uw navel).
- Bloedstolsels in uw aderen of longen. Deze kunnen ernstige problemen veroorzaken, waaronder de dood. U kunt tot 2-3 maanden nadat u stopt met het gebruik van NOLVADEX (tamoxifencitraat) stolsels krijgen. De tekenen van bloedstolsels zijn:
- plotselinge pijn op de borst, kortademigheid, bloed ophoesten
- pijn, gevoeligheid of zwelling in een of beide benen
- Hartinfarct. Een beroerte kan ernstige medische problemen veroorzaken, waaronder de dood. De tekenen van een beroerte zijn:
- plotselinge zwakte, tintelingen of gevoelloosheid in uw gezicht, arm of been, vooral aan één kant van uw lichaam
- plotselinge verwarring, moeite met spreken of begrijpen
- plotselinge moeite met zien in één of beide ogen
- plotselinge moeite met lopen, duizeligheid, verlies van evenwicht of coördinatie
- plotselinge ernstige hoofdpijn zonder bekende oorzaak
- Cataract of verhoogde kans op een staaroperatie. Het teken van deze problemen is een langzame vervaging van uw zicht.
- Leverproblemen, waaronder geelzucht. De tekenen van leverproblemen zijn onder meer gebrek aan eetlust en geelverkleuring van uw huid of het wit van uw ogen.
Dit zijn niet alle mogelijke bijwerkingen van NOLVADEX (tamoxifencitraat). Vraag uw arts of apotheker om een volledige lijst.
Wie mag NOLVADEX (tamoxifencitraat) niet gebruiken?
Neem NOLVADEX (tamoxifencitraat) om welke reden dan ook niet in als u:
- Bent u zwanger of bent u van plan zwanger te worden terwijl u NOLVADEX (tamoxifencitraat) gebruikt of gedurende de 2 maanden nadat u bent gestopt met het gebruik van NOLVADEX (tamoxifencitraat). NOLVADEX (tamoxifencitraat) kan uw ongeboren baby schaden. Het duurt ongeveer 2 maanden om NOLVADEX (tamoxifencitraat) uit uw lichaam te verwijderen. Om er zeker van te zijn dat u niet zwanger bent, kunt u beginnen met het innemen van NOLVADEX (tamoxifencitraat) tijdens uw menstruatie. Of u kunt een zwangerschapstest doen om er zeker van te zijn dat u niet zwanger bent voordat u begint.
- Zijn borstvoeding. We weten niet of NOLVADEX (tamoxifencitraat) door uw melk kan gaan en uw baby kan schaden.
- Een allergische reactie hebben gehad op NOLVADEX (tamoxifencitraat) of tamoxifen (de andere naam voor NOLVADEX (tamoxifencitraat)), of voor een van de inactieve ingrediënten.
Als u zwanger wordt terwijl u NOLVADEX (tamoxifencitraat) gebruikt, stop dan onmiddellijk met het gebruik en neem contact op met uw arts. NOLVADEX (tamoxifencitraat) kan uw ongeboren baby schaden. Gebruik NOLVADEX (tamoxifencitraat) niet om uw kans op het krijgen van borstkanker te verkleinen als:
- U heeft ooit een bloedstolsel gehad waarvoor medische behandeling nodig was.
- U gebruikt medicijnen om uw bloed te verdunnen, zoals warfarine (ook wel Coumadin®* genoemd).
- Uw vermogen om te bewegen is gedurende de meeste van uw wakkere uren beperkt.
- U loopt risico op bloedstolsels. Uw arts kan u vertellen of u een hoog risico loopt op bloedstolsels.
- U heeft geen grotere kans dan normaal om borstkanker te krijgen. Uw arts kan u vertellen of u een vrouw met een hoog risico bent.
Hoe moet ik NOLVADEX (tamoxifencitraat) gebruiken?
- Slik de tablet(ten) heel door met water of een andere alcoholvrije vloeistof. U kunt NOLVADEX (tamoxifencitraat) met of zonder voedsel innemen. Neem uw geneesmiddel elke dag in. Het is misschien gemakkelijker te onthouden als u het elke dag op hetzelfde tijdstip inneemt.
- Als u een dosis bent vergeten, neem deze dan in wanneer u het zich herinnert en neem dan de volgende dosis zoals gewoonlijk. Als het bijna tijd is voor uw volgende dosis of als u het zich herinnert aan uw volgende dosis, neem dan geen extra tabletten in om de vergeten dosis in te halen.
- Neem NOLVADEX (tamoxifencitraat) gedurende 5 jaar in, tenzij uw arts u anders vertelt.
Wat moet ik vermijden tijdens het gebruik van NOLVADEX (tamoxifencitraat)?
- Word niet zwanger tijdens het gebruik van NOLVADEX (tamoxifencitraat) of gedurende 2 maanden nadat u bent gestopt. NOLVADEX (tamoxifencitraat) kan ervoor zorgen dat hormonale anticonceptiemethoden niet meer werken. Hormonale methoden omvatten anticonceptiepillen, pleisters, injecties, ringen en implantaten. Daarom, terwijl u NOLVADEX (tamoxifencitraat) gebruikt, gebruik anticonceptiemethoden die geen hormonen gebruiken, zoals condooms, diafragma's met zaaddodend middel of gewone spiraaltjes. Als u zwanger wordt, stop dan onmiddellijk met het gebruik van NOLVADEX (tamoxifencitraat) en bel uw arts.
- Geef geen borstvoeding. We weten niet of NOLVADEX (tamoxifencitraat) door uw melk kan gaan en of het schadelijk kan zijn voor de baby.
Wat moet ik doen tijdens het gebruik van NOLVADEX (tamoxifencitraat)?
- Zorg voor regelmatige gynaecologische controles (“vrouwelijke onderzoeken”), borstonderzoeken en mammogrammen. Uw arts zal u vertellen hoe vaak. Deze zullen controleren op tekenen van borstkanker en kanker van het endometrium (slijmvlies van de baarmoeder). Omdat NOLVADEX (tamoxifencitraat) niet alle borstkankers voorkomt en u andere soorten kanker kunt krijgen, heeft u deze onderzoeken nodig om kanker zo vroeg mogelijk te vinden.
- Omdat NOLVADEX (tamoxifencitraat) ernstige bijwerkingen kan veroorzaken, moet u goed op uw lichaam letten. Tekenen waar u op moet letten, staan vermeld in "Wat zijn de mogelijke bijwerkingen van NOLVADEX (tamoxifencitraat)?"
- Vertel alle artsen die u ziet dat u NOLVADEX (tamoxifencitraat) gebruikt.
- Vertel het uw arts meteen als u nieuwe borstknobbels heeft.
Algemene informatie over het veilige en effectieve gebruik van NOLVADEX (tamoxifencitraat)
Medicijnen worden soms voorgeschreven voor andere doeleinden dan die in een Medicatiewijzer vermeld staan. Uw arts heeft alleen u NOLVADEX (tamoxifencitraat) voorgeschreven. Geef het niet aan andere mensen, zelfs niet als ze een vergelijkbare aandoening hebben, omdat het hen kan schaden. Gebruik het niet voor een aandoening waarvoor het niet is voorgeschreven.
Deze medicatiehandleiding is een samenvatting van informatie over NOLVADEX (tamoxifencitraat) voor vrouwen die NOLVADEX (tamoxifencitraat) gebruiken om hun grote kans op het krijgen van borstkanker te verlagen of die DCIS hebben. Als u meer informatie wilt over NOLVADEX (tamoxifencitraat), vraag dan uw arts of apotheker. Zij kunnen u informatie geven over NOLVADEX (tamoxifencitraat) die is geschreven voor gezondheidswerkers. Ga voor meer informatie over NOLVADEX (tamoxifencitraat) of borstkanker naar www.NOLVADEX (tamoxifencitraat) .com of bel 1-800-236-9933.
Ingrediënten: tamoxifencitraat, carboxymethylcellulosecalcium, magnesiumstearaat, mannitol en zetmeel.
Deze medicatiehandleiding is goedgekeurd door de Amerikaanse Food and Drug Administration
