Feldene 10mg, 20mg Piroxicam Gebruik, bijwerkingen en dosering. Prijs in online apotheek. Generieke medicijnen zonder recept.
Wat is Feldene 20 mg en hoe wordt het gebruikt?
Piroxicam is een receptgeneesmiddel dat wordt gebruikt om de pijn of ontsteking van reumatoïde artritis (inclusief juveniele artritis) of osteoartritis te behandelen. Piroxicam kan alleen of in combinatie met andere medicijnen worden gebruikt.
Piroxicam is een niet-steroïde anti-inflammatoir geneesmiddel (NSAID).
Het is niet bekend of Piroxicam veilig en effectief is bij kinderen jonger dan 12 jaar.
Wat zijn de mogelijke bijwerkingen van Feldene?
Feldene 10 mg kan ernstige bijwerkingen veroorzaken, waaronder:
- bonzen in nek of oren,
- slaperigheid,
- wazig zien,
- zwelling,
- snelle gewichtstoename,
- kortademigheid,
- verlies van eetlust,
- buikpijn,
- vermoeidheid,
- jeuk,
- donkere urine,
- klei gekleurde ontlasting,
- geel worden van de huid of ogen (geelzucht),
- bloederige of teerachtige ontlasting,
- bloed ophoesten of braaksel dat op koffiedik lijkt,
- weinig of geen plassen,
- zwelling in uw voeten of enkels,
- licht in het hoofd voelen,
- koude handen of voeten,
- bleke huid, en
- ernstige hoofdpijn,
Roep meteen medische hulp in als u een van de bovenstaande symptomen heeft.
De meest voorkomende bijwerkingen van Feldene zijn:
- abnormale leverfunctietesten,
- moeite met plassen,
- maagklachten,
- maagzuur,
- verlies van eetlust,
- buikpijn,
- misselijkheid,
- braken,
- gas,
- diarree,
- constipatie,
- duizeligheid,
- hoofdpijn,
- jeuk of uitslag, en
- oorsuizen,
Vertel het uw arts als u een bijwerking heeft die u hindert of die niet weggaat.
Dit zijn niet alle mogelijke bijwerkingen van Feldene. Vraag uw arts of apotheker om meer informatie.
Bel uw arts voor medisch advies over bijwerkingen. U kunt bijwerkingen melden aan de FDA op 1-800-FDA-1088.
WAARSCHUWING
RISICO OP ERNSTIGE CARDIOVASCULAIRE EN GASTRO-INTESTINALE GEBEURTENISSEN
Cardiovasculaire trombotische gebeurtenissen
- Niet-steroïde anti-inflammatoire geneesmiddelen (NSAID's) veroorzaken een verhoogd risico op ernstige cardiovasculaire trombotische voorvallen, waaronder myocardinfarct en beroerte, die fataal kunnen zijn. Dit risico kan vroeg in de behandeling optreden en kan toenemen met de duur van het gebruik. [zien WAARSCHUWINGEN EN VOORZORGSMAATREGELEN ].
- FELDENE 20 mg is gecontra-indiceerd in de setting van coronaire bypassoperatie (CABG) [zie CONTRA-INDICATIES en WAARSCHUWINGEN EN VOORZORGSMAATREGELEN ].
Gastro-intestinale bloeding, ulceratie en perforatie
- NSAID's veroorzaken een verhoogd risico op ernstige gastro-intestinale (GI) bijwerkingen, waaronder bloedingen, ulceratie en perforatie van de maag of darmen, die fataal kunnen zijn. Deze gebeurtenissen kunnen op elk moment tijdens het gebruik en zonder waarschuwingssymptomen optreden. Oudere patiënten en patiënten met een voorgeschiedenis van ulcus pepticum en/of gastro-intestinale bloeding lopen een groter risico op ernstige gastro-intestinale voorvallen [zie WAARSCHUWINGEN EN VOORZORGSMAATREGELEN ].
OMSCHRIJVING
FELDENE (piroxicam) capsule is een niet-steroïde anti-inflammatoir geneesmiddel, verkrijgbaar als kastanjebruin en blauw #322 10 mg capsules en kastanjebruin #323 20 mg capsules voor orale toediening. De chemische naam is 4-hydroxyl-2-methyl-N-2-pyridinyl-2H-1,2-benzothiazine-3-carboxamide 1,1-dioxide. Het molecuulgewicht is 331,35. De moleculaire formule is C15H13N3O4S en heeft de volgende chemische structuur.
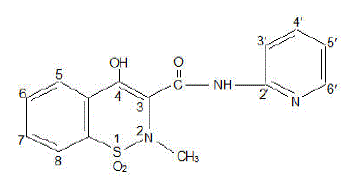
Piroxicam komt voor als een witte kristallijne vaste stof, slecht oplosbaar in water, verdund zuur en de meeste organische oplosmiddelen. Het is slecht oplosbaar in alcohol en in waterige oplossingen. Het vertoont een zwak zuur 4-hydroxy proton (pKa 5,1) en een zwak basische pyridyl stikstof (pKa 1,8).
De inactieve ingrediënten in FELDENE 10 mg zijn: Blauw 1, Rood 3, lactose, magnesiumstearaat, natriumlaurylsulfaat, zetmeel.
INDICATIES
FELDENE wordt aangegeven:
- Voor verlichting van de tekenen en symptomen van artrose.
- Voor verlichting van de tekenen en symptomen van reumatoïde artritis.
DOSERING EN ADMINISTRATIE
Overweeg zorgvuldig de mogelijke voordelen en risico's van FELDENE 20 mg en andere behandelingsopties voordat u besluit FELDENE te gebruiken. Gebruik de laagste effectieve dosering voor de kortste duur in overeenstemming met de individuele behandeldoelen van de patiënt [zie WAARSCHUWINGEN EN VOORZORGSMAATREGELEN ].
Na het observeren van de respons op de initiële therapie met FELDENE 20 mg, moeten de dosis en frequentie worden aangepast aan de behoeften van de individuele patiënt.
Voor de verlichting van reumatoïde artritis en osteoartritis is de dosering 20 mg eenmaal daags oraal. Indien gewenst kan de dagelijkse dosis worden verdeeld. Vanwege de lange halfwaardetijd van FELDENE worden steady-state bloedspiegels pas na 7-12 dagen bereikt. Daarom, hoewel de therapeutische effecten van FELDENE vroeg in de behandeling duidelijk zijn, is er een progressieve toename van de respons gedurende meerdere weken en dient het effect van de therapie pas na twee weken te worden beoordeeld.
HOE GELEVERD
Doseringsvormen en sterke punten
FELDENE (piroxicam)-capsules
10 mg kastanjebruin en blauw #322 20 mg kastanjebruin #323
Opslag en behandeling
FELDENE® (piroxicam) 10 mg capsules zijn kastanjebruin en blauw #322, geleverd als:
FELDENE® (piroxicam) 20 mg capsules zijn kastanjebruin #323, geleverd als:
Opslag
Bewaren bij kamertemperatuur 20°C tot 25°C (68°F tot 77°F); excursies toegestaan tussen 15 ° C en 30 ° C (59 ° F tot 86 ° F) [zie USP-gecontroleerde kamertemperatuur].
Gedistribueerd door: Pfizer Labs, Division of Pfizer Inc., 235 East 42nd Street, New York, NY 10017. Herzien: april 2017.
BIJWERKINGEN
De volgende bijwerkingen worden in andere secties van de etikettering in meer detail besproken:
- Cardiovasculaire trombotische gebeurtenissen [zie WAARSCHUWINGEN EN VOORZORGSMAATREGELEN ]
- GI-bloeding, ulceratie en perforatie [zie WAARSCHUWINGEN EN VOORZORGSMAATREGELEN ]
- Hepatotoxiciteit [zie WAARSCHUWINGEN EN VOORZORGSMAATREGELEN ]
- Hypertensie [zie WAARSCHUWINGEN EN VOORZORGSMAATREGELEN ]
- Hartfalen en oedeem [zie WAARSCHUWINGEN EN VOORZORGSMAATREGELEN ]
- Niertoxiciteit en hyperkaliëmie [zie WAARSCHUWINGEN EN VOORZORGSMAATREGELEN ]
- Anafylactische reacties [zie WAARSCHUWINGEN EN VOORZORGSMAATREGELEN ]
- Ernstige huidreacties [zie WAARSCHUWINGEN EN VOORZORGSMAATREGELEN ]
- Hematologische toxiciteit [zie WAARSCHUWINGEN EN VOORZORGSMAATREGELEN ]
Ervaring met klinische proeven
Omdat klinische onderzoeken onder sterk uiteenlopende omstandigheden worden uitgevoerd, kunnen de bijwerkingen die in de klinische onderzoeken van een geneesmiddel zijn waargenomen niet direct worden vergeleken met de percentages in de klinische onderzoeken van een ander geneesmiddel en komen mogelijk niet overeen met de percentages die in de praktijk worden waargenomen.
Bij patiënten die FELDENE 10 mg of andere NSAID's gebruiken, zijn de meest gemelde bijwerkingen die optreden bij ongeveer 1-10% van de patiënten:
Cardiovasculair systeem: Oedeem
Spijsverteringsstelsel: Anorexia, buikpijn, obstipatie, diarree, winderigheid, misselijkheid, braken
Zenuwstelsel : Duizeligheid, hoofdpijn, draaiduizeligheid
Huid en aanhangsels: Jeuk, uitslag
Speciale zintuigen: Tinnitus
Bijkomende bijwerkingen die af en toe worden gemeld, zijn onder meer:
Cardiovasculair systeem: Hartkloppingen
Spijsverteringsstelsel: stomatitis
Zenuwstelsel: Slaperigheid
Speciale zintuigen: Wazig zien
Postmarketingervaring
De volgende bijwerkingen zijn vastgesteld tijdens het gebruik van FELDENE na goedkeuring. Omdat deze reacties vrijwillig worden gemeld door een populatie van onbekende grootte, is het niet altijd mogelijk om op betrouwbare wijze hun frequentie te schatten of een oorzakelijk verband met blootstelling aan geneesmiddelen vast te stellen.
Lichaam als geheel: Koorts, infectie, sepsis, anafylactische reacties, veranderingen in eetlust, overlijden, griepachtig syndroom, pijn (koliek), serumziekte
Cardiovasculair systeem: Congestief hartfalen, hypertensie, tachycardie, syncope, aritmie, verergering van angina, hypotensie, myocardinfarct, vasculitis
Spijsverteringsstelsel: Dyspepsie, verhoogde leverenzymen, grove bloeding/perforatie, brandend maagzuur, zweren (maag/duodenale), droge mond, oesofagitis, gastritis, glossitis, hematemesis, hepatitis, geelzucht, melena, rectale bloeding, oprisping, leverfalen, pancreatitis
Hemic en lymfatisch systeem: Bloedarmoede, verhoogde bloedingstijd, e cchymose, eosinofilie, epistaxis, leukopenie, purpura, petechiale uitslag, trombocytopenie, agranulocytose, hemolytische anemie, aplastische anemie, lymfadenopathie, pancytopenie
Overgevoeligheid: Positieve ANA
Metabool en voedingswaarde: Gewichtsveranderingen, vochtretentie, hyperglykemie, hypoglykemie
Zenuwstelsel: Angst, asthenie, verwardheid, depressie, droomafwijkingen, slapeloosheid, malaise, nervositeit, paresthesie, slaperigheid, tremoren, acathisie, convulsies, coma, hallucinaties, meningitis, stemmingswisselingen
Ademhalingssysteem: Astma, dyspneu, ademhalingsdepressie, longontsteking
Huid en aanhangsels: Alopecia, blauwe plekken, afschilfering, erytheem, lichtgevoeligheid, zweet, angio-oedeem, toxische epidermale necrose, erythema multiforme, exfoliatieve dermatitis, onycholyse, Stevens-Johnson-syndroom, urticaria, vesiculobulleuze reactie
Speciale zintuigen: Conjunctivitis, gehoorbeschadiging, gezwollen ogen
Urogenitaal systeem: Abnormale nierfunctie, c ystitis, dysurie, hematurie, hyperkaliëmie, interstitiële nefritis, nefrotisch syndroom, oligurie/polyurie, proteïnurie, nierfalen, glomerulonefritis
Voortplantingsstelsel- en borstaandoeningen: Vrouwelijke vruchtbaarheid afgenomen
DRUG-INTERACTIES
Zie Tabel 1 voor klinisch significante geneesmiddelinteracties met piroxicam.
WAARSCHUWINGEN
Inbegrepen als onderdeel van de "PREVENTIEVE MAATREGELEN" Sectie
PREVENTIEVE MAATREGELEN
Cardiovasculaire trombotische gebeurtenissen
Klinische onderzoeken met verschillende COX-2-selectieve en niet-selectieve NSAID's met een duur tot drie jaar hebben een verhoogd risico op ernstige cardiovasculaire (CV) trombotische voorvallen aangetoond, waaronder myocardinfarct (MI) en beroerte, die fataal kunnen zijn. Op basis van beschikbare gegevens is het onduidelijk dat het risico op CV trombotische voorvallen gelijk is voor alle NSAID's. De relatieve toename van ernstige CV trombotische voorvallen ten opzichte van baseline, veroorzaakt door het gebruik van NSAID's, lijkt vergelijkbaar te zijn bij degenen met en zonder bekende CV ziekte of risicofactoren voor CV ziekte. Patiënten met bekende CV ziekte of risicofactoren hadden echter een hogere absolute incidentie van overmatige ernstige CV trombotische voorvallen, vanwege hun verhoogde baseline percentage. Sommige observationele studies vonden dat dit verhoogde risico op ernstige CV trombotische voorvallen al in de eerste weken van de behandeling begon. De toename van het cardiovasculaire trombotische risico is het meest consistent waargenomen bij hogere doses.
Gebruik de laagst effectieve dosis voor de kortst mogelijke duur om het potentiële risico op een ongunstige CV-gebeurtenis bij met NSAID behandelde patiënten te minimaliseren. Artsen en patiënten moeten alert blijven op de ontwikkeling van dergelijke gebeurtenissen, gedurende de gehele behandelingskuur, zelfs als er geen eerdere CV-symptomen zijn. Patiënten moeten worden geïnformeerd over de symptomen van ernstige CV-gebeurtenissen en de te nemen stappen als deze zich voordoen.
Er is geen consistent bewijs dat gelijktijdig gebruik van aspirine het verhoogde risico op ernstige CV trombotische voorvallen geassocieerd met NSAID-gebruik vermindert. Het gelijktijdig gebruik van aspirine en een NSAID, zoals piroxicam, verhoogt het risico op ernstige gastro-intestinale (GI) gebeurtenissen [zie Gastro-intestinale bloedingen, ulceraties en perforaties ].
Status Post coronaire bypassoperatie (CABG)
Twee grote, gecontroleerde klinische onderzoeken met een COX-2-selectieve NSAID voor de behandeling van pijn in de eerste 10-14 dagen na CABG-chirurgie vonden een verhoogde incidentie van myocardinfarct en beroerte. NSAID's zijn gecontra-indiceerd bij CABG [zie CONTRA-INDICATIES ].
Post-MI-patiënten
Observationele studies uitgevoerd in het Deense Nationale Register hebben aangetoond dat patiënten die in de post-MI-periode met NSAID's werden behandeld een verhoogd risico hadden op een her-infarct, CV-gerelateerd overlijden en mortaliteit door alle oorzaken vanaf de eerste week van de behandeling. In hetzelfde cohort was de incidentie van overlijden in het eerste jaar na MI 20 per 100 persoonsjaren bij NSAID-behandelde patiënten vergeleken met 12 per 100 persoonsjaren bij niet-NSAID-blootgestelde patiënten. Hoewel het absolute sterftecijfer enigszins daalde na het eerste jaar na MI, bleef het verhoogde relatieve risico op overlijden bij NSAID-gebruikers gedurende ten minste de volgende vier jaar van follow-up bestaan.
Vermijd het gebruik van FELDENE 10 mg bij patiënten met een recent MI, tenzij verwacht wordt dat de voordelen opwegen tegen het risico op terugkerende CV trombotische voorvallen. Als FELDENE wordt gebruikt bij patiënten met een recent MI, moet u de patiënten controleren op tekenen van cardiale ischemie.
Gastro-intestinale bloedingen, ulceraties en perforaties
NSAID's, waaronder FELDENE, veroorzaken ernstige gastro-intestinale (GI) bijwerkingen, waaronder ontsteking, bloeding, ulceratie en perforatie van de slokdarm, maag, dunne darm of dikke darm, die fataal kan zijn. Deze ernstige bijwerkingen kunnen op elk moment optreden, met of zonder waarschuwingssymptomen, bij patiënten die worden behandeld met NSAID's. Slechts één op de vijf patiënten die een ernstige bijwerking van het bovenste deel van het maagdarmkanaal ontwikkelen bij behandeling met NSAID's, is symptomatisch. Zweren van het bovenste deel van het maagdarmkanaal, grove bloeding of perforatie veroorzaakt door NSAID's kwamen voor bij ongeveer 1% van de patiënten die gedurende 3-6 maanden werden behandeld en bij ongeveer 2%-4% van de patiënten die gedurende een jaar werden behandeld. Zelfs kortdurende NSAID-therapie is echter niet zonder risico.
Risicofactoren voor GI-bloeding, ulceratie en perforatie
Patiënten met een voorgeschiedenis van ulcus pepticum en/of gastro-intestinale bloeding die NSAID's gebruikten, hadden een meer dan 10-voudig verhoogd risico op het ontwikkelen van een gastro-intestinale bloeding in vergelijking met patiënten zonder deze risicofactoren. Andere factoren die het risico op gastro-intestinale bloedingen verhogen bij patiënten die met NSAID's worden behandeld, zijn onder meer een langere behandeling met NSAID's; gelijktijdig gebruik van orale corticosteroïden, aspirine, anticoagulantia of selectieve serotonineheropnameremmers (SSRI's); roken; gebruik van alcohol; oudere leeftijd; en een slechte algemene gezondheidstoestand. De meeste postmarketingmeldingen van fatale GI-voorvallen kwamen voor bij oudere of verzwakte patiënten. Bovendien lopen patiënten met gevorderde leverziekte en/of coagulopathie een verhoogd risico op gastro-intestinale bloedingen.
Strategieën om de GI-risico's bij met NSAID behandelde patiënten te minimaliseren
- Gebruik de laagste effectieve dosering voor de kortst mogelijke duur.
- Vermijd toediening van meer dan één NSAID tegelijk.
- Vermijd het gebruik bij patiënten met een hoger risico, tenzij verwacht wordt dat de voordelen opwegen tegen het verhoogde risico op bloedingen. Overweeg voor dergelijke patiënten, evenals voor patiënten met actieve gastro-intestinale bloedingen, andere alternatieve therapieën dan NSAID's.
- Blijf alert op tekenen en symptomen van gastro-intestinale ulceratie en bloeding tijdens NSAID-therapie.
- Als een ernstige GI-bijwerking wordt vermoed, start dan onmiddellijk met evaluatie en behandeling en stop FELDENE totdat een ernstige GI-bijwerking is uitgesloten.
- In de setting van gelijktijdig gebruik van een lage dosis aspirine voor hartprofylaxe, moet u patiënten nauwlettender controleren op tekenen van gastro-intestinale bloeding [zie DRUG-INTERACTIES ].
Hepatotoxiciteit
Verhogingen van ALAT of ASAT (drie of meer keer de bovengrens van normaal [ULN]) zijn gemeld bij ongeveer 1% van de met NSAID behandelde patiënten in klinische onderzoeken. Daarnaast zijn zeldzame, soms fatale gevallen van ernstig leverletsel gemeld, waaronder fulminante hepatitis, levernecrose en leverfalen.
Verhogingen van ALAT of ASAT (minder dan driemaal de ULN) kunnen voorkomen bij maximaal 15% van de patiënten die worden behandeld met NSAID's, waaronder piroxicam.
Informeer patiënten over de waarschuwingssignalen en symptomen van hepatotoxiciteit (bijv. misselijkheid, vermoeidheid, lethargie, diarree, jeuk, geelzucht, gevoeligheid van het rechter bovenste kwadrant en "griepachtige" symptomen). Als zich klinische tekenen en symptomen ontwikkelen die overeenkomen met een leverziekte, of als systemische verschijnselen optreden (bijv. eosinofilie, huiduitslag, enz.), stop dan onmiddellijk met FELDENE en voer een klinische evaluatie van de patiënt uit.
Hypertensie
NSAID's, waaronder FELDENE, kunnen leiden tot het ontstaan van hypertensie of verergering van reeds bestaande hypertensie, die beide kunnen bijdragen aan de verhoogde incidentie van CV events. Patiënten die angiotensineconverterend enzym (ACE)-remmers, thiazidediuretica of lisdiuretica gebruiken, kunnen een verminderde respons op deze therapieën hebben wanneer ze NSAID's gebruiken (zie DRUG-INTERACTIES ].
Controleer de bloeddruk (BP) tijdens de start van de NSAID-behandeling en tijdens de behandeling.
Hartfalen en oedeem
De meta-analyse van Coxib en traditionele NSAID Trialists' Collaboration van gerandomiseerde gecontroleerde onderzoeken toonde een ongeveer tweevoudige toename van ziekenhuisopnames voor hartfalen aan bij met COX-2 selectief behandelde patiënten en niet-selectieve NSAID-behandelde patiënten in vergelijking met met placebo behandelde patiënten. In een Deense National Registry-studie van patiënten met hartfalen verhoogde het gebruik van NSAID's het risico op MI, ziekenhuisopname voor hartfalen en overlijden.
Bovendien zijn vochtretentie en oedeem waargenomen bij sommige patiënten die met NSAID's werden behandeld. Het gebruik van piroxicam kan de CV-effecten van verschillende therapeutische middelen die worden gebruikt om deze medische aandoeningen te behandelen (bijv. diuretica, ACE-remmers of angiotensinereceptorblokkers [ARB's]) afzwakken (zie DRUG-INTERACTIES ].
Vermijd het gebruik van FELDENE 10 mg bij patiënten met ernstig hartfalen, tenzij verwacht wordt dat de voordelen opwegen tegen het risico op verergering van hartfalen. Als FELDENE wordt gebruikt bij patiënten met ernstig hartfalen, controleer de patiënten dan op tekenen van verergering van hartfalen.
Niertoxiciteit en hyperkaliëmie
Niertoxiciteit
Langdurige toediening van NSAID's heeft geresulteerd in renale papillaire necrose en ander nierletsel.
Niertoxiciteit is ook waargenomen bij patiënten bij wie renale prostaglandines een compenserende rol spelen bij het in stand houden van de nierperfusie. Bij deze patiënten kan toediening van een NSAID een dosisafhankelijke vermindering van de vorming van prostaglandine veroorzaken en, in tweede instantie, van de renale bloedstroom, wat een duidelijke nierdecompensatie kan veroorzaken. Patiënten met het grootste risico op deze reactie zijn patiënten met een verminderde nierfunctie, uitdroging, hypovolemie, hartfalen, leverdisfunctie, patiënten die diuretica en ACE-remmers of ARB's gebruiken, en ouderen. Stopzetting van de NSAID-therapie wordt meestal gevolgd door herstel naar de toestand van voor de behandeling.
Er is geen informatie beschikbaar uit gecontroleerde klinische onderzoeken over het gebruik van FELDENE 20 mg bij patiënten met gevorderde nierziekte. De niereffecten van FELDENE 20 mg kunnen de progressie van nierdisfunctie versnellen bij patiënten met een reeds bestaande nierziekte.
Corrigeer de volumestatus bij gedehydrateerde of hypovolemische patiënten voordat FELDENE wordt gestart. Controleer de nierfunctie bij patiënten met nier- of leverinsufficiëntie, hartfalen, uitdroging of hypovolemie tijdens het gebruik van FELDENE (zie DRUG-INTERACTIES ]. Vermijd het gebruik van FELDENE bij patiënten met gevorderde nierziekte, tenzij verwacht wordt dat de voordelen opwegen tegen het risico op verslechtering van de nierfunctie. Als FELDENE wordt gebruikt bij patiënten met gevorderde nierziekte, controleer de patiënten dan op tekenen van verslechtering van de nierfunctie.
Hyperkaliëmie
Verhogingen van de serumkaliumconcentratie, waaronder hyperkaliëmie, zijn gemeld bij gebruik van NSAID's, zelfs bij sommige patiënten zonder nierfunctiestoornis. Bij patiënten met een normale nierfunctie zijn deze effecten toegeschreven aan een toestand van hyporeninemisch-hypoaldosteronisme.
Anafylactische reacties
Piroxicam is in verband gebracht met anafylactische reacties bij patiënten met en zonder bekende overgevoeligheid voor piroxicam en bij patiënten met aspirinegevoelig astma [zie CONTRA-INDICATIES en Exacerbatie van astma gerelateerd aan aspirinegevoeligheid ].
Zoek noodhulp als er een anafylactische reactie optreedt.
Exacerbatie van astma gerelateerd aan aspirinegevoeligheid
Een subpopulatie van patiënten met astma kan aspirinegevoelig astma hebben, waaronder chronische rhinosinusitis gecompliceerd door neuspoliepen; ernstige, mogelijk fatale bronchospasmen; en/of intolerantie voor aspirine en andere NSAID's. Omdat kruisreactiviteit tussen aspirine en andere NSAID's is gemeld bij dergelijke aspirinegevoelige patiënten, is FELDENE 20 mg gecontra-indiceerd bij patiënten met deze vorm van aspirinegevoeligheid [zie CONTRA-INDICATIES ]. Als FELDENE wordt gebruikt bij patiënten met reeds bestaand astma (zonder bekende gevoeligheid voor aspirine), moet u de patiënten controleren op veranderingen in de tekenen en symptomen van astma.
Ernstige huidreacties
NSAID's, waaronder piroxicam, kunnen ernstige huidbijwerkingen veroorzaken, zoals exfoliatieve dermatitis, Stevens-Johnson-syndroom (SJS) en toxische epidermale necrolyse (TEN), die fataal kan zijn. Deze ernstige gebeurtenissen kunnen zonder waarschuwing plaatsvinden. Informeer patiënten over de tekenen en symptomen van ernstige huidreacties en stop met het gebruik van FELDENE 10 mg bij het eerste optreden van huiduitslag of enig ander teken van overgevoeligheid. FELDENE 20 mg is gecontra-indiceerd bij patiënten met eerdere ernstige huidreacties op NSAID's [zie: CONTRA-INDICATIES ].
Voortijdige sluiting van foetale ductus arteriosus
Piroxicam kan voortijdige sluiting van de foetale ductus arteriosus veroorzaken. Vermijd het gebruik van NSAID's, inclusief FELDENE 20 mg, bij zwangere vrouwen vanaf 30 weken zwangerschap (derde trimester) [zie Gebruik bij specifieke populaties ].
Hematologische toxiciteit
Bloedarmoede is opgetreden bij met NSAID behandelde patiënten. Dit kan te wijten zijn aan occult of grof bloedverlies, vochtretentie of een onvolledig beschreven effect op erytropoëse. Als een met FELDENE behandelde patiënt tekenen of symptomen van bloedarmoede heeft, controleer hemoglobine of hematocriet.
NSAID's, waaronder FELDENE, kunnen het risico op bloedingen verhogen. Comorbide aandoeningen zoals stollingsstoornissen, gelijktijdig gebruik van warfarine, andere anticoagulantia, plaatjesaggregatieremmers (bijv. aspirine), serotonineheropnameremmers (SSRI's) en serotonine-noradrenalineheropnameremmers (SNRI's) kunnen dit risico verhogen. Controleer deze patiënten op tekenen van bloeding [zie DRUG-INTERACTIES ].
Maskeren van ontsteking en koorts
De farmacologische activiteit van FELDENE 10 mg bij het verminderen van ontstekingen en mogelijk koorts kan het nut van diagnostische symptomen bij het opsporen van infecties verminderen.
Laboratoriumbewaking
Omdat ernstige gastro-intestinale bloedingen, hepatotoxiciteit en nierbeschadiging kunnen optreden zonder waarschuwingssymptomen of tekenen, kunt u overwegen patiënten die een langdurige NSAID-behandeling ondergaan, periodiek te controleren met een CBC en een chemieprofiel [zie Gastro-intestinale bloeding, ulceratie en perforatie, hepatotoxiciteit, niertoxiciteit en hyperkaliëmie ] .
Oftalmologische effecten
Vanwege meldingen van nadelige oogbevindingen met niet-steroïde anti-inflammatoire middelen, wordt aanbevolen dat patiënten die tijdens de behandeling met FELDENE visuele klachten ontwikkelen, oogonderzoeken ondergaan.

Informatie over patiëntbegeleiding
Adviseer de patiënt om de door de FDA goedgekeurde patiëntetikettering te lezen ( Medicatiegids ) bij elk verstrekt recept. Informeer patiënten, families of hun verzorgers over de volgende informatie voordat de behandeling met FELDENE wordt gestart en periodiek tijdens de lopende therapie.
Cardiovasculaire trombotische gebeurtenissen
Adviseer patiënten alert te zijn op de symptomen van cardiovasculaire trombotische voorvallen, waaronder pijn op de borst, kortademigheid, zwakte of onduidelijke spraak, en om elk van deze symptomen onmiddellijk aan hun zorgverlener te melden [zie WAARSCHUWINGEN EN VOORZORGSMAATREGELEN ].
Gastro-intestinale bloedingen, ulceraties en perforaties
Adviseer patiënten om symptomen van ulceraties en bloedingen, waaronder epigastrische pijn, dyspepsie, melena en hematemesis, aan hun zorgverlener te melden. In de setting van gelijktijdig gebruik van een lage dosis aspirine voor hartprofylaxe, informeer patiënten over het verhoogde risico op en de tekenen en symptomen van gastro-intestinale bloeding [zie WAARSCHUWINGEN EN VOORZORGSMAATREGELEN ].
Hepatotoxiciteit
Informeer patiënten over de waarschuwingssignalen en symptomen van hepatotoxiciteit (bijv. misselijkheid, vermoeidheid, lethargie, jeuk, diarree, geelzucht, gevoeligheid van het rechter bovenste kwadrant en "griepachtige" symptomen). Als deze zich voordoen, instrueer patiënten dan om te stoppen met FELDENE en onmiddellijk medische therapie te zoeken [zie: WAARSCHUWINGEN EN VOORZORGSMAATREGELEN ].
Hartfalen en oedeem
Adviseer patiënten alert te zijn op de symptomen van congestief hartfalen, waaronder kortademigheid, onverklaarbare gewichtstoename of oedeem, en om contact op te nemen met hun zorgverlener als dergelijke symptomen optreden [zie WAARSCHUWINGEN EN VOORZORGSMAATREGELEN ].
Anafylactische reacties
Informeer patiënten over de tekenen van een anafylactische reactie (bijv. ademhalingsmoeilijkheden, zwelling van het gezicht of de keel). Instrueer patiënten om onmiddellijk noodhulp te zoeken als deze zich voordoen [zie CONTRA-INDICATIES en WAARSCHUWINGEN EN VOORZORGSMAATREGELEN ].
Ernstige huidreacties
Adviseer patiënten om onmiddellijk te stoppen met FELDENE als ze huiduitslag krijgen en om zo snel mogelijk contact op te nemen met hun zorgverlener [zie WAARSCHUWINGEN EN VOORZORGSMAATREGELEN ].
Vrouwelijke vruchtbaarheid
Adviseer vrouwen in de vruchtbare leeftijd die zwanger willen worden dat NSAID's, waaronder FELDENE 20 mg, in verband kunnen worden gebracht met een omkeerbare vertraging in de eisprong [zie Gebruik bij specifieke populaties ].
Foetale toxiciteit
Informeer zwangere vrouwen om het gebruik van FELDENE en andere NSAID's te vermijden vanaf 30 weken zwangerschap vanwege het risico op voortijdige sluiting van de foetale ductus arteriosus [zie WAARSCHUWINGEN EN VOORZORGSMAATREGELEN en Gebruik bij specifieke populaties ].
Vermijd gelijktijdig gebruik van NSAID's
Informeer patiënten dat gelijktijdig gebruik van FELDENE met andere NSAID's of salicylaten (bijv. diflunisal, salsalaat) niet wordt aanbevolen vanwege het verhoogde risico op gastro-intestinale toxiciteit en weinig of geen toename van de werkzaamheid (zie WAARSCHUWINGEN EN VOORZORGSMAATREGELEN en DRUG-INTERACTIES ]. Waarschuw patiënten dat NSAID's aanwezig kunnen zijn in "vrij verkrijgbare" medicijnen voor de behandeling van verkoudheid, koorts of slapeloosheid.
Gebruik van NSAID's en een lage dosis aspirine
Informeer patiënten om geen lage dosis aspirine gelijktijdig met FELDENE te gebruiken totdat ze met hun zorgverlener hebben gesproken [zie DRUG-INTERACTIES ].
Niet-klinische toxicologie
Carcinogenese, mutagenese, verminderde vruchtbaarheid
Carcinogenese
Er zijn geen dierstudies op lange termijn uitgevoerd om het carcinogene potentieel van piroxicam te karakteriseren.
Mutagenese
Piroxicam was niet mutageen in een bacteriële reverse-mutatietest van Ames, of in een dominante letale mutatietest bij muizen, en was niet clastogeen in een in vivo test op chromosoomafwijkingen bij muizen.
Aantasting van de vruchtbaarheid
Voortplantingsstudies waarbij ratten piroxicam kregen toegediend in doses van 2, 5 of 10 mg/kg/dag (tot 5 maal de maximaal aanbevolen dosis voor de mens [MRHD] van 20 mg op basis van mg/m2 lichaamsoppervlak [BSA]) toonden geen aantasting van de mannelijke of vrouwelijke vruchtbaarheid.
Gebruik bij specifieke populaties
Zwangerschap
Risico Samenvatting
Het gebruik van NSAID's, waaronder FELDENE 20 mg, tijdens het derde trimester van de zwangerschap verhoogt het risico op voortijdige sluiting van de foetale ductus arteriosus. Vermijd het gebruik van NSAID's, inclusief FELDENE 10 mg, bij zwangere vrouwen vanaf 30 weken zwangerschap (derde trimester).
Er zijn geen adequate en goed gecontroleerde onderzoeken met FELDENE 20 mg bij zwangere vrouwen.
Gegevens uit observationele onderzoeken met betrekking tot mogelijke embryofoetale risico's van NSAID-gebruik bij vrouwen in het eerste of tweede trimester van de zwangerschap zijn niet overtuigend. In de algemene Amerikaanse populatie hebben alle klinisch erkende zwangerschappen, ongeacht de blootstelling aan geneesmiddelen, een achtergrondpercentage van 2-4% voor ernstige misvormingen en 15-20% voor zwangerschapsverlies.
In reproductiestudies bij dieren bij ratten en konijnen was er geen bewijs van teratogeniteit bij blootstellingen tot respectievelijk 5 en 10 keer de MRHD. In studies met piroxicam bij ratten werd foetotoxiciteit (verlies na implantatie) waargenomen bij blootstellingen van 2 keer de MRHD, en vertraagde partus en een verhoogde incidentie van doodgeboorte werden waargenomen bij doses die gelijk waren aan de MRHD van piroxicam. Op basis van diergegevens is aangetoond dat prostaglandinen een belangrijke rol spelen bij de vasculaire permeabiliteit van het endometrium, de implantatie van blastocysten en de decidualisatie. In dierstudies resulteerde toediening van prostaglandinesyntheseremmers zoals piroxicam in verhoogd pre- en postimplantatieverlies.
Klinische overwegingen
Arbeid of levering
Er zijn geen onderzoeken naar de effecten van FELDENE tijdens de bevalling of bevalling. In dierstudies remmen NSAID's, waaronder piroxicam, de prostaglandinesynthese, veroorzaken ze een vertraagde bevalling en verhogen ze de incidentie van doodgeboorte.
Gegevens
Diergegevens
Zwangere ratten die piroxicam toegediend kregen in een dosis van 2, 5 of 10 mg/kg/dag tijdens de periode van organogenese (Draagdag 6 tot 15) vertoonden verhoogde post-implantatieverliezen met 5 en 10 mg/kg/dag piroxicam (gelijk aan 2 en 5 maal de maximaal aanbevolen dosis voor de mens [MRHD], van respectievelijk 20 mg, gebaseerd op een mg/m2 lichaamsoppervlak [BSA]). Er werden geen geneesmiddelgerelateerde ontwikkelingsafwijkingen opgemerkt bij de nakomelingen. De toxiciteit van het maag-darmkanaal was verhoogd bij drachtige ratten in het laatste trimester van de dracht in vergelijking met niet-zwangere ratten of ratten in eerdere trimesters van de dracht. Zwangere konijnen die piroxicam toegediend kregen in een dosis van 2, 5 of 10 mg/kg/dag tijdens de periode van organogenese (draagtijd 7 tot 18) vertoonden geen geneesmiddelgerelateerde ontwikkelingsafwijkingen bij nakomelingen (tot 10 keer de MRHD op basis van een mg/m2 BSA).
In een pre- en postnataal ontwikkelingsonderzoek waarbij zwangere ratten piroxicam kregen toegediend in een dosis van 2, 5 of 10 mg/kg/dag op dag 15 van de dracht tot aan de geboorte en het spenen van nakomelingen, werd een verminderde gewichtstoename en sterfte waargenomen bij moederdieren op 10 mg/kg/dag (5 maal de MRHD gebaseerd op een mg/m2 BSA) vanaf dracht 20. Behandelde moederdieren vertoonden peritonitis, verklevingen, maagbloeding, hemorragische enteritis en dode foetussen in utero. De bevalling was vertraagd en er was een verhoogde incidentie van doodgeboorte in alle met piroxicam behandelde groepen (in doses die gelijk waren aan de MRHD). De postnatale ontwikkeling kon niet betrouwbaar worden beoordeeld vanwege het ontbreken van moederlijke zorg die secundair was aan ernstige maternale toxiciteit.
Borstvoeding
Risico Samenvatting
Beperkte gegevens van 2 gepubliceerde rapporten met in totaal 6 vrouwen die borstvoeding gaven en 2 zuigelingen toonden aan dat piroxicam wordt uitgescheiden in de moedermelk bij ongeveer 1% tot 3% van de maternale concentratie. Tijdens de behandeling trad er geen accumulatie van piroxicam op in de melk in vergelijking met die in het plasma van de moeder. De ontwikkelings- en gezondheidsvoordelen van borstvoeding moeten worden overwogen, samen met de klinische behoefte van de moeder aan FELDENE 20 mg en eventuele nadelige effecten op de zuigeling die borstvoeding krijgt van de FELDENE of van de onderliggende maternale aandoening.
Vrouwtjes en mannetjes met reproductief potentieel
Onvruchtbaarheid
vrouwen
Op basis van het werkingsmechanisme kan het gebruik van door prostaglandine gemedieerde NSAID's, waaronder FELDENE, het scheuren van de eierstokfollikels vertragen of voorkomen, wat bij sommige vrouwen in verband is gebracht met omkeerbare onvruchtbaarheid. Gepubliceerde dierstudies hebben aangetoond dat toediening van prostaglandinesyntheseremmers de potentie heeft om prostaglandine-gemedieerde folliculaire ruptuur die nodig is voor ovulatie te verstoren. Kleine studies bij vrouwen die werden behandeld met NSAID's hebben ook een omkeerbare vertraging van de eisprong aangetoond. Overweeg het stopzetten van NSAID's, waaronder FELDENE, bij vrouwen die moeite hebben om zwanger te worden of die een onvruchtbaarheidsonderzoek ondergaan.
Pediatrisch gebruik
FELDENE 20 mg is niet onderzocht bij pediatrische patiënten. De veiligheid en werkzaamheid van FELDENE 10 mg zijn niet vastgesteld.
Geriatrisch gebruik
Oudere patiënten lopen, vergeleken met jongere patiënten, een groter risico op NSAID-gerelateerde ernstige cardiovasculaire, gastro-intestinale en/of renale bijwerkingen. Als het verwachte voordeel voor de oudere patiënt opweegt tegen deze mogelijke risico's, begin dan met de dosering aan de lage kant van het doseringsbereik en controleer de patiënten op bijwerkingen [zie WAARSCHUWINGEN EN VOORZORGSMAATREGELEN ].
OVERDOSERING
Symptomen na acute overdoses van NSAID's waren doorgaans beperkt tot lethargie, slaperigheid, misselijkheid, braken en epigastrische pijn, die over het algemeen omkeerbaar zijn met ondersteunende zorg. Gastro-intestinale bloedingen zijn opgetreden. Hypertensie, acuut nierfalen, ademhalingsdepressie en coma zijn opgetreden, maar waren zeldzaam [zie: WAARSCHUWINGEN EN VOORZORGSMAATREGELEN ].
Beheer patiënten met symptomatische en ondersteunende zorg na een overdosis NSAID's. Er zijn geen specifieke antidota. Overweeg braken en/of actieve kool (60-100 gram bij volwassenen, 1-2 gram per kg lichaamsgewicht bij pediatrische patiënten) en/of osmotische catharsis bij symptomatische patiënten die binnen vier uur na inname worden waargenomen of bij patiënten met een grote overdosering ( 5 tot 10 keer de aanbevolen dosering).
Bij de behandeling van een overdosis met piroxicam moet rekening worden gehouden met de lange plasmahalfwaardetijd van piroxicam. Geforceerde diurese, alkalisering van urine, hemodialyse of hemoperfusie zijn mogelijk niet nuttig vanwege de hoge eiwitbinding.
Neem voor meer informatie over een behandeling met overdosering contact op met een antigifcentrum (1-800-222-1222).
CONTRA-INDICATIES
FELDENE 10 mg is gecontra-indiceerd bij de volgende patiënten:
- Bekende overgevoeligheid (bijv. anafylactische reacties en ernstige huidreacties) voor piroxicam of enig bestanddeel van het geneesmiddel [zie WAARSCHUWINGEN EN VOORZORGSMAATREGELEN ]
- Voorgeschiedenis van astma, urticaria of andere allergische reacties na inname van aspirine of andere NSAID's. Ernstige, soms fatale, anafylactische reacties op NSAID's zijn gemeld bij dergelijke patiënten [zie: WAARSCHUWINGEN EN VOORZORGSMAATREGELEN ]
- In de setting van coronaire bypass-transplantaat (CABG) chirurgie [zie WAARSCHUWINGEN EN VOORZORGSMAATREGELEN ]
KLINISCHE FARMACOLOGIE
Werkingsmechanisme
Piroxicam heeft pijnstillende, ontstekingsremmende en koortswerende eigenschappen.
Het werkingsmechanisme van FELDENE 20 mg is, net als dat van andere NSAID's, niet volledig bekend, maar omvat remming van cyclo-oxygenase (COX-1 en COX-2).
Piroxicam is een krachtige remmer van de prostaglandine (PG)-synthese in vitro. Piroxicamconcentraties die tijdens de therapie worden bereikt, hebben in vivo effecten veroorzaakt. Prostaglandinen sensibiliseren afferente zenuwen en versterken de werking van bradykinine bij het induceren van pijn in diermodellen. Prostaglandinen zijn mediatoren van ontstekingen. Omdat piroxicam een remmer is van de prostaglandinesynthese, kan het werkingsmechanisme het gevolg zijn van een afname van prostaglandinen in perifere weefsels.
Farmacokinetiek
Algemene farmacokinetische kenmerken
De farmacokinetiek van piroxicam is gekarakteriseerd bij gezonde proefpersonen, speciale populaties en patiënten. De farmacokinetiek van piroxicam is lineair. Een proportionele toename van de blootstelling wordt waargenomen bij toenemende doses. De verlengde halfwaardetijd (50 uur) resulteert in het handhaven van relatief stabiele plasmaconcentraties gedurende de dag bij eenmaal daagse doses en significante accumulatie bij meervoudige dosering. De meeste patiënten benaderen de steady-state plasmaspiegels binnen 7-12 dagen. Hogere spiegels, die de steady-state na twee tot drie weken benaderen, zijn waargenomen bij patiënten bij wie langere plasmahalfwaardetijden van piroxicam optraden.
Absorptie
Piroxicam wordt goed geabsorbeerd na orale toediening. De plasmaconcentraties van geneesmiddelen zijn proportioneel voor doses van 10 en 20 mg en pieken over het algemeen binnen drie tot vijf uur na toediening. Een enkele dosis van 20 mg produceert over het algemeen piekplasmaspiegels van piroxicam van 1,5 tot 2 mcg/ml, terwijl maximale plasmaconcentraties van het geneesmiddel, na herhaalde dagelijkse toediening van 20 mg piroxicam, gewoonlijk stabiliseren op 3-8 mcg/ml.
Met voedsel is er een lichte vertraging in de snelheid, maar niet in de mate van absorptie na orale toediening. Het is aangetoond dat de gelijktijdige toediening van antacida (aluminiumhydroxide of aluminiumhydroxide met magnesiumhydroxide) geen effect heeft op de plasmaspiegels van oraal toegediend piroxicam.
Verdeling
Het schijnbare distributievolume van piroxicam is ongeveer 0,14 l/kg. Negenennegentig procent van plasma piroxicam is gebonden aan plasma-eiwitten. Piroxicam wordt uitgescheiden in de moedermelk. De aanwezigheid in moedermelk is vastgesteld tijdens initiële en langdurige aandoeningen (52 dagen). Piroxicam verscheen in de moedermelk bij ongeveer 1% tot 3% van de maternale concentratie. Tijdens de behandeling trad er geen accumulatie van piroxicam op in melk in vergelijking met die in plasma.
Eliminatie
Metabolisme
Metabolisme van piroxicam vindt plaats door hydroxylering op positie 5 van de pyridylzijketen en conjugatie van dit product; door cyclodehydratatie; en door een opeenvolging van reacties waarbij hydrolyse van de amidebinding, decarboxylering, ringcontractie en N-demethylering betrokken zijn. In vitro-onderzoeken wijzen uit dat cytochroom P4502C9 (CYP2C9) het belangrijkste enzym is dat betrokken is bij de vorming tot 5'-hydroxy-piroxicam, de belangrijkste metaboliet [zie farmacogenomica ]. Van de biotransformatieproducten van het metabolisme van piroxicam is gemeld dat ze geen ontstekingsremmende werking hebben.
Er is een hogere systemische blootstelling aan piroxicam waargenomen bij proefpersonen met CYP2C9-polymorfismen in vergelijking met proefpersonen van het normale metaboliseerdertype (zie farmacogenomica ].
uitscheiding
Piroxicam en zijn biotransformatieproducten worden uitgescheiden in de urine en feces, waarbij ongeveer tweemaal zoveel in de urine verschijnt als in de feces. Ongeveer 5% van een dosis FELDENE 10 mg wordt onveranderd uitgescheiden. De plasmahalfwaardetijd (t½ ) van piroxicam is ongeveer 50 uur.
Specifieke populaties
pediatrisch
Piroxicam is niet onderzocht bij pediatrische patiënten.
Ras
Farmacokinetische verschillen als gevolg van ras zijn niet vastgesteld.
Leverfunctiestoornis
De effecten van leverziekte op de farmacokinetiek van piroxicam zijn niet vastgesteld. Een aanzienlijk deel van de eliminatie van piroxicam vindt echter plaats via levermetabolisme. Dientengevolge kunnen patiënten met een leveraandoening lagere doses piroxicam nodig hebben in vergelijking met patiënten met een normale leverfunctie.
Nierfunctiestoornis
De farmacokinetiek van piroxicam is onderzocht bij patiënten met nierinsufficiëntie. Studies tonen aan dat patiënten met een lichte tot matige nierfunctiestoornis mogelijk geen dosisaanpassingen nodig hebben. De farmacokinetische eigenschappen van piroxicam bij patiënten met ernstige nierinsufficiëntie of bij patiënten die hemodialyse ondergaan, zijn echter niet bekend.
Geneesmiddelinteractiestudies
Antacida
Gelijktijdige toediening van antacida had geen effect op de plasmaspiegels van piroxicam.
Aspirine
Wanneer piroxicam samen met aspirine werd toegediend, was de eiwitbinding verminderd, hoewel de klaring van vrij FELDENE 20 mg niet veranderde. Plasmaspiegels van piroxicam waren verlaagd tot ongeveer 80% van hun normale waarden wanneer FELDENE (20 mg/dag) werd toegediend in combinatie met aspirine (3900 mg/dag). De klinische betekenis van deze interactie is niet bekend [zie: DRUG-INTERACTIES ].
farmacogenomica
De CYP2C9-activiteit is verminderd bij personen met genetische polymorfismen, zoals de CYP2C9*2- en CYP2C9*3-polymorfismen. Beperkte gegevens uit twee gepubliceerde rapporten toonden aan dat proefpersonen met heterozygote CYP2C9*1/*2 (n=9), heterozygote CYP2C9*1/*3 (n=9) en homozygote CYP2C9*3/*3 (n=1) genotypen vertoonden respectievelijk 1,7-, 1,7- en 5,3-voudig hogere systemische piroxicamspiegels dan de proefpersonen met CYP2C9*1/*1 (n=17, genotype van de normale metaboliseerder) na toediening van een enkelvoudige orale dosis. De gemiddelde eliminatiehalfwaardetijd van piroxicam voor proefpersonen met CYP2C9*1/*3 (n=9) en CYP2C9*3/*3 (n=1) genotypen waren 1,7- en 8,8-voudig hoger dan bij proefpersonen met CYP2C9*1 /*1 (n=17). Geschat wordt dat de frequentie van het homozygote*3/*3 genotype 0% tot 1% is in de gehele populatie; bij bepaalde etnische groepen zijn echter frequenties tot 5,7% gemeld.
Slechte metaboliseerders van CYP2C9-substraten
Bij patiënten van wie bekend is of vermoed wordt dat ze slechte CYP2C9-metaboliseerders zijn op basis van het genotype of eerdere voorgeschiedenis/ervaring met andere CYP2C9-substraten (zoals warfarine en fenytoïne), overweeg dan dosisverlaging omdat ze abnormaal hoge plasmaspiegels kunnen hebben als gevolg van verminderde metabole klaring.
Klinische studies
In gecontroleerde klinische onderzoeken is de werkzaamheid van FELDENE vastgesteld voor zowel acute exacerbaties als langdurige behandeling van reumatoïde artritis en osteoartritis.
De therapeutische effecten van FELDENE 20 mg zijn al vroeg in de behandeling van beide ziekten duidelijk met een progressieve toename van de respons gedurende meerdere (8-12) weken. De werkzaamheid wordt gezien in termen van pijnverlichting en, indien aanwezig, verzakking van ontsteking.
Doses van 20 mg/dag FELDENE 20 mg vertonen een therapeutisch effect dat vergelijkbaar is met therapeutische doses aspirine, met een lagere incidentie van lichte gastro-intestinale effecten en tinnitus.
FELDENE 10 mg is gelijktijdig toegediend met vaste doses goud en corticosteroïden. Het bestaan van een "steroïde sparend" effect is tot op heden niet voldoende onderzocht.
PATIËNT INFORMATIE
Wat is de belangrijkste informatie die ik moet weten over geneesmiddelen die niet-steroïde anti-inflammatoire geneesmiddelen (NSAID's) worden genoemd?
NSAID's kunnen ernstige bijwerkingen veroorzaken, waaronder:
- Verhoogd risico op een hartaanval of beroerte die tot de dood kan leiden. Dit risico kan vroeg in de behandeling optreden en kan toenemen:
- met toenemende doses NSAID's
- bij langer gebruik van NSAID's
- Verhoogd risico op bloedingen, zweren en tranen (perforatie) van de slokdarm (buis die van de mond naar de maag loopt), maag en darmen:
- op elk moment tijdens gebruik
- zonder waarschuwingssymptomen
- dat kan de dood veroorzaken
Het risico op het krijgen van een maagzweer of bloeding neemt toe met:
- voorgeschiedenis van maagzweren, of maag- of darmbloedingen bij gebruik van NSAID's
- geneesmiddelen gebruiken die "corticosteroïden", "anticoagulantia", "SSRI's" of "SNRI's" worden genoemd
- toenemende doses NSAID's
- langer gebruik van NSAID's
- roken
- alcohol drinken
- oudere leeftijd
- slechte gezondheid
- gevorderde leverziekte
- bloedingsproblemen
NSAID's mogen alleen worden gebruikt:
- precies zoals voorgeschreven
- in de laagst mogelijke dosis voor uw behandeling
- voor de kortst benodigde tijd
Neem geen NSAID's vlak voor of na een hartoperatie die een 'coronaire bypass-transplantaat (CABG)' wordt genoemd.
Vermijd het gebruik van NSAID's na een recente hartaanval, tenzij uw zorgverlener u dat zegt. U heeft mogelijk een verhoogd risico op een nieuwe hartaanval als u NSAID's gebruikt na een recente hartaanval
Wat zijn NSAID's?
NSAID's worden gebruikt voor de behandeling van pijn en roodheid, zwelling en hitte (ontsteking) door medische aandoeningen zoals verschillende soorten artritis, menstruatiekrampen en andere soorten kortdurende pijn.
Wie mag geen NSAID's gebruiken?
Gebruik geen NSAID's:
- als u een astma-aanval, netelroos of een andere allergische reactie heeft gehad met aspirine of andere NSAID's.
- vlak voor of na een bypassoperatie van het hart.
Vertel uw zorgverlener voordat u NSAID's gebruikt over al uw medische aandoeningen, ook als u:
- lever- of nierproblemen heeft
- hoge bloeddruk hebben
- astma hebben
- zwanger bent of van plan bent zwanger te worden. Neem contact op met uw zorgverlener als u overweegt NSAID's te gebruiken tijdens de zwangerschap. U mag geen NSAID's gebruiken na 29 weken zwangerschap
- borstvoeding geeft of van plan bent borstvoeding te geven.
Vertel uw zorgverlener over alle geneesmiddelen die u gebruikt, inclusief receptgeneesmiddelen of zelfzorggeneesmiddelen, vitamines of kruidensupplementen. NSAID's en sommige andere geneesmiddelen kunnen met elkaar interageren en ernstige bijwerkingen veroorzaken. Begin niet met het innemen van een nieuw geneesmiddel zonder eerst met uw zorgverlener te overleggen.
Wat zijn de mogelijke bijwerkingen van NSAID's?
NSAID's kunnen ernstige bijwerkingen veroorzaken, waaronder:
Zie "Wat is de belangrijkste informatie die ik moet weten over geneesmiddelen die niet-steroïde anti-inflammatoire geneesmiddelen (NSAID's) worden genoemd)?
- nieuwe of ergere hoge bloeddruk
- hartfalen
- leverproblemen waaronder leverfalen
- nierproblemen waaronder nierfalen
- lage rode bloedcellen (bloedarmoede)
- levensbedreigende huidreacties
- levensbedreigende allergische reacties
- Andere bijwerkingen van NSAID's zijn onder meer: maagpijn, constipatie, diarree, gas, brandend maagzuur, misselijkheid, braken en duizeligheid.
Schakel onmiddellijk noodhulp in als u een van de volgende symptomen krijgt:
- kortademigheid of moeite met ademhalen
- pijn op de borst
- zwakte in een deel of zijkant van uw lichaam
- onduidelijke spraak
- zwelling van het gezicht of de keel
Stop met het gebruik van uw NSAID en bel onmiddellijk uw zorgverlener als u een van de volgende symptomen krijgt:
- misselijkheid
- vermoeider of zwakker dan normaal
- diarree
- jeuk
- je huid of ogen zien er geel uit
- indigestie of maagpijn
- griepachtige symptomen
- bloed overgeven
- er zit bloed in uw stoelgang of het is zwart en plakkerig als teer
- ongebruikelijke gewichtstoename
- huiduitslag of blaren met koorts
- zwelling van de armen, benen, handen en voeten
Als u te veel van uw NSAID heeft ingenomen, neem dan onmiddellijk contact op met uw zorgverlener of roep medische hulp in.
Dit zijn niet alle mogelijke bijwerkingen van NSAID's. Vraag uw zorgverlener of apotheker om meer informatie over NSAID's.
Bel uw arts voor medisch advies over bijwerkingen. U kunt bijwerkingen melden aan de FDA op 1-800-FDA-1088.
Overige informatie over NSAID's
- Aspirine is een NSAID maar verhoogt de kans op een hartaanval niet. Aspirine kan bloedingen in de hersenen, maag en darmen veroorzaken. Aspirine kan ook zweren in de maag en darmen veroorzaken.
- Sommige NSAID's worden zonder recept in lagere doses verkocht (zonder recept verkrijgbaar). Praat met uw zorgverlener voordat u vrij verkrijgbare NSAID's langer dan 10 dagen gebruikt.
Algemene informatie over veilig en effectief gebruik van NSAID's
Medicijnen worden soms voorgeschreven voor andere doeleinden dan die in een Medicatiewijzer vermeld staan. Gebruik NSAID's niet voor een aandoening waarvoor het niet is voorgeschreven. Geef geen NSAID's aan andere mensen, ook niet als zij dezelfde symptomen hebben als u. Het kan hen schaden.
Als u meer informatie wilt over NSAID's, neem dan contact op met uw zorgverlener. U kunt uw apotheker of zorgverlener om informatie vragen over NSAID's die zijn geschreven voor gezondheidswerkers.
Deze medicatiehandleiding is goedgekeurd door de Amerikaanse Food and Drug Administration.
