Lozol 1.5mg, 2.5mg Indapamide Gebruik, bijwerkingen en dosering. Prijs in online apotheek. Generieke medicijnen zonder recept.
Wat is Lozol en hoe wordt het gebruikt?
Lozol (indapamide) is een oraal antihypertensivum/diureticum (plaspil) dat wordt gebruikt om vochtretentie (oedeem) te behandelen bij mensen met congestief hartfalen. Lozol wordt ook gebruikt voor de behandeling van hoge bloeddruk (hypertensie). Lozol 1,5 mg is een stopgezette merknaam en is verkrijgbaar als generiek indapamide.
Wat zijn bijwerkingen van Lozol 2,5 mg?
Vaak voorkomende bijwerkingen van Lozol (indapamide) zijn onder meer:
- duizeligheid,
- hoofdpijn, of
- huiduitslag.
Lozol (indapamide) kan uitdroging veroorzaken. Vertel het uw arts als u symptomen van uitdroging heeft, waaronder een snelle of onregelmatige hartslag, ongewone droge mond, dorst, spierkrampen of pijn, ongewoon verminderd plassen of zwakte.
OMSCHRIJVING
Lozol® (indapamide) is een oraal antihypertensivum/diureticum. Het molecuul bevat zowel een polair sulfamoylchloorbenzamide-deel als een in vet oplosbaar methylindoline-deel. Het verschilt chemisch van de thiaziden doordat het niet het thiazideringsysteem bezit en slechts één sulfonamidegroep bevat. De chemische naam van Lozol (indapamide) is 1-(4-chloor-3sulfamoylbenzamido)-2-methylindoline en het molecuulgewicht is 365,84. De verbinding is een zwak zuur, pKa=8,8, en is oplosbaar in waterige oplossingen van sterke basen. Het is een wit tot geelwit kristallijn (tetragonaal) poeder.
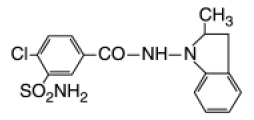
De tabletten bevatten ook microkristallijne cellulose, kleurstof, maïszetmeel, gepregelatineerd zetmeel, hypromellose, lactose, magnesiumstearaat, polyethyleenglycol en talk.
INDICATIES
Lozol is geïndiceerd voor de behandeling van hypertensie, alleen of in combinatie met andere antihypertensiva.
Lozol 2,5 mg is ook geïndiceerd voor de behandeling van zout- en vochtretentie geassocieerd met congestief hartfalen.
Gebruik tijdens de zwangerschap
Het routinematig gebruik van diuretica bij een overigens gezonde vrouw is ongepast en stelt moeder en foetus bloot aan onnodige gevaren (zie: PREVENTIEVE MAATREGELEN onderstaand).
Diuretica voorkomen de ontwikkeling van toxemie tijdens de zwangerschap niet en er is geen bevredigend  bewijs dat ze nuttig zijn bij de behandeling van ontwikkelde toxemie.
Oedeem tijdens de zwangerschap kan het gevolg zijn van pathologische oorzaken of van de fysiologische en mechanische gevolgen van zwangerschap. Indapamide is geïndiceerd tijdens de zwangerschap wanneer oedeem het gevolg is van pathologische oorzaken, net als bij afwezigheid van zwangerschap (zie echter PREVENTIEVE MAATREGELEN onderstaand). Afhankelijk oedeem tijdens de zwangerschap, als gevolg van beperking van de veneuze terugkeer door de uitgezette baarmoeder, wordt goed behandeld door middel van elevatie van de onderste ledematen en het gebruik van een steunslang; het gebruik van diuretica om het intravasculaire volume te verlagen is in dit geval onlogisch en onnodig. Er is hypervolemie tijdens een normale zwangerschap die niet schadelijk is voor de foetus of de moeder (bij afwezigheid van hart- en vaatziekten), maar die gepaard gaat met oedeem, inclusief gegeneraliseerd oedeem bij de meeste zwangere vrouwen. Als dit oedeem ongemak veroorzaakt, zal een verhoogde lighouding vaak verlichting bieden. In zeldzame gevallen kan dit oedeem extreem ongemak veroorzaken dat niet wordt verlicht door rust. In deze gevallen kan een korte kuur met diuretica verlichting bieden en passend zijn.
DOSERING EN ADMINISTRATIE
Hypertensie
De startdosis indapamide voor volwassenen voor hypertensie is 1,25 mg als een enkele dagelijkse dosis, 's ochtends ingenomen. Als de respons op 1,25 mg na vier weken niet bevredigend is, kan de dagelijkse dosis worden verhoogd tot 2,5 mg eenmaal daags. Als de respons op 2,5 mg na vier weken niet bevredigend is, kan de dagelijkse dosis worden verhoogd tot eenmaal daags 5,0 mg, maar het toevoegen van een ander antihypertensivum moet worden overwogen.
Oedeem van congestief hartfalen
De startdosis indapamide voor volwassenen voor oedeem of congestief hartfalen is 2,5 mg als een enkele dagelijkse dosis 's ochtends. Als de respons op 2,5 mg na een week niet bevredigend is, kan de dagelijkse dosis worden verhoogd tot eenmaal daags 5,0 mg.
Als de antihypertensieve respons op indapamide onvoldoende is, kan Lozol worden gecombineerd met andere antihypertensiva, met zorgvuldige controle van de bloeddruk. Het wordt aanbevolen om de gebruikelijke dosis van andere middelen tijdens de initiële combinatietherapie met 50% te verlagen. Naarmate de bloeddrukrespons duidelijk wordt, kunnen verdere dosisaanpassingen nodig zijn.
Over het algemeen lijken doses van 5,0 mg en hoger geen extra effecten op bloeddruk of hartfalen te hebben, maar zijn ze in verband gebracht met een grotere mate van hypokaliëmie. Er is minimale ervaring in klinische onderzoeken bij patiënten met doses hoger dan 5,0 mg eenmaal daags.
HOE GELEVERD
Buiten bereik van kinderen bewaren.
Goed gesloten bewaren. Bewaren bij een gecontroleerde kamertemperatuur van 20 tot 25°C (68 tot 77°F) [zie USP ]. Vermijd overmatige hitte. Dit product moet worden afgeleverd in een container met een kindveilige dop.
sanofi-aventis US LLC Bridgewater, NJ 08807 EEN SANOFI-BEDRIJF. Herzien: maart 2021
BIJWERKINGEN
De meeste bijwerkingen waren mild en van voorbijgaande aard.
De klinische bijwerkingen vermeld in tabel 1 vertegenwoordigen gegevens uit fase II/III placebogecontroleerde onderzoeken (306 patiënten die indapamide 1,25 mg kregen). De klinische bijwerkingen in tabel 2 vertegenwoordigen gegevens uit fase II placebogecontroleerde onderzoeken en gecontroleerde klinische onderzoeken op lange termijn (426 patiënten die Lozol 2,5 mg of 5,0 mg kregen). De reacties zijn in twee groepen gerangschikt: 1) een cumulatieve incidentie gelijk aan of groter dan 5%; 2) een cumulatieve incidentie van minder dan 5%. Reacties worden geteld ongeacht de relatie met het geneesmiddel.
TABEL 1: Bijwerkingen van onderzoeken van 1,25 mg
Alle andere klinische bijwerkingen traden op met een incidentie van
Ongeveer 4% van de patiënten die indapamide 1,25 mg kregen, vergeleken met 5% van de patiënten die placebo kregen, stopten met de behandeling in de onderzoeken van maximaal acht weken vanwege bijwerkingen. In gecontroleerde klinische onderzoeken met een duur van zes tot acht weken had 20% van de patiënten die indapamide 1,25 mg kregen, 61% van de patiënten die indapamide 5,0 mg kregen en 80% van de patiënten die indapamide 10,0 mg kregen ten minste één kaliumwaarde lager dan 3,4 mEq/L . In de groep met indapamide 1,25 mg keerde ongeveer 40% van de patiënten die hypokaliëmie als laboratoriumbijwerking meldden terug naar normale serumkaliumwaarden zonder tussenkomst. Hypokaliëmie met gelijktijdige klinische tekenen of symptomen trad op bij 2% van de patiënten die 1,25 mg indapamide kregen.
TABEL 2: Bijwerkingen van onderzoeken met 2,5 mg en 5,0 mg
Omdat de meeste van deze gegevens afkomstig zijn uit langetermijnonderzoeken (tot 40 weken behandeling), is het waarschijnlijk dat veel van de gemelde bijwerkingen te wijten zijn aan andere oorzaken dan het geneesmiddel. Ongeveer 10% van de patiënten die indapamide kregen, stopte met de behandeling in langetermijnonderzoeken vanwege reacties die al dan niet gerelateerd waren aan het geneesmiddel.
Hypokaliëmie met gelijktijdige klinische tekenen of symptomen trad op bij 3% van de patiënten die indapamide 2,5 mg eenmaal daags kregen en 7% van de patiënten die indapamide 5 mg eenmaal daags kregen. % van de patiënten die indapamide 2,5 mg kregen, 72% van de patiënten die indapamide 5 mg kregen en 44% van de patiënten die 50 mg hydrochloorthiazide kregen, had ten minste één kaliumwaarde (van de in totaal 11 die tijdens het onderzoek werden ingenomen) lager dan 3,5 mEq/l. In de indapamide-groep van 2,5 mg keerde meer dan 50% van die patiënten zonder interventie terug naar normale serumkaliumwaarden.
In klinische onderzoeken van zes tot acht weken waren de gemiddelde veranderingen in geselecteerde waarden zoals weergegeven in de onderstaande tabellen.
Gemiddelde veranderingen ten opzichte van baseline na 8 weken behandeling - 1,25 mg
Geen van de patiënten die indapamide 1,25 mg kregen, ondervonden hyponatriëmie die mogelijk klinisch significant werd geacht (
Indapamide had geen nadelige effecten op lipiden.
Gemiddelde veranderingen ten opzichte van baseline na 40 weken behandeling - 2,5 mg en 5,0 mg
De volgende reacties zijn gemeld bij klinisch gebruik van Lozol: geelzucht (intrahepatische cholestatische geelzucht), hepatitis, pancreatitis en abnormale leverfunctietesten. Deze reacties waren omkeerbaar bij stopzetting van het geneesmiddel.
Ook gemeld zijn erythema multiforme, Stevens-Johnson-syndroom, bulleuze erupties, purpura, lichtgevoeligheid, koorts, pneumonitis, anafylactische reacties, agranulocytose, leukopenie, trombocytopenie en aplastische anemie. Andere bijwerkingen die zijn gemeld bij antihypertensiva/diuretica zijn necrotiserende angiitis, ademnood, sialadenitis, xanthopsie.
Postmarketingervaring
Oogaandoeningen
Choroïdale effusie, acute bijziendheid en kamerhoekglaucoom (frequentie niet bekend).1
DRUG-INTERACTIES
Andere antihypertensiva
Lozol kan de werking van andere antihypertensiva versterken of versterken. In beperkte gecontroleerde onderzoeken waarin het effect van indapamide in combinatie met andere antihypertensiva werd vergeleken met het effect van de andere geneesmiddelen die alleen werden toegediend, was er geen opmerkelijke verandering in de aard of frequentie van bijwerkingen die verband hielden met de gecombineerde therapie.
Lithium
Zien WAARSCHUWINGEN .
Patiënt na sympathectomie
Het antihypertensieve effect van het geneesmiddel kan worden versterkt bij de patiënt die een sympathectomie heeft ondergaan.
noradrenaline
Indapamide kan, net als de thiaziden, de arteriële respons op noradrenaline verminderen, maar deze vermindering is niet voldoende om de werkzaamheid van het pressormiddel voor therapeutisch gebruik uit te sluiten.
1 Module 2.5 SER-indapamide-choroïdale effusie-acute bijziendheid en geslotenhoekglaucoom
juli 2020
WAARSCHUWINGEN
Ernstige gevallen van hyponatriëmie, vergezeld van hypokaliëmie, zijn gemeld bij aanbevolen doses indapamide. Dit kwam vooral voor bij oudere vrouwen. (Zien PREVENTIEVE MAATREGELEN , Geriatrisch gebruik .) Dit lijkt dosisgerelateerd te zijn. Ook wijst een groot geval-gecontroleerd farmaco-epidemiologisch onderzoek erop dat er een verhoogd risico is op hyponatriëmie met indapamide 2,5 mg en 5 mg doses. Hyponatriëmie die mogelijk klinisch significant wordt geacht ( PREVENTIEVE MAATREGELEN ). Daarom moeten patiënten worden gestart met de dosis van 1,25 mg en worden gehandhaafd met de laagst mogelijke dosis. (Zien DOSERING EN ADMINISTRATIE .)
Hypokaliëmie komt vaak voor bij diuretica (zie: ONGEWENSTE REACTIES , hypokaliëmie ), en het controleren van de elektrolyten is essentieel, vooral bij patiënten die een verhoogd risico lopen op hypokaliëmie, zoals patiënten met hartritmestoornissen of die gelijktijdig hartglycosiden krijgen.
Over het algemeen mogen diuretica niet gelijktijdig met lithium worden gegeven, omdat ze de renale klaring verminderen en een hoog risico op lithiumtoxiciteit opleveren. Lees de voorschrijfinformatie voor lithiumpreparaten vóór gebruik van dergelijke gelijktijdige therapie.
PREVENTIEVE MAATREGELEN
Algemeen
Hypokaliëmie, hyponatriëmie en andere vocht- en elektrolytenonevenwichtigheden
Periodieke bepalingen van serumelektrolyten moeten met geschikte tussenpozen worden uitgevoerd. Bovendien moeten patiënten worden geobserveerd op klinische tekenen van een verstoorde vocht- of elektrolytenbalans, zoals hyponatriëmie, hypochloremische alkalose of hypokaliëmie. Waarschuwingssignalen zijn onder meer een droge mond, dorst, zwakte, vermoeidheid, lethargie, slaperigheid, rusteloosheid, spierpijn of -krampen, hypotensie, oligurie, tachycardie en gastro-intestinale stoornissen. De bepaling van de elektrolyten is vooral belangrijk bij patiënten die overmatig braken of parenterale vloeistoffen krijgen, bij patiënten met een verstoorde elektrolytenbalans (inclusief patiënten met hartfalen, nierziekte en cirrose) en bij patiënten die een zoutarm dieet volgen.
Het risico op hypokaliëmie secundair aan diurese en natriurese is verhoogd wanneer grotere doses worden gebruikt, wanneer de diurese krachtig is, wanneer ernstige cirrose aanwezig is en tijdens gelijktijdig gebruik van corticosteroïden of ACTH. Interferentie met een adequate orale inname van elektrolyten zal ook bijdragen aan hypokaliëmie. Hypokaliëmie kan de reactie van het hart op de toxische effecten van digitalis, zoals verhoogde ventriculaire prikkelbaarheid, sensibiliseren of overdrijven.
Verdunningshyponatriëmie kan optreden bij oedemateuze patiënten; de juiste behandeling is beperking van water in plaats van toediening van zout, behalve in zeldzame gevallen wanneer de hyponatriëmie levensbedreigend is. Bij daadwerkelijke zoutuitputting is een geschikte vervanging echter de voorkeursbehandeling. Elk chloridetekort dat kan optreden tijdens de behandeling is over het algemeen mild en vereist gewoonlijk geen specifieke behandeling, behalve in buitengewone omstandigheden zoals bij lever- of nierziekte. Van thiazide-achtige diuretica is aangetoond dat ze de urinaire excretie van magnesium verhogen; dit kan leiden tot hypomagnesiëmie.
Hyperurikemie en jicht
De serumconcentraties van urinezuur namen toe met gemiddeld 0,69 mg/100 ml bij patiënten die werden behandeld met indapamide 1,25 mg en met gemiddeld 1,0 mg/100 ml bij patiënten die werden behandeld met indapamide 2,5 mg en 5,0 mg, en uitgesproken jicht kan worden versneld bij bepaalde patiënten die indapamide krijgen (zie: ONGEWENSTE REACTIES onderstaand). De serumconcentraties van urinezuur moeten daarom tijdens de behandeling periodiek worden gecontroleerd.
Nierfunctiestoornis
Indapamide moet, net als de thiaziden, met voorzichtigheid worden gebruikt bij patiënten met ernstige nierziekte, aangezien een verminderd plasmavolume azotemie kan verergeren of versnellen. Als een progressieve nierfunctiestoornis wordt waargenomen bij een patiënt die indapamide krijgt, moet worden overwogen om de behandeling met diuretica te staken of stop te zetten. Tijdens de behandeling met indapamide moeten regelmatig nierfunctietesten worden uitgevoerd.
Verminderde leverfunctie
Indapamide moet, net als de thiaziden, met voorzichtigheid worden gebruikt bij patiënten met een verminderde leverfunctie of progressieve leverziekte, aangezien kleine veranderingen in de vocht- en elektrolytenhuishouding een levercoma kunnen veroorzaken.
Glucosetolerantie
Latente diabetes kan zich manifesteren en de insulinebehoefte bij diabetespatiënten kan veranderen tijdens de toediening van thiazide. Bij patiënten die met indapamide 1,25 mg werden behandeld, werd een gemiddelde toename van glucose van 6,47 mg/dl waargenomen, wat in deze onderzoeken niet als klinisch significant werd beschouwd. Serumconcentraties van glucose moeten routinematig worden gecontroleerd tijdens de behandeling met Lozol.
Calciumuitscheiding
De uitscheiding van calcium wordt verminderd door diuretica die farmacologisch verwant zijn aan indapamide. Na zes tot acht weken behandeling met indapamide 1,25 mg en in langetermijnonderzoeken bij hypertensieve patiënten met hogere doses indapamide, stegen de serumconcentraties van calcium echter slechts licht met indapamide. Langdurige behandeling met geneesmiddelen die farmacologisch verwant zijn aan indapamide kan in zeldzame gevallen gepaard gaan met hypercalciëmie en hypofosfatemie als gevolg van fysiologische veranderingen in de bijschildklier; de gebruikelijke complicaties van hyperparathyreoïdie, zoals nierlithiasis, botresorptie en maagzweer, zijn echter niet waargenomen. De behandeling moet worden stopgezet voordat tests voor de bijschildklierfunctie worden uitgevoerd. Net als de thiaziden kan indapamide de serum-PBI-spiegels verlagen zonder tekenen van schildklierstoornissen.
Interactie met systemische lupus erythematodes
Thiaziden hebben systemische lupus erythematodes verergerd of geactiveerd en met indapamide moet ook rekening worden gehouden met deze mogelijkheid.
Acuut geslotenhoekglaucoom, acute bijziendheid en choroïdale effusie
Sulfonamide of sulfonamidederivaten, zoals indapamide, kunnen een idiosyncratische reactie veroorzaken die resulteert in acuut geslotenhoekglaucoom en verhoogde intraoculaire druk met of zonder een merkbare acute myopische verschuiving en/of choroïdale effusies. Symptomen kunnen zijn een acuut begin van verminderde gezichtsscherpte of oculaire pijn en treden meestal op binnen enkele uren tot weken na het starten van het geneesmiddel. Onbehandeld kan het gesloten hoekglaucoom resulteren in permanent gezichtsveldverlies. De primaire behandeling is om zo snel mogelijk te stoppen met indapamide. Als de intraoculaire druk ongecontroleerd blijft, moeten mogelijk onmiddellijke medische of chirurgische behandelingen worden overwogen. Risicofactoren voor het ontwikkelen van acuut geslotenhoekglaucoom kunnen een voorgeschiedenis van sulfonamide- of penicilline-allergie zijn.
Niet-klinische toxicologie
Carcinogenese, mutagenese, verminderde vruchtbaarheid
Er werden zowel levenslange carcinogeniteitsstudies bij muizen als bij ratten uitgevoerd. Er was geen significant verschil in de incidentie van tumoren tussen de met indapamide behandelde dieren en de controlegroepen.
Zwangerschap
Teratogene effecten
Er zijn reproductieonderzoeken uitgevoerd bij ratten, muizen en konijnen in doses tot 6.250 maal de therapeutische dosis voor de mens en er zijn geen aanwijzingen gevonden voor verminderde vruchtbaarheid of schade aan de foetus als gevolg van Lozol (indapamide). De postnatale ontwikkeling bij ratten en muizen werd niet beïnvloed door voorbehandeling van ouderdieren tijdens de dracht. Er zijn echter geen adequate en goed gecontroleerde onderzoeken bij zwangere vrouwen. Bovendien is bekend dat diuretica de placentabarrière passeren en in navelstrengbloed verschijnen. Omdat reproductiestudies bij dieren niet altijd voorspellend zijn voor de respons van de mens, mag dit medicijn alleen tijdens de zwangerschap worden gebruikt als dit duidelijk nodig is. Er kunnen gevaren verbonden zijn aan dit gebruik, zoals foetale of neonatale geelzucht, trombocytopenie en mogelijk andere bijwerkingen die bij volwassenen zijn opgetreden.
Moeders die borstvoeding geven
Het is niet bekend of dit geneesmiddel wordt uitgescheiden in de moedermelk. Omdat de meeste geneesmiddelen worden uitgescheiden in de moedermelk, moet de patiënt stoppen met borstvoeding geven als het gebruik van dit geneesmiddel essentieel wordt geacht.
Pediatrisch gebruik
De veiligheid en werkzaamheid van indapamide bij pediatrische patiënten zijn niet vastgesteld.
Geriatrisch gebruik
Klinische onderzoeken met indapamide omvatten niet voldoende aantallen proefpersonen van 65 jaar en ouder om te bepalen of zij anders reageren dan jongere proefpersonen. Andere gerapporteerde klinische ervaringen hebben geen verschillen in respons tussen oudere en jongere patiënten aangetoond. Over het algemeen moet de dosiskeuze voor een oudere patiënt voorzichtig zijn, meestal beginnend aan het lage uiteinde van het doseringsbereik, als gevolg van de grotere frequentie van verminderde lever-, nier- of hartfunctie en van gelijktijdige ziekte of andere medicamenteuze behandeling.
Ernstige gevallen van hyponatriëmie, vergezeld van hypokaliëmie, zijn gemeld met aanbevolen doses indapamide bij oudere vrouwen (zie WAARSCHUWINGEN ).
OVERDOSERING
Symptomen van overdosering zijn misselijkheid, braken, zwakte, gastro-intestinale stoornissen en verstoringen van de elektrolytenbalans. In ernstige gevallen kunnen hypotensie en depressieve ademhaling worden waargenomen. Als dit gebeurt, moet ondersteuning van de ademhaling en de hartcirculatie worden ingesteld. Er is geen specifiek tegengif. Een evacuatie van de maag wordt aanbevolen door braken en maagspoeling, waarna de elektrolyten- en vochtbalans zorgvuldig moeten worden beoordeeld.
CONTRA-INDICATIES
anurie.
Bekende overgevoeligheid voor indapamide of voor andere van sulfonamide afgeleide geneesmiddelen.
KLINISCHE FARMACOLOGIE
Indapamide is de eerste van een nieuwe klasse van antihypertensiva/diuretica, de indolines. De orale toediening van 2,5 mg (twee tabletten van 1,25 mg) indapamide aan mannelijke proefpersonen produceerde binnen twee uur piekconcentraties van ongeveer 115 ng/ml van het geneesmiddel in het bloed. De orale toediening van 5 mg (twee tabletten van 2,5 mg) indapamide aan gezonde mannelijke proefpersonen produceerde binnen twee uur piekconcentraties van ongeveer 260 ng/ml van het geneesmiddel in het bloed. Minimaal 70% van een enkelvoudige orale dosis wordt uitgescheiden door de nieren en nog eens 23% door het maagdarmkanaal, waarschijnlijk inclusief de galwegen. De halfwaardetijd van Lozol 1,5 mg in volbloed is ongeveer 14 uur.
Lozol wordt bij voorkeur en omkeerbaar opgenomen door de erytrocyten in het perifere bloed. De volbloed/plasmaverhouding is ongeveer 6:1 op het moment van de piekconcentratie en neemt af tot 3,5:1 na acht uur. Van 71 tot 79% van de Lozol in plasma is reversibel gebonden aan plasma-eiwitten.
Lozol 2,5 mg is een extensief gemetaboliseerd geneesmiddel, waarbij slechts ongeveer 7% van de totale toegediende dosis in de urine als onveranderd geneesmiddel wordt teruggevonden gedurende de eerste 48 uur na toediening. De urinaire eliminatie van 14C-gelabeld indapamide en metabolieten is bifasisch met een terminale excretiehalfwaardetijd van de totale radioactiviteit van 26 uur.
In een dubbelblind, placebogecontroleerd onderzoek naar hypertensie met parallel opzet, veroorzaakten dagelijkse doses indapamide tussen 1,25 mg en 10,0 mg dosisgerelateerde antihypertensieve effecten. Doses van 5,0 en 10,0 mg waren niet van elkaar te onderscheiden, hoewel elk was gedifferentieerd van placebo en 1,25 mg indapamide. Bij dagelijkse doses van 1,25 mg, 5,0 mg en 10,0 mg werd een gemiddelde afname van het serumkalium van respectievelijk 0,28, 0,61 en 0,76 mEq/L waargenomen en nam het urinezuur toe met ongeveer 0,69 mg/100 ml.
In andere parallelle klinische onderzoeken met doseringsbereik bij hypertensie en oedeem, veroorzaakten dagelijkse doses indapamide tussen 0,5 en 5,0 mg dosisgerelateerde effecten. Over het algemeen waren doses van 2,5 en 5,0 mg niet van elkaar te onderscheiden, hoewel elk verschilde van placebo en van 0,5 of 1,0 mg indapamide. Bij dagelijkse doses van 2,5 en 5,0 mg werd een gemiddelde afname van het serumkalium van respectievelijk 0,5 en 0,6 mEq/liter waargenomen en het urinezuur steeg met ongeveer 1,0 mg/100 ml.
Bij deze doses zijn de effecten van indapamide op bloeddruk en oedeem ongeveer gelijk aan die verkregen met conventionele doses van andere antihypertensiva/diuretica.
Bij hypertensieve patiënten hebben dagelijkse doses van 1,25, 2,5 en 5,0 mg indapamide geen merkbaar inotroop of chronotroop effect op het hart. Het medicijn vermindert de perifere weerstand met weinig of geen effect op het hartminuutvolume, de snelheid of het ritme. Chronische toediening van indapamide aan hypertensieve patiënten heeft weinig of geen effect op de glomerulaire filtratiesnelheid of de renale plasmastroom.
Lozol had een antihypertensief effect bij patiënten met verschillende gradaties van nierinsufficiëntie, hoewel in het algemeen de diuretische effecten afnamen naarmate de nierfunctie verminderde.
In een klein aantal gecontroleerde onderzoeken bleek Indapamide, samen met andere antihypertensiva zoals hydralazine, propranolol, guanethidine en methyldopa, het additieve effect te hebben dat typisch is voor diuretica van het thiazide-type.
PATIËNT INFORMATIE
Geen informatie verstrekt. Raadpleeg de WAARSCHUWINGEN EN VOORZORGSMAATREGELEN sectie.
